关键词:氨基胍;内毒素
摘要 目的:观察比较iNOS抑制药AG对鼠离体主动脉和肺动脉环张力的影响。方法:测定血管对NE的量-效反应,在LPS(300ng/ml)中孵育4小时后。分为L-NAME(300μmol/L)或AG(100μmol/L)孵育60或20分钟共8组。结果:LPS孵育后动脉环对NE的反应明显降低,给予L-NAME或AG后均升高以10-6 mol/L NE作比较,L-NAME组主动脉20分钟时反应性明显高于AG组。L-NAME组肺动脉较AG组明显升高(P <0.01)。AG60分钟组主动脉升高的幅度明显大于肺动脉组(P <0.01)。L-NAME引起的血管收缩高峰时间较AG组出现的早,且峰值高。结论:L-NAME和AG都可增加已降低的对NE的反应性;但AG仅使主动脉环的敏感性明显增加。
Effects of aminoguanidine on endotoxin-treated rat aorta and
pulmonary artery in vitro
Wang Junke,Song Bingbing,Sheng
Zhuoren,et al.Department of Anesthesiology,First Affiliated
Hospital,China Medical University,Shenyang 110001
Abstract Objective:To investigate the effects of selective NOS inhibitor aminoguanidine (AG)on endotoxin-treated rat aorta (AO)and pulmonary artery (PA)in vitro.Method:The reaction to noradrenaline(NE)(10-9 -10-4 mmol/L)was measured in the vessels with complete endothelium,then the vessels were divided into 8 groups after incubated in LPS(300ng/ml)for 4 hours.Each group was
incubated with AG(100μmol/L)or L-NAME (300μmol/L)for 20,or 60 min,respectively.Result:Both AO and PA showed hyporeactivity to NE after incubated in LPS,and the reactivity of AO and PA to L-NAME and AG increased significantly after incubated in them for 60min or 20min.The sensitivities of AO to AG,AO and PA to L-NAME increased greatly.AO had a higher reactivity to AG in 60min than in 20min.L-NAME caused earlier and greater contraction than AG in both 60 min and 20 min groups.Conclusion:L-NAME and AG can both increase the decreased reactivities
of AO and PA to NE.AG only increases the AO sensitivity.
Key words Aminoguanidine Endotoxin
在感染性休克的治疗中,非选择性一氧化氮(NO)合酶(NOS)抑制药L-N-位硝基精氨甲酯(L-NAME)可同时明显收缩外周血管和肺动脉,使离体主动脉和肺动脉对血管收缩药的敏感性增加。目前尚不清楚选择性诱导性NOS(iNOS)抑制药氨基胍(AG)对外周血管和肺动脉的影响是否存在差异。本研究的目的就是通过用L-NAME和AG孵育内毒素处理的主动脉环和肺动脉环对去甲肾上腺素的反应性,研究L-NAME和AG对不同部位血管作用的差异。
资料与方法
试剂 去甲肾上腺素(NE,Fluka Chemie AG,瑞士,1克/支,纯度99%),乙酰胆碱(Ach,上海试剂公司进口分装,1克/支,纯度99%),L-NAME(Sigma,5克/瓶,纯度99%)、AG(Sigma,50克/瓶,纯度99%)、内毒素(LPS,北京邦定公司,1毫克/支)。
实验方法 雄性Wistar大鼠(190~250g),断头处死后速取主肺动脉及胸主动脉环悬挂于麦氏水浴管内,加入Krebs Buffer液10ml,通混合气体(95% O2 ,5% CO2 ),调节温度37.0℃±0.5℃,给予静止肌张力1.0g(1g=25mm)后检测血管内皮细胞的完整性,即用10-6 mol/L NE使血管环收缩达最大且平衡后,加入10-5 mol/L的Ach,若出现50%以上的舒张反应,为内皮细胞完整,将内皮细胞完整的血管环冲洗后加入累积剂量的NE(10-9 ~10-4 mol/L),测定量-效反应曲线,然后将主动脉和肺动脉环置含有LPS(300ng/ml)的组织培养液中,置37℃ CO2 孵育箱中孵育4小时,测定量-效反应曲线。冲洗后随机分为L-NAME(300μ mol/L)孵育60及20分钟的主动脉(n =8只)和肺动脉(n =6只)或AG(100 μmol/L)孵育60及20分钟的主动脉(n =8只)和肺动脉(n =6只)共8组,分别在孵育60和20分钟后观察量-效反应曲线。
统计学处理 实验数据以平均值±s(mm/g)表示。组内行单因素方差分析和q检验。组间行团体t检验。P <0.05有统计学差异。
结果
对NE的量-效反应曲线 给予LPS后所有动脉环对NE的反应性均降低;给予L-NAME或AG后,对高浓度NE的反应性均明显增加。以对10-6 mol/L的NE的反应性比较,给LPS前主动脉较肺动脉的反应性稍高(P >0.05)。给予L-NAME或AG后各组反应性均有升高,60分钟时L-NAME组主动脉较AG组稍高(P >0.05),而20分钟时明显高于AG组(P <0.05)。肺动脉各时段较AG组明显升高(P <0.05)。L-NAME组主动脉环和肺动脉环的升高幅度无明显差异;而60分钟组的反应性均略低于20分钟组(P <0.05)。AG60分钟组主动脉升高的幅度明显大于肺动脉(P <0.05)。而20分钟组两者无明显差异(P >0.05)。说明L-NAME可使主动脉和肺动脉对NE的敏感性增高。AG仅使主动脉的敏感性增加(见图1~2)。
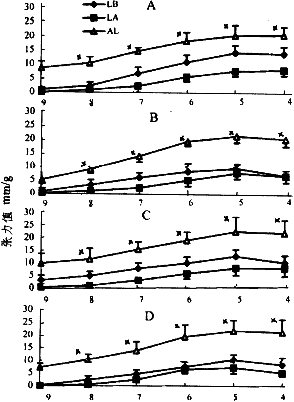
NE浓度〔-Log(mol/L)〕
图1 L-NAME处理60及20分钟主动脉和肺动脉对NE反应曲线
LB为给予LPS前反应值 LA为给予LPS后反应值
AL为给予L-NAME后反应值 x为AL与LA相比有统计学差异,P<0.05
A:60分钟主动脉反应曲线 B:60分钟肺动脉反应曲线
C:20分钟主动脉反应曲线 D:20分钟肺动脉反应曲线
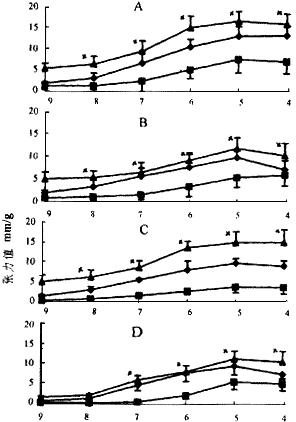
NE浓度〔-Log(mol/L)〕
图2 AG处理60及20分钟主动脉和肺动脉对NE反应曲线
LB为给予LPS前反应值 LA为给予LPS后反应值
AL为给予AG后反应值 x为AL与LA相比有统计学差异,P<0.05
A:60分钟主动脉反应曲线 B:60分钟肺动脉反应曲线
C:20分钟主动脉反应曲线 D:20分钟肺动脉反应曲线
高峰时间和高峰值 从L-NAME或AG本身引起的收缩高峰时间看,L-NAME引起的血管收缩高峰较AG出现的早,AG组肺动脉收缩高峰早于主动脉(P <0.05)。AG组主动脉收缩高峰值明显高于肺动脉,而L-NAME组两者无明显差异,L-NAME引起的肺动脉收缩高峰明显大于AG(P <0.05)。见附表。
附表 L-NAME与AG所引起主动脉和肺动脉收缩高峰值和时间比较(±s)
| L-NAME | AG | ||
| 主动脉 | 高峰时间(min) | 13.81±2.39▲ | 52.38±5.44 |
| 高峰值(mm/g) | 6.17±2.81 | 4.97±1.29☆ | |
| 肺动脉 | 高峰时间(min) | 12.94±2.69▲ | 40.71±4.18☆ |
| 高峰值(mm/g) | 6.09±0.25▲ | 1.58±0☆ |
L-NAME与AG间比较,▲ P<0.05 主动脉与肺动脉间比较,☆ P<0.05
讨论
研究发现在人体血管内皮细胞中有两种NOS,一种为结构性(cNOS),对维持正常的血管舒缩状态有重要作用,给予LPS后很快即被激活。另一种为诱导性(iNOS),在正常情况下无活性,给予LPS后3~4小时达最大活性值。LPS所引起的NOS,尤其是iNOS的激活,可引起NO合成明显增加,激活血管平滑肌中的鸟苷酸环化酶,使cGMP浓度增加、血管扩张。同时血管对血管收缩物质,如NE、血管紧张素Ⅱ的反应性下降〔1,2〕 。用LPS100ng/ml孵育无血管内皮细胞的离体动脉环,在6小时后出现明显的血管舒张反应,而血管内皮细胞完整者在4小时即出现血管舒张反应,说明感染性休克中NO的增加是血管内皮细胞依赖性的〔3、4〕 。
L-NAME和AG均可产生剂量依赖性血管收缩反应。Julou-Schaeffer等〔5,6〕 报道用Ach、L-精氨酸和LPS处理后,内皮细胞完整的离体动脉环对NE的反应性均降低,而L-NAME(300μmol/L)可使之逆转,L-NAME还可使对照组动脉环对间羟胺的收缩性增强,说明它对cNOS有抑制作用〔3〕 。AG(100μ mol/L)对对照组间羟胺引起的动脉收缩和Ach引起的舒张无明显影响,而对LPS处理的动脉环的收缩作用与L-NAME相似〔7,8〕 ,并同时增加血管对NE的敏感性,说明它对cNOS无抑制作用,而对iNOS有明显的抑制作用。
从本研究可见,给予处理因素后L-NAME 组主动脉和肺动脉、AG组主动脉对NE的反应性都明显高于基础值,L-NAME组更加明显;而AG组肺动脉与基础值无明显差异。说明L-NAME使主动脉和肺动脉、AG使主动脉对NE的敏感性增加,且L-NAME大于AG;而AG不影响肺动脉对NE的敏感性。从两种抑制药的收缩峰值看也存在着明显的差异:L-NAME使主动脉和肺动脉明显收缩,AG仅明显收缩主动脉,这与我们在另一在体实验中所观察到的L-NAME使MAP和PAP升高,AG仅使MAP升高,且程度小于L-NAME〔9〕 一致。肺循环是一低压循环系统,肺动脉壁的平滑肌层较薄,仅为主动脉壁的1/3,已有研究发现主动脉和肺动脉对某些静脉麻醉药的反应性不同,但目前尚不清楚肺动脉与主动脉内皮细胞中iNOS及血管平滑肌细胞中鸟苷酸环化酶的活性是否存在差异。结构和功能上的差异可能造成了主动脉和肺动脉对选择性NOS抑制药反应性的不同。
本实验中处理因素本身引起的高峰时间L-NAME明显快于AG组,肺动脉组略快于主动脉组。这可能与L-NAME抑制cNOS,导致较快的血管收缩有关。AG为特异iNOS抑制药,iNOS被激活的过程慢,需3~4小时,其作用被抑制的过程也可能相对较慢。AG组20分钟时主动脉与肺动脉对NE的反应值无明显差异,可能与肺动脉反应性出现快,接近达到高峰值,而主动脉尚未达到有关。60分钟时L-NAME组主动脉和肺动脉对10-6 mol/L NE的反应性小于20分钟时,说明L-NAME对cNOS的作用强于iNOS。
由此可见,AG对体循环和肺循环血管的作用有很明显的差异,使用AG选择性地抑制感染性休克体循环中iNOS的激活,升高血压而不影响肺循环,可能对感染性休克的治疗有重要意义。
本研究为1996年卫生部科学基金资助项目
参考文献
1 Flemming I,Gray GA,Stoclet JC.Influence of endothelium on induction
of the L-arginine-nitric oxide pathway in rat aortas.Am J Physiol,1993,264:H1200-1206.
2 Szabo C,Mitchell JA,Thiemermann C,et al.Nitric oxide-mediated hyporeactivity to noradrenaline precedes
the induction of nitric oxide synthase in endotoxin shock.Br J Pharmacol,1993,108:786-791.
3 Wakabayashi I,Hatake K,Kakishita E,et al.Diminution of contractile response of the aorta from
endotoxin-injected rats.Eur J Pharmacol,1987,114:117-122.
4 Julou-Schaeffer G,Gray GA,Fleming GI,et al.Loss of vascular responsiveness induced by endotoxin
involves L-arginine pathway.Am J Physiol,1990,259:H1038-1045.
5 Julou-Schaeffer G,Gray GA,Fleming GI,et al.Activation of the L-arginine/nitric oxide pathway is involved in
vascular hyporeactivity induced by endotoxin.J Cardiovasc Pharmacol,1991,17:S207-210.
6 Joly GA,Ayre M,Chelly FC,et al.Effects of NG -methyl-L-arginine,NG -nitro-L-arginine,and aminoguanidine on constitutive and inducible nitric oxide
sysnthase in rat aorta.Bioch Biophy Res Commun,1994,199:147-155.
7 Griffiths MJD,Messent M,MacAllister RJ,et al.Amiogu-
anidine selectively inhibits inducible nitric oxide synthase.Br J Pharmacol,1993,110:963-968.
8 Wu CH,Chen SHJ,Szabo C,et al.Aminoguanidine attenuates the delayed circulatory failure and
improves survival in rodent models of endotoxic shock. Br J Pharmacol,1995,114:1666-1672.
9 宋冰冰,王俊科,盛卓人,等.诱导性一氧化氮合酶抑制药对感染性休克治疗作用的研究.中华麻醉学杂志,1998,18:90-92.
(收稿:1997-11-18 修回:1998-07-10)
, http://www.100md.com