IFNα、IL-1β和IL-2对登革Ⅱ型病毒复制的影响
作者:曹艳英 郭辉玉
单位:510630 广州,暨南大学(曹艳英);中山医科大学(郭辉玉)
关键词:
中华传染病杂志980122 登革病毒感染是热带和亚热带地区严重的公共卫生健康问题,登革病毒的主要靶细胞是单核细胞。有关其发病机制近年来注意到细胞因子的释放,本课题以人单核细胞为登革Ⅱ型病毒(D2V)感染的靶细胞,研究IFNα、IL-1β和IL-2对D2V复制的影响,试图对其发病机制进行探讨。
材料和方法
一、材料
(一) IL-1β、IL-2、IFNα,军事医学科学院生物制剂部提供。
(二) 病毒 D2V标准株(New Guinea C株),本室自行传代保存。
, 百拇医药
二、方法
(一) 人单核细胞的分离 取正常人外周血和脐带抗凝血,用淋巴细
表1 IFNα对人单核细胞中D2V复制的影响 (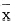 ±s) IFNα(u/ml)
±s) IFNα(u/ml)
病毒滴度(103pfu/ml) (n=6)
病毒吸附前
病毒吸附同时
病毒吸附后
0
9.42±2.81
, http://www.100md.com 8.08±2.79
8.17±2.52
10
6.67±3.32
7.92±3.11
7.75±2.39
100
3.00±0.67*
6.08±1.67
7.08±1.91
1000
0.25±0.25*
, http://www.100md.com
0.67±0.38*
1.38±0.64*
* P<0.05
表2 IL-1β对人单核细胞中D2V复制的影响 (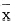 ±s) IL-1β(u/ml)
±s) IL-1β(u/ml)
浓度
病毒滴度(103pfu/ml) (n=6)
病毒吸附前
病毒吸附同时
病毒吸附后
, 百拇医药
0
10.50±3.78
11.58±4.04
8.42±1.75
1
7.67±3.75
10.42±5.13
8.08±2.26
10
5.25±2.50*
6.25±2.54*
6.00±2.18
, 百拇医药
100
2.84±0.52*
4.50±1.09*
5.58±1.51*
* P<0.05
表3 IL-2对人单核细胞中D2V复制的影响 (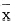 ±s) IL-2(u/ml)
±s) IL-2(u/ml)
浓度
病毒滴度(103pfu/ml) (n=6)
病毒吸附前
, http://www.100md.com
病毒吸附同时
病毒吸附后
0
7.83±2.13
8.25±2.46
8.75±1.75
1
13.83±3.62*
9.25±2.28
17.83±2.57*
10
21.75±4.56*
, 百拇医药
11.83±3.82*
21.17±3.66*
100
6.92±2.32*
7.50±2.29*
8.33±1.91*
* P<0.05 胞分层液分离出单个核细胞。细胞贴壁培养3天去非贴壁细胞,等量0.02%EDTA与20%FCS1640混合液消化15分钟后收集贴壁细胞,用培养液洗两遍,细胞用于D2V感染。
(二) D2V感染人单核细胞 取人单核细胞计数1×105/孔 加入24孔板中,设四组,阴性对照组,细胞因子低浓度(IL-1β lU/ml、IL-2 1U/ml、IFNα 10U/ml)、中浓度(IL-1β 10U/ml、IL-2 10U/ml、IFNα 100U/ml)、高浓度(IL-1β 100U/ml、IL-2 100U/ml、IFNα 1000U/ml)。选择不同的时间加入细胞因子:病毒吸附前为细胞因子与细胞温育24小时再感染D2V;病毒吸附同时为细胞因子和病毒同时与细胞温育2小时;病毒吸附后为病毒吸附细胞2小时后再加入细胞因子。取48小时感染上清测定病毒滴度。
, 百拇医药
(三) 病毒滴度的测定[1] 用D2V敏感的C6/36单层细胞与甲基纤维素覆盖层的微量浊斑法滴定D2V,病毒滴度以病毒空斑形成单位(pfu)表示。
(四) 统计学处理 每次实验取实验组与对照组,每例作两个平行孔,实验数据用平均值±标准差表示,组间比较用t检验。
结 果
一、人单核细胞感染性测定
用5pfu/cell的D2V感染脐带血人单核细胞,取不同时间的上清测定病毒滴度,结果表明病毒感染48小时达高峰,以后逐渐下降。
二、IFNα对D2V复制的影响
选择病毒感染的不同时间加入IFNα作用于正常人单核细胞,取48小时感染上清测定病毒滴度,结果表明IFNα能抑制D2V复制,并与剂量正相关,抑制作用以病毒吸附前作用明显(见表1)。
, 百拇医药
三、IL-1β对D2V复制的影响
选择病毒感染的不同时间加入IL-1β作用于正常人单核细胞,取48小时感染上清测定病毒滴度。结果表明IL-1β能抑制D2V复制,并与剂量正相关,抑制作用以病毒吸附前作用明显(见表2)。
四、IL-2对D2V复制的影响
选择病毒感染的不同时间加入IL-2作用于正常人单核细胞,取48小时感染上清测定病毒滴度。结果表明IL-2低、中浓度 在病毒吸附前、吸附后能增加D2V复制,高浓度的IL-2对D2V复制无明显影响(见表3)。
五、IFNα、IL-1β和IL-2对未感染和感染的人单核细胞数量的影响
用不同浓度的IFNα、IL-1β和IL-2与未感染和感染的人单核细胞温育24小时,用结晶紫染色法在490nm处测A值。结果表明IFNα、IL-1β和IL-2对未感染和感染的人单核细胞数量无明显影响(P>0.05)。
, 百拇医药
讨 论
细胞因子与微生物感染密切相关,一方面病原体的感染能诱导宿主细胞产生细胞因子,另一方面细胞因子又能刺激或抑制病原体在宿主细胞中的增殖。国外有报道登革病毒感染人单核细胞产生IFNα,IFNα能抑制登革病毒的复制[2]登革病毒特异的CD4+CD8T细胞产生IL-2[3];最近有学者提出登革病毒感染的发病机制与细胞因子的释放有关。本课题以人单核细胞为D2V感染的靶细胞,研究了IFNα、IL-1β和IL-2对D2V复制的影响,实验发现IFNα和IL-1β具抗病毒作用,与剂量正相关,这种效应在病毒吸附前加入明显,高浓度的IFNα在病毒吸附同时甚至病毒吸附后加入也能发挥较强的抗病毒作用,这是与最近的进展IFNα存在快速调控途径有关[4]。IL-1β具抗病毒作用,其机制有待近一步阐明。在IL-2对D2V影响的研究中发现,IL-2能增加病毒的复制,国外有学者报道IL-2处理能诱导低毒株柯萨奇病毒引起心肌炎[5],提示IL-2增强病毒感染心肌细胞。我们的实验发现高浓度的IL-2对D2V复制无明显影响,推测细胞因子存在负反馈调节。三种细胞因子对正常的和感染的人单核细胞数量无明显影响,说明它们是通过调节细胞功能来影响病毒增殖。我们的实验结果提示IFNα、IL-1β和IL-2在登革病毒感染中起重要作用。
, 百拇医药
参考文献
1 陈佩嘉,郭辉玉.登革病毒单克隆抗体和登革热病人血清对人单核细胞系U937的促进作用.中国临床和病毒学杂志,1988,2:20.
2 Halstead SBO,Rouke EJ,Allison AC.Dengue virus and mononuclear phagocytes.J Exp Med 1977,146:201-217.
3 Balkwill FR,Burke F.The cytokine network. Immunol Today,1989,10:299-304.
4 Burke DS,Morrill JC.Levels of IFN in the plasma and cerebrospinal fluid of patients with acute Japanese encephalitis.J Infect Dis,1987,155:797-799.
5 Huber SA,Polgar J.Augmentation of pathogenesis of coxackievirus B3 infection in mice by exogenous administration of IL-1 and IL-2. J Virol,1994,68:195-206., 百拇医药
单位:510630 广州,暨南大学(曹艳英);中山医科大学(郭辉玉)
关键词:
中华传染病杂志980122 登革病毒感染是热带和亚热带地区严重的公共卫生健康问题,登革病毒的主要靶细胞是单核细胞。有关其发病机制近年来注意到细胞因子的释放,本课题以人单核细胞为登革Ⅱ型病毒(D2V)感染的靶细胞,研究IFNα、IL-1β和IL-2对D2V复制的影响,试图对其发病机制进行探讨。
材料和方法
一、材料
(一) IL-1β、IL-2、IFNα,军事医学科学院生物制剂部提供。
(二) 病毒 D2V标准株(New Guinea C株),本室自行传代保存。
, 百拇医药
二、方法
(一) 人单核细胞的分离 取正常人外周血和脐带抗凝血,用淋巴细
表1 IFNα对人单核细胞中D2V复制的影响 (
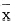 ±s) IFNα(u/ml)
±s) IFNα(u/ml)病毒滴度(103pfu/ml) (n=6)
病毒吸附前
病毒吸附同时
病毒吸附后
0
9.42±2.81
, http://www.100md.com 8.08±2.79
8.17±2.52
10
6.67±3.32
7.92±3.11
7.75±2.39
100
3.00±0.67*
6.08±1.67
7.08±1.91
1000
0.25±0.25*
, http://www.100md.com
0.67±0.38*
1.38±0.64*
* P<0.05
表2 IL-1β对人单核细胞中D2V复制的影响 (
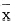 ±s) IL-1β(u/ml)
±s) IL-1β(u/ml)浓度
病毒滴度(103pfu/ml) (n=6)
病毒吸附前
病毒吸附同时
病毒吸附后
, 百拇医药
0
10.50±3.78
11.58±4.04
8.42±1.75
1
7.67±3.75
10.42±5.13
8.08±2.26
10
5.25±2.50*
6.25±2.54*
6.00±2.18
, 百拇医药
100
2.84±0.52*
4.50±1.09*
5.58±1.51*
* P<0.05
表3 IL-2对人单核细胞中D2V复制的影响 (
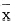 ±s) IL-2(u/ml)
±s) IL-2(u/ml)浓度
病毒滴度(103pfu/ml) (n=6)
病毒吸附前
, http://www.100md.com
病毒吸附同时
病毒吸附后
0
7.83±2.13
8.25±2.46
8.75±1.75
1
13.83±3.62*
9.25±2.28
17.83±2.57*
10
21.75±4.56*
, 百拇医药
11.83±3.82*
21.17±3.66*
100
6.92±2.32*
7.50±2.29*
8.33±1.91*
* P<0.05 胞分层液分离出单个核细胞。细胞贴壁培养3天去非贴壁细胞,等量0.02%EDTA与20%FCS1640混合液消化15分钟后收集贴壁细胞,用培养液洗两遍,细胞用于D2V感染。
(二) D2V感染人单核细胞 取人单核细胞计数1×105/孔 加入24孔板中,设四组,阴性对照组,细胞因子低浓度(IL-1β lU/ml、IL-2 1U/ml、IFNα 10U/ml)、中浓度(IL-1β 10U/ml、IL-2 10U/ml、IFNα 100U/ml)、高浓度(IL-1β 100U/ml、IL-2 100U/ml、IFNα 1000U/ml)。选择不同的时间加入细胞因子:病毒吸附前为细胞因子与细胞温育24小时再感染D2V;病毒吸附同时为细胞因子和病毒同时与细胞温育2小时;病毒吸附后为病毒吸附细胞2小时后再加入细胞因子。取48小时感染上清测定病毒滴度。
, 百拇医药
(三) 病毒滴度的测定[1] 用D2V敏感的C6/36单层细胞与甲基纤维素覆盖层的微量浊斑法滴定D2V,病毒滴度以病毒空斑形成单位(pfu)表示。
(四) 统计学处理 每次实验取实验组与对照组,每例作两个平行孔,实验数据用平均值±标准差表示,组间比较用t检验。
结 果
一、人单核细胞感染性测定
用5pfu/cell的D2V感染脐带血人单核细胞,取不同时间的上清测定病毒滴度,结果表明病毒感染48小时达高峰,以后逐渐下降。
二、IFNα对D2V复制的影响
选择病毒感染的不同时间加入IFNα作用于正常人单核细胞,取48小时感染上清测定病毒滴度,结果表明IFNα能抑制D2V复制,并与剂量正相关,抑制作用以病毒吸附前作用明显(见表1)。
, 百拇医药
三、IL-1β对D2V复制的影响
选择病毒感染的不同时间加入IL-1β作用于正常人单核细胞,取48小时感染上清测定病毒滴度。结果表明IL-1β能抑制D2V复制,并与剂量正相关,抑制作用以病毒吸附前作用明显(见表2)。
四、IL-2对D2V复制的影响
选择病毒感染的不同时间加入IL-2作用于正常人单核细胞,取48小时感染上清测定病毒滴度。结果表明IL-2低、中浓度 在病毒吸附前、吸附后能增加D2V复制,高浓度的IL-2对D2V复制无明显影响(见表3)。
五、IFNα、IL-1β和IL-2对未感染和感染的人单核细胞数量的影响
用不同浓度的IFNα、IL-1β和IL-2与未感染和感染的人单核细胞温育24小时,用结晶紫染色法在490nm处测A值。结果表明IFNα、IL-1β和IL-2对未感染和感染的人单核细胞数量无明显影响(P>0.05)。
, 百拇医药
讨 论
细胞因子与微生物感染密切相关,一方面病原体的感染能诱导宿主细胞产生细胞因子,另一方面细胞因子又能刺激或抑制病原体在宿主细胞中的增殖。国外有报道登革病毒感染人单核细胞产生IFNα,IFNα能抑制登革病毒的复制[2]登革病毒特异的CD4+CD8T细胞产生IL-2[3];最近有学者提出登革病毒感染的发病机制与细胞因子的释放有关。本课题以人单核细胞为D2V感染的靶细胞,研究了IFNα、IL-1β和IL-2对D2V复制的影响,实验发现IFNα和IL-1β具抗病毒作用,与剂量正相关,这种效应在病毒吸附前加入明显,高浓度的IFNα在病毒吸附同时甚至病毒吸附后加入也能发挥较强的抗病毒作用,这是与最近的进展IFNα存在快速调控途径有关[4]。IL-1β具抗病毒作用,其机制有待近一步阐明。在IL-2对D2V影响的研究中发现,IL-2能增加病毒的复制,国外有学者报道IL-2处理能诱导低毒株柯萨奇病毒引起心肌炎[5],提示IL-2增强病毒感染心肌细胞。我们的实验发现高浓度的IL-2对D2V复制无明显影响,推测细胞因子存在负反馈调节。三种细胞因子对正常的和感染的人单核细胞数量无明显影响,说明它们是通过调节细胞功能来影响病毒增殖。我们的实验结果提示IFNα、IL-1β和IL-2在登革病毒感染中起重要作用。
, 百拇医药
参考文献
1 陈佩嘉,郭辉玉.登革病毒单克隆抗体和登革热病人血清对人单核细胞系U937的促进作用.中国临床和病毒学杂志,1988,2:20.
2 Halstead SBO,Rouke EJ,Allison AC.Dengue virus and mononuclear phagocytes.J Exp Med 1977,146:201-217.
3 Balkwill FR,Burke F.The cytokine network. Immunol Today,1989,10:299-304.
4 Burke DS,Morrill JC.Levels of IFN in the plasma and cerebrospinal fluid of patients with acute Japanese encephalitis.J Infect Dis,1987,155:797-799.
5 Huber SA,Polgar J.Augmentation of pathogenesis of coxackievirus B3 infection in mice by exogenous administration of IL-1 and IL-2. J Virol,1994,68:195-206., 百拇医药