糖尿病大鼠脑组织一氧化氮合酶表达的变化
作者:贾军宏 田东华 于国平 马学毅
单位:贾军宏 马学毅:解放军304医院内分泌科,北京 100037;田东华 于国平:解放军总医院神经内科,北京 100853
关键词:糖尿病;一氧化氮合酶;中枢神经系统
糖尿病大鼠脑组织一氧化氮合酶表达的变化 摘要 目的:探讨一氧化氮在糖尿病神经病变发病机制中的作用。方法:采用硫辛氨脱氢酶(NADPH)酶组织化学染色法测定糖尿病大鼠脑组织一氧化氮合酶(NOS)表达的变化。结果:糖尿病成模后3个月,大脑皮层区NOS阳性神经元明显减少,但在海马区却发现NOS阳性细胞。结论:NOS的改变,可能参与糖尿病中枢神经系统病变的发病过程。
中国图书资料分类法分类号 R 587.1
The change of the nitric oxidesynthase expression
, http://www.100md.com
in brain ofdiabetic rats
Jia Junhong,Tiandonghua,Yuguoping,Ma Xueyi
(Department of Endocrinology,304thhospital of PLA,Beijing 100037)
Abstract Objective:To explore the effects of nitric oxide on themechanism ofdiabetic neuropathy.Methods:The changes of nitric oxidesynthase (NOS) expression in the brain ofdiabetic rats weremeasured by thehistochemiscal technique with nicotinamide adeninedinucleotide phosphate (NADPH-d).Results:After inducing themodel ofdiabetes for threemonths,the positive neurons of NOS in the brain contex were obviouslydecreased in thediabetesgroup than the normal controlgroup.While the positive neuron of NOS were found in thehippocampal area ofdiabetesgroup. Conclusion:The changes of NOS expressionmay be a factor in the impact ofdiabetes on the central nervoussystem.
, 百拇医药
Key words diabetes; NOS; CNS
一氧化氮(NO)是一种无机气体,具有多种生物活性〔1〕。在糖尿病神经病变病原学的研究中,NO及一氧化氮合酶(NOS)的作用引人注目,有人认为它是连接糖尿病神经系统病变代谢假说和血管假说之间的桥梁〔2〕。为此,采用组织化学方法我们观察了成模 3 个月的糖尿病大鼠脑组织一氧化氮合酶表达的变化。
1 材料和方法
1.1 大鼠糖尿病模型制备 雄性Wistar大鼠体重 170~230g,按体重随机分为两组:正常对照(NC)组;糖尿病(DM)组。
大鼠禁食 12h,DM组按 75mg/kg单剂腹腔注射枸橼酸缓冲液配制的链脲佐菌素(STZ,Sigma),NC组注射等体积枸橼酸缓冲液。注射 3d后用血糖仪(ONE TOUCH Ⅱ,强生公司)测大鼠尾静脉血糖,DM组>13mmol/L者入选。两组动物同等条件下饲养,自由摄食水。
, http://www.100md.com
1.2 观察指标
1.2.1 一般检查 包括体重、血糖、糖化血红蛋白。其中体重、血糖每月测定 1 次,糖化血红蛋白于实验结束时心脏取血用微柱法测定。
1.2.2 大脑一氧化氮合酶(NOS)表达的变化 大鼠喂养 3 个月后用 10% 水合氯醛(400mg/kg)腹腔注射麻醉,迅速剪开胸腔暴露心脏,经左心室插管至升主动脉,然后快速灌注肝素化生理盐水,同时剪开右心房,当灌注量达 100ml时,换液为 4% 多聚甲醛(0.1mol/LPB配制)500ml,灌注压约 9.8 kPa,灌注时间约 1h。用小咬骨钳仔细去除颅骨,完整取出大脑。脑组织浸于 20% 蔗糖溶液,4°C过夜。脑组织在Leica冰冻切片机上行连续冰冻切片,厚度为 50μm,切片入孵育液,孵育液包含 1mmol/L NADPH, 1mmol/L NBT,孵育时间为 30min。1%明胶贴片,常规脱水透明,DPX封片。Olympus BH-2 显微镜下观察。阴性对照染色:用PBS替换NADPH,余步骤同上。
, 百拇医药
2 结果
2.1 体重变化 实验前两组体重无明显差异,实验后DM组体重增长明显低于NC组,P<0.000 1,见表 1。
表 1 体重变化(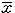 ±s,W/g)
±s,W/g)
分组
n
实验前
1个月
2个月
3个月
, 百拇医药
NC
8
226.25±18.48
370.63±43.21
496.25±66.10
601.34±58.23
DM
9
222.44±47.20
296.66±51.72*
318.33±53.27*
, 百拇医药
285.55±69.63*
*表示与NC组比较,P<0.000 1
2.2 生化指标 见表 2。DM组血糖和糖化血红蛋白明显高于NC组,P<0.000 1。
表 2 血糖、糖化血红蛋白比较(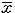 ±s)
±s)
分组
n
血糖(mmol/L)
GHb(%)
, 百拇医药
成模时
2个月
3个月
NC
8
4.02±0.56
3.79±1.02
3.69±0.47
6.98±1.39
DM
9
16.73±3.43*
, 百拇医药
19.49±4.66*
17.79±3.37*
12.06±1.77*
*表示与NC组比较,P<0.0001
2.3 脑组织NOS的变化 NADPH-d组织化学染色可清晰显示脑组织中含NOS神经元,NOS阳性神经元散在分布于各脑区在大脑皮层,DM组皮层中NOS阳性神经元较NC组明显减少,但在正常大鼠的海马区NADPH-d染色未发现NOS阳性神经元,糖尿病大鼠的海马区却发现有散在的NOS阳性细胞。
3 讨论
NO是由L-精氨酸在NOS的作用下产生的,由于半衰期很短,仅 4~5s,难以测定,所以一般多以NOS的活性表示NO的多少。已证实,当组织在用福尔马林固定情况下,NADPH还原酶(NADPH-d)组织化学染色可准确显示含NOS的细胞或组织,并可准确反映NOS的活性〔3〕。本实验用此方法显示的大鼠脑组织NOS阳性神经元呈深蓝色,其胞体和树突清晰可见。
, 百拇医药
已有很多实验证明DNP时多元醇旁路被激活,醛糖还原酶(Aldose reductase,AR)活性增加,神经内山梨醇积聚,而与此时神经内微循环也发生障碍,动静脉短路,神经营养血管狭窄闭锁,从而使神经内血流量减低,神经缺血、缺氧〔4,5〕。提示代谢与血管因素之间有一种内在的联系。有人认为NO即是连接代谢因素与血管因素之间的桥梁〔6〕,因为NOS和AR的活性都取决于NADPH,由于高血糖激活了多元醇旁路使AR活性增加,于是NADPH被竞争性消耗,NOS活性则被抑制,NO产生下降,从而使血管舒张障碍、张力增加,造成缺血。在我们的观察中发现,糖尿病时的大脑皮层NOS阳性神经元确有减少,并发现了缺血性病理改变,但有趣的是在一般认为无NOS神经元的海马区〔7〕,却发现了散在的NOS阳性神经元。此现象的病理生理学意义有待进一步探讨。
参考文献
[1]MarlettamA.Nitric oxidesynthasestructure andmechanism.J Biol Chem,1993,268∶12231
, 百拇医药
[2]Way KJ,Reid JJ.Nitric oxide-mediated neurotransmission is attenuated in the aboccygeusmuscle fromdiabetic rats.Diabetologia,1994,37(3)∶232
[3]Dawson TM,BredtdS,Fotuhim et al.Nitric oxidesynthase and neuronal NADPHdiaphorase are identical in brain and peripheral tissues.Proc Natl Acadsci USA,1991,88∶7797
[4]Akgoren N,Fabriciusm,Lauritzenm.Importance of nitric oxide for local increases of blood flow in rat cerebella cortexduring electricalstimulation.Proc Natl Acadsci USA,1994,91∶5903
, 百拇医药
[5]Uccioli L,Monticoneg,Russo F et al.Autonomic neuropathy and transcutaneous oxymetry indiabetic lower extremities.Diabetology,1994,37(10)∶1051
[6]StevensmJ.Nitric oxide as a potential bridge between themetabolic and vascularhypotheses ofdiabetic neuropathy.Diabet-Med,1995,12(4)∶292
[7]Dinerman JL,Dawson TM,SchellmJ et al.Endothelial nitric oxidesynthase localized tohippocampal pyramidal cell: implication forsynaptic plaspicity.Proc Natl Acadsci USA,1994,91∶4214
(1998―08―06收稿,1998―09―15修回), 百拇医药
单位:贾军宏 马学毅:解放军304医院内分泌科,北京 100037;田东华 于国平:解放军总医院神经内科,北京 100853
关键词:糖尿病;一氧化氮合酶;中枢神经系统
糖尿病大鼠脑组织一氧化氮合酶表达的变化 摘要 目的:探讨一氧化氮在糖尿病神经病变发病机制中的作用。方法:采用硫辛氨脱氢酶(NADPH)酶组织化学染色法测定糖尿病大鼠脑组织一氧化氮合酶(NOS)表达的变化。结果:糖尿病成模后3个月,大脑皮层区NOS阳性神经元明显减少,但在海马区却发现NOS阳性细胞。结论:NOS的改变,可能参与糖尿病中枢神经系统病变的发病过程。
中国图书资料分类法分类号 R 587.1
The change of the nitric oxidesynthase expression
, http://www.100md.com
in brain ofdiabetic rats
Jia Junhong,Tiandonghua,Yuguoping,Ma Xueyi
(Department of Endocrinology,304thhospital of PLA,Beijing 100037)
Abstract Objective:To explore the effects of nitric oxide on themechanism ofdiabetic neuropathy.Methods:The changes of nitric oxidesynthase (NOS) expression in the brain ofdiabetic rats weremeasured by thehistochemiscal technique with nicotinamide adeninedinucleotide phosphate (NADPH-d).Results:After inducing themodel ofdiabetes for threemonths,the positive neurons of NOS in the brain contex were obviouslydecreased in thediabetesgroup than the normal controlgroup.While the positive neuron of NOS were found in thehippocampal area ofdiabetesgroup. Conclusion:The changes of NOS expressionmay be a factor in the impact ofdiabetes on the central nervoussystem.
, 百拇医药
Key words diabetes; NOS; CNS
一氧化氮(NO)是一种无机气体,具有多种生物活性〔1〕。在糖尿病神经病变病原学的研究中,NO及一氧化氮合酶(NOS)的作用引人注目,有人认为它是连接糖尿病神经系统病变代谢假说和血管假说之间的桥梁〔2〕。为此,采用组织化学方法我们观察了成模 3 个月的糖尿病大鼠脑组织一氧化氮合酶表达的变化。
1 材料和方法
1.1 大鼠糖尿病模型制备 雄性Wistar大鼠体重 170~230g,按体重随机分为两组:正常对照(NC)组;糖尿病(DM)组。
大鼠禁食 12h,DM组按 75mg/kg单剂腹腔注射枸橼酸缓冲液配制的链脲佐菌素(STZ,Sigma),NC组注射等体积枸橼酸缓冲液。注射 3d后用血糖仪(ONE TOUCH Ⅱ,强生公司)测大鼠尾静脉血糖,DM组>13mmol/L者入选。两组动物同等条件下饲养,自由摄食水。
, http://www.100md.com
1.2 观察指标
1.2.1 一般检查 包括体重、血糖、糖化血红蛋白。其中体重、血糖每月测定 1 次,糖化血红蛋白于实验结束时心脏取血用微柱法测定。
1.2.2 大脑一氧化氮合酶(NOS)表达的变化 大鼠喂养 3 个月后用 10% 水合氯醛(400mg/kg)腹腔注射麻醉,迅速剪开胸腔暴露心脏,经左心室插管至升主动脉,然后快速灌注肝素化生理盐水,同时剪开右心房,当灌注量达 100ml时,换液为 4% 多聚甲醛(0.1mol/LPB配制)500ml,灌注压约 9.8 kPa,灌注时间约 1h。用小咬骨钳仔细去除颅骨,完整取出大脑。脑组织浸于 20% 蔗糖溶液,4°C过夜。脑组织在Leica冰冻切片机上行连续冰冻切片,厚度为 50μm,切片入孵育液,孵育液包含 1mmol/L NADPH, 1mmol/L NBT,孵育时间为 30min。1%明胶贴片,常规脱水透明,DPX封片。Olympus BH-2 显微镜下观察。阴性对照染色:用PBS替换NADPH,余步骤同上。
, 百拇医药
2 结果
2.1 体重变化 实验前两组体重无明显差异,实验后DM组体重增长明显低于NC组,P<0.000 1,见表 1。
表 1 体重变化(
分组
n
实验前
1个月
2个月
3个月
, 百拇医药
NC
8
226.25±18.48
370.63±43.21
496.25±66.10
601.34±58.23
DM
9
222.44±47.20
296.66±51.72*
318.33±53.27*
, 百拇医药
285.55±69.63*
*表示与NC组比较,P<0.000 1
2.2 生化指标 见表 2。DM组血糖和糖化血红蛋白明显高于NC组,P<0.000 1。
表 2 血糖、糖化血红蛋白比较(
分组
n
血糖(mmol/L)
GHb(%)
, 百拇医药
成模时
2个月
3个月
NC
8
4.02±0.56
3.79±1.02
3.69±0.47
6.98±1.39
DM
9
16.73±3.43*
, 百拇医药
19.49±4.66*
17.79±3.37*
12.06±1.77*
*表示与NC组比较,P<0.0001
2.3 脑组织NOS的变化 NADPH-d组织化学染色可清晰显示脑组织中含NOS神经元,NOS阳性神经元散在分布于各脑区在大脑皮层,DM组皮层中NOS阳性神经元较NC组明显减少,但在正常大鼠的海马区NADPH-d染色未发现NOS阳性神经元,糖尿病大鼠的海马区却发现有散在的NOS阳性细胞。
3 讨论
NO是由L-精氨酸在NOS的作用下产生的,由于半衰期很短,仅 4~5s,难以测定,所以一般多以NOS的活性表示NO的多少。已证实,当组织在用福尔马林固定情况下,NADPH还原酶(NADPH-d)组织化学染色可准确显示含NOS的细胞或组织,并可准确反映NOS的活性〔3〕。本实验用此方法显示的大鼠脑组织NOS阳性神经元呈深蓝色,其胞体和树突清晰可见。
, 百拇医药
已有很多实验证明DNP时多元醇旁路被激活,醛糖还原酶(Aldose reductase,AR)活性增加,神经内山梨醇积聚,而与此时神经内微循环也发生障碍,动静脉短路,神经营养血管狭窄闭锁,从而使神经内血流量减低,神经缺血、缺氧〔4,5〕。提示代谢与血管因素之间有一种内在的联系。有人认为NO即是连接代谢因素与血管因素之间的桥梁〔6〕,因为NOS和AR的活性都取决于NADPH,由于高血糖激活了多元醇旁路使AR活性增加,于是NADPH被竞争性消耗,NOS活性则被抑制,NO产生下降,从而使血管舒张障碍、张力增加,造成缺血。在我们的观察中发现,糖尿病时的大脑皮层NOS阳性神经元确有减少,并发现了缺血性病理改变,但有趣的是在一般认为无NOS神经元的海马区〔7〕,却发现了散在的NOS阳性神经元。此现象的病理生理学意义有待进一步探讨。
参考文献
[1]MarlettamA.Nitric oxidesynthasestructure andmechanism.J Biol Chem,1993,268∶12231
, 百拇医药
[2]Way KJ,Reid JJ.Nitric oxide-mediated neurotransmission is attenuated in the aboccygeusmuscle fromdiabetic rats.Diabetologia,1994,37(3)∶232
[3]Dawson TM,BredtdS,Fotuhim et al.Nitric oxidesynthase and neuronal NADPHdiaphorase are identical in brain and peripheral tissues.Proc Natl Acadsci USA,1991,88∶7797
[4]Akgoren N,Fabriciusm,Lauritzenm.Importance of nitric oxide for local increases of blood flow in rat cerebella cortexduring electricalstimulation.Proc Natl Acadsci USA,1994,91∶5903
, 百拇医药
[5]Uccioli L,Monticoneg,Russo F et al.Autonomic neuropathy and transcutaneous oxymetry indiabetic lower extremities.Diabetology,1994,37(10)∶1051
[6]StevensmJ.Nitric oxide as a potential bridge between themetabolic and vascularhypotheses ofdiabetic neuropathy.Diabet-Med,1995,12(4)∶292
[7]Dinerman JL,Dawson TM,SchellmJ et al.Endothelial nitric oxidesynthase localized tohippocampal pyramidal cell: implication forsynaptic plaspicity.Proc Natl Acadsci USA,1994,91∶4214
(1998―08―06收稿,1998―09―15修回), 百拇医药