喜树碱及其衍生物的比较分子力场分析(CoMFA)研究*
作者:朱 杰 张万年 季海涛 周有骏 朱 驹 吕加国
单位:第二军医大学药学院,上海 200433
关键词:喜树碱;三维定量构效关系;比较分子力场分析法;偏最小二乘法
摘 要 采用最小二乘匹配和场匹配两种不同叠合规则
摘 要 采用最小二乘匹配和场匹配两种不同叠合规则,以sp3C+,sp3O0.4-和sp3O2-3种不同探针对喜树碱类化合物进行了比较分子力场分析法(CoMFA)研究,并对CoMFA中降低静电势的选项及偏最小二乘法(PLS)分析中的比例调整方法选项的设置进行了比较.对所得较佳模型进行网格空间的系统平移获得了有更强预测能力的三维定量构效关系(3D-QSAR)模型,并成功地对检验组化合物作了活性预测.通过对模型的势场图分析,获得了该类化合物与受体相互作用的大量信息,为指导新的高活性化合物的设计提供了理论依据.
, 百拇医药
Comparative Moleculer Field Analysis(CoMFA)
of Camptothecin Analogs
Zhu Jie,Zhang Wannian,Ji Haitao,Zhou Youjun,Zhu Jü,Lü Jiaguo
(School of Pharmacy,Second Military Medical University,Shanghai 200433)
Abstract Comparative molecular field analysis(CoMFA)using three different probes has been used to establish 3D-QSAR models of camptothecin analogs which were aligned by two different alignment rules:rms Fit and Field Fit.And the settings of Drop Electrostatics in CoMFA option and the Scaling method in PLS option were studied too.To the resultant good models,the Region′s systemic moving was enforced and the best models were obtained and their powerful predictive abilities were proved by predicting ten camptothecin analogs in the test set.By analyzing the contour plots of CoMFA models,a lot of information about the interaction between the CPT and receptor was obtained,which would be in favour of designing the novel high potent analogs.
, 百拇医药
Key words camptothecin;3D-QSAR;CoMFA;PLS
喜树碱(camptothecin/CPT)是从珙王 同科植物喜树中分离得到的一种生物碱〔1〕.由于其对肝癌、胃癌、膀胱癌及白血病等有着较好的近期疗效〔2〕而引起了研究人员的广泛重视,近年来不断有新的喜树碱类药物上市或进入临床研究〔3〕.对该类药物的酶学及药效学研究表明:(S)-CPT是拓朴异构酶Ⅰ(ToPo Ⅰ)的专属性抑制剂〔4〕,它通过与ToPo Ⅰ-DNA的可裂解复合物可逆结合形成三元复合物而抑制了DNA的解旋,导致DNA磷酸二酯键的断裂,产生细胞毒作用〔5〕.但该类药物具水溶性差和临床应用副作用较严重〔6〕的缺点,为了进一步提高药效、降低毒性,有必要对该类药物的抑酶作用机理作进一步深入研究,实验采用比较分子力场分析(CoMFA)方法研究了该类化合物在三维空间中静电相互作用、范德华力等非共价键与生物活性的关系,建立了具较强预测能力的3D-QSAR模型,并用检验组化合物成功进行了模型预测能力的验证,为今后的合理药物设计提供了依据.
, 百拇医药
1 材料与方法
1.1 化合物及活性数据的选择
从文献〔7~9〕中选取43个7,9,10,11位取代的喜树碱衍生物〔见表1,其中(1)~(33)为训练组化合物,其余为检验组化合物〕.所有化合物均以抑制ToPo Ⅰ-DNA可裂解复合物形成的IC50值(μmol/L)表示活性,并以喜树碱为共同对照品,数据间有可比性.采用其IC50的负对数值(pIC50)作为活性数据.化合物选取遵循以下原则:尽量使各取代基的电性、立体因素均匀分布;最高活性与最低活性化合物间的IC50值需相差100倍以上;化合物的立体构型相同,均为S型;排除以钠盐形式和以前药原理设计的化合物.
Tab.1 Compounds studied in training and test sets
, 百拇医药
No.
X
R1
R2
R3
R4
ref.
No.
X
R1
R2
R3
, 百拇医药
R4
ref.
1
C
H
H
H
H
7
18
N
Et
H
C≡CCH2NMe2
, 百拇医药
9
2
C
H
F
H
H
7
19
N
H
H
H
9
, 百拇医药
3
C
H
H
CH3
H
7
20
N
Me
H
CH2NH2
O
, 百拇医药
4
C
H
H
F
H
7
21
C
H
Cl
OCH2O
7
5
, http://www.100md.com
C
H
H
NO2
H
7
22
C
H
Cl
Cl
H
7
6
, 百拇医药
C
H
OH
H
H
7
23
C
H
H
NH2
H
7
7
, 百拇医药
C
H
H
CO2H
H
7
24
N
Et
H
Br
9
8
C
, 百拇医药
H
OCH2O
8
25
N
Et
H
C≡CCH2NH2
9
9
C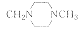
, 百拇医药
H
OCH2CH2O
8
26
C
H
NH2
OCH2O
7
10
C
CH2Cl
, http://www.100md.com
H
OCH2O
8
27
N
Me
H
BocNHCH2
O
9
11
C
CH2Cl
, 百拇医药
H
OCH2CH2O
8
28
C
H
H
Br
H
7
12
C
H
, 百拇医药
H
OCH2O
7
29
C
H
H
Cl
H
7
13
N
Et
, http://www.100md.com H
H
9
30
C
H
CH2NMe2
OH
H
7
14
N
Et
, 百拇医药
H
CN
9
31
C
H
CH3
H
H
7
15
N
CH3
, 百拇医药
H
CH2NH2
9
32
C
H
Cl
H
H
7
16
N
Et
, 百拇医药
H
C(NH2)NOH
9
33
C
H
NH2
H
H
7
17
N
Et
, http://www.100md.com
H
C(NH2)NH
9
34
C
H
H
OH
H
7
39
N
Et
, http://www.100md.com H
(CH2)4NMe2
9
35
N
Me
H
CN
9
40
N
H
H
, http://www.100md.com
H
O
9
36
N
Et
H
CH2NH2
9
41
N
Me
H
, http://www.100md.com
C≡CCH2NH2
9
37
N
Et
H
CO2Et
9
42
C
H
NO2
, 百拇医药
OCH2O
7
38
N
Me
H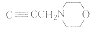
9
43
C
H
H
, 百拇医药
CN
H
7
1.2 分子构建及优化
分子的构建采用SYBYL 6.2软件包〔10〕在SGI Indigo2 R4400图形工作站上完成.采用分子力学方法进行优化:在Tripos标准力场下先用Simplex方法初始优化,再用Powell方法进行分子结构完全优化,选用Gasterger-H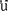 ckle电荷、距离依赖性介电常数,优化收敛标准为0.021 kJ/mol.
ckle电荷、距离依赖性介电常数,优化收敛标准为0.021 kJ/mol.
1.3 构象搜寻与分析
, 百拇医药
为搜寻确证喜树碱类化合物的药效构象,首先选择基本母环化合物(1),(19)以及高活性化合物(11)和上市药物(30),以随机构象搜寻(random search)得到的低能构象进行分子力学和分子动力学反复操作(分子动力学采用模拟退火方法:高温模拟温度为1000K,平台处理时间1 000 fs;退火到250 K,时间1500 fs),得到各化合物的最低能量构象.以此构建的其他化合物也采用上述高温分子动力学模拟退火条件进行构象分析.研究中发现喜树碱类化合物低能构象的基本母核的骨架原子空间取向相同,且都具A,B两种不同构型:A构型的E环羰基与20位羟基处在分子平面的同侧,而B构型的羰基则与乙基同侧,见图1.经分子力学计算B构型的能量较A构型低2.1~6.3 kJ/mol〔化合物(40)例外,其A构型能量较B构型低〕,但另一喜树碱类药物(irinotecan)的晶体结构〔11〕却与A构型相似.药效构象的确定对CoMFA研究至关重要.对药效构象的确定人们通常倾向于考察其晶体结构,但由于在形成晶体时存在着敛集效应故而得到的晶体构象不一定就是完全最低能量构象.此外当药物存在着数个能量相近的低能构象时,其也未必就以完全最低能量构象与受体结合,而极可能转变成能量稍高的局部低能构象与受体结合.基于上述原因,分别选取了各化合物A,B两种构型的最低能量构象,对上述两种构型都进行了CoMFA研究.

, http://www.100md.com
Fig.1 Two different conformations of CPT
1.4 分子叠合
叠合规则的选择是CoMFA研究能否成功的另一关键性问题.本实验采用了最小二乘匹配(rms Fit)和场匹配(Field Fit)两种不同的叠合方式分别对喜树碱衍生物进行了叠合研究.两种匹配规则都以活性最高的化合物(11)作为模板分子.rms Fit时考虑到喜树碱类化合物的刚性结构,且SAR研究表明母核的多环共轭同平面结构为活性必需单元〔12〕,故将喜树碱分子中的所有骨架原子都作为叠合点;Field Fit时则依据其原理〔13〕,将各化合物的立体场、静电场与模板化合物的分子力场进行匹配.为比较两种匹配规则对该类化合物CoMFA结果的影响,化合物均采用完全相同的构象.
1.5 CoMFA能量计算与PLS分析
, http://www.100md.com
选择sp3C+,sp3O0.4-和sp3O2-3种探针对叠合分子外周网格点上的静电场能及立体场能的大小和分布进行了探测,步长2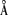 ,静电能和立体能阈值均设为126 kJ/mol.PLS分析时首先用leave-one-out方法进行交叉验证,最小行过滤值(σmin)设为8.4 kJ/mol;再以获得的最优组分数(ONC)进行非交叉验证以建立模型.实验中还对CoMFA中的drop electrostatics及PLS分析中的scaling method选项的设置进行了研究.
,静电能和立体能阈值均设为126 kJ/mol.PLS分析时首先用leave-one-out方法进行交叉验证,最小行过滤值(σmin)设为8.4 kJ/mol;再以获得的最优组分数(ONC)进行非交叉验证以建立模型.实验中还对CoMFA中的drop electrostatics及PLS分析中的scaling method选项的设置进行了研究.
1.6 Region的系统平移研究
由CoMFA原理知其正是通过Region内大量的网格点来描述化合物的分子力场从而关联活性并拟合方程的.但是其Region的生成具有一定的随机性,网格点位置的变化会因改变了对分子力场的模拟而影响CoMFA结果〔14〕.为得到最佳模型,对A,B两种构型所得的较佳模型进行了Region的系统平移研究:在一步长(2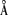 )范围内以0.1个步长为单位分别沿X,Y,Z轴对Region进行了1 000次平移.以得到的最佳模型(高Q2值)对检验组的10个化合物进行活性预测,并将预测活性与文献给出的活性进行比较,得出R2pred值〔15〕.R2pred=1-PRESS/SD〔PRESS=∑(Ypred-Yactual)2,SD=∑(Yactual-Ymean)2〕.其中Ypred为检验组化合物预测活性,Yactual为检验组化合物实际活性,Ymean为训练组化合物的平均活性.
)范围内以0.1个步长为单位分别沿X,Y,Z轴对Region进行了1 000次平移.以得到的最佳模型(高Q2值)对检验组的10个化合物进行活性预测,并将预测活性与文献给出的活性进行比较,得出R2pred值〔15〕.R2pred=1-PRESS/SD〔PRESS=∑(Ypred-Yactual)2,SD=∑(Yactual-Ymean)2〕.其中Ypred为检验组化合物预测活性,Yactual为检验组化合物实际活性,Ymean为训练组化合物的平均活性.
, 百拇医药
2 结果与讨论
2.1 最佳CoMFA模型的确定
首先用sp3C+探针对以rms Fit方式叠合的33个训练组化合物进行了CoMFA研究,A,B两种构型的Q2(ONC)值不高,分别为0.586和0.565.经残差分析发现,化合物(31~33)在模型中具有相当大的残差,明显区别于其他化合物.为获得理想的有较好统计值的模型,将上述3个化合物从训练组中删除,CoMFA方程的相关性有大幅提高,Q2值分别达到0.757和0.745(见表2,表3中的A2,B2模型).为进一步考察CoMFA方法中一些可调因素对模型的影响,又采用了三种探针、两种匹配规则对剩下的30个训练组化合物(1~30)进行了CoMFA模型的比较研究(表2,表3).以三种探针对不同叠合规则的比较研究均发现,rms Fit所得模型比Field Fit有着更高的Q2值和更低的PRESS值,说明按rms Fit方式更适合喜树碱这类刚性结构的化合物.PLS分析中Scaling方法的默认选项为CoMFASTD,其目的是使立体场和静电场有着近似相等的权重,以改变最终模型中静电场的相对贡献值太低的情况.多数情况下CoMFASTD可较No Scaling获得更好的结果.但是针对rms Fit模型对Scaling方法作进一步研究时发现:当对B构型以sp3O0.4-和sp3O2-探针进行模拟时,No Scaling可获得更好的模型.可见对Scaling方法的最佳选择还须视具体情况而定.鉴于所得各模型的静电相对贡献值较低,取消了Dropelec的限制,以增加那些因立体相互作用能超过阈值而被排除的网格点上的静电能.结果发现各模型的静电相对贡献值有所增加的同时,Q2值却在降低,模型预测能力下降.综观上述实验结果,发现rms Fit+sp3C+探针+CoMFASTD Scaling+Dropelec可获得较好的CoMFA模型,并且A,B两种构型所得的CoMFA模型结果相当,推其原因在于喜树碱为平面刚性结构,E环部分的空间取向对骨架结构影响不大,且所研究化合物均为A,B环取代,不反映E环信息.
, http://www.100md.com
Tab.2 Different settings and results of the CoMFA run with the A-type conformation of CPT
CoFMA
model
Fit
method
Probe
type
Atom
charge
Scaling
method
, 百拇医药
Drop
elec
Q2①
ONC②
PRESS③
Steric.
Contrib.
Elec.
Contrib.
R2
SEE④
, 百拇医药
F
A1
Field
C sp3
+1.0
CoSTD
YES
0.651
4
0.476
0.820
0.180
, 百拇医药 0.869
0.215
41.495
A2
rms
C sp3
+1.0
CoSTD
YES
0.757
5
0.452
0.833
, 百拇医药
0.167
0.921
0.171
55.636
A3
rms
C sp3
+1.0
NONE
YES
0.755
5
, 百拇医药 0.446
0.851
0.149
0.920
0.172
55.195
A4
rms
C sp3
+1.0
CoSTD
NO
, 百拇医药 0.717
5
0.468
0.750
0.250
0.928
0.163
61.728
A5
rms
C sp3
+1.0
, 百拇医药 NONE
NO
0.664
5
0.513
0.603
0.397
0.921
0.171
55.868
A6
Field
O sp3
, 百拇医药
-0.4
CoSTD
YES
0.651
3
0.501
0.839
0.161
0.845
0.230
47.177
A7
rms
, 百拇医药
O sp3
-0.4
CoSTD
YES
0.753
6
0.455
0.841
0.159
0.933
0.161
53.138
A8
, 百拇医药
rms
O sp3
-0.4
NONE
YES
0.722
4
0.436
0.959
0.041
0.882
0.205
46.541
, 百拇医药
A9
rms
O sp3
-0.4
CoSTD
NO
0.658
4
0.487
0.761
0.239
0.881
, 百拇医药 0.206
46.124
A10
rms
O sp3
-0.4
NONE
NO
0.655
4
0.493
0.753
0.247
, 百拇医药
0.874
0.212
43.192
A11
Field
O sp3
-2.0
CoSTD
YES
0.655
4
0.490
, 百拇医药
0.797
0.203
0.877
0.209
44.385
A12
rms
O sp3
-2.0
CoSTD
YES
0.739
, 百拇医药
5
0.455
0.811
0.189
0.910
0.182
48.531
A13
rms
O sp3
-2.0
NONE
, 百拇医药
YES
0.714
5
0.503
0.699
0.301
0.911
0.181
49.328
A14
rms
O sp3
, 百拇医药
-2.0
CoSTD
NO
0.681
4
0.469
0.758
0.242
0.901
0.187
57.011
A15
rms
, http://www.100md.com
O sp3
-2.0
NONE
NO
0.579
5
0.537
0.459
0.541
0.915
0.177
51.594
①Maximum cross-validated r2,②Optional number of components,③Predictive sum of squares of cross-validated predictions,④Standard error of estimateTab.3 Different settings and results of the CoMFA run with the B-type conformation of CPT
, 百拇医药
CoMFA
model
Fit
method
Probe
type
Atom
charge
Scaling
method
Drop
elec
Q2①
, 百拇医药
ONC②
PRESS③
Steric.
Contrib.
Elec.
Contrib.
R2
SEE④
F
B1
Field
, 百拇医药 C sp3
+1.0
CoSTD
YES
0.648
5
0.443
0.830
0.170
0.909
0.183
47.877
B2
, 百拇医药
rms
C sp3
+1.0
CoSTD
YES
0.745
5
0.426
0.931
0.069
0.895
0.197
40.871
, http://www.100md.com
B3
rms
C sp3
+1.0
NONE
YES
0.754
5
0.418
0.944
0.056
0.895
, 百拇医药 0.197
40.778
B4
rms
C sp3
+1.0
CoSTD
NO
0.712
5
0.421
0.735
0.265
, 百拇医药
0.917
0.175
52.781
B5
rms
C sp3
+1.0
NONE
NO
0.640
5
0.455
, http://www.100md.com 0.572
0.428
0.917
0.175
53.193
B6
Field
O sp3
-0.4
CoSTD
YES
0.647
, 百拇医药 4
0.470
0.737
0.263
0.868
0.216
41.143
B7
rms
O sp3
-0.4
CoSTD
, 百拇医药 YES
0.742
5
0.442
0.923
0.077
0.898
0.194
42.403
B8
rms
O sp3
-0.4
, 百拇医药
NONE
YES
0.761
5
0.415
0.981
0.019
0.907
0.185
47.024
B9
rms
O sp3
, http://www.100md.com
-0.4
CoSTD
NO
0.698
4
0.430
0.733
0.267
0.899
0.189
55.573
B10
rms
, http://www.100md.com
O sp3
-0.4
NONE
NO
0.698
5
0.429
0.753
0.247
0.909
0.183
47.953
B11
, http://www.100md.com
Field
O sp3
-2.0
CoSTD
YES
0.617
4
0.468
0.775
0.225
0.869
0.215
41.526
, http://www.100md.com
B12
rms
O sp3
-2.0
CoSTD
YES
0.725
5
0.448
0.868
0.132
0.902
, 百拇医药 0.190
44.369
B13
rms
O sp3
-2.0
NONE
YES
0.683
5
0.497
0.724
0.276
, 百拇医药
0.908
0.184
47.622
B14
rms
O sp3
-2.0
CoSTD
NO
0.694
5
0.434
, 百拇医药 0.734
0.266
0.914
0.178
51.145
B15
rms
O sp3
-2.0
NONE
NO
0.562
, http://www.100md.com 4
0.488
0.386
0.614
0.907
0.181
61.132
①Maximum cross-validated r2,②Optional number of components,③Predictive sum of squares of cross-validated predictions,④Standard error of estimate
为寻找最佳模型,对有较好预测能力的A2和B2模型进行了Region的系统平移研究,发现网格点的平移可对结果产生极大影响:A2模型平移所得的最差结果Q2值仅为0.305,最优模型Amax的Q2则达0.832;而B2模型平移所得的最差结果Q2等于0.414,最优模型Bmax的Q2值为0.845.以所得最优模型Amax和Bmax对检验组10个化合物进行活性预测,预测残差值均小于1个对数单位,R2pred值分别为0.716和0.685,亦充分说明了模型具有较高的预测能力.对部分预测偏差较大的化合物进行分析,发现预测组化合物的结构超出模型范围可能是导致预测偏差的一个原因.如(38,39)两化合物,10位均被大基团取代,其结构伸展已超出训练组各化合物所占有的空间.而(40)可能因11位氮上引入氧的缘故,构象分析时就发现其有别于其他化合物:B构型能量较A构型高,而Bmax模型对其预测的残差明显高于Amax,很可能与该化合物B构型的较高能量有关.
, http://www.100md.com
Tab.4 PLS analysis results of model Amax and model Bmax
Model
Base
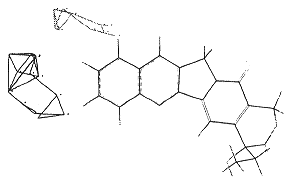
Region moving/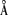
Q2
ONC
PRESS
SDEP
, 百拇医药 R2
F
SEE
Pvalue
Elect.
contrib.
Steric.
contrib.
R2pred
X
Y
Z
, http://www.100md.com
Amax
A2
1.8
0.0
0.2
0.832
6
0.440
0.121
0.950
73.203
0.138
, 百拇医药 0.000
0.224
0.776
0.806
Bmax
B2
0.6
0.0
0.2
0.845
6
0.403
0.116
, 百拇医药
0.960
92.350
0.124
0.000
0.163
0.837
0.715
Tab.5 The Comparision of predicted activity and actual activity
No.
PIC
actual
, 百拇医药
PIC
Amax
Residue
Amax
PIC
Bmax
Residue
Bmax
No.
PIC
actual
PIC
, 百拇医药
Amax
Residue
Amax
PIC
Bmax
Residue
Bmax
No.
PIC
actual
PIC
Amax
, 百拇医药
Residue
Amax
PIC
Bmax
Residue
Bmax
1
0.167
0.445
0.278
0.396
0.229
, 百拇医药
11
1.959
1.978
0.019
1.922
-0.037
21
1.215
1.360
0.145
1.226
0.011
2
, 百拇医药
0.796
0.524
-0.272
0.459
-0.337
12
1.569
1.532
-0.037
1.585
0.016
22
0.959
, 百拇医药
0.694
-0.265
1.107
0.148
3
0.523
0.635
0.112
0.558
0.035
13
0.474
0.481
, 百拇医药
0.007
0.497
0.023
23
0.854
0.837
-0.017
0.860
0.006
4
0.432
0.482
0.050
, 百拇医药
0.440
0.008
14
0.572
0.673
0.101
0.769
0.197
24
0.914
0.923
0.009
0.861
, 百拇医药
-0.053
5
0.194
0.439
0.245
0.360
0.166
15
0.634
0.652
0.018
0.654
0.020
, 百拇医药
25
-0.031
-0.022
0.009
-0.139
-0.108
6
0.060
0.135
0.075
0.129
0.069
16
, 百拇医药
1.149
0.961
-0.188
1.075
-0.074
26
1.319
1.234
-0.085
1.230
-0.089
7
0.000
, 百拇医药
-0.040
-0.040
0.033
0.033
17
1.481
1.386
-0.095
1.433
-0.048
27
0.664
0.655
, 百拇医药
-0.009
0.624
-0.040
8
0.523
0.415
-0.108
0.491
-0.032
18
-0.124
-0.102
-0.022
, 百拇医药
-0.091
0.033
28
0.886
0.912
0.026
0.741
-0.145
9
0.381
0.459
0.078
0.432
, 百拇医药
0.051
19
0.417
0.252
-0.165
0.333
-0.084
29
0.854
0.842
-0.012
0.729
-0.125
, http://www.100md.com
10
1.824
1.927
0.103
1.908
0.084
20
0.721
0.719
-0.002
0.767
0.046
30
, 百拇医药
0.000
-0.041
-0.041
-0.045
-0.045
34
0.959
0.769
-0.190
0.774
-0.185
38
-0.046
, 百拇医药
-0.189
-0.143
0.266
0.312
42
0.824
1.316
0.492
1.207
0.383
35
0.845
0.897
, 百拇医药
0.052
0.810
-0.035
39
-0.174
0.392
0.566
0.308
0.482
343
-0.279
0.254
0.533
, 百拇医药
0.217
0.496
36
0.777
0.819
0.042
0.822
0.045
40
-0.073
0.175
0.248
0.474
, http://www.100md.com
0.547
37
0.023
-0.211
-0.234
0.314
0.291
41
0.297
0.138
-0.159
0.436
0.139
, 百拇医药
2.2 立体能和静电能的分布
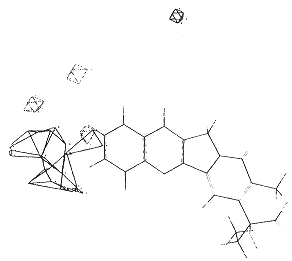
由CoMFA模型的立体、静电相对贡献值可看出,该类化合物立体因素对活性影响较静电因素更为重要.图2和图3是以喜树碱为例所显示的Amax和Bmax模型的CoMFA势场轮廓图,可以看出A,B两种构型所得模型基本一致.SAR研究一般认为9位和7位处在药物与受体结合的外部,故设计新化合物时通常用较大基团取代以作为增加药物水溶性的手段;而11位却被认为是紧靠与酶紧密接触的12位,取代时会因立体禁阻而效果不好.但是从CoMFA研究所得的势场图来看,立体取代不利区对7,9,10位成一环状包围,而11位及与10位接近的区域恰有一立体取代有利区,这正为10,11位成环化合物的高活性提供了理论依据,而且也可对训练组化合物(18),(25)与(27)同是10位大基团取代,但活性却较(27)低很多的现象进行合理的解释:通过构象分析发现(18)和(25)的10位因炔基的缘故使得基团在空间直线伸展,与立体禁阻区相接触从而导致低活性,而(27)却可通过键的旋转使得支链避开立体禁阻区因而保持了较好的活性.由此可以推测11位及10位作适当取代(10位取代基团可通过键的旋转或与11位成环而处在近11位空间),可以恰好进入受体表面的空腔中与其发生相互作用.而且从图中可以看出该处区域为正电有利区,推测受体在该位置存在亲核基团.对7位的研究发现在其与9位相近的位置也有立体禁阻区,而Bmax模型则清楚地显示在该立体不利区旁有一小块正电有利区,推测受体可能在该处尚存在一辅助结合位点.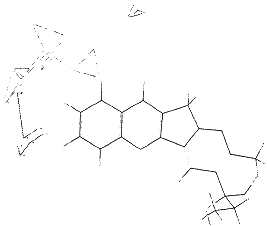
, 百拇医药
(a)Steric field
black:sterically favored area
gray:sterically disfavored area
(b)Electric field
black:positive charge favored area
gray:negative charge favored area
Fig.2 Stereoview of CoMFA contour plots of Amax model
, http://www.100md.com
(a)Steric field
black:sterically favored area
gray:sterically disfavored area
(b)Electric field
black:positive charge favored area
gray:negative charge favored area
Fig.3 Stereoview of CoMFA contour plots of Bmax model
3 结论
, 百拇医药
本实验通过构象分析,发现喜树碱类化合物因其E环部分的羰基取向不同而具有A,B两种构型.通过对33个训练组化合物进行CoMFA研究,以其中的30个化合物建立了较佳的模型,并在此基础上对CoMFA建模条件进行了选择研究,结果发现A,B两种构型有着相近的结果:rms Fit方式更适合于喜树碱这类刚性结构,而以sp3C+探针、CoMFASTD加上Dropelec可得到较好的结果.对所得较佳模型进行了Region的系统平移研究,得到了两种构型的最佳CoMFA模型,并对10个检验组化合物进行了预测,结合充分证明了该模型有着很强的预测能力.通过对所得模型的CoMFA势场图的分析,推翻了以往SAR研究的一些错误结果,并发现了喜树碱类化合物11位(或10位)的正电取代基团可进入受体表面的空腔中,与其中的亲核基团作用,而且喜树碱7位取代亦存在着与受体辅助结合位点相作用的可能.这些结论深化了对喜树碱类化合物与酶-DNA相互作用方式的理解,为今后对其进行合理的结构修饰与改造提供了有利的依据.
*973国家重点基础研究资助项目No.G1998051104
, 百拇医药
作者简介:张万年 通讯联系人
参考文献
1 Wall ME,Wani MC,Cook CE,et al.Plant antitumor agents I.The isolation and structure of camptothecin,a novel alkaloidal and tumor inhibition from camptotheca acuminata.J Am Chem Soc,1966,88(16):3888~3890
2 Slichenmyer WJ,von Hoff DD.New natural products in cancer chemotherapy.J Clin Pharmacol,1990,30(9):770~788
3 Potmesil M.Camptothecins:From bench research to hopsital wards.Cancer Res.1994,54:1431~1439
, 百拇医药
4 Hsiang YH,Hertzberg R,Hecht S,et al.Camptothecin induces protein linked breaks via mammalian DNA topoisomerase I.J Biol Chem,1985,260:14873~14878
5 Hertzberg RP,Caranfa MJ,Hecht S,et al.On the mechanism of topoisomerase I inhibition by camptothecin:Evidence for binding to an enzyme-DNA complex.Biochemistry,1989,28:4629~4638
6 Giovanella BC,Stehlin JS,Wall ME,et al.DNA topoisomerase I-targeted chemotherapy of human colon cancer in sxenografts.Science,1989,246:1046~1048
, http://www.100md.com
7 Wall ME,Wani MC,Nicholas AW,et al.Plant antitumor agents.30.Synthesis,topoisomerase I inhibitory activity,and in vivo evalution of 11-azcamptothecin analyogs.J Med Chem,1995,38:1106~1118
8 Luzzio MJ,Besterman JM,Emerson DL,et al.Synthesis and antitumor activity of noval water soluble derivatives of camptothecin as inhibitors of topoisomerase I.J Med Chem,1995,38:395~401
9 Uehling DE,Nanthakumar SS,Croom D,et al.Synthesis,topoisomerase I inhibitory activity,and in vivo evalution of 11-aza camptothecin analogs.J Med Chem,1995,38:1106~1118
, http://www.100md.com
10 SYBYL,V.6.2,Tripos associates,St Louis,MO,USA
11 Sawada S,Okajima S,Aiyama R,et al.Synthesis and antitumor activity of 20(S)-campotothecin derivatives:carbamate-linked,water-soluble derivatives of 7-ethyl-10-hydroxycampgtothecin.Chem Pharm Bull,1991,39(6):1446~1454
12 Wani MC,Ronman PE,Lindley JT,et al.Plant antitumor agents.18.Synthesis and biological activity of camptothecin analogues.J Med Chem,1980,23:554~560
, http://www.100md.com
13 Cramer Ⅲ RD,Patterson DE,Bunce JD.Comparative molecular field analysis(CoMFA)1.Effect of shape on binding of steroids to carrier proteins.J Am Chem Soc,1988,110:5959~5967
14 朱杰,张万年,周有骏,等.CoMFA网格点的生成及选取对结果影响的研究.中国药学杂志,1999,34(6):417~420
15 DePriest SA,Mayer D,Naylor CB,et al.3D-QSAR of angiotensin-converting enzyme and thermolysin inhibitors:a comparison of CoMFA models based on deduced and experimeentally determined active site geometries.J Am Chem Soc,1993,115:5372~5384
收稿日期:1999-04-30, http://www.100md.com
单位:第二军医大学药学院,上海 200433
关键词:喜树碱;三维定量构效关系;比较分子力场分析法;偏最小二乘法
摘 要 采用最小二乘匹配和场匹配两种不同叠合规则
摘 要 采用最小二乘匹配和场匹配两种不同叠合规则,以sp3C+,sp3O0.4-和sp3O2-3种不同探针对喜树碱类化合物进行了比较分子力场分析法(CoMFA)研究,并对CoMFA中降低静电势的选项及偏最小二乘法(PLS)分析中的比例调整方法选项的设置进行了比较.对所得较佳模型进行网格空间的系统平移获得了有更强预测能力的三维定量构效关系(3D-QSAR)模型,并成功地对检验组化合物作了活性预测.通过对模型的势场图分析,获得了该类化合物与受体相互作用的大量信息,为指导新的高活性化合物的设计提供了理论依据.
, 百拇医药
Comparative Moleculer Field Analysis(CoMFA)
of Camptothecin Analogs
Zhu Jie,Zhang Wannian,Ji Haitao,Zhou Youjun,Zhu Jü,Lü Jiaguo
(School of Pharmacy,Second Military Medical University,Shanghai 200433)
Abstract Comparative molecular field analysis(CoMFA)using three different probes has been used to establish 3D-QSAR models of camptothecin analogs which were aligned by two different alignment rules:rms Fit and Field Fit.And the settings of Drop Electrostatics in CoMFA option and the Scaling method in PLS option were studied too.To the resultant good models,the Region′s systemic moving was enforced and the best models were obtained and their powerful predictive abilities were proved by predicting ten camptothecin analogs in the test set.By analyzing the contour plots of CoMFA models,a lot of information about the interaction between the CPT and receptor was obtained,which would be in favour of designing the novel high potent analogs.
, 百拇医药
Key words camptothecin;3D-QSAR;CoMFA;PLS
喜树碱(camptothecin/CPT)是从珙王 同科植物喜树中分离得到的一种生物碱〔1〕.由于其对肝癌、胃癌、膀胱癌及白血病等有着较好的近期疗效〔2〕而引起了研究人员的广泛重视,近年来不断有新的喜树碱类药物上市或进入临床研究〔3〕.对该类药物的酶学及药效学研究表明:(S)-CPT是拓朴异构酶Ⅰ(ToPo Ⅰ)的专属性抑制剂〔4〕,它通过与ToPo Ⅰ-DNA的可裂解复合物可逆结合形成三元复合物而抑制了DNA的解旋,导致DNA磷酸二酯键的断裂,产生细胞毒作用〔5〕.但该类药物具水溶性差和临床应用副作用较严重〔6〕的缺点,为了进一步提高药效、降低毒性,有必要对该类药物的抑酶作用机理作进一步深入研究,实验采用比较分子力场分析(CoMFA)方法研究了该类化合物在三维空间中静电相互作用、范德华力等非共价键与生物活性的关系,建立了具较强预测能力的3D-QSAR模型,并用检验组化合物成功进行了模型预测能力的验证,为今后的合理药物设计提供了依据.
, 百拇医药
1 材料与方法
1.1 化合物及活性数据的选择
从文献〔7~9〕中选取43个7,9,10,11位取代的喜树碱衍生物〔见表1,其中(1)~(33)为训练组化合物,其余为检验组化合物〕.所有化合物均以抑制ToPo Ⅰ-DNA可裂解复合物形成的IC50值(μmol/L)表示活性,并以喜树碱为共同对照品,数据间有可比性.采用其IC50的负对数值(pIC50)作为活性数据.化合物选取遵循以下原则:尽量使各取代基的电性、立体因素均匀分布;最高活性与最低活性化合物间的IC50值需相差100倍以上;化合物的立体构型相同,均为S型;排除以钠盐形式和以前药原理设计的化合物.
Tab.1 Compounds studied in training and test sets

, 百拇医药
No.
X
R1
R2
R3
R4
ref.
No.
X
R1
R2
R3
, 百拇医药
R4
ref.
1
C
H
H
H
H
7
18
N
Et
H
C≡CCH2NMe2
, 百拇医药
9
2
C
H
F
H
H
7
19
N
H
H
H
9
, 百拇医药
3
C
H
H
CH3
H
7
20
N
Me
H
CH2NH2
O
, 百拇医药
4
C
H
H
F
H
7
21
C
H
Cl
OCH2O
7
5
, http://www.100md.com
C
H
H
NO2
H
7
22
C
H
Cl
Cl
H
7
6
, 百拇医药
C
H
OH
H
H
7
23
C
H
H
NH2
H
7
7
, 百拇医药
C
H
H
CO2H
H
7
24
N
Et
H
Br
9
8
C
, 百拇医药
H
OCH2O
8
25
N
Et
H
C≡CCH2NH2
9
9
C
, 百拇医药
H
OCH2CH2O
8
26
C
H
NH2
OCH2O
7
10
C
CH2Cl
, http://www.100md.com
H
OCH2O
8
27
N
Me
H
BocNHCH2
O
9
11
C
CH2Cl
, 百拇医药
H
OCH2CH2O
8
28
C
H
H
Br
H
7
12
C
H
, 百拇医药
H
OCH2O
7
29
C
H
H
Cl
H
7
13
N
Et
, http://www.100md.com H
H
9
30
C
H
CH2NMe2
OH
H
7
14
N
Et
, 百拇医药
H
CN
9
31
C
H
CH3
H
H
7
15
N
CH3
, 百拇医药
H
CH2NH2
9
32
C
H
Cl
H
H
7
16
N
Et
, 百拇医药
H
C(NH2)NOH
9
33
C
H
NH2
H
H
7
17
N
Et
, http://www.100md.com
H
C(NH2)NH
9
34
C
H
H
OH
H
7
39
N
Et
, http://www.100md.com H
(CH2)4NMe2
9
35
N
Me
H
CN
9
40
N
H
H
, http://www.100md.com
H
O
9
36
N
Et
H
CH2NH2
9
41
N
Me
H
, http://www.100md.com
C≡CCH2NH2
9
37
N
Et
H
CO2Et
9
42
C
H
NO2
, 百拇医药
OCH2O
7
38
N
Me
H
9
43
C
H
H
, 百拇医药
CN
H
7
1.2 分子构建及优化
分子的构建采用SYBYL 6.2软件包〔10〕在SGI Indigo2 R4400图形工作站上完成.采用分子力学方法进行优化:在Tripos标准力场下先用Simplex方法初始优化,再用Powell方法进行分子结构完全优化,选用Gasterger-H
1.3 构象搜寻与分析
, 百拇医药
为搜寻确证喜树碱类化合物的药效构象,首先选择基本母环化合物(1),(19)以及高活性化合物(11)和上市药物(30),以随机构象搜寻(random search)得到的低能构象进行分子力学和分子动力学反复操作(分子动力学采用模拟退火方法:高温模拟温度为1000K,平台处理时间1 000 fs;退火到250 K,时间1500 fs),得到各化合物的最低能量构象.以此构建的其他化合物也采用上述高温分子动力学模拟退火条件进行构象分析.研究中发现喜树碱类化合物低能构象的基本母核的骨架原子空间取向相同,且都具A,B两种不同构型:A构型的E环羰基与20位羟基处在分子平面的同侧,而B构型的羰基则与乙基同侧,见图1.经分子力学计算B构型的能量较A构型低2.1~6.3 kJ/mol〔化合物(40)例外,其A构型能量较B构型低〕,但另一喜树碱类药物(irinotecan)的晶体结构〔11〕却与A构型相似.药效构象的确定对CoMFA研究至关重要.对药效构象的确定人们通常倾向于考察其晶体结构,但由于在形成晶体时存在着敛集效应故而得到的晶体构象不一定就是完全最低能量构象.此外当药物存在着数个能量相近的低能构象时,其也未必就以完全最低能量构象与受体结合,而极可能转变成能量稍高的局部低能构象与受体结合.基于上述原因,分别选取了各化合物A,B两种构型的最低能量构象,对上述两种构型都进行了CoMFA研究.


, http://www.100md.com
Fig.1 Two different conformations of CPT
1.4 分子叠合
叠合规则的选择是CoMFA研究能否成功的另一关键性问题.本实验采用了最小二乘匹配(rms Fit)和场匹配(Field Fit)两种不同的叠合方式分别对喜树碱衍生物进行了叠合研究.两种匹配规则都以活性最高的化合物(11)作为模板分子.rms Fit时考虑到喜树碱类化合物的刚性结构,且SAR研究表明母核的多环共轭同平面结构为活性必需单元〔12〕,故将喜树碱分子中的所有骨架原子都作为叠合点;Field Fit时则依据其原理〔13〕,将各化合物的立体场、静电场与模板化合物的分子力场进行匹配.为比较两种匹配规则对该类化合物CoMFA结果的影响,化合物均采用完全相同的构象.
1.5 CoMFA能量计算与PLS分析
, http://www.100md.com
选择sp3C+,sp3O0.4-和sp3O2-3种探针对叠合分子外周网格点上的静电场能及立体场能的大小和分布进行了探测,步长2
1.6 Region的系统平移研究
由CoMFA原理知其正是通过Region内大量的网格点来描述化合物的分子力场从而关联活性并拟合方程的.但是其Region的生成具有一定的随机性,网格点位置的变化会因改变了对分子力场的模拟而影响CoMFA结果〔14〕.为得到最佳模型,对A,B两种构型所得的较佳模型进行了Region的系统平移研究:在一步长(2
, 百拇医药
2 结果与讨论
2.1 最佳CoMFA模型的确定
首先用sp3C+探针对以rms Fit方式叠合的33个训练组化合物进行了CoMFA研究,A,B两种构型的Q2(ONC)值不高,分别为0.586和0.565.经残差分析发现,化合物(31~33)在模型中具有相当大的残差,明显区别于其他化合物.为获得理想的有较好统计值的模型,将上述3个化合物从训练组中删除,CoMFA方程的相关性有大幅提高,Q2值分别达到0.757和0.745(见表2,表3中的A2,B2模型).为进一步考察CoMFA方法中一些可调因素对模型的影响,又采用了三种探针、两种匹配规则对剩下的30个训练组化合物(1~30)进行了CoMFA模型的比较研究(表2,表3).以三种探针对不同叠合规则的比较研究均发现,rms Fit所得模型比Field Fit有着更高的Q2值和更低的PRESS值,说明按rms Fit方式更适合喜树碱这类刚性结构的化合物.PLS分析中Scaling方法的默认选项为CoMFASTD,其目的是使立体场和静电场有着近似相等的权重,以改变最终模型中静电场的相对贡献值太低的情况.多数情况下CoMFASTD可较No Scaling获得更好的结果.但是针对rms Fit模型对Scaling方法作进一步研究时发现:当对B构型以sp3O0.4-和sp3O2-探针进行模拟时,No Scaling可获得更好的模型.可见对Scaling方法的最佳选择还须视具体情况而定.鉴于所得各模型的静电相对贡献值较低,取消了Dropelec的限制,以增加那些因立体相互作用能超过阈值而被排除的网格点上的静电能.结果发现各模型的静电相对贡献值有所增加的同时,Q2值却在降低,模型预测能力下降.综观上述实验结果,发现rms Fit+sp3C+探针+CoMFASTD Scaling+Dropelec可获得较好的CoMFA模型,并且A,B两种构型所得的CoMFA模型结果相当,推其原因在于喜树碱为平面刚性结构,E环部分的空间取向对骨架结构影响不大,且所研究化合物均为A,B环取代,不反映E环信息.
, http://www.100md.com
Tab.2 Different settings and results of the CoMFA run with the A-type conformation of CPT
CoFMA
model
Fit
method
Probe
type
Atom
charge
Scaling
method
, 百拇医药
Drop
elec
Q2①
ONC②
PRESS③
Steric.
Contrib.
Elec.
Contrib.
R2
SEE④
, 百拇医药
F
A1
Field
C sp3
+1.0
CoSTD
YES
0.651
4
0.476
0.820
0.180
, 百拇医药 0.869
0.215
41.495
A2
rms
C sp3
+1.0
CoSTD
YES
0.757
5
0.452
0.833
, 百拇医药
0.167
0.921
0.171
55.636
A3
rms
C sp3
+1.0
NONE
YES
0.755
5
, 百拇医药 0.446
0.851
0.149
0.920
0.172
55.195
A4
rms
C sp3
+1.0
CoSTD
NO
, 百拇医药 0.717
5
0.468
0.750
0.250
0.928
0.163
61.728
A5
rms
C sp3
+1.0
, 百拇医药 NONE
NO
0.664
5
0.513
0.603
0.397
0.921
0.171
55.868
A6
Field
O sp3
, 百拇医药
-0.4
CoSTD
YES
0.651
3
0.501
0.839
0.161
0.845
0.230
47.177
A7
rms
, 百拇医药
O sp3
-0.4
CoSTD
YES
0.753
6
0.455
0.841
0.159
0.933
0.161
53.138
A8
, 百拇医药
rms
O sp3
-0.4
NONE
YES
0.722
4
0.436
0.959
0.041
0.882
0.205
46.541
, 百拇医药
A9
rms
O sp3
-0.4
CoSTD
NO
0.658
4
0.487
0.761
0.239
0.881
, 百拇医药 0.206
46.124
A10
rms
O sp3
-0.4
NONE
NO
0.655
4
0.493
0.753
0.247
, 百拇医药
0.874
0.212
43.192
A11
Field
O sp3
-2.0
CoSTD
YES
0.655
4
0.490
, 百拇医药
0.797
0.203
0.877
0.209
44.385
A12
rms
O sp3
-2.0
CoSTD
YES
0.739
, 百拇医药
5
0.455
0.811
0.189
0.910
0.182
48.531
A13
rms
O sp3
-2.0
NONE
, 百拇医药
YES
0.714
5
0.503
0.699
0.301
0.911
0.181
49.328
A14
rms
O sp3
, 百拇医药
-2.0
CoSTD
NO
0.681
4
0.469
0.758
0.242
0.901
0.187
57.011
A15
rms
, http://www.100md.com
O sp3
-2.0
NONE
NO
0.579
5
0.537
0.459
0.541
0.915
0.177
51.594
①Maximum cross-validated r2,②Optional number of components,③Predictive sum of squares of cross-validated predictions,④Standard error of estimateTab.3 Different settings and results of the CoMFA run with the B-type conformation of CPT
, 百拇医药
CoMFA
model
Fit
method
Probe
type
Atom
charge
Scaling
method
Drop
elec
Q2①
, 百拇医药
ONC②
PRESS③
Steric.
Contrib.
Elec.
Contrib.
R2
SEE④
F
B1
Field
, 百拇医药 C sp3
+1.0
CoSTD
YES
0.648
5
0.443
0.830
0.170
0.909
0.183
47.877
B2
, 百拇医药
rms
C sp3
+1.0
CoSTD
YES
0.745
5
0.426
0.931
0.069
0.895
0.197
40.871
, http://www.100md.com
B3
rms
C sp3
+1.0
NONE
YES
0.754
5
0.418
0.944
0.056
0.895
, 百拇医药 0.197
40.778
B4
rms
C sp3
+1.0
CoSTD
NO
0.712
5
0.421
0.735
0.265
, 百拇医药
0.917
0.175
52.781
B5
rms
C sp3
+1.0
NONE
NO
0.640
5
0.455
, http://www.100md.com 0.572
0.428
0.917
0.175
53.193
B6
Field
O sp3
-0.4
CoSTD
YES
0.647
, 百拇医药 4
0.470
0.737
0.263
0.868
0.216
41.143
B7
rms
O sp3
-0.4
CoSTD
, 百拇医药 YES
0.742
5
0.442
0.923
0.077
0.898
0.194
42.403
B8
rms
O sp3
-0.4
, 百拇医药
NONE
YES
0.761
5
0.415
0.981
0.019
0.907
0.185
47.024
B9
rms
O sp3
, http://www.100md.com
-0.4
CoSTD
NO
0.698
4
0.430
0.733
0.267
0.899
0.189
55.573
B10
rms
, http://www.100md.com
O sp3
-0.4
NONE
NO
0.698
5
0.429
0.753
0.247
0.909
0.183
47.953
B11
, http://www.100md.com
Field
O sp3
-2.0
CoSTD
YES
0.617
4
0.468
0.775
0.225
0.869
0.215
41.526
, http://www.100md.com
B12
rms
O sp3
-2.0
CoSTD
YES
0.725
5
0.448
0.868
0.132
0.902
, 百拇医药 0.190
44.369
B13
rms
O sp3
-2.0
NONE
YES
0.683
5
0.497
0.724
0.276
, 百拇医药
0.908
0.184
47.622
B14
rms
O sp3
-2.0
CoSTD
NO
0.694
5
0.434
, 百拇医药 0.734
0.266
0.914
0.178
51.145
B15
rms
O sp3
-2.0
NONE
NO
0.562
, http://www.100md.com 4
0.488
0.386
0.614
0.907
0.181
61.132
①Maximum cross-validated r2,②Optional number of components,③Predictive sum of squares of cross-validated predictions,④Standard error of estimate
为寻找最佳模型,对有较好预测能力的A2和B2模型进行了Region的系统平移研究,发现网格点的平移可对结果产生极大影响:A2模型平移所得的最差结果Q2值仅为0.305,最优模型Amax的Q2则达0.832;而B2模型平移所得的最差结果Q2等于0.414,最优模型Bmax的Q2值为0.845.以所得最优模型Amax和Bmax对检验组10个化合物进行活性预测,预测残差值均小于1个对数单位,R2pred值分别为0.716和0.685,亦充分说明了模型具有较高的预测能力.对部分预测偏差较大的化合物进行分析,发现预测组化合物的结构超出模型范围可能是导致预测偏差的一个原因.如(38,39)两化合物,10位均被大基团取代,其结构伸展已超出训练组各化合物所占有的空间.而(40)可能因11位氮上引入氧的缘故,构象分析时就发现其有别于其他化合物:B构型能量较A构型高,而Bmax模型对其预测的残差明显高于Amax,很可能与该化合物B构型的较高能量有关.
, http://www.100md.com
Tab.4 PLS analysis results of model Amax and model Bmax
Model
Base
Region moving/
Q2
ONC
PRESS
SDEP
, 百拇医药 R2
F
SEE
Pvalue
Elect.
contrib.
Steric.
contrib.
R2pred
X
Y
Z
, http://www.100md.com
Amax
A2
1.8
0.0
0.2
0.832
6
0.440
0.121
0.950
73.203
0.138
, 百拇医药 0.000
0.224
0.776
0.806
Bmax
B2
0.6
0.0
0.2
0.845
6
0.403
0.116
, 百拇医药
0.960
92.350
0.124
0.000
0.163
0.837
0.715
Tab.5 The Comparision of predicted activity and actual activity
No.
PIC
actual
, 百拇医药
PIC
Amax
Residue
Amax
PIC
Bmax
Residue
Bmax
No.
PIC
actual
PIC
, 百拇医药
Amax
Residue
Amax
PIC
Bmax
Residue
Bmax
No.
PIC
actual
PIC
Amax
, 百拇医药
Residue
Amax
PIC
Bmax
Residue
Bmax
1
0.167
0.445
0.278
0.396
0.229
, 百拇医药
11
1.959
1.978
0.019
1.922
-0.037
21
1.215
1.360
0.145
1.226
0.011
2
, 百拇医药
0.796
0.524
-0.272
0.459
-0.337
12
1.569
1.532
-0.037
1.585
0.016
22
0.959
, 百拇医药
0.694
-0.265
1.107
0.148
3
0.523
0.635
0.112
0.558
0.035
13
0.474
0.481
, 百拇医药
0.007
0.497
0.023
23
0.854
0.837
-0.017
0.860
0.006
4
0.432
0.482
0.050
, 百拇医药
0.440
0.008
14
0.572
0.673
0.101
0.769
0.197
24
0.914
0.923
0.009
0.861
, 百拇医药
-0.053
5
0.194
0.439
0.245
0.360
0.166
15
0.634
0.652
0.018
0.654
0.020
, 百拇医药
25
-0.031
-0.022
0.009
-0.139
-0.108
6
0.060
0.135
0.075
0.129
0.069
16
, 百拇医药
1.149
0.961
-0.188
1.075
-0.074
26
1.319
1.234
-0.085
1.230
-0.089
7
0.000
, 百拇医药
-0.040
-0.040
0.033
0.033
17
1.481
1.386
-0.095
1.433
-0.048
27
0.664
0.655
, 百拇医药
-0.009
0.624
-0.040
8
0.523
0.415
-0.108
0.491
-0.032
18
-0.124
-0.102
-0.022
, 百拇医药
-0.091
0.033
28
0.886
0.912
0.026
0.741
-0.145
9
0.381
0.459
0.078
0.432
, 百拇医药
0.051
19
0.417
0.252
-0.165
0.333
-0.084
29
0.854
0.842
-0.012
0.729
-0.125
, http://www.100md.com
10
1.824
1.927
0.103
1.908
0.084
20
0.721
0.719
-0.002
0.767
0.046
30
, 百拇医药
0.000
-0.041
-0.041
-0.045
-0.045
34
0.959
0.769
-0.190
0.774
-0.185
38
-0.046
, 百拇医药
-0.189
-0.143
0.266
0.312
42
0.824
1.316
0.492
1.207
0.383
35
0.845
0.897
, 百拇医药
0.052
0.810
-0.035
39
-0.174
0.392
0.566
0.308
0.482
343
-0.279
0.254
0.533
, 百拇医药
0.217
0.496
36
0.777
0.819
0.042
0.822
0.045
40
-0.073
0.175
0.248
0.474
, http://www.100md.com
0.547
37
0.023
-0.211
-0.234
0.314
0.291
41
0.297
0.138
-0.159
0.436
0.139
, 百拇医药
2.2 立体能和静电能的分布
由CoMFA模型的立体、静电相对贡献值可看出,该类化合物立体因素对活性影响较静电因素更为重要.图2和图3是以喜树碱为例所显示的Amax和Bmax模型的CoMFA势场轮廓图,可以看出A,B两种构型所得模型基本一致.SAR研究一般认为9位和7位处在药物与受体结合的外部,故设计新化合物时通常用较大基团取代以作为增加药物水溶性的手段;而11位却被认为是紧靠与酶紧密接触的12位,取代时会因立体禁阻而效果不好.但是从CoMFA研究所得的势场图来看,立体取代不利区对7,9,10位成一环状包围,而11位及与10位接近的区域恰有一立体取代有利区,这正为10,11位成环化合物的高活性提供了理论依据,而且也可对训练组化合物(18),(25)与(27)同是10位大基团取代,但活性却较(27)低很多的现象进行合理的解释:通过构象分析发现(18)和(25)的10位因炔基的缘故使得基团在空间直线伸展,与立体禁阻区相接触从而导致低活性,而(27)却可通过键的旋转使得支链避开立体禁阻区因而保持了较好的活性.由此可以推测11位及10位作适当取代(10位取代基团可通过键的旋转或与11位成环而处在近11位空间),可以恰好进入受体表面的空腔中与其发生相互作用.而且从图中可以看出该处区域为正电有利区,推测受体在该位置存在亲核基团.对7位的研究发现在其与9位相近的位置也有立体禁阻区,而Bmax模型则清楚地显示在该立体不利区旁有一小块正电有利区,推测受体可能在该处尚存在一辅助结合位点.


, 百拇医药
(a)Steric field
black:sterically favored area
gray:sterically disfavored area
(b)Electric field
black:positive charge favored area
gray:negative charge favored area
Fig.2 Stereoview of CoMFA contour plots of Amax model


, http://www.100md.com
(a)Steric field
black:sterically favored area
gray:sterically disfavored area
(b)Electric field
black:positive charge favored area
gray:negative charge favored area
Fig.3 Stereoview of CoMFA contour plots of Bmax model
3 结论
, 百拇医药
本实验通过构象分析,发现喜树碱类化合物因其E环部分的羰基取向不同而具有A,B两种构型.通过对33个训练组化合物进行CoMFA研究,以其中的30个化合物建立了较佳的模型,并在此基础上对CoMFA建模条件进行了选择研究,结果发现A,B两种构型有着相近的结果:rms Fit方式更适合于喜树碱这类刚性结构,而以sp3C+探针、CoMFASTD加上Dropelec可得到较好的结果.对所得较佳模型进行了Region的系统平移研究,得到了两种构型的最佳CoMFA模型,并对10个检验组化合物进行了预测,结合充分证明了该模型有着很强的预测能力.通过对所得模型的CoMFA势场图的分析,推翻了以往SAR研究的一些错误结果,并发现了喜树碱类化合物11位(或10位)的正电取代基团可进入受体表面的空腔中,与其中的亲核基团作用,而且喜树碱7位取代亦存在着与受体辅助结合位点相作用的可能.这些结论深化了对喜树碱类化合物与酶-DNA相互作用方式的理解,为今后对其进行合理的结构修饰与改造提供了有利的依据.
*973国家重点基础研究资助项目No.G1998051104
, 百拇医药
作者简介:张万年 通讯联系人
参考文献
1 Wall ME,Wani MC,Cook CE,et al.Plant antitumor agents I.The isolation and structure of camptothecin,a novel alkaloidal and tumor inhibition from camptotheca acuminata.J Am Chem Soc,1966,88(16):3888~3890
2 Slichenmyer WJ,von Hoff DD.New natural products in cancer chemotherapy.J Clin Pharmacol,1990,30(9):770~788
3 Potmesil M.Camptothecins:From bench research to hopsital wards.Cancer Res.1994,54:1431~1439
, 百拇医药
4 Hsiang YH,Hertzberg R,Hecht S,et al.Camptothecin induces protein linked breaks via mammalian DNA topoisomerase I.J Biol Chem,1985,260:14873~14878
5 Hertzberg RP,Caranfa MJ,Hecht S,et al.On the mechanism of topoisomerase I inhibition by camptothecin:Evidence for binding to an enzyme-DNA complex.Biochemistry,1989,28:4629~4638
6 Giovanella BC,Stehlin JS,Wall ME,et al.DNA topoisomerase I-targeted chemotherapy of human colon cancer in sxenografts.Science,1989,246:1046~1048
, http://www.100md.com
7 Wall ME,Wani MC,Nicholas AW,et al.Plant antitumor agents.30.Synthesis,topoisomerase I inhibitory activity,and in vivo evalution of 11-azcamptothecin analyogs.J Med Chem,1995,38:1106~1118
8 Luzzio MJ,Besterman JM,Emerson DL,et al.Synthesis and antitumor activity of noval water soluble derivatives of camptothecin as inhibitors of topoisomerase I.J Med Chem,1995,38:395~401
9 Uehling DE,Nanthakumar SS,Croom D,et al.Synthesis,topoisomerase I inhibitory activity,and in vivo evalution of 11-aza camptothecin analogs.J Med Chem,1995,38:1106~1118
, http://www.100md.com
10 SYBYL,V.6.2,Tripos associates,St Louis,MO,USA
11 Sawada S,Okajima S,Aiyama R,et al.Synthesis and antitumor activity of 20(S)-campotothecin derivatives:carbamate-linked,water-soluble derivatives of 7-ethyl-10-hydroxycampgtothecin.Chem Pharm Bull,1991,39(6):1446~1454
12 Wani MC,Ronman PE,Lindley JT,et al.Plant antitumor agents.18.Synthesis and biological activity of camptothecin analogues.J Med Chem,1980,23:554~560
, http://www.100md.com
13 Cramer Ⅲ RD,Patterson DE,Bunce JD.Comparative molecular field analysis(CoMFA)1.Effect of shape on binding of steroids to carrier proteins.J Am Chem Soc,1988,110:5959~5967
14 朱杰,张万年,周有骏,等.CoMFA网格点的生成及选取对结果影响的研究.中国药学杂志,1999,34(6):417~420
15 DePriest SA,Mayer D,Naylor CB,et al.3D-QSAR of angiotensin-converting enzyme and thermolysin inhibitors:a comparison of CoMFA models based on deduced and experimeentally determined active site geometries.J Am Chem Soc,1993,115:5372~5384
收稿日期:1999-04-30, http://www.100md.com