急性一氧化碳中毒大鼠脑MDA和SOD的变化及高压氧影响
http://www.100md.com
《急诊医学》
作者:刘 郁 王 燕
单位:刘 郁 王 燕,中国医科大学第一临床学院急诊教研室 110001 沈阳
关键词:一氧化碳中毒;丙二醛;超氧化物歧化酶;脑组织;高压氧
急诊医学990402 摘要:目的:观察急性一氧化碳(CO)中毒大鼠脑组织中脂质过氧化终产物丙二醛(MDA)、超氧化物歧化酶(SOD)的变化及高压氧(HBO)对其的影响。方法:建立实验性大鼠CO中毒模型。分别测定一氧化碳染毒及高压氧或常压氧治疗后大脑和小脑中MDA、SOD活性。结果:CO中毒后小脑和大脑MDA分别较染毒前增加了57%和50%;SOD活性分别下降到染毒前的84%和75%。MDA与SOD间呈明显负相关,小脑和大脑r值分别为-0.80和-0.68。2ATAHBO治疗使MDA、SOD恢复到正常水平。结论:急性CO中毒使小脑及大脑MDA、SOD均发生改变,这种改变可能参与CO造成的脑损伤。HBO治疗对CO介导的脑脂质过氧化和自由基清除系统变化有有益的调节作用。
, http://www.100md.com
Carbon monoxide-mediated brain malondialdehyde production and superoxide dismutase inhibitation in the rat.
Liu Yu,Wang Yan.Department of Emergency Medicine,First Clinical College,China Medical University,Shenyang 110001
Abstract Objective:The purpose of this study was to evaluate levels of malondialdehyde(MDA)and superoxide dismutase(SOD) in the rat brain after exposure to carbon monoxide with or without HBO therapy.Methods:Eighty male Wistar rats were randomly divided into 5 groups.The rats were killed after different therapies.Cerebellum as well as cerebrum were seperated and MDA and SOD activity were measured and MDA、SOD levels were compared among the 5 groups.Results were analyzed using one-way analysis of variance(ANOVA)following q-test.Results:In the rat cerebellum and cerebrum,the production of MDA were increased by 57% and 50% over the base-line values after CO exposure.The activities of SOD were inhibitated by 84% and 75% of base-line values after CO exposure.The level of MDA decreased after HBO,but not NBO therapy.HBO also resulted in a return of SOD levels to baseline.Conclusions:The demonstrated changes in levels of MDA and SOD may play an important role in the neurologic damage resulting from CO poisoning.HBO has significant effect on MDA production and SOD activity in cerebellum and cerebrum after CO exposure in rats.
, 百拇医药
Key words Carbon monoxide poisoning Malondialdehyde Superoxide dismutase Brain Hyperbaric oxygen
一氧化碳(carbon monoxide,CO)是自然界中最常引起人类中毒的物质。但一氧化碳中毒致脑损伤的机制至今未明。近年来的研究表明,自由基反应在CO中毒中占一定地位。为进一步探讨一氧化碳中毒时脑内脂质过氧化(lipid peroxidation,LPO)和超氧化物歧化酶(superoxide dismutase,SOD)的变化,以及这些变化与脑损伤的关系,本实验应用动物模型,观察了一氧化碳染毒和高压氧(hyperbaric oxygen,HBO)治疗前后大鼠脑组织中丙二醛(malondialdehyde,MDA)和SOD水平。
1 材料和方法
1.1 动物分组 健康雄性Wistar大鼠80只(中国医科大学实验动物部),体重280~320g,随机分成5组:正常对照组(C组);一氧化碳染毒组(CO组);一氧化碳染毒及高压氧一次治疗组(HBO1组);一氧化碳染毒及高压氧三次治疗组(HBO3组);一氧化碳染毒及常压氧一次治疗组(NBO1组)。
, http://www.100md.com
1.2 CO中毒模型建立参照Ishiropoulos H[1]的方法。把鼠放入自制染毒瓶中,充入99.99%CO气,以CO快速检测管测定染毒瓶中CO浓度,使CO浓度维持在3500~4000ppm,大鼠静式吸入CO气40~60min至昏迷。
1.3 动物处置 高压氧治疗:使用48cm×48cm实验动物用高压氧舱(本院高压氧科)。染毒后20min将动物放入高压氧舱内,压力2ATA,60min。HBO1组治疗一次,HBO3组每天在同一时间治疗连续三天。常压氧治疗:染毒后20min将动物放入高压氧舱内,通入100%氧气,流量2~3L/min,压力为1ATA,治疗60min。大鼠处死取脑:C组不染毒不治疗,随机分入C组后即时处死;CO组染毒模型建立后10min处死;HBO1组、HBO3组、NBO1组均在治疗后10min处死。大鼠断头取脑,分离出大脑、小脑保存于-70℃待测。
, 百拇医药
1.4 标本测定 大、小脑组织样品分别按20%(重量/体积)比例加入pH7.2的磷酸钾缓冲液,匀浆离心取上清。1)MDA测定:硫代巴比妥酸比色法[2]。用Lowery法测定上清中的蛋白含量。单位为μmol.gprot-1。2)SOD测定:羟胺氧化法[3]。用Lowery法测定上清中蛋白含量,SOD单位为NU.gprot-1。
1.5 统计学处理 各项指标均以平均值加减标准差(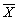 ±s)表示,用单因素方差分析,若有意义,则进一步用两两比较的q检验。以P<0.05表示在统计学上有显著性差异,P<0.01表示有非常显著差异。
±s)表示,用单因素方差分析,若有意义,则进一步用两两比较的q检验。以P<0.05表示在统计学上有显著性差异,P<0.01表示有非常显著差异。
, http://www.100md.com
2 结果
2.1 大鼠小脑及大脑MDA变化
CO染毒使MDA在大脑和小脑的测定值均明显增加,与对照组比有显著差异。HBO抑制了这种增加,尤其是三次治疗更为显著,而NBO无此作用。详见表1,表2。
表1 小脑中各组MDA和SOD变化(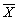 ±s) 组别
±s) 组别
n
MDA
(μmol.gprot-1)
, http://www.100md.com
SOD
(NU.gprot-1)
C
13
132.45±44.87
147.42±27.36
CO
13
208.09±59.09*
124.07±20.59*
NBO1
, http://www.100md.com
12
183.22±51.36*
135.25±22.27
HBO1
12
173.23±51.72
142.07±18.59#
HBO3
14
149.36±49.75#
146.29±21.49#
, http://www.100md.com
注:*代表与C组相比差异显著(P<0.05),#代表与CO组相比差异显著(P<0.05)表2 大脑中各组MDA和SOD变化(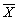 ±s) 组别
±s) 组别
n
MDA
(μmol.gprot-1)
SOD
(NU.gprot-1)
C
, http://www.100md.com 12
112.64±20.90
108.65±20.91
CO
15
168.67±28.18**
81.29±19.44**
NBO1
12
163.34±38.22**△
84.43±17.18*△△
, http://www.100md.com
HBO1
15
124.31±332.05##
90.70±19.99*△
HBO3
15
113.90±16.21##
106.92±16.82##
注:*代表与C组相比差异显著(P<0.05),**代表与C组相比差异非常显著(P<0.01); #代表与CO组相比差异显著(P<0.05),##代表与CO组相比差异非常显著(P<0.01); △代表与HBO3组相比差异显著(P<0.05),△△代表与HBO3组相比差异非常显著(P<0.01)
, 百拇医药
2.2 大鼠小脑及大脑SOD变化
CO染毒后,小脑、大脑中SOD活性均明显受抑制,与对照组比有显著差异。HBO治疗有效地恢复了小脑、大脑中SOD活性,HBO三次治疗效果更好。NBO对SOD无明显影响。详见表1,表2。
3 讨论
急性一氧化碳中毒在我国是危害人民健康的严重疾病之一,也是许多发达的工业国家中毒致死的重要原因。CO中毒后涉及的最重要器官是脑。临床很难在细胞和分子生物学水平上直接观察人体中毒后器官受损情况。本实验通过动物模型,直接研究脑组织匀浆中MDA、SOD变化,在国内外鲜有报道。
我们的研究发现,一氧化碳中毒后10min,大鼠脑内MDA明显增加。小脑和大脑中MDA分别较对照增加57%和50%,与Thom[4]报道的接触CO后90min,LPO较基础值增加75%相一致。MDA是脂质过氧化的终末代谢产物。CO中毒时,脑内黄嘌呤脱氢酶转化为黄嘌呤氧化酶。黄嘌呤氧化酶以O2作为电子受体,催化次黄嘌呤的酶促反应时,生成超氧自由基,进而形成羟基自由基[5]。这些自由基作用于细胞膜上的不饱和脂肪酸,使之发生过氧化反应而生成LPO,LPO可使Na+-K+ATP酶失去活性,膜通透性改变,溶酶体崩解而导致细胞坏死或功能障碍。
, 百拇医药
我们同时测定的大小脑中SOD结果表现出,CO中毒使其活性明显下降。小脑和大脑中SOD活性分别减少到对照的84%和75%。SOD是机体主要的抗氧化酶。SOD活性不足意味着自由基清除能力下降。CO中毒时SOD活性降低的原因可能是LPO过多,消耗了大量SOD酶活性;也可能是CO直接抑制SOD活性。我们的结果表明MDA与SOD存在明显负相关,小脑和大脑中r值分别为-0.80和-0.68。CO引起的这种变化使组织对自由基的敏感性增强。自由基和LPO可以通过氧化、交联、肽链断裂、碱基修饰等方式使蛋白质、脂蛋白、酶蛋白变性,引起酶失活和脑细胞功能结构损伤坏死。
我们使用2ATA的HBO治疗后小脑、大脑组织中MDA减少,SOD活性明显恢复。Thom[4]等使用3ATA的HBO观察到其拮抗脂质过氧化作用。我们的研究发现,三次HBO的效果更好,常压氧没有这样的作用。推测HBO可阻止黄嘌呤脱氢酶向黄嘌呤氧化酶的转化,从而阻断氧自由基的生成;HBO可激活脑内自由基清除系统,恢复SOD活性而进一步清除氧自由基。
, http://www.100md.com
LPO生成增多,SOD活性下降,均参与了急性CO中毒脑损伤的病理过程。HBO可逆转这一病理过程;给予自由基清除剂及抗氧化剂,对于减轻自由基造成的脑细胞损伤将是有益的尝试。
参考文献
1 H.Ischiropoulos,M.F Beers,S.Tohnishi,et al.Nitric oxide production and perivascular tyrosine nitration in brain after carbon monoxide poisoning in the rat.J.Clin.Invest,1996,97:2260
2 陈顺志,金有余,李常厚,等.过氧化脂质TAB显色的三种方法学比较.临床检验杂志,1984,2:176
3 季建平,吴再彬,刘歧山,等.超氧化物歧化酶微量快速测定法.南京铁道医学院学报,1991,10:27
, 百拇医药
4 Thom SR.Carbon monoxide-mediated brain lipid peroxidation in the rat.J.Appl.Physiol,1990,68:997
5 Thom SR.Dehydrogenase conversion to oxidase and lipid peroxidation in brain after carbon monoxide poisoning.J.Appl.Physiol,1992,73:1584
6 Thom SR.Antagonism of carbon monoxide-mdiated brain lipid peroxidation by hyperbaric oxygen.Toxicol.Appl.Pharmacol,1990,105:340
收稿:1998-11-08, 百拇医药
单位:刘 郁 王 燕,中国医科大学第一临床学院急诊教研室 110001 沈阳
关键词:一氧化碳中毒;丙二醛;超氧化物歧化酶;脑组织;高压氧
急诊医学990402 摘要:目的:观察急性一氧化碳(CO)中毒大鼠脑组织中脂质过氧化终产物丙二醛(MDA)、超氧化物歧化酶(SOD)的变化及高压氧(HBO)对其的影响。方法:建立实验性大鼠CO中毒模型。分别测定一氧化碳染毒及高压氧或常压氧治疗后大脑和小脑中MDA、SOD活性。结果:CO中毒后小脑和大脑MDA分别较染毒前增加了57%和50%;SOD活性分别下降到染毒前的84%和75%。MDA与SOD间呈明显负相关,小脑和大脑r值分别为-0.80和-0.68。2ATAHBO治疗使MDA、SOD恢复到正常水平。结论:急性CO中毒使小脑及大脑MDA、SOD均发生改变,这种改变可能参与CO造成的脑损伤。HBO治疗对CO介导的脑脂质过氧化和自由基清除系统变化有有益的调节作用。
, http://www.100md.com
Carbon monoxide-mediated brain malondialdehyde production and superoxide dismutase inhibitation in the rat.
Liu Yu,Wang Yan.Department of Emergency Medicine,First Clinical College,China Medical University,Shenyang 110001
Abstract Objective:The purpose of this study was to evaluate levels of malondialdehyde(MDA)and superoxide dismutase(SOD) in the rat brain after exposure to carbon monoxide with or without HBO therapy.Methods:Eighty male Wistar rats were randomly divided into 5 groups.The rats were killed after different therapies.Cerebellum as well as cerebrum were seperated and MDA and SOD activity were measured and MDA、SOD levels were compared among the 5 groups.Results were analyzed using one-way analysis of variance(ANOVA)following q-test.Results:In the rat cerebellum and cerebrum,the production of MDA were increased by 57% and 50% over the base-line values after CO exposure.The activities of SOD were inhibitated by 84% and 75% of base-line values after CO exposure.The level of MDA decreased after HBO,but not NBO therapy.HBO also resulted in a return of SOD levels to baseline.Conclusions:The demonstrated changes in levels of MDA and SOD may play an important role in the neurologic damage resulting from CO poisoning.HBO has significant effect on MDA production and SOD activity in cerebellum and cerebrum after CO exposure in rats.
, 百拇医药
Key words Carbon monoxide poisoning Malondialdehyde Superoxide dismutase Brain Hyperbaric oxygen
一氧化碳(carbon monoxide,CO)是自然界中最常引起人类中毒的物质。但一氧化碳中毒致脑损伤的机制至今未明。近年来的研究表明,自由基反应在CO中毒中占一定地位。为进一步探讨一氧化碳中毒时脑内脂质过氧化(lipid peroxidation,LPO)和超氧化物歧化酶(superoxide dismutase,SOD)的变化,以及这些变化与脑损伤的关系,本实验应用动物模型,观察了一氧化碳染毒和高压氧(hyperbaric oxygen,HBO)治疗前后大鼠脑组织中丙二醛(malondialdehyde,MDA)和SOD水平。
1 材料和方法
1.1 动物分组 健康雄性Wistar大鼠80只(中国医科大学实验动物部),体重280~320g,随机分成5组:正常对照组(C组);一氧化碳染毒组(CO组);一氧化碳染毒及高压氧一次治疗组(HBO1组);一氧化碳染毒及高压氧三次治疗组(HBO3组);一氧化碳染毒及常压氧一次治疗组(NBO1组)。
, http://www.100md.com
1.2 CO中毒模型建立参照Ishiropoulos H[1]的方法。把鼠放入自制染毒瓶中,充入99.99%CO气,以CO快速检测管测定染毒瓶中CO浓度,使CO浓度维持在3500~4000ppm,大鼠静式吸入CO气40~60min至昏迷。
1.3 动物处置 高压氧治疗:使用48cm×48cm实验动物用高压氧舱(本院高压氧科)。染毒后20min将动物放入高压氧舱内,压力2ATA,60min。HBO1组治疗一次,HBO3组每天在同一时间治疗连续三天。常压氧治疗:染毒后20min将动物放入高压氧舱内,通入100%氧气,流量2~3L/min,压力为1ATA,治疗60min。大鼠处死取脑:C组不染毒不治疗,随机分入C组后即时处死;CO组染毒模型建立后10min处死;HBO1组、HBO3组、NBO1组均在治疗后10min处死。大鼠断头取脑,分离出大脑、小脑保存于-70℃待测。
, 百拇医药
1.4 标本测定 大、小脑组织样品分别按20%(重量/体积)比例加入pH7.2的磷酸钾缓冲液,匀浆离心取上清。1)MDA测定:硫代巴比妥酸比色法[2]。用Lowery法测定上清中的蛋白含量。单位为μmol.gprot-1。2)SOD测定:羟胺氧化法[3]。用Lowery法测定上清中蛋白含量,SOD单位为NU.gprot-1。
1.5 统计学处理 各项指标均以平均值加减标准差(
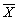 ±s)表示,用单因素方差分析,若有意义,则进一步用两两比较的q检验。以P<0.05表示在统计学上有显著性差异,P<0.01表示有非常显著差异。
±s)表示,用单因素方差分析,若有意义,则进一步用两两比较的q检验。以P<0.05表示在统计学上有显著性差异,P<0.01表示有非常显著差异。, http://www.100md.com
2 结果
2.1 大鼠小脑及大脑MDA变化
CO染毒使MDA在大脑和小脑的测定值均明显增加,与对照组比有显著差异。HBO抑制了这种增加,尤其是三次治疗更为显著,而NBO无此作用。详见表1,表2。
表1 小脑中各组MDA和SOD变化(
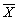 ±s) 组别
±s) 组别n
MDA
(μmol.gprot-1)
, http://www.100md.com
SOD
(NU.gprot-1)
C
13
132.45±44.87
147.42±27.36
CO
13
208.09±59.09*
124.07±20.59*
NBO1
, http://www.100md.com
12
183.22±51.36*
135.25±22.27
HBO1
12
173.23±51.72
142.07±18.59#
HBO3
14
149.36±49.75#
146.29±21.49#
, http://www.100md.com
注:*代表与C组相比差异显著(P<0.05),#代表与CO组相比差异显著(P<0.05)表2 大脑中各组MDA和SOD变化(
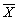 ±s) 组别
±s) 组别n
MDA
(μmol.gprot-1)
SOD
(NU.gprot-1)
C
, http://www.100md.com 12
112.64±20.90
108.65±20.91
CO
15
168.67±28.18**
81.29±19.44**
NBO1
12
163.34±38.22**△
84.43±17.18*△△
, http://www.100md.com
HBO1
15
124.31±332.05##
90.70±19.99*△
HBO3
15
113.90±16.21##
106.92±16.82##
注:*代表与C组相比差异显著(P<0.05),**代表与C组相比差异非常显著(P<0.01); #代表与CO组相比差异显著(P<0.05),##代表与CO组相比差异非常显著(P<0.01); △代表与HBO3组相比差异显著(P<0.05),△△代表与HBO3组相比差异非常显著(P<0.01)
, 百拇医药
2.2 大鼠小脑及大脑SOD变化
CO染毒后,小脑、大脑中SOD活性均明显受抑制,与对照组比有显著差异。HBO治疗有效地恢复了小脑、大脑中SOD活性,HBO三次治疗效果更好。NBO对SOD无明显影响。详见表1,表2。
3 讨论
急性一氧化碳中毒在我国是危害人民健康的严重疾病之一,也是许多发达的工业国家中毒致死的重要原因。CO中毒后涉及的最重要器官是脑。临床很难在细胞和分子生物学水平上直接观察人体中毒后器官受损情况。本实验通过动物模型,直接研究脑组织匀浆中MDA、SOD变化,在国内外鲜有报道。
我们的研究发现,一氧化碳中毒后10min,大鼠脑内MDA明显增加。小脑和大脑中MDA分别较对照增加57%和50%,与Thom[4]报道的接触CO后90min,LPO较基础值增加75%相一致。MDA是脂质过氧化的终末代谢产物。CO中毒时,脑内黄嘌呤脱氢酶转化为黄嘌呤氧化酶。黄嘌呤氧化酶以O2作为电子受体,催化次黄嘌呤的酶促反应时,生成超氧自由基,进而形成羟基自由基[5]。这些自由基作用于细胞膜上的不饱和脂肪酸,使之发生过氧化反应而生成LPO,LPO可使Na+-K+ATP酶失去活性,膜通透性改变,溶酶体崩解而导致细胞坏死或功能障碍。
, 百拇医药
我们同时测定的大小脑中SOD结果表现出,CO中毒使其活性明显下降。小脑和大脑中SOD活性分别减少到对照的84%和75%。SOD是机体主要的抗氧化酶。SOD活性不足意味着自由基清除能力下降。CO中毒时SOD活性降低的原因可能是LPO过多,消耗了大量SOD酶活性;也可能是CO直接抑制SOD活性。我们的结果表明MDA与SOD存在明显负相关,小脑和大脑中r值分别为-0.80和-0.68。CO引起的这种变化使组织对自由基的敏感性增强。自由基和LPO可以通过氧化、交联、肽链断裂、碱基修饰等方式使蛋白质、脂蛋白、酶蛋白变性,引起酶失活和脑细胞功能结构损伤坏死。
我们使用2ATA的HBO治疗后小脑、大脑组织中MDA减少,SOD活性明显恢复。Thom[4]等使用3ATA的HBO观察到其拮抗脂质过氧化作用。我们的研究发现,三次HBO的效果更好,常压氧没有这样的作用。推测HBO可阻止黄嘌呤脱氢酶向黄嘌呤氧化酶的转化,从而阻断氧自由基的生成;HBO可激活脑内自由基清除系统,恢复SOD活性而进一步清除氧自由基。
, http://www.100md.com
LPO生成增多,SOD活性下降,均参与了急性CO中毒脑损伤的病理过程。HBO可逆转这一病理过程;给予自由基清除剂及抗氧化剂,对于减轻自由基造成的脑细胞损伤将是有益的尝试。
参考文献
1 H.Ischiropoulos,M.F Beers,S.Tohnishi,et al.Nitric oxide production and perivascular tyrosine nitration in brain after carbon monoxide poisoning in the rat.J.Clin.Invest,1996,97:2260
2 陈顺志,金有余,李常厚,等.过氧化脂质TAB显色的三种方法学比较.临床检验杂志,1984,2:176
3 季建平,吴再彬,刘歧山,等.超氧化物歧化酶微量快速测定法.南京铁道医学院学报,1991,10:27
, 百拇医药
4 Thom SR.Carbon monoxide-mediated brain lipid peroxidation in the rat.J.Appl.Physiol,1990,68:997
5 Thom SR.Dehydrogenase conversion to oxidase and lipid peroxidation in brain after carbon monoxide poisoning.J.Appl.Physiol,1992,73:1584
6 Thom SR.Antagonism of carbon monoxide-mdiated brain lipid peroxidation by hyperbaric oxygen.Toxicol.Appl.Pharmacol,1990,105:340
收稿:1998-11-08, 百拇医药