乳腺癌前哨淋巴结活检研究进展
 |
 |
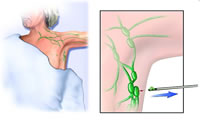
乳腺癌前哨淋巴结活检(SLNB)已迅速替代腋淋巴结清扫术(ALND)成为多数早期乳腺癌的标准治疗方法。作为一项对腋窝准确分期的微创活检技术,SLNB代表着乳腺癌外科治疗的发展水平。SLNB阴性者可避免ALND,从而避免相应的术后并发症,提高了长期生活质量。然而,SLNB的广泛开展可能超越了已有的支持证据,目前仍有一些问题尚未明确。本次会议主要讨论的是以下五方面内容。
1 SLN微小转移预后价值仍不明确
2002年第6版美国癌症联合委员会(AJCC)/国际抗癌联盟(UICC)肿瘤分期推荐,乳腺癌淋巴结微转移(0.2 mm~2.0 mm,通常由连续切片HE染色发现)为pN1mi,孤立肿瘤细胞群(ITC,≤0.2 mm,通常仅由免疫组化发现)为pN0(i+),而无大体转移、微转移及ITC为pN0(i-)。
目前资料表明,微小转移(包括微转移和ITC)对乳腺癌患者的预后价值不明或非常有限,单因素分析10年相关生存率至多降低5%,预后作用依赖于微小转移灶的大小,但其阈值尚无明确界定。而原发肿瘤的大小和分级等对预后的影响更为重要。目前ASCO推荐对前哨淋巴结(SLN)微转移者行ALND,而对ITC则按腋窝淋巴结阴性者处理。对于不需要进一步的预后资料的保乳治疗患者,也可选择腋窝放疗替代ALND。
, 百拇医药
美国John Wayne癌症研究所的Hansen报告了其纳入790例腋淋巴结阴性的Ⅰ、Ⅱ期乳腺癌患者的前瞻性研究结果。在无病生存(DFS)率、无远处转移生存率及总生存(OS)率方面,SLN阴性、ITC及微转移者无差异,但均显著优于SLN大体转移者。而该研究的一个潜在混淆因素在于,多数微小转移者及25%的SLN阴性者接受了辅助化疗,这可能影响了各组的生存率。但在之后的讨论中,有专家指出,2006年Kahn报告的研究显示,患者均未接受辅助治疗,而淋巴结阴性、ITC及微转移者的生存率同样无显著性差异。最近结束患者入组的ACOSOG Z0010试验结果将提供进一步的证据。
Kelten等的报告也验证了上述观点。研究纳入常规病理检测腋淋巴结阴性且未接受辅助治疗的267例乳腺癌患者,中位随访159个月,10年DFS率为76.4%。进一步检测发现,39例患者存在隐匿性转移灶,包括8例大体转移、15例微转移和16例ITC。DFS率与雌激素受体(ER)状态相关(P=0.03),而与隐匿性转移(P=0.34)、发病年龄、组织学类型、核分级、孕激素受体(PR)状态及病期无关。作者指出,早期乳腺癌伴或不伴腋淋巴结隐匿性转移的DFS率相似,这对推荐SLN微小转移者接受ALND的观点提出了挑战。
, 百拇医药
2 PNSN预测指标可确定SLNB后是否行ALND
对25项临床试验的荟萃分析表明,有SLN微转移及ITC者的腋窝其他淋巴结转移的几率分别约为20%和9%。美国纽约Sloan Kettering纪念医院根据SLN与乳腺原发肿瘤特点,包括原发肿瘤大小、组织学类型、核分级、淋巴管侵犯、多灶性或多中心性、ER状态、阳性和阴性SLN数目及SLN病理检测方法,建立了一项腋窝非SLN转移几率列线图(MSKCC BCN),目前越来越多的医院用其确定SLN阳性者SLNB后是否需接受ALND。
本次会议上,Julian报告了NSABP B-32试验的亚组研究结果。将5611例临床淋巴结阴性者随机分组,分别在SLNB后全部接受ALND或SLN阳性者接受ALND,而阴性者不接受。目的是确定SLN阳性者非SLN阳性(PNSN)的可能预测指标。
24.3%(1361/5611例)患者为SLN阳性并接受了ALND,研究者对其中1166例患者进行了多因素分析。PNSN显著的独立预测指标依次为阳性SLN数目、淋巴管和血管侵犯情况、检出SLN数目、临床肿瘤大小、核素显像SLN数目及手术类型。随着SLN检出数目的增加和阳性SLN数目的减少,PNSN的几率降低;肿瘤减小及无淋巴管和血管侵犯则可进一步降低PNSN的几率;然而,即使是预后指标良好者仍有较高的PNSN几率(≥10%,依据不同的指标组合)。此外,年龄、切除活检类型、组织学分级、Her-2状态、肿瘤部位及ER/PR状态均不是独立的预测指标。
, 百拇医药
尽管对多数SLN阳性者行ALND是必需的,但Julian等认为,对于有选择性且预测指标显示PNSN的可能性小者仍有可能避免行ALND,如原发肿瘤很小(≤1 cm),无淋巴管和血管侵犯以及检出5个以上SLN中只有1个阳性。
然而,由于该试验起始时的资金和技术限制,使得本亚组研究有局限性。SLN诊断如仅靠常规HE染色,倾向于检出SLN中较大的转移灶。而本项研究未检测SLN转移灶的大小,因此无法评估ITC、微转移及大体转移的相对危险性。
此外,Gilles等报告,是否有SLN微转移和ITC对确定PNSN无预测作用。该研究纳入了14个中心的688例SLNB后接受ALND的患者,其中PNSN为13.4%。有SLN微转移(437例)和ITC(251例)的PNSN分别为12.8%和14.3%,无显著性差异。作者认为,MSKCC BCN可能更为准确。
3 术中诊断SLN转移BLN检测渐显优势
, 百拇医药
2005年,第二届国际乳腺癌共识会认为,SLN术中诊断推荐使用的是印片细胞学和冰冻快速病理检查,但目前二者诊断的敏感性都较低。而逆转录―聚合酶链反应(RT-PCR)技术则极为敏感,可检测单个细胞的基因表达。
2006年的圣安东尼奥乳腺癌会议上,美国Morton Plant Mease 保健中心的Blumencranz报告了一种基于RT-PCR的乳腺癌SLN术中快速检测技术――Gene SearchTM BLN检测。检测目标为上皮细胞特异性基因CK-19和乳球蛋白(MG)。以石蜡切片组织学作为金标准,BLN检测显著优于冰冻快速病理,特别是印片细胞学诊断。
BLN检测相对快速,经过简单培训即可掌握,能确定是否有SLN转移。更重要的是其还可检测50%的淋巴结组织,并能同时检测6个淋巴结。BLN检测的高敏感性意味着其可降低患者接受二次ALND的风险,从而降低医疗费用。该技术已于2006年11月16日获得美国FDA批准用于临床。
, http://www.100md.com
本次会议上,Blumencranz再次报告,BLN检测SLN转移的敏感性显著高于冰冻快速病理(91%对82.1%,P<0.05),尤其是BLN检测微转移的优势更为显著(68.2%对40.9%),但二者特异性无显著差异。部分患者SLN的术中冰冻快速病理诊断尤为困难,包括浸润性小叶癌、原发肿瘤较小(T1)、低分级及接受新辅助化疗者。但对所有患者的SLN,BLN检测微转移和大体转移的敏感性均显著优于冰冻快速病理。
因此,研究者相信,BLN检测是SLN术中冰冻快速病理诊断的可靠替代或有益补充,有助于多数SLN阳性患者一次完成ALND。未来的定量RT-PCR研究将提供SLN肿瘤负荷的定量评估。
此外,Goyal等报告,术中BLN检测较术后病理检查可使乳腺癌手术费用降低8%,费用-效益比合理。Kurosumi等发现,BLN联合检测CK-19和MG比单独CK-19检测的敏感性提高5.9%。
另一项基于RT-LAMP(逆转录-环状介导等温DNA扩增)的一步核酸扩增(OSNA)检测,目标为CK-19,并具有不需mRNA纯化步骤,应用6个引物以提高特异性等优势。初步结果显示,其特异性和敏感性与BLN检测相当,是SLN的术中诊断的又一快速检测手段。
, 百拇医药
4 新辅助化疗后SLNB仍待进一步证实
对新辅助化疗患者行前哨淋巴结活检(SLNB)的时机仍存在争议。此前多数学者推荐,在新辅助化疗前行SLNB,其中SLN阳性者的ALND通常在新辅助化疗完成后进行,而对SLN阴性者则不行ALND。但近年来,部分学者认为,可于新辅助化疗后行SLNB。其理由包括:①18项新辅助化疗后SLNB的研究结果显示,SLNB的平均成功率为89%,平均假阴性率为10%(0~33%),接近常规SLNB的相关数据;②新辅助化疗可使约1/3的腋淋巴结阳性者转为阴性(降级),若在新辅助化疗前行SLNB将使该部分患者接受ALND,就不能从新辅助化疗的降级或腋窝淋巴结缩小(降期)中获益,而对于仅有SLN转移者,则同样不能评估其腋窝降期与获益;③新辅助化疗方案也可根据乳腺原发肿瘤大小、生物学特点及临床腋淋巴结状况确定。
本次会议上法国一项前瞻性多中心研究――GANEA试验,其主要研究目的是评估局部晚期乳腺癌新辅助化疗后SLNB的可行性和准确性。195例Ⅱ、Ⅲ期乳腺癌患者中,新辅助化疗后行SLNB的成功率、假阴性率和准确率分别为90.2%、11.5%和96.6%,其中新辅助化疗前腋窝淋巴结阴性者(130例)接受SLNB的成功率、假阴性率和准确率分别为94.6%、9.4%和97.5%,而腋窝淋巴结阳性者(65例)的成功率、假阴性率和准确率则分别为81.5%、15.0%和94.3%,均无显著差异。
, 百拇医药
作者认为,局部晚期乳腺癌新辅助化疗后SLNB的成功率、假阴性率及准确率与新辅助化疗前腋淋巴结是否阳性无关,新辅助化疗后SLNB可行、准确,可使新辅助化疗后腋窝降期者免行ALND。
Bauerfeind等还报告了一项回顾性多中心研究结果,其中71.9%(92/128例)接受了新辅助化疗后SLNB,假阴性率为16.6%。因此,新辅助化疗后SLNB的最终可行性还需要前瞻性试验的进一步证实。
5 SLNB技术使腋窝分期更为准确
大样本前瞻性随机临床试验,包括英国的ALMANAC试验、意大利米兰的SNB 185试验及美国的NSABP B-32试验均证实,SLNB可提供准确的腋窝淋巴结分期,SLNB组与ALND组有相同的腋淋巴结阳性率。
理论上,SLNB存在较低的假阴性率,可能降低接受SLNB乳腺癌患者的腋窝阳性率,同时,由于其对数目较少的SLN可进行更为仔细的病理检测,又会增加腋淋巴结转移,特别是微小转移的检出,两者相抵可使腋窝淋巴结阳性率保持稳定。在美国,SLNB已被纳入乳腺癌患者的标准外科治疗。
, 百拇医药
本次会议上,Helyer等首次报告,在基于人群的队列研究中,SLNB广泛应用后美国乳腺癌患者腋窝淋巴结阳性率改变。该研究对1992-2003年期间的美国NIH-NCI监测、流行病学和最终结果(SEER)数据库中,接受乳腺及腋窝手术的112,740例T1/T2期乳腺癌患者的腋淋巴结状况,进行了单因素和多因素分析。腋窝淋巴结阳性的预测指标包括肿瘤大小、分级、受体状态、乳腺手术和腋窝手术类型及诊断日期。
结果显示,从1998年到2003年,SLNB比例从1.3%增加到57.4%,腋淋巴结阳性率从26.6%增加到29.4%(P=0.001),微小转移从3.3%增加到5.5%(P<0.001)。多因素回归分析显示,若肿瘤体积增加、分级差或中等、ER阳性、乳房切除术(与保乳术相比)及SLNB(与ALND相比),则腋窝淋巴结阳性率增加,且淋巴结阳性率的增加与SLNB的广泛应用呈正相关(P=0.005)。
因此,在未来,监控调整后的腋窝淋巴结阳性率可以成为SLNB假阴性率的有效替代指标(质控指标)。, http://www.100md.com