全球第一个多靶点抗肿瘤药物索拉非尼(多吉美) 中国上市1周年回顾
 |
进入新世纪,临床肿瘤领域的热点之一是靶向治疗。自20余年前肾细胞癌(RCC)有了生物治疗以来,截至目前一直未有重要的研究进展。2005年底,第一个被美国FDA批准用于治疗晚期RCC的分子靶向药物――索拉非尼(多吉美)成为业界广泛关注的研究成果, 2006年该药在我国成功上市,为我国晚期RCC患者带来了福音,也提供给临床医师一种新的治疗方案。
在过去的1年中,我国临床医师成功地将多吉美用于晚期RCC患者,从此开创了中国晚期RCC靶向治疗新时代。1年多来,多吉美在临床上的应用也逐渐得到普及,越来越多的晚期肿瘤患者从中受益,生活质量得到改善,生存时间得以延长。
为了不断扩大和推广多吉美用药经验,使更多晚期肿瘤患者获益,2007年12月,拜耳医药保健有限公司在北京举行了多吉美上市1周年庆典活动,会上对多吉美在中国进行的晚期RCC临床试验、上市后在晚期肝细胞癌(HCC)、非小细胞肺癌(NSCLC)、黑色素瘤等方面进行的临床研究现状及多吉美中国患者援助计划(NCPAP)的进展情况进行了总结。
, 百拇医药
多吉美中国用药经验
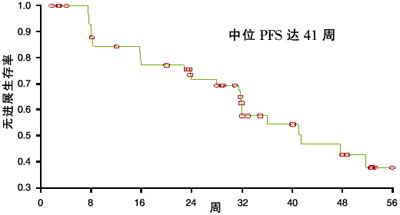
IIT研究结果显示,中国转移性RCC患者服用多吉美治疗可使PFS延长至41周,1年PFS率为42.7%,1年生存率高达93.2%
2005年5月首先在我国开展了一项由研究者发起的临床多中心研究(IIT),旨在评价索拉非尼治疗中国转移性RCC患者的疗效和安全性。参加研究的中心包括中国医学科学院肿瘤医院内科、北京大学第一医院泌尿外科、武汉同济医院化疗内科和浙江省肿瘤医院化疗中心。ITT试验患者入组标准为:组织学或细胞学确诊的不能手术切除和(或)转移性RCC,有可测量病灶,ECOG 体力状态评分为0~2,预期生存期>12 周,患者有良好的主要脏器功能,无脑转移。排除标准为既往或同时伴有其他恶性肿瘤,已知或可疑脑转移,有出血史或出血体质的患者,已知对研究药物过敏者,有异体器官移植史、妊娠或哺乳的患者。
IIT试验共纳入62例转移性RCC患者,平均年龄53(19~86)岁,病理类型以透明细胞癌为主(48例,占77.4%),既往接受过免疫治疗和(或)化疗的患者为57例(91.94%)。随诊至2007年8月,62例患者中有5例患者在治疗初期因出现药物相关毒副反应而退出研究,在57例可进行疗效评价患者中,1例完全缓解(CR),11例部分缓解(PR),总缓解率为21.1%,36例疾病稳定(SD),疾病控制率为84.21%(表1)。随访至2007年8月底,患者持续用药最长时间为407天,中位无进展生存(PFS)时间为41周(图1),1年PFS率为42.7%,1年生存率为93.2%,中位生存时间尚未达到,说明多吉美已显示较好的提高生存率的益处。
, 百拇医药
IIT试验中索拉非尼也具有靶向药物的常见不良反应,包括疲乏、手足皮肤反应、腹泻、高血压等。这些不良反应多数为1~2级,不需要特殊处理,仅少数患者不良反应为3~4级(表2),可通过减量或停药来缓解症状或对症治疗,其中索拉非尼的手足皮肤反应是导致患者停药的主要原因之一,但如果在用药早期注意预防或出现不良反应后及时处理,则可将其控制在1~2级,当出现3级皮肤反应时须停药,一般停药后患者症状可明显缓解。症状缓解低于2级以下,需要再次使用足量索拉非尼,手足皮肤反应症状一般不会加重。
ITT临床中期分析结果证实,索拉非尼治疗中国转移性RCC患者的疗效及安全性与2003年至2005年进行的索拉非尼治疗晚期RCC患者全球多中心Ⅲ期临床试验研究(TARGET)结果相近。与TARGET研究相比,IIT研究中索拉非尼对晚期RCC患者的疾病控制率相近,但中国患者中位PFS长达41周,比TARGET中的24周显著延长(表1)。为此,2006年9月索拉非尼获得国家食品药品管理局(SFDA)批准用于晚期RCC治疗,并注册中文商品名为多吉美。2006年12月拜耳医药保健有限公司分别在北京、成都、广州、上海举办了多吉美上市会,从此多吉美开始正式在我国临床应用。
, http://www.100md.com
表1 IIT研究与TARGET研究结果比较
主要疗效指标IIT 中国(n=57)TARGET(n=451)
完全缓解1例(1.75%)1例(<1)
部分缓解11例(19.30%)43例(10%)
疾病稳定36例(63.16%)333例(74%)
临床控制率84.21% 84%
中位PFS41周24周
中位TTP41周NA
中位OS未达到17.8个月
表2 IIT中国研究与TARGET研究不良反应比较
, 百拇医药
严重不良反应IIT 中国(n=57) 3/4 级TARGET(n=451) 3/4 级
手足皮肤反应10例(16.1%)25例(6%)
脱发01例(<1%)
疲乏022例(5%)
厌食1例(1.6%)4例(1%)
腹泻4例(6.45%)11例(2%)
高血压8例(12.9%)16例(4%)
出血013例(3%)
图1 IIT中晚期RCC患者的PFS
多吉美患者援助计划
, 百拇医药
多吉美中国患者援助计划使更多的RCC患者得到救治,截至目前已有218例患者获得免费多吉美药物捐助
2007年4月拜耳医药保健有限公司与中华慈善总会携手建立了多吉美中国患者援助计划(NCPAP),并与医学专家们确定了多吉美在中国实施慈善援助计划的条件和标准。此援助计划针对经病理检查证实为晚期RCC患者,包括RCC术后出现复发或(和)转移的患者。对无RCC手术史且不能手术的晚期患者须行穿刺活检或切取活检以获取RCC的病理证据。低保、特困晚期RCC患者可享受多吉美免费治疗,这无疑会给广大RCC患者带来裨益。晚期RCC普通居民在自费接受常规剂量多吉美治疗4个月后,经RECIST评估确认患者获益于多吉美治疗,即可向中华慈善总会多吉美办公室提出申请(网址为www.ncpap.cn),申请获批后,患者将享受免费多吉美治疗,并进行定期医学评估,只要评估结果显示多吉美治疗对患者有益,即可继续享受多吉美免费治疗直至病情进展。NCPAP实现了WHO使癌症变为慢性过程,并使患者保留生活质量良好的愿望。
, http://www.100md.com
在全国33家医院参与患者援助计划的注册医师有45位,为了便于患者了解NCPAP,2007年6月14日开通了多吉美官方网站(www.NCPAP.com.cn),所有服用多吉美治疗的晚期RCC患者均可申请入组。2007年5月22日第1位申请患者获得多吉美免费捐助服务。从2007年4月开始,截至2008年1月,NCPAP共收到223例晚期RCC患者的申请,已经批准获得免费药物捐助的患者达209例,此外还有9例低保或特困患者获得完全免费服用多吉美治疗的批准。大多数申请加入NCPAP的晚期RCC患者均可获得免费捐助而继续服药治疗。
现有的临床研究结果已经充分显示出,绝大多数晚期RCC患者可受益于多吉美治疗,且耐受性良好。众所周知,多吉美在HCC、NSCLC等晚期肿瘤患者的治疗中也收到了一定疗效,说明多吉美还有进一步扩大临床适应证的可能。多吉美联合其他生物制剂或(和)化疗也有望为更多的晚期癌症患者奏响感动生命的乐章。, http://www.100md.com