黑便、鲜血便17年

病历摘要
患者,女,68岁;因“间断便血17年”入院。
患者于17年和12年前无诱因排黑色成形便,无呕血;当地医院查便潜血阳性,未予对症治疗,便潜血转阴。3年前病人自觉乏力、头晕,当地医院查Hb 70 g/L,便潜血阴性,胃镜检查未见异常,诊为“缺铁性贫血”,予补铁治疗,Hb升至108 g/L。2年前患者再次出现黑便,1~2次/d,不成形,行结肠镜检查未见异常,自服云南白药后大便颜色转黄。10天前患者出现鲜红色稀水样便,3次/d,伴头晕,当地医院查Hb 59 g/L,给予止血、抑酸、补液、输血治疗,便潜血转阴出院。因再次出现鲜红色稀水样便患者来我院急诊,查血常规WBC 3.46×109/L,RBC 4.18×1012/L,Hb 108g/L,Pkt 155×109/L;PT+A正常。发病以来病人体重无明显变化,否认类似疾病家族史,无高血压病、冠心病及糖尿病史。
入院查体:BP 100/60 mmHg,无肝掌、蜘蛛痣及皮肤毛细血管扩张,睑结膜略苍白,心肺未见异常,腹软,肝脾肋下未及,全腹无压痛和包块。肛门指诊指套有黑便。
 分析讨论
分析讨论患者老年女性,慢性病程达17年,表现为反复便血,未出现过呕血、反酸、腹痛,发作间期无大便性状改变,无肝病史,发病以来体重无明显变化。体格检查主要表现为贫血貌,肝脾无肿大,无腹水征,肛门指诊指套有黑便。消化道出血诊断明确,但需要明确出血的部位及病因。
便血的颜色取决于消化道出血的部位、出血量、出血速度及在胃肠道滞留的时间。上消化道及高位小肠出血多表现为呕血和黑便,如出血量较小可无呕血,仅仅表现为黑便,但如果出血量大、速度快,也可出现鲜血便。同样下消化道出血可出现鲜血便,或仅表现为黑便或便潜血阳性。本患者虽未呕血,但根据病史及每次情况并不能完全确定是单纯的上消化道出血还是下消化道出血,应进一步完善相关检查,明确出血的部位。
 病因方面:(1)消化性溃疡 本病在上消化道出血病因中居首位,且部分患者可以表现为无痛性出血,但该患者既往胃镜检查阴性,故此诊断难以解释疾病全貌。(2)食管-胃底静脉曲张破裂出血患者无慢性肝病病史及临床表现,查体无慢性肝病的体征,血白蛋白及PT+A正常,不支持此诊断。(3)药物相关性胃肠道黏膜损伤 患者既往无NSAID类药物服用史,故可排除。(4)缺血性肠病 无基础疾病,无典型的餐后腹痛症状,暂不考虑。(5)消化道肿瘤 老年女性,应当考虑到有无肿瘤方面的原因,但患者病史较长,一般状态较好,近期体重无明显变化,且发病间歇期便潜血为阴性。因此诊断消化道肿瘤的证据不足。(6)肠道血管畸形 患者老年女性,反复便血,每次便血量不等,无消化系统其他症状,一般情况好,尽管既往院外胃镜、结肠镜阴性,也应考虑到胃肠道血管畸形特别是小肠血管畸形的可能,本病可累及上、下消化道,入院后可安排胃镜、结肠镜,必要时进行胶囊内镜或小肠镜检查。
病因方面:(1)消化性溃疡 本病在上消化道出血病因中居首位,且部分患者可以表现为无痛性出血,但该患者既往胃镜检查阴性,故此诊断难以解释疾病全貌。(2)食管-胃底静脉曲张破裂出血患者无慢性肝病病史及临床表现,查体无慢性肝病的体征,血白蛋白及PT+A正常,不支持此诊断。(3)药物相关性胃肠道黏膜损伤 患者既往无NSAID类药物服用史,故可排除。(4)缺血性肠病 无基础疾病,无典型的餐后腹痛症状,暂不考虑。(5)消化道肿瘤 老年女性,应当考虑到有无肿瘤方面的原因,但患者病史较长,一般状态较好,近期体重无明显变化,且发病间歇期便潜血为阴性。因此诊断消化道肿瘤的证据不足。(6)肠道血管畸形 患者老年女性,反复便血,每次便血量不等,无消化系统其他症状,一般情况好,尽管既往院外胃镜、结肠镜阴性,也应考虑到胃肠道血管畸形特别是小肠血管畸形的可能,本病可累及上、下消化道,入院后可安排胃镜、结肠镜,必要时进行胶囊内镜或小肠镜检查。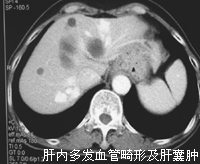 入院后实验室检查:血常规WBC(2.51~4.78)×109/L,Neu 58.9%,Hb 86~106 g/L,Pkt(145~215)×109/L。大便潜血多次阳性。肝肾功能正常。血氨51.1 μmok/L(11~35 μmok/L),ESR、CRP正常。PPD(-)。糖蛋白抗原CA199 、CA50、CEA、CA125及甲胎蛋白(AFP)均正常;自身免疫学指标阴性。
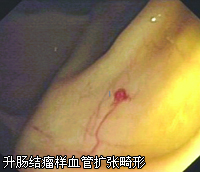
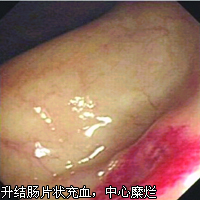
入院后实验室检查:血常规WBC(2.51~4.78)×109/L,Neu 58.9%,Hb 86~106 g/L,Pkt(145~215)×109/L。大便潜血多次阳性。肝肾功能正常。血氨51.1 μmok/L(11~35 μmok/L),ESR、CRP正常。PPD(-)。糖蛋白抗原CA199 、CA50、CEA、CA125及甲胎蛋白(AFP)均正常;自身免疫学指标阴性。胸腹X线片未见明显异常。口服小肠造影:十二指肠憩室。腹部B超:肝多发囊肿。胃镜:胃及十二指肠多发毛细血管扩张(图1)。结肠镜:结肠多发毛细血管扩张,可见小血管瘤样扩张病变(图2);升结肠起始部可见大小约1.2 cm×0.8 cm片状充血灶,中心可见糜烂(图3)。入院后给予止血、补铁治疗,并采用内镜下氩气血浆凝固(APC)方法治疗胃、十二指肠及结肠毛细血管畸形,过程顺利。复查大便潜血阴性,Hb 105 g/L,门诊随诊。
患者入院后经胃镜、结肠镜检查确诊为胃肠道多发血管畸形,可以解释患者反复消化道出血且表现为黑便间或暗红色血便的情况。
胃肠道血管畸形诊断方法有:(1)内镜检查对血管畸形的检出率较高,可定位、定性诊断部分消化道出血,常被作为首选的检查方法。(2)钡剂消化道造影检查可排除其他原因消化道出血,但对本病诊断价值不大。(3)ECT检查较敏感,但对于出血间歇期的病变检出率不高,且定位较差,不能明确病变的性质,从而限制了其诊断价值,可与内镜检查结合。(4)选择性血管造影:可显示肠道血管的形态、分布,可准确定位,在明确出血部位后,可采用血管内介入治疗。但该检查有创,有一定的并发症,故不能常规作为诊断首选;后两种检查对于毛细血管扩张敏感性均差。(5)对反复消化道出血而又不能明确诊断者,应尽早行剖腹探查,结合术中肠镜可明确出血的准确部位。治疗方面:(1)内镜治疗包括内镜下电凝、激光以及硬化剂注射等,安全方便,并发症少,且可反复进行。对手术后复发、手术禁忌者可考虑内镜下治疗。(2)手术切除病变部位,是最有效的治疗方法。对于出血不明显者可结合术中小肠镜检查以确定病变部位。(3)介入治疗具有快速、简便、疗效确切的优点,主要用于胃和十二指肠,不用于小肠和结肠,有引起肠梗死的可能性。至此,患者消化道出血的病因诊断似乎已经明确,但是我们又发现了另外一些有趣的资料。
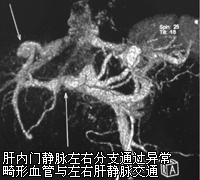
患者入院后为除外门脉高压症,行血管彩超:肝静脉三支显像正常,门静脉主干1.1 cm,左支1.2 cm,右支1.0 cm,流速44 cm/s,提示门静脉左支及矢状部稍宽;下腔静脉增强CT及门静脉、腔静脉CT三维血管重建显示,肝内多发血管畸形(图4);肝内门静脉左右分支主干通过异常畸形血管分别与左右肝静脉交通,门静脉右支分支与右肝静脉属支有交通畸形(图5);腹膜后血管畸形(脾静脉-左肾静脉交通畸形)(图6);腹部CT三维血管重建未见明显异常。
腹部影像学检查发现患者肝内及肝外门-腔分流畸形,结合患者肝功能正常,可除外门静脉血栓及肝硬化导致门脉高压症,考虑为先天性门静脉畸形。临床上常见的自发性门腔分流多继发于肝硬化、门脉高压,先天性门腔分流罕见。至2000年文献报道不到50例肝内型自发性门腔分流(SPVSs),其中大部分为肝硬化、门脉高压所致,先天因素导致者仅有个案报告。至2003年文献报告仅61例肝外型先天性门腔分流畸形(CEPS),亦称Abernethy畸形。
Watanabe于2000年将先天原因不明的门腔分流分为5型,Ⅰ型为肝内型即在肝内形成门静脉与肝静脉之间的分流(三个亚型:Ⅰa型系左右肝脏弥漫性分流交通支形成,Ⅰb型指仅在部分肝脏出现分流交通支,Ⅰc型为遗传性出血性毛细血管扩张症(Rendu-Osker-Weber病)出现肝内门腔分流畸形,又称混合型);Ⅱ型为肝内/肝外型,指门静脉发出迂曲的交通支穿过肝脏进入下腔静脉;Ⅲ型指肝外型即门静脉属支在进入肝脏前已有部分血流分流入下腔静脉及其分支;Ⅳ型为门脉高压表现合并Ⅲ型改变;Ⅴ型为门静脉缺如。先天门腔静脉分流患者多经查体发现,部分是由于出现肝性脑病而就诊,另有部分患者可出现消化道出血,但并无门脉高压症。该患者的诊断为先天性肝内/肝外门腔分流合并胃肠道毛细血管畸形,尚无文献报道。
 先天门腔分流畸形的诊断有血管造影、腹部CT、MRI及超声多普勒等手段,近年来随着多层螺旋CT(MSCT)的问世及血管三维重建技术(CTA及CTV)的应用推广,诊断手段趋于无创、准确,CTV诊断门腔分流方面尚无系统报道,应进一步积累经验指导临床诊断。先天门腔分流畸形的治疗尚无成熟经验,应控制饮食、密切随访,出现肝性脑病时对症处理。以往人们认为外科手术(包括肝移植)为唯一有效的根治方法,近年血管介入栓塞技术的开展为先天门腔分流畸形的治疗提供了新的思路。
先天门腔分流畸形的诊断有血管造影、腹部CT、MRI及超声多普勒等手段,近年来随着多层螺旋CT(MSCT)的问世及血管三维重建技术(CTA及CTV)的应用推广,诊断手段趋于无创、准确,CTV诊断门腔分流方面尚无系统报道,应进一步积累经验指导临床诊断。先天门腔分流畸形的治疗尚无成熟经验,应控制饮食、密切随访,出现肝性脑病时对症处理。以往人们认为外科手术(包括肝移植)为唯一有效的根治方法,近年血管介入栓塞技术的开展为先天门腔分流畸形的治疗提供了新的思路。点 评
作者在诊断了消化道出血的部位和病因后,又发现了新的令人感兴趣的资料,是什么呢?结合文献复习,作者发现这是1例自发性门腔分流伴消化道血管畸形的罕见病例。这一病例的诊断过程提示我们,在临床上只要细心观察,善于发现,就会得到更多的收获。 (刘晓红), http://www.100md.com