曲尼司特片芯缓释胶囊人体生物利用度研究
作者:董 皎 蒋雪涛 王振国△ 董志超 韩艳丽△ 辛益妹△
单位:
关键词:曲尼司特;生物利用度;缓释制剂
曲尼司特 曲尼司特(Tranilast)为新型抗变态反应药,是一种针对变态反应疾病发生机制的病因治疗性药。本品不同于对症治疗用药,它抑制肥大细胞脱颗粒,阻滞组胺等过敏反应介质的释放[1,2]。临床上主要用于治疗和预防支气管哮喘、过敏性鼻炎、过敏性皮炎等症。与一直视为首选药的色甘酸钠相比,其安全性高,不良反应少,可减少抗组胺药引起的嗜睡现象,因此,颇受重视和好评。但曲尼司特需日服3次,且往往在没有症状的情况下提前使用,给患者的工作和生活带来不便。我们根据曲尼司特的理化性质及药理作用特点,对其进行了缓释制剂的研究。本研究仅报道其人体生物利用度。
1 材料和方法
, 百拇医药
1.1 仪器与试药 HPLC仪991型 (美国 Waters公司),TGL-16G高速台式离心机 (上海医用分析仪器厂),MVS-1 旋涡混合器 (北京北德科学仪器有限公司),LDZ5-2低速自动平衡离心机 (北京医用离心机厂),WFZ800-D3 A 紫外分光光度计 (北京瑞利分析仪器厂),TDP单冲压片机 (中国制药机械厂),RC-6智能型药物溶出仪(天津医疗器械研究所)。曲尼司特原料药(中国药科大学),羧甲基淀粉钠 (台湾永日化学工业股份有限公司),羟丙基甲基纤维素(HPMC) K4m (Colorcon 公司),Carbopol 934p (Goodrich 公司),曲尼司特普通胶囊 (沈阳延风制药厂),甲醇和其他试剂均为分析纯。
1.2 缓释胶囊的制备 取曲尼司特与羧甲基淀粉钠适量,湿法制粒后,干燥压片,得速释片。取曲尼司特与HPMC和Carbopol 934p适量,干法制粒压片,得缓释片。将一定比例的两片芯填充于空芯胶囊中,制得曲尼司特片芯缓释胶囊 (每粒胶囊中片芯含药量相当于曲尼司特300 mg)。
, 百拇医药
1.3 体外溶出度测定
1.3.1 标准曲线、回收率与精密度 精密称取105℃恒质量后的曲尼司特适量置于100 ml量瓶中,加pH 7.3磷酸盐缓冲液至刻度,得到浓度为0.32 mg/ml的标准储备液;分别精密吸取此储备液0.10,0.20,0.30,0.40,0.50,0.60 ml置于25 ml量瓶中,加入无水乙醇0.50 ml,然后用磷酸盐缓冲液稀释至刻度,摇匀,在波长330 nm处测定光密度(D)。求得D对浓度c(μg/ml)的标准曲线为:D=0.0174+0.965 c(μg/ml), r=0.999(n=6)。用本法测定了0.982,4.910,6.547 μg/ml 3个浓度,每个浓度进行6次实验,其平均回收率为(99.64±0.40)%,日内RSD为2.63%,日间RSD为2.97%。
1.3.2 体外溶出度 参照中国药典1995年版二部附录66页规定的转篮法,测定条件参照部颁标准[3],37℃,150 r/min,于0.5,1,2,3,4,5,6,8,10 h取样,于330 nm波长处测定D值,累积释药百分率(%)分别为23.85,27.94,35.45,43.89,51.57,58.15,67.54,83.85,95.44。缓释胶囊体外溶出符合零级动力学过程,F=20.85+7.68 t,r=0.996。
, http://www.100md.com
1.4 血药浓度测定[4,5]
1.4.1 色谱条件 色谱柱:μBondapak,3.9 mm×30 cm; 保护柱: C18; 流动相:甲醇-KH2PO4 (60∶40,pH 4.2); 灵敏度:0.02 AUFS; 检测波长:330 nm; 流速:0.8 ml/min; 内标:硝基安定。内标与曲尼司特的保留时间分别为6.37和4.81 min。
1.4.2 标准曲线 取空白人血清200 μl, 分别加入相当于曲尼司特2.5, 5.0, 10.0, 20.0, 30.0, 40.0 μg/ml的标准液, 各加入内标液500 μl, 振荡均匀后, 1.5×104 r/min离心10 min, 取上清液用0.45 μm滤膜过滤, 取续滤液10 μl进样测定。 以曲尼司特与内标峰高之比对曲尼司特浓度(c)进行线性回归, 得标准曲线方程为: c=12.835H/Hi-1.303, (r=0.9996, n=6; H,Hi分别为曲尼司特和内标的峰高)。
, 百拇医药
1.4.3 回收率和精密度 取空白人血清分别加入曲尼司特标准液5.0,20.0,50.0 μg/ml,按标准曲线项下方法操作,测得方法的回收率分别为(104.40±6.12)%, (96.58±5.32)%,(100.08±3.21)%,(n=5); 日内差异 RSD=0.040% (n=5),日间差异RSD=0.050% (n=5)。
1.5 志愿者选择、给药方法、样本采集 10名健康志愿者,年龄18~20岁,平均年龄 (18.7±1.3)岁,体质量(63.2±5.0)kg,随机分成2组,空腹12 h,于清晨抽血后,单剂量交叉口服曲尼司特普通胶囊(100 mg×3) 和缓释胶囊(300 mg×1)。为保持胶囊外观一致,服药前将普通胶囊的内容物取出,放入与缓释胶囊同批号的空心胶囊中。两次服药间隔14 d,普通胶囊于服药后1,2,3,4,6,8,12,24 h,缓释胶囊于服药后1,2,3,4,6,8,10,12,14,24,36 h分别取血,分离血清,用HPLC法测定血药浓度。
, 百拇医药
2 结 果
2.1 血药浓度 10名志愿者口服单剂量曲尼司特普通胶囊和缓释胶囊300 mg后,平均血药浓度-时间曲线见图1。曲尼司特缓释胶囊血药水平明显比普通胶囊稳定,持续时间长,达到了良好的缓释效果。
采用3P87药代动力学程序,按一室模型拟合,计算缓释胶囊和普通胶囊的AUC分别为(392.26±71.72) 和 (372.21±85.77) μg*h/ml; 体内平均驻留时间(MRT)分别为17.00和 10.75 h,可见缓释胶囊的体内MRT显著长于普通胶囊,说明缓释效果良好。
2.2 生物利用度 根据公式计算缓释胶囊的相对生物利用度如下: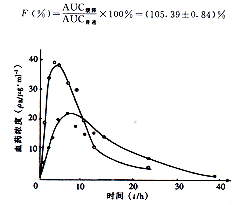
, http://www.100md.com
图 1 曲尼司特胶囊血药浓度-时间曲线
● 缓释胶囊; ○普通胶囊
2.3 体内外相关性试验 用Wagner-Nelson方法,由缓释胶囊血药浓度测定结果,计算各时间体内吸收百分率,对相应时间的体外溶出百分率作图,可得一直线,回归方程为Y=9.8025+78.123X(r=0.9019),两者呈显著线性相关。
3 讨 论
曲尼司特缓释胶囊体外释药2 h为35.45%,10 h为95.44%,持续释药时间达10 h以上,符合缓释制剂的要求;体内血药浓度平稳,持续时间长,达到了良好的控释效果,其生物利用度略高于普通胶囊。
曲尼司特缓释胶囊体内外试验结果有良好的相关性,说明所用溶出度测定方法及结果可作为处方筛选及产品质量控制的重要依据。
, http://www.100md.com
中国图书资料分类法分类号 R912
参 考 文 献
1 杨 玉. 曲尼司特治疗支气管哮喘和变应性鼻炎的临床对照试验. 新药与临床,1988,7(3):129
2 顾啸龙,李苏芹,王 虹,等. 口服曲尼司特和药代动力学研究. 南京医学院学报,1988,8(1):21
3 中华人民共和国卫生部. 曲尼司特. 部标准(试行),Ws-073(x-95)-92
4 Kohji T, Yoshimitsu Y, Isamu A, et al. High-performance liquid chromatographic determination of tranilast in plasma. Chromatographia,1985,341(1):228
5 王德华,于河舟,胡成久,等. 曲尼司特在人体内的药动学及生物利用度研究. 中国药学杂志,1996,31(11):670
(1998-01-04收稿, 1998-06-08修回), http://www.100md.com
单位:
关键词:曲尼司特;生物利用度;缓释制剂
曲尼司特 曲尼司特(Tranilast)为新型抗变态反应药,是一种针对变态反应疾病发生机制的病因治疗性药。本品不同于对症治疗用药,它抑制肥大细胞脱颗粒,阻滞组胺等过敏反应介质的释放[1,2]。临床上主要用于治疗和预防支气管哮喘、过敏性鼻炎、过敏性皮炎等症。与一直视为首选药的色甘酸钠相比,其安全性高,不良反应少,可减少抗组胺药引起的嗜睡现象,因此,颇受重视和好评。但曲尼司特需日服3次,且往往在没有症状的情况下提前使用,给患者的工作和生活带来不便。我们根据曲尼司特的理化性质及药理作用特点,对其进行了缓释制剂的研究。本研究仅报道其人体生物利用度。
1 材料和方法
, 百拇医药
1.1 仪器与试药 HPLC仪991型 (美国 Waters公司),TGL-16G高速台式离心机 (上海医用分析仪器厂),MVS-1 旋涡混合器 (北京北德科学仪器有限公司),LDZ5-2低速自动平衡离心机 (北京医用离心机厂),WFZ800-D3 A 紫外分光光度计 (北京瑞利分析仪器厂),TDP单冲压片机 (中国制药机械厂),RC-6智能型药物溶出仪(天津医疗器械研究所)。曲尼司特原料药(中国药科大学),羧甲基淀粉钠 (台湾永日化学工业股份有限公司),羟丙基甲基纤维素(HPMC) K4m (Colorcon 公司),Carbopol 934p (Goodrich 公司),曲尼司特普通胶囊 (沈阳延风制药厂),甲醇和其他试剂均为分析纯。
1.2 缓释胶囊的制备 取曲尼司特与羧甲基淀粉钠适量,湿法制粒后,干燥压片,得速释片。取曲尼司特与HPMC和Carbopol 934p适量,干法制粒压片,得缓释片。将一定比例的两片芯填充于空芯胶囊中,制得曲尼司特片芯缓释胶囊 (每粒胶囊中片芯含药量相当于曲尼司特300 mg)。
, 百拇医药
1.3 体外溶出度测定
1.3.1 标准曲线、回收率与精密度 精密称取105℃恒质量后的曲尼司特适量置于100 ml量瓶中,加pH 7.3磷酸盐缓冲液至刻度,得到浓度为0.32 mg/ml的标准储备液;分别精密吸取此储备液0.10,0.20,0.30,0.40,0.50,0.60 ml置于25 ml量瓶中,加入无水乙醇0.50 ml,然后用磷酸盐缓冲液稀释至刻度,摇匀,在波长330 nm处测定光密度(D)。求得D对浓度c(μg/ml)的标准曲线为:D=0.0174+0.965 c(μg/ml), r=0.999(n=6)。用本法测定了0.982,4.910,6.547 μg/ml 3个浓度,每个浓度进行6次实验,其平均回收率为(99.64±0.40)%,日内RSD为2.63%,日间RSD为2.97%。
1.3.2 体外溶出度 参照中国药典1995年版二部附录66页规定的转篮法,测定条件参照部颁标准[3],37℃,150 r/min,于0.5,1,2,3,4,5,6,8,10 h取样,于330 nm波长处测定D值,累积释药百分率(%)分别为23.85,27.94,35.45,43.89,51.57,58.15,67.54,83.85,95.44。缓释胶囊体外溶出符合零级动力学过程,F=20.85+7.68 t,r=0.996。
, http://www.100md.com
1.4 血药浓度测定[4,5]
1.4.1 色谱条件 色谱柱:μBondapak,3.9 mm×30 cm; 保护柱: C18; 流动相:甲醇-KH2PO4 (60∶40,pH 4.2); 灵敏度:0.02 AUFS; 检测波长:330 nm; 流速:0.8 ml/min; 内标:硝基安定。内标与曲尼司特的保留时间分别为6.37和4.81 min。
1.4.2 标准曲线 取空白人血清200 μl, 分别加入相当于曲尼司特2.5, 5.0, 10.0, 20.0, 30.0, 40.0 μg/ml的标准液, 各加入内标液500 μl, 振荡均匀后, 1.5×104 r/min离心10 min, 取上清液用0.45 μm滤膜过滤, 取续滤液10 μl进样测定。 以曲尼司特与内标峰高之比对曲尼司特浓度(c)进行线性回归, 得标准曲线方程为: c=12.835H/Hi-1.303, (r=0.9996, n=6; H,Hi分别为曲尼司特和内标的峰高)。
, 百拇医药
1.4.3 回收率和精密度 取空白人血清分别加入曲尼司特标准液5.0,20.0,50.0 μg/ml,按标准曲线项下方法操作,测得方法的回收率分别为(104.40±6.12)%, (96.58±5.32)%,(100.08±3.21)%,(n=5); 日内差异 RSD=0.040% (n=5),日间差异RSD=0.050% (n=5)。
1.5 志愿者选择、给药方法、样本采集 10名健康志愿者,年龄18~20岁,平均年龄 (18.7±1.3)岁,体质量(63.2±5.0)kg,随机分成2组,空腹12 h,于清晨抽血后,单剂量交叉口服曲尼司特普通胶囊(100 mg×3) 和缓释胶囊(300 mg×1)。为保持胶囊外观一致,服药前将普通胶囊的内容物取出,放入与缓释胶囊同批号的空心胶囊中。两次服药间隔14 d,普通胶囊于服药后1,2,3,4,6,8,12,24 h,缓释胶囊于服药后1,2,3,4,6,8,10,12,14,24,36 h分别取血,分离血清,用HPLC法测定血药浓度。
, 百拇医药
2 结 果
2.1 血药浓度 10名志愿者口服单剂量曲尼司特普通胶囊和缓释胶囊300 mg后,平均血药浓度-时间曲线见图1。曲尼司特缓释胶囊血药水平明显比普通胶囊稳定,持续时间长,达到了良好的缓释效果。
采用3P87药代动力学程序,按一室模型拟合,计算缓释胶囊和普通胶囊的AUC分别为(392.26±71.72) 和 (372.21±85.77) μg*h/ml; 体内平均驻留时间(MRT)分别为17.00和 10.75 h,可见缓释胶囊的体内MRT显著长于普通胶囊,说明缓释效果良好。
2.2 生物利用度 根据公式计算缓释胶囊的相对生物利用度如下:

, http://www.100md.com
图 1 曲尼司特胶囊血药浓度-时间曲线
● 缓释胶囊; ○普通胶囊
2.3 体内外相关性试验 用Wagner-Nelson方法,由缓释胶囊血药浓度测定结果,计算各时间体内吸收百分率,对相应时间的体外溶出百分率作图,可得一直线,回归方程为Y=9.8025+78.123X(r=0.9019),两者呈显著线性相关。
3 讨 论
曲尼司特缓释胶囊体外释药2 h为35.45%,10 h为95.44%,持续释药时间达10 h以上,符合缓释制剂的要求;体内血药浓度平稳,持续时间长,达到了良好的控释效果,其生物利用度略高于普通胶囊。
曲尼司特缓释胶囊体内外试验结果有良好的相关性,说明所用溶出度测定方法及结果可作为处方筛选及产品质量控制的重要依据。
, http://www.100md.com
中国图书资料分类法分类号 R912
参 考 文 献
1 杨 玉. 曲尼司特治疗支气管哮喘和变应性鼻炎的临床对照试验. 新药与临床,1988,7(3):129
2 顾啸龙,李苏芹,王 虹,等. 口服曲尼司特和药代动力学研究. 南京医学院学报,1988,8(1):21
3 中华人民共和国卫生部. 曲尼司特. 部标准(试行),Ws-073(x-95)-92
4 Kohji T, Yoshimitsu Y, Isamu A, et al. High-performance liquid chromatographic determination of tranilast in plasma. Chromatographia,1985,341(1):228
5 王德华,于河舟,胡成久,等. 曲尼司特在人体内的药动学及生物利用度研究. 中国药学杂志,1996,31(11):670
(1998-01-04收稿, 1998-06-08修回), http://www.100md.com