模拟失重引起的大鼠基底动脉收缩反应性增强*
作者:张乐宁 马进 张立藩
单位:第四军医大学航空生理学教研室,西安 710032
关键词:大鼠;失重模拟;基底动脉;血管反应性;血管收缩
航天医学与医学工程990103 摘要:目的 为了阐明模拟失重是否引起头部的动脉血管,如基底动脉的收缩反应性增强。方法 采用尾部悬吊大鼠模型模拟失重影响,利用离体基底动脉血管环制备测定其对几种血管收缩剂反应性的变化。结果 悬吊4wk组大鼠的基底动脉血管环对KCl[(10~100) mmol/L]、精氨酸加压素[(10-15~10-7)mol/L]或5-羟色胺[(10-12~10-4)mol/L]的等长收缩反应较同步对照组均显著升高。两组大鼠基底动脉血管环对上述血管收缩剂收缩反应的EC50值无显著差别。结论 为期4 wk的模拟失重可使大鼠头部的血管,如基底动脉的收缩反应性显著增强。上述结果对“脑血管性晕厥始动机制”假说是一个有力的支持。
, http://www.100md.com
中图分类号:R852.22 文献标识码:A 文章编号:1002-0837(1999)01-0010-04
Vasoconstrictor Responsiveness of Rat Basilar Artery Enhanced by Simulated Weightlessness
ZHANG Le-ning
(Department of Aerospace Physiology,The Fourth Military Medical University,Xi'an 710032,China)
MA Jin,ZHANG Li-fan
Abstract:Objective To investigate the effects of simulated weightlessness on contractile responsiveness of the basilar artery.Methods Rats were subjected to tail-suspension for 4-wk to simulate the effect of weightlessness,responses of perfused isolated basilar arterial rings to various vasoactive compounds were examined.Results Maximal isometric contractile responses to KCl [(10~100)mmol/L],arginine vasopressin[AVP,(10-15~10-7)mol/L],or 5-hydroxytryptamine [5-HT,(10-12~10-4)mol/L] were significantly enhanced in arterial rings isolated from 4-wk tail-suspended as compared with that from simultaneous control rats.Conclusion These results indicate that medium-term simulated weightlessness may result in an enhanced contractile responsiveness in rat basilar artery,and strongly support the hypothesis of cerebrovascular syncope-initiating mechanism.
, 百拇医药
Key words:rats;weightlessness simulation;basilar artery;vasoreactivity;vasoconstriction
航天返回地面后,航天员在立位应激作用下(如站立、头高位倾斜、下体负压)普遍出现心血管失调及立位耐力下降。对这一问题的研究一直受到重视[1~3]。现普遍认为,飞行后立位耐力降低的发生涉及多重机制[1]。除已被阐明的血量减少基本原因外,近年还提出血管机制的重要性不容忽视[3,4]。有的作者根据其人体实验结果又进一步提出,微重力下脑血管的适应性改变也可能是造成飞行后心血管失调的主要原因之一,并提出了“脑血管晕厥始动机制”假说[2]。我实验室近年的工作则发现:模拟失重可引起大鼠不同部位动脉血管发生性质相反的结构重塑变化。在身体后部,可引起萎缩性改变;在头部,则见出现肥大性变化[4]。还观察到模拟失重可引起大鼠后身动脉/小动脉的收缩反应性普遍降低现象[4]。模拟失重下,脑血管是否会发生收缩反应性增高引起我们极大兴趣。如得证实,则对“脑血管晕厥始动机制”假说不啻为一支持。本文采用离体血管环技术观察了4周尾部悬吊大鼠基底动脉收缩反应性的变化结果。
, 百拇医药
方 法
动物模型 选取雄性SD大鼠20只(由第四军医大学动物中心提供),体重200 g左右。先饲养1周后,再按体重配对原则随机分为对照与悬吊组,每组10只。尾部悬吊采用陈杰等改进的方法[7]。两组动物在相同条件下饲养,室温(23±2)℃,每日光照12 h。动物饲养与实验遵守第四军医大学实验动物有关规定进行。
血管反应性测定 悬吊4周后,在同一实验日同时对悬吊与对照大鼠进行实验。用戊巴比妥钠(腹腔内注射,50 mg/kg)将尾部悬吊与同步对照大鼠麻醉,放血处死,断头取出脑干部,置于Krebs液中。在体视显微镜下分离基底动脉(basilar artery),去除周围结缔组织,于近Willis环段取下长约4 mm的血管环,将两根外径75 μm的不锈钢丝穿过血管环,并借与细钢丝相连的挂钩将其悬挂于盛有10 ml Krebs液的恒温浴槽内。Krebs液用95%O2及5%CO2混合气充分氧合,浴槽内液体温度(37.2±1)℃。血管环在浴槽中平衡1 h。在此过程中,以40 mg的步幅,逐步将血管环张力拉至200 mg。此后的实验即在此预负荷条件下进行。不同试剂实验之间均间隔40min,以洗脱前一试剂的影响。平衡过程中,每隔15 min换一次液体;洗脱过程中,每隔5 min换一次液体。收缩反应性通过测定动脉环对10~100 mmol/L氯化钾(KCl) 、(10-15~10-7)mol/L精氨酸加压素(AVP)或(10-12~10-4)mol/L 5-羟色胺(5-HT) 的等长收缩反应测得。由浓度-效应关系进一步求出EC50值,即反应达50%最大效应时血管激动剂的浓度,以表示血管对激动剂的敏感性。
, 百拇医药
大鼠体重结果以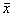 ±s表示,其余实验数据以
±s表示,其余实验数据以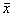 ±s
±s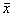 表示,用配对t检验作统计学分析,以P<0.05为差别显著的界限。
表示,用配对t检验作统计学分析,以P<0.05为差别显著的界限。
结 果
实验期间动物生长情况良好。实验开始前,对照组与模拟失重组大鼠的体重(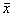 ±s)分别为(343.6±8.2)g与(346.7±7.5)g。4周后,两组体重已分别增长至(397.7±12.5)g与(384.7±10.2)g;两组间无显著差别(P>0.05)。
±s)分别为(343.6±8.2)g与(346.7±7.5)g。4周后,两组体重已分别增长至(397.7±12.5)g与(384.7±10.2)g;两组间无显著差别(P>0.05)。
大鼠基底动脉血管环对KCl、AVP及5-HT的反应分别如图1、图2及图3所示,悬吊大鼠基底动脉环的收缩张力在多个浓度点均显著高于对照大鼠(P<0.05)。悬吊大鼠与对照大鼠对KCl收缩反应的EC50分别是(32.16±9.42)mmol/L和(28.54±6.87)mmol/L;对AVP收缩反应的EC50分别是(13.57±0.25)[-log(mol/L)]和(12.92±0.49)[-log(mol/L)];对5-HT收缩反应的EC50分别是(8.30±0.63)[-log(mol/L)]和(7.82±0.23)[-log(mol/L)]。各组间均无显著差别。
, 百拇医药
图1 基底动脉环对氯化钾的等长收缩反应
Fig.1 Isometric contraction responses(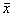 ±s
±s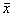 ) of basilar arterial rings to KCl
) of basilar arterial rings to KCl 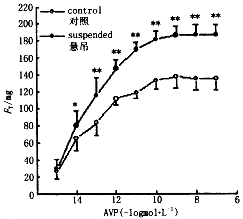
图2 基底动脉环对精氨酸加压素的等长收缩反应
Fig.2 Isomertric contraction responses of basilar arterial rings to AVP
, 百拇医药
图3 基底动脉环对5-羟色胺的等长收缩反应
Fig.3 Isometric contraction responses of basilar arterial rings to 5-HT
讨 论
本实验之目的在于检验模拟失重是否可引起头部血管的收缩反应性增强。以基底动脉环进行实验,我们果然观察到4周尾部悬吊已引起大鼠基底动脉对KCl、AVP或5-HT的收缩反应都较对照组显著升高。于是,我们不仅已观察到模拟失重下脑部血管的肥大性结构重塑和血管周围神经支配增强变化[4],且证实其收缩反应性也是增强的。
血管平滑肌的收缩张力与多个环节有关。在本工作中,无论受体介导(AVP、5-HT)还是非受体介导(KCl)的收缩反应均显著增强,提示收缩装置的改变可能是共同的原因。根据形态学研究结果,收缩蛋白数量增多可能是重要原因之一。至于其细节,则尚有待进一步阐明。
, http://www.100md.com
任何组织均能以其特有的方式对持续性的局部活动及/或负荷变化发生结构和功能性的适应改变。真实/模拟失重下,骨骼肌肉系统的适应性结构重塑变化表现最为明显,心血管系统自也不应例外。任何持续的动脉血压增高/降低皆将导致血管壁的肥大/萎缩,而平均血管内径将分别减小/增大。在高血压时,较小动脉或小动脉会出现平滑肌细胞增生、肥大,血管管壁增厚,血管壁厚与管径之比提高。这种改变可导致血管的收缩反应性增强;并具有“结构性放大器”的作用,使血压升高[6]。模拟失重时,脑部动脉血管的跨壁压力持续升高可能既是造成脑血管肥大性重塑及收缩反应性增强的始动原因。推想在真实失重下,人的脑血管也应有类似改变发生。当然其发生时程可能尚有所不同,因人的代谢率较低。
近年的一些发现均提出,血管机制在飞行后立位耐力不良发生中的重要性不容忽视[1~4]。对航天员飞行后的观察结果[1~3],以及动物模拟失重研究结果[4]均提示,真实或模拟失重所引起的身体下部/后部动脉血管结构与功能的变化,可能是导致飞行后立位耐力不良的重要原因之一。然而,还有一些证据表明,失重时脑血管的适应性变化则可能是加重飞行后立位心血管失调的另一种血管机制[3]。其主要依据有:飞行后进行30°HDT试验可引起航天员脑血管发生较飞行前强烈的收缩反应,且微重力暴露时间越长,影响也越加严重,恢复时间也越长(Gazenko等,1981):在LBNP、HUT耐力试验中可见到先发生脑部缺血再出现晕厥前心血管反应的现象。最近在地面研究中已观察到2周卧床后下肢肌肉交感神经发放(MSNA)减弱与脑循环自体调节减弱(根据对血压与脑血流信号的相干分析等)的证据[2]。我室先前的工作已发现:模拟失重可引起大鼠脑血管出现肥大性结构重塑及神经支配增强的变化[4]。本工作则首次证实模拟失重还可引起脑血管的收缩反应性增强。故我们关于模拟失重下脑血管结构与功能变化的发现对于“脑血管晕厥始动机制”[2]假说也是一个有力的支持。此外,Baylis等报道,模拟失重被试者晕厥前的血浆加压素浓度较正常升高300倍,可使脑缺血程度进一步加重,进而导致晕厥[2]。
, http://www.100md.com
总之,本工作发现4周模拟失重已可引起大鼠基底动脉的收缩反应性显著升高。此结果进一步提示,失重导致的脑血管结构与功能的适应性变化在航天后立位耐力不良的发生机理中可能有着重要的作用。
*基金项目:国家自然科学基金资助项目(39380021)
[参考文献]
[1] Blomqvist CG,Buckey JC,Gaffney FA et al.Mechanism of post-flight orthostatic intolerance[J].J Gravitational Physiol,1994,1(1):122~124
[2] Watenpaugh DE,AR Hargens.The cardiovascular system in microgravity[M].In: Fregly MJ and CM Blattis,eds.Handbook of Physiology: Environmental Physiology.New York:Oxford University Press,1996:631~674
, 百拇医药
[3] 张立藩.微重力心血管生理研究的回顾与展望[J].航天医学与医学工程,1998,11(5):378~382
[4] Zhang LF,Ma J,Mao QW et al.Plasticitiy of arterial vasculature during simulated weightlessness and its possible role in the genesis of postflight orthostatic intolerance[J].J Gravitational Physiology,1997,4(2)97~100
[5] Folkow B.Structure and function of the arteries in hypertension[J].Am J Physiol,1987,114:938~948
[6] Mulvany MJ.The structure of the resistance vasculatuer in essential hypertension[J].J Hypertens,1987,5: 129~136
[7] 陈 杰,马 进,丁兆平等.一种模拟失重影响的大鼠尾部悬吊模型[J].空间科学学报,1993,13:159~162
收稿日期:1998-04-20, http://www.100md.com
单位:第四军医大学航空生理学教研室,西安 710032
关键词:大鼠;失重模拟;基底动脉;血管反应性;血管收缩
航天医学与医学工程990103 摘要:目的 为了阐明模拟失重是否引起头部的动脉血管,如基底动脉的收缩反应性增强。方法 采用尾部悬吊大鼠模型模拟失重影响,利用离体基底动脉血管环制备测定其对几种血管收缩剂反应性的变化。结果 悬吊4wk组大鼠的基底动脉血管环对KCl[(10~100) mmol/L]、精氨酸加压素[(10-15~10-7)mol/L]或5-羟色胺[(10-12~10-4)mol/L]的等长收缩反应较同步对照组均显著升高。两组大鼠基底动脉血管环对上述血管收缩剂收缩反应的EC50值无显著差别。结论 为期4 wk的模拟失重可使大鼠头部的血管,如基底动脉的收缩反应性显著增强。上述结果对“脑血管性晕厥始动机制”假说是一个有力的支持。
, http://www.100md.com
中图分类号:R852.22 文献标识码:A 文章编号:1002-0837(1999)01-0010-04
Vasoconstrictor Responsiveness of Rat Basilar Artery Enhanced by Simulated Weightlessness
ZHANG Le-ning
(Department of Aerospace Physiology,The Fourth Military Medical University,Xi'an 710032,China)
MA Jin,ZHANG Li-fan
Abstract:Objective To investigate the effects of simulated weightlessness on contractile responsiveness of the basilar artery.Methods Rats were subjected to tail-suspension for 4-wk to simulate the effect of weightlessness,responses of perfused isolated basilar arterial rings to various vasoactive compounds were examined.Results Maximal isometric contractile responses to KCl [(10~100)mmol/L],arginine vasopressin[AVP,(10-15~10-7)mol/L],or 5-hydroxytryptamine [5-HT,(10-12~10-4)mol/L] were significantly enhanced in arterial rings isolated from 4-wk tail-suspended as compared with that from simultaneous control rats.Conclusion These results indicate that medium-term simulated weightlessness may result in an enhanced contractile responsiveness in rat basilar artery,and strongly support the hypothesis of cerebrovascular syncope-initiating mechanism.
, 百拇医药
Key words:rats;weightlessness simulation;basilar artery;vasoreactivity;vasoconstriction
航天返回地面后,航天员在立位应激作用下(如站立、头高位倾斜、下体负压)普遍出现心血管失调及立位耐力下降。对这一问题的研究一直受到重视[1~3]。现普遍认为,飞行后立位耐力降低的发生涉及多重机制[1]。除已被阐明的血量减少基本原因外,近年还提出血管机制的重要性不容忽视[3,4]。有的作者根据其人体实验结果又进一步提出,微重力下脑血管的适应性改变也可能是造成飞行后心血管失调的主要原因之一,并提出了“脑血管晕厥始动机制”假说[2]。我实验室近年的工作则发现:模拟失重可引起大鼠不同部位动脉血管发生性质相反的结构重塑变化。在身体后部,可引起萎缩性改变;在头部,则见出现肥大性变化[4]。还观察到模拟失重可引起大鼠后身动脉/小动脉的收缩反应性普遍降低现象[4]。模拟失重下,脑血管是否会发生收缩反应性增高引起我们极大兴趣。如得证实,则对“脑血管晕厥始动机制”假说不啻为一支持。本文采用离体血管环技术观察了4周尾部悬吊大鼠基底动脉收缩反应性的变化结果。
, 百拇医药
方 法
动物模型 选取雄性SD大鼠20只(由第四军医大学动物中心提供),体重200 g左右。先饲养1周后,再按体重配对原则随机分为对照与悬吊组,每组10只。尾部悬吊采用陈杰等改进的方法[7]。两组动物在相同条件下饲养,室温(23±2)℃,每日光照12 h。动物饲养与实验遵守第四军医大学实验动物有关规定进行。
血管反应性测定 悬吊4周后,在同一实验日同时对悬吊与对照大鼠进行实验。用戊巴比妥钠(腹腔内注射,50 mg/kg)将尾部悬吊与同步对照大鼠麻醉,放血处死,断头取出脑干部,置于Krebs液中。在体视显微镜下分离基底动脉(basilar artery),去除周围结缔组织,于近Willis环段取下长约4 mm的血管环,将两根外径75 μm的不锈钢丝穿过血管环,并借与细钢丝相连的挂钩将其悬挂于盛有10 ml Krebs液的恒温浴槽内。Krebs液用95%O2及5%CO2混合气充分氧合,浴槽内液体温度(37.2±1)℃。血管环在浴槽中平衡1 h。在此过程中,以40 mg的步幅,逐步将血管环张力拉至200 mg。此后的实验即在此预负荷条件下进行。不同试剂实验之间均间隔40min,以洗脱前一试剂的影响。平衡过程中,每隔15 min换一次液体;洗脱过程中,每隔5 min换一次液体。收缩反应性通过测定动脉环对10~100 mmol/L氯化钾(KCl) 、(10-15~10-7)mol/L精氨酸加压素(AVP)或(10-12~10-4)mol/L 5-羟色胺(5-HT) 的等长收缩反应测得。由浓度-效应关系进一步求出EC50值,即反应达50%最大效应时血管激动剂的浓度,以表示血管对激动剂的敏感性。
, 百拇医药
大鼠体重结果以
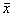 ±s表示,其余实验数据以
±s表示,其余实验数据以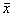 ±s
±s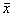 表示,用配对t检验作统计学分析,以P<0.05为差别显著的界限。
表示,用配对t检验作统计学分析,以P<0.05为差别显著的界限。结 果
实验期间动物生长情况良好。实验开始前,对照组与模拟失重组大鼠的体重(
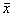 ±s)分别为(343.6±8.2)g与(346.7±7.5)g。4周后,两组体重已分别增长至(397.7±12.5)g与(384.7±10.2)g;两组间无显著差别(P>0.05)。
±s)分别为(343.6±8.2)g与(346.7±7.5)g。4周后,两组体重已分别增长至(397.7±12.5)g与(384.7±10.2)g;两组间无显著差别(P>0.05)。大鼠基底动脉血管环对KCl、AVP及5-HT的反应分别如图1、图2及图3所示,悬吊大鼠基底动脉环的收缩张力在多个浓度点均显著高于对照大鼠(P<0.05)。悬吊大鼠与对照大鼠对KCl收缩反应的EC50分别是(32.16±9.42)mmol/L和(28.54±6.87)mmol/L;对AVP收缩反应的EC50分别是(13.57±0.25)[-log(mol/L)]和(12.92±0.49)[-log(mol/L)];对5-HT收缩反应的EC50分别是(8.30±0.63)[-log(mol/L)]和(7.82±0.23)[-log(mol/L)]。各组间均无显著差别。

, 百拇医药
图1 基底动脉环对氯化钾的等长收缩反应
Fig.1 Isometric contraction responses(
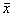 ±s
±s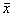 ) of basilar arterial rings to KCl
) of basilar arterial rings to KCl 
图2 基底动脉环对精氨酸加压素的等长收缩反应
Fig.2 Isomertric contraction responses of basilar arterial rings to AVP

, 百拇医药
图3 基底动脉环对5-羟色胺的等长收缩反应
Fig.3 Isometric contraction responses of basilar arterial rings to 5-HT
讨 论
本实验之目的在于检验模拟失重是否可引起头部血管的收缩反应性增强。以基底动脉环进行实验,我们果然观察到4周尾部悬吊已引起大鼠基底动脉对KCl、AVP或5-HT的收缩反应都较对照组显著升高。于是,我们不仅已观察到模拟失重下脑部血管的肥大性结构重塑和血管周围神经支配增强变化[4],且证实其收缩反应性也是增强的。
血管平滑肌的收缩张力与多个环节有关。在本工作中,无论受体介导(AVP、5-HT)还是非受体介导(KCl)的收缩反应均显著增强,提示收缩装置的改变可能是共同的原因。根据形态学研究结果,收缩蛋白数量增多可能是重要原因之一。至于其细节,则尚有待进一步阐明。
, http://www.100md.com
任何组织均能以其特有的方式对持续性的局部活动及/或负荷变化发生结构和功能性的适应改变。真实/模拟失重下,骨骼肌肉系统的适应性结构重塑变化表现最为明显,心血管系统自也不应例外。任何持续的动脉血压增高/降低皆将导致血管壁的肥大/萎缩,而平均血管内径将分别减小/增大。在高血压时,较小动脉或小动脉会出现平滑肌细胞增生、肥大,血管管壁增厚,血管壁厚与管径之比提高。这种改变可导致血管的收缩反应性增强;并具有“结构性放大器”的作用,使血压升高[6]。模拟失重时,脑部动脉血管的跨壁压力持续升高可能既是造成脑血管肥大性重塑及收缩反应性增强的始动原因。推想在真实失重下,人的脑血管也应有类似改变发生。当然其发生时程可能尚有所不同,因人的代谢率较低。
近年的一些发现均提出,血管机制在飞行后立位耐力不良发生中的重要性不容忽视[1~4]。对航天员飞行后的观察结果[1~3],以及动物模拟失重研究结果[4]均提示,真实或模拟失重所引起的身体下部/后部动脉血管结构与功能的变化,可能是导致飞行后立位耐力不良的重要原因之一。然而,还有一些证据表明,失重时脑血管的适应性变化则可能是加重飞行后立位心血管失调的另一种血管机制[3]。其主要依据有:飞行后进行30°HDT试验可引起航天员脑血管发生较飞行前强烈的收缩反应,且微重力暴露时间越长,影响也越加严重,恢复时间也越长(Gazenko等,1981):在LBNP、HUT耐力试验中可见到先发生脑部缺血再出现晕厥前心血管反应的现象。最近在地面研究中已观察到2周卧床后下肢肌肉交感神经发放(MSNA)减弱与脑循环自体调节减弱(根据对血压与脑血流信号的相干分析等)的证据[2]。我室先前的工作已发现:模拟失重可引起大鼠脑血管出现肥大性结构重塑及神经支配增强的变化[4]。本工作则首次证实模拟失重还可引起脑血管的收缩反应性增强。故我们关于模拟失重下脑血管结构与功能变化的发现对于“脑血管晕厥始动机制”[2]假说也是一个有力的支持。此外,Baylis等报道,模拟失重被试者晕厥前的血浆加压素浓度较正常升高300倍,可使脑缺血程度进一步加重,进而导致晕厥[2]。
, http://www.100md.com
总之,本工作发现4周模拟失重已可引起大鼠基底动脉的收缩反应性显著升高。此结果进一步提示,失重导致的脑血管结构与功能的适应性变化在航天后立位耐力不良的发生机理中可能有着重要的作用。
*基金项目:国家自然科学基金资助项目(39380021)
[参考文献]
[1] Blomqvist CG,Buckey JC,Gaffney FA et al.Mechanism of post-flight orthostatic intolerance[J].J Gravitational Physiol,1994,1(1):122~124
[2] Watenpaugh DE,AR Hargens.The cardiovascular system in microgravity[M].In: Fregly MJ and CM Blattis,eds.Handbook of Physiology: Environmental Physiology.New York:Oxford University Press,1996:631~674
, 百拇医药
[3] 张立藩.微重力心血管生理研究的回顾与展望[J].航天医学与医学工程,1998,11(5):378~382
[4] Zhang LF,Ma J,Mao QW et al.Plasticitiy of arterial vasculature during simulated weightlessness and its possible role in the genesis of postflight orthostatic intolerance[J].J Gravitational Physiology,1997,4(2)97~100
[5] Folkow B.Structure and function of the arteries in hypertension[J].Am J Physiol,1987,114:938~948
[6] Mulvany MJ.The structure of the resistance vasculatuer in essential hypertension[J].J Hypertens,1987,5: 129~136
[7] 陈 杰,马 进,丁兆平等.一种模拟失重影响的大鼠尾部悬吊模型[J].空间科学学报,1993,13:159~162
收稿日期:1998-04-20, http://www.100md.com