Ѫ����Ƥ�������ӻ�������֫�嶯����������ʵ���о�
���ߣ�ʢ�ٻ� ���Ӣ �ܰ��� ��� ���� ��� ��С�� ţ��� ������ �¹�� ����
��λ��100083 ����ҽ�ƴ�ѧ��Ѫ���о���
�ؼ��ʣ������Ʒ�����Ƥ�������ӣ�����Ѫ�ܼ���
�л�ҽѧ��־990216 ��ժҪ�� Ŀ�� ��֤Ѫ����Ƥ��������(VEGF)��������֫�嶯������������Ч�ԺͰ�ȫ�ԡ����� ��������VEGF�������˱�������pcD2/VEGF����Ч�����飺�Ʊ�֫�嶯���������ĺ�ģ�ͣ�ͨ�����������߷��ͼ��ڶ��ע�䷨����VEGF��������ת����������������ȫ�����飺�������������Ƽ�����VEGF����ֱ���5ֻС��(1 000 ��g��ΪС�����Ƽ���20 ��g��50��)��10ֻ����(2 000 ��g��Ϊ���Ƽ�����10��)��5ֻ��(2 000 ��g�����Ƽ���)���ڹ۲��䶾�����ã�������PCR���ͼ��ELISA�����з����Ŵ�ѧ������ѧ����������� תVEGF�����1��Ѫ����Ӱ����ʾ�������㸽���н϶��ӯСѪ�ܣ�Զ�˶�����ʼ��ӯ��2��ʱ��Ϊ���ԣ�1�º�����СѪ����Ϊ�ḻ���ɼ�Զ�˶������Գ�ӯ��Ѫ�ܼ�����ʾVEGF��(1��ʱ5/100 cm2��1��12/100 cm2)���Զ��ڶ�����(1��1/100 cm2��1��4/100 cm2)�������ȼ�飬֤��VEGF����Ը������ܵ�������Ӱ�죬δ�����������������仯�������VEGF������ھֲ�������֯�б���4�������ϣ����ۼ�������������֯������ѭ��������������� �����VEGF��������֫�嶯������������Ч�Ͱ�ȫ�ģ�ͨ��ҩ���������ٴ����顣
, ��Ĵҽҩ
Vascular endothelial growth factor gene therapy for peripheral artery disease��experimental study SHENG Qinhui, ZHU Guoying, ZHOU Airu, et al. Institute of Cardiovascular Research, Beijing Medical University, Beijing 100083
��Abstract�� Objective To Study experimentally VEGF gene for treatment of peripheral artery disease.Methods The human VEGF cDNA was cloned into the eukaryotic expression vector pcD2.Using gene suture, the recombinant plasmid was transferred into the hindlimbs�� adductor of Rhesus monkey, of which the distal end of the external iliac arteries were ligated and the femoral arteries were completely excised. With angiography, the biological effect of VEGF gene in experimental animals was investigated. Safey tests were analyzed by transferring of VEGF into mouse, rat, and Rhesus monkey, evaluated by biochemistry analysis, histopathological examination, PCR, and indirect ELISA.Results The transfer of VEGF gene stimulated the formation of focal microvessels, established collateral circulation, and augmented blood perfusion. The system had no adverse effect and remarkable pathological change in mouse, rat, and Rhesus monkey.Conclusion The experimental studies indicated that VEGF would be effective and safe for clinical trial after approval.
, http://www.100md.com
��Key words�� Gene therapy Endothelial growth factor Peripheral vascular diseases
(Natl Med J China, 1999,79:129-132)
֫�嶯����������һ�����ص�Ѫ�ܲ���Ŀǰ������Ч���Ʒ������������н�֫������Ԥ��ܲ�[1]����ˣ��о��µ����Ʒ�����Ϊ���С����������й�����������Ѫ����Ƥ��������(VEGF)�����Ʊ��ɻ�����ߣ�֤������Ч�ٽ�����Ѫ�ܵIJ�֧ѭ����ͨ��С����ļ����Զ����������飬�������ƻ�����ȫ�������ٴ������Ҫ��
���Ϻͷ���
һ������
1.����VEGF����������Ϊ��һ�����VEGF�ı���Ч�ʣ������ҹ�����pcDNA��3/VEGF����[2]�پ�BamHI��XbaI����������ͬ��ø�е�pcD2��Ч��˱������壬������pcD2/VEGF����������Ŀ�Ļ���Ϊ�ɱ���121���������VEGF121�������ź������У�����·����ͼ1�����ü��ѽⷨ��ȡ��������PEG-8000����������ˮ���á�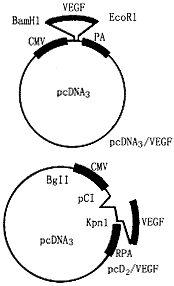
, http://www.100md.com
ͼ1 pcD2/VEGF�����Ĺ��� 2.VEGF������ߺͻ���ת�ƣ���һ�����ȵ�2��ҽ�÷���߽���������1%�㾫����ע��Һ�У����ɣ�������Σ�ֱ���㾫������Һȫ�������ڷ����ϣ��ٷ���ͿĨ�����������������ɺ��ã����ϲ���ȫ���������ڽ��С����ڻ���ת�Ʋ��ü����ڻ�����߷��ͼ����ڶ��ע�䷨��
3.֫�嶯������������ģ�ͣ��������Ժ�Ӻ�5ֻ������4��5 kg�����й�ҽѧ��ѧԺ�����������ṩ��Ӧ�ü���ע���Ȱ�ͪ(10 mg/kg)������ת����ǰ3�죬�ں��������ڲ༡Ⱥ�ڶ��ע�伡��������0.5%���߿���ʹ�ֲ�����������������ȡ��Դ����3���ͬ����֫�������Զ�˺ͷ�֧�ж����������֫������Ѫ�ܲ�ģ�͡�
��������
1.��Ч�����飺������Ѫ�ܲ��ĺ�ģ�ͣ�ʵ����(3ֻ)תpcD2/VEGF����(�������1 200 ��g��ע��800 ��g������Ϊ2 mg)��������(2ֻ)ͬ��ת������������pcD2���ڻ���ת��ǰ������ת�ƺ�1�ܡ�2�ܡ�1�¡�3�¡�6�·ֱ����Ķ�����Ӱ��(6F��cordis pigtail)�����Ҳ�ɶ�����ܣ�����ͷ�����ڸ���������β�����Ӹ�ѹע������ע��76%��Ӱ�ϰ�������������Ӱ��Ӱ��¼��Ӱ������Թ۲�����Ѫ�ܺͲ�֧ѭ�����γ������Ѫ����Ӱ��Ϊ�¹������ӹ�˾����Ӱ�ٶ�Ϊ25��/�롣
, ��Ĵҽҩ
2.��ȫ�����飺(1)С���Զ������飺��������С��5ֻ�����ԣ�����20 g���ҡ�ͨ��������ߺͼ���ע�䷨������ת��pcD2/VEGF����1 000 ��g(ΪС��������Ƽ���20 ��g��50��)�����ߺ�����10��۲�С�������������쳣���֡�(2)�����������飺����Wistar���Դ���10ֻ������200 g���ҡ�������飬5ֻת��pcD2/VEGF����2 000 ��g(Ϊ����������Ƽ���200 ��g��10��)��5ֻΪ����������ˮ�����顣1���º��ͷ�������ȡѪ���иΡ������ܵ�����ָ���⣬��ȡ�ԡ��ġ��Ρ�Ƣ���Ρ�����غ�輰���߾ֲ�������֯����������顣(3)��Ķ����������飺���Ϻͷ���ͬ��Ч�����顣��Ѫ����ӰͬʱȡѪ����������⣬6���º��и���B�ͳ�����ȫ��CTɨ�輰�۵�飬����������в����۲졣
3.�����Ŵ�ѧ������ѧ����������ֱ��ڼ��ڻ������ת��pcD2/VEGF 200 ��g���ڷ��ߺ�1�ܡ�2�ܡ�1�¡�2�¡�4�·����������ȡѪ���ü��ELISA���������VEGF���������ͬʱ�ֱ���ȡ���ߴ����⼰�ġ��Ρ��Ρ������ԡ�غ�������DNA��ͨ��PCR���˽����ķֲ�����ͳ���ʱ�䡣
, http://www.100md.com
�� ��
һ����Ч������
�ڽ�������Ѫ����Ӱ���ɼ����ɶ�����֧�����˱�����Զ��Ѫ�ܲ��ܳ�ӯ��������������ģ���Ʊ��ɹ�������1�ܼ���ʾ��VEGF���Ľ����㸽���н϶��ӯСѪ�ܣ����ڲ����Ų�֧ѭ�����γɣ��ϵ�Զ�˵Ķ�����ʼ��ӯ����pcD2���պ�����㸽����ӯСѪ���������٣�����Ѫ�ܼ���VEGF��(5/100 cm2)���Զ��ڶ�����(1/100 cm2)������2�ܣ�VEGF���������Χ�зḻ�ij�ӯСѪ�ܣ��ϵ�Զ�˶�����ӯ���ã����������������Ա仯��1���º�VEGF���������Χ��СѪ�ܸ�Ϊ�ḻ��Զ�˶������Գ�ӯ��Ѫ�ܼ���12/100 cm2����������Ľ����㸽����������СѪ�����ɣ�Զ�˶���Ҳ��һ����ӯ(��������)�����ܲ���֣�Ѫ�ܼ�����Ϊ4/100 cm2�����Բ���ͬ�ڵ�VEGF����������(ͼ2��3)���˺����3����6��Ѫ����Ӱ��VEGF�����鼰pcD2����������������Ա仯����δ��Ѫ�������ɡ�
, ��Ĵҽҩ
ͼ2 ת�����2��Ѫ����Ӱ.��ͼΪ����(תpcD2)���ɼ�����Ѫ�ܽ�����Զ�˽�����������Ѫ���γɣ���ͼΪתpcD2/VEGF���ɼ��н����Ե�����Ѫ�ܺͲ�֧ѭ���γ�.
ͼ3 ת�����1��Ѫ����Ӱ��ͼΪ����(תpcD2)��ʾ����Ѫ�ܽ϶���2��ʱֻ���������ӣ���ͼΪתpcD2/VEGF������ʾ�������������Ѫ�ܺͲ�֧ѭ�� ��ͼΪ��Ӱͼ
������ȫ������
1.�����������飺(1)С�������۲�10�죬ȫ�������쳣���֡�(2)����1�����ڶ������쳣���֣�ȫ����1���º�������ܼ��δ���쳣(��1)����֯ѧ�۲죬��������֯Ѫ�ֲܷ�VEGF��϶�����ḻ��������Ҫ������δ���쳣�����仯��(3)��ת����ǰ��ͬʱ��תVEGF����ԸΡ������ܵ�Ҳ������Ӱ��(��2)��6�º��۵��ɼ�Ѫ�ֲܷ�����̬������δ��Ѫ��������ȫ��CT��������������������֯����ѧ��飬δ�������������쳣�����仯�����Ͻ��˵��������ת�����Ƽ����ͳ�������VEGF�����С����������Զ������á�
, ��Ĵҽҩ
��1 ������VEGF����ת�ƺ����������ܲⶨ( ��s) ���
��s) ���
����
������ת��ø
(U/L)
�춬����ת��ø
(U/L)
�ܵ�����
(��mol/L)
���ص�
(mmol/L)
����
, ��Ĵҽҩ
(��mol/L)
������
5
74��9
296��70
0.93��0.25
7.7��0.7
68.3��0.6
VEGF��
5
68��9
220��18*
, http://www.100md.com
1.10��0.43*
7.0��1.4*
67.6��4.2*
������Ƚ� *P>0.05
��2 ������תVEGF������ѪҺ����ָ��ⶨ( ��s) ʱ��
��s) ʱ��
����
ALT
(U/L)
AST
(U/L)
, http://www.100md.com
L
(mmol/L)
TG
(mmol/L)
Ѫ��
(mmol/L)
����
(��mol/L)
���ص�
(mmol/L)
0��
5
14.5��7.8
, ��Ĵҽҩ
29.5��2.2
2.4��0.3
0.58��0.64
4.2��1.0
79��14
6.55��0.07
2��
5
11.8��3.8
33.3��17.5
3.1��0.8
0.49��0.10
, ��Ĵҽҩ
4.1��0.8
73��28
6.03��1.20
1��
5
12.5��0.7
30.0��10.5
2.4��1.0
0.44��0.07
3.3��1.4
78��18
6.90��1.40
, ��Ĵҽҩ
6��
5
18.0��4.2
34.5�� 2.1
3.4��0.6
0.67��0.10
3.4��0.7
84��14
6.55��1.06
2.�����Ŵ�ѧ������ѧ��������1�ܡ�2�ܡ�1�¡�2�¡�4�¾����ڷ��ߴ������ڼ���Դ��VEGF����ķֲ��������ڸ�������δ�����иû���ķֲ������ELISA���ⶨ��ʾ��ת�����ͬʱ�ڣ�Ѫ��VEGF�����Ϊ����(ͼ4)��
, ��Ĵҽҩ
ע����ͼΪת����2�ܣ���ͼΪת����4�£�0Ϊ���Զ��գ�MΪDNA����1���⣻2�ģ�3�Σ�4����5�Σ�6�ԣ�7غ��
ͼ4 תpcD2/VEGF���������VEGF����ķֲ�
�� ��
֫�嶯�������������ƣ��ٴ�����Ҫ����Ѫ�ܳ���������ƴ����������մ���֢�࣬��Ч������������������Ϊ�俪����һ���µ�;��������Isner��[2]��phVEGF165����Ķ�����ˮ�������ҵ��ܽ��л���ת�ƣ����Ƽ���֫��Ѫ�ܱ���֢��óɹ������ѻ������ٴ����飬ȡ���˳�����Ч[3��4]����ˮ�����ױ�Ѫ����ɢ���ڶ�������Ӳ��Ѫ���ڵ�ת��Ч�ʼ��͡���������Bupivacaine�̼����������������ת�Ƶ�Ч��[5]�����ü����ڻ�����߷������������㣬�ҿɴﵽ��Ч������Ŀ�ġ�
, http://www.100md.com
��������֫�嶯�������Ĵ����Ȯģ���ϣ�Ӧ��pcDNA3/VEGF165���оֲ����������ߣ���������������ٽ���֫������Ѫ�ܺͲ�֧ѭ��������֫�廵������֮Ϊ�����Ӵ�������[6��7]��Ϊ�˽�һ�����VEGF�ı���Ч�ʣ���pcDNA3/VEGF�����ϣ������¹�����pcD2/VEGF121������������CMV�������⣬�����ں��ӣ�������������ӵ����ã�����V1��V2Ƭ�Σ��Ӷ����������ӵ����á�Ѫ��ƽ����ϸ��תȾ�Ľ����ʾ��pcD2/VEGF�ı���Ч�ʸ���pcDNA3/VEGF(������)���øû��������Զ��������ĺ�ģ�ͽ��������ƣ��ɴٽ�����Ѫ���γɺͲ�֧ѭ���Ľ�����������6���¹۲죬δ������Ѫ��������������ʵ��֤����ͨ��������ߣ���ȱѪ��λת��VEGF����ʹѪ��Ѹ�ٻָ������ƾֲ�Ѫ������ֹ��֯������
��С����Ӻﶾ�����ù۲죬����Ѫ����ָ�����֯���������쳣����ʾ��VEGF�����ڶ������ڵİ�ȫ�ԡ��ɴ˿ɼ���VEGF�����֫�嶯������֢�ɴﵽ��ȫ��Ч������Ŀ�ģ���Ϊ����ȱѪ��֯�ָ�Ѫ������;����
, http://www.100md.com
������Ϊ���ҡ����������ƻ����\��������Ŀ(BH-03)
����� 1 European Working Group on Critical Ischemia. Second European consensus document on chronic critical leg ischemia. Circulation, 1991,84(suppl IV):IV1-IV26.
2 Isner JM, Walsh K, Symes J, et al. Clinical protocol: Arterial gene transfer for therapeutic angiogenesis in patients with peripheral artery disease. Hum Gene Ther 1996,7:959-988.
3 Isner JM, Pieczek A, Schainfeld R, et al. Clinical evidence of angiogenesis after arterial gene transfer of phVEGF165 in patient with ischemic limb. Lancet, 1996,348:370-374.
, http://www.100md.com
4 Baumgartner I, Pieczek A, Manor O, et al. Constitutive expression of phVEGF165 after intramuscular gene transfer promotes collateral vessel development in patients with critical limb ischemia. Circulation, 1998,97:1114-1123.
5 Danko I, Fritz JD, Jiao S, et al. Pharmacological enhancement of in vivo foreign gene expression in muscle. Gene Ther,1994,1:114-121.
6 �ܰ���,֣��,�ϵ���,��.���Ӵ�����-VEGF�������ƴ��������Ѫ�ܲ���ʵ���о�,�л�ҽѧ��־,1996��76:662-666.
7 ֣��,����,�ϵ���,��.Ѫ����Ƥ�������ӻ�������Ȯ������Ѫ�ܲ��ij����о�,�л���Ѫ�ܲ���־��1998��26:62-64.
(�ո壺1998-02-19 �أ�1998-11-28), ��Ĵҽҩ
��λ��100083 ����ҽ�ƴ�ѧ��Ѫ���о���
�ؼ��ʣ������Ʒ�����Ƥ�������ӣ�����Ѫ�ܼ���
�л�ҽѧ��־990216 ��ժҪ�� Ŀ�� ��֤Ѫ����Ƥ��������(VEGF)��������֫�嶯������������Ч�ԺͰ�ȫ�ԡ����� ��������VEGF�������˱�������pcD2/VEGF����Ч�����飺�Ʊ�֫�嶯���������ĺ�ģ�ͣ�ͨ�����������߷��ͼ��ڶ��ע�䷨����VEGF��������ת����������������ȫ�����飺�������������Ƽ�����VEGF����ֱ���5ֻС��(1 000 ��g��ΪС�����Ƽ���20 ��g��50��)��10ֻ����(2 000 ��g��Ϊ���Ƽ�����10��)��5ֻ��(2 000 ��g�����Ƽ���)���ڹ۲��䶾�����ã�������PCR���ͼ��ELISA�����з����Ŵ�ѧ������ѧ����������� תVEGF�����1��Ѫ����Ӱ����ʾ�������㸽���н϶��ӯСѪ�ܣ�Զ�˶�����ʼ��ӯ��2��ʱ��Ϊ���ԣ�1�º�����СѪ����Ϊ�ḻ���ɼ�Զ�˶������Գ�ӯ��Ѫ�ܼ�����ʾVEGF��(1��ʱ5/100 cm2��1��12/100 cm2)���Զ��ڶ�����(1��1/100 cm2��1��4/100 cm2)�������ȼ�飬֤��VEGF����Ը������ܵ�������Ӱ�죬δ�����������������仯�������VEGF������ھֲ�������֯�б���4�������ϣ����ۼ�������������֯������ѭ��������������� �����VEGF��������֫�嶯������������Ч�Ͱ�ȫ�ģ�ͨ��ҩ���������ٴ����顣
, ��Ĵҽҩ
Vascular endothelial growth factor gene therapy for peripheral artery disease��experimental study SHENG Qinhui, ZHU Guoying, ZHOU Airu, et al. Institute of Cardiovascular Research, Beijing Medical University, Beijing 100083
��Abstract�� Objective To Study experimentally VEGF gene for treatment of peripheral artery disease.Methods The human VEGF cDNA was cloned into the eukaryotic expression vector pcD2.Using gene suture, the recombinant plasmid was transferred into the hindlimbs�� adductor of Rhesus monkey, of which the distal end of the external iliac arteries were ligated and the femoral arteries were completely excised. With angiography, the biological effect of VEGF gene in experimental animals was investigated. Safey tests were analyzed by transferring of VEGF into mouse, rat, and Rhesus monkey, evaluated by biochemistry analysis, histopathological examination, PCR, and indirect ELISA.Results The transfer of VEGF gene stimulated the formation of focal microvessels, established collateral circulation, and augmented blood perfusion. The system had no adverse effect and remarkable pathological change in mouse, rat, and Rhesus monkey.Conclusion The experimental studies indicated that VEGF would be effective and safe for clinical trial after approval.
, http://www.100md.com
��Key words�� Gene therapy Endothelial growth factor Peripheral vascular diseases
(Natl Med J China, 1999,79:129-132)
֫�嶯����������һ�����ص�Ѫ�ܲ���Ŀǰ������Ч���Ʒ������������н�֫������Ԥ��ܲ�[1]����ˣ��о��µ����Ʒ�����Ϊ���С����������й�����������Ѫ����Ƥ��������(VEGF)�����Ʊ��ɻ�����ߣ�֤������Ч�ٽ�����Ѫ�ܵIJ�֧ѭ����ͨ��С����ļ����Զ����������飬�������ƻ�����ȫ�������ٴ������Ҫ��
���Ϻͷ���
һ������
1.����VEGF����������Ϊ��һ�����VEGF�ı���Ч�ʣ������ҹ�����pcDNA��3/VEGF����[2]�پ�BamHI��XbaI����������ͬ��ø�е�pcD2��Ч��˱������壬������pcD2/VEGF����������Ŀ�Ļ���Ϊ�ɱ���121���������VEGF121�������ź������У�����·����ͼ1�����ü��ѽⷨ��ȡ��������PEG-8000����������ˮ���á�

, http://www.100md.com
ͼ1 pcD2/VEGF�����Ĺ��� 2.VEGF������ߺͻ���ת�ƣ���һ�����ȵ�2��ҽ�÷���߽���������1%�㾫����ע��Һ�У����ɣ�������Σ�ֱ���㾫������Һȫ�������ڷ����ϣ��ٷ���ͿĨ�����������������ɺ��ã����ϲ���ȫ���������ڽ��С����ڻ���ת�Ʋ��ü����ڻ�����߷��ͼ����ڶ��ע�䷨��
3.֫�嶯������������ģ�ͣ��������Ժ�Ӻ�5ֻ������4��5 kg�����й�ҽѧ��ѧԺ�����������ṩ��Ӧ�ü���ע���Ȱ�ͪ(10 mg/kg)������ת����ǰ3�죬�ں��������ڲ༡Ⱥ�ڶ��ע�伡��������0.5%���߿���ʹ�ֲ�����������������ȡ��Դ����3���ͬ����֫�������Զ�˺ͷ�֧�ж����������֫������Ѫ�ܲ�ģ�͡�
��������
1.��Ч�����飺������Ѫ�ܲ��ĺ�ģ�ͣ�ʵ����(3ֻ)תpcD2/VEGF����(�������1 200 ��g��ע��800 ��g������Ϊ2 mg)��������(2ֻ)ͬ��ת������������pcD2���ڻ���ת��ǰ������ת�ƺ�1�ܡ�2�ܡ�1�¡�3�¡�6�·ֱ����Ķ�����Ӱ��(6F��cordis pigtail)�����Ҳ�ɶ�����ܣ�����ͷ�����ڸ���������β�����Ӹ�ѹע������ע��76%��Ӱ�ϰ�������������Ӱ��Ӱ��¼��Ӱ������Թ۲�����Ѫ�ܺͲ�֧ѭ�����γ������Ѫ����Ӱ��Ϊ�¹������ӹ�˾����Ӱ�ٶ�Ϊ25��/�롣
, ��Ĵҽҩ
2.��ȫ�����飺(1)С���Զ������飺��������С��5ֻ�����ԣ�����20 g���ҡ�ͨ��������ߺͼ���ע�䷨������ת��pcD2/VEGF����1 000 ��g(ΪС��������Ƽ���20 ��g��50��)�����ߺ�����10��۲�С�������������쳣���֡�(2)�����������飺����Wistar���Դ���10ֻ������200 g���ҡ�������飬5ֻת��pcD2/VEGF����2 000 ��g(Ϊ����������Ƽ���200 ��g��10��)��5ֻΪ����������ˮ�����顣1���º��ͷ�������ȡѪ���иΡ������ܵ�����ָ���⣬��ȡ�ԡ��ġ��Ρ�Ƣ���Ρ�����غ�輰���߾ֲ�������֯����������顣(3)��Ķ����������飺���Ϻͷ���ͬ��Ч�����顣��Ѫ����ӰͬʱȡѪ����������⣬6���º��и���B�ͳ�����ȫ��CTɨ�輰�۵�飬����������в����۲졣
3.�����Ŵ�ѧ������ѧ����������ֱ��ڼ��ڻ������ת��pcD2/VEGF 200 ��g���ڷ��ߺ�1�ܡ�2�ܡ�1�¡�2�¡�4�·����������ȡѪ���ü��ELISA���������VEGF���������ͬʱ�ֱ���ȡ���ߴ����⼰�ġ��Ρ��Ρ������ԡ�غ�������DNA��ͨ��PCR���˽����ķֲ�����ͳ���ʱ�䡣
, http://www.100md.com
�� ��
һ����Ч������
�ڽ�������Ѫ����Ӱ���ɼ����ɶ�����֧�����˱�����Զ��Ѫ�ܲ��ܳ�ӯ��������������ģ���Ʊ��ɹ�������1�ܼ���ʾ��VEGF���Ľ����㸽���н϶��ӯСѪ�ܣ����ڲ����Ų�֧ѭ�����γɣ��ϵ�Զ�˵Ķ�����ʼ��ӯ����pcD2���պ�����㸽����ӯСѪ���������٣�����Ѫ�ܼ���VEGF��(5/100 cm2)���Զ��ڶ�����(1/100 cm2)������2�ܣ�VEGF���������Χ�зḻ�ij�ӯСѪ�ܣ��ϵ�Զ�˶�����ӯ���ã����������������Ա仯��1���º�VEGF���������Χ��СѪ�ܸ�Ϊ�ḻ��Զ�˶������Գ�ӯ��Ѫ�ܼ���12/100 cm2����������Ľ����㸽����������СѪ�����ɣ�Զ�˶���Ҳ��һ����ӯ(��������)�����ܲ���֣�Ѫ�ܼ�����Ϊ4/100 cm2�����Բ���ͬ�ڵ�VEGF����������(ͼ2��3)���˺����3����6��Ѫ����Ӱ��VEGF�����鼰pcD2����������������Ա仯����δ��Ѫ�������ɡ�

, ��Ĵҽҩ
ͼ2 ת�����2��Ѫ����Ӱ.��ͼΪ����(תpcD2)���ɼ�����Ѫ�ܽ�����Զ�˽�����������Ѫ���γɣ���ͼΪתpcD2/VEGF���ɼ��н����Ե�����Ѫ�ܺͲ�֧ѭ���γ�.

ͼ3 ת�����1��Ѫ����Ӱ��ͼΪ����(תpcD2)��ʾ����Ѫ�ܽ϶���2��ʱֻ���������ӣ���ͼΪתpcD2/VEGF������ʾ�������������Ѫ�ܺͲ�֧ѭ�� ��ͼΪ��Ӱͼ
������ȫ������
1.�����������飺(1)С�������۲�10�죬ȫ�������쳣���֡�(2)����1�����ڶ������쳣���֣�ȫ����1���º�������ܼ��δ���쳣(��1)����֯ѧ�۲죬��������֯Ѫ�ֲܷ�VEGF��϶�����ḻ��������Ҫ������δ���쳣�����仯��(3)��ת����ǰ��ͬʱ��תVEGF����ԸΡ������ܵ�Ҳ������Ӱ��(��2)��6�º��۵��ɼ�Ѫ�ֲܷ�����̬������δ��Ѫ��������ȫ��CT��������������������֯����ѧ��飬δ�������������쳣�����仯�����Ͻ��˵��������ת�����Ƽ����ͳ�������VEGF�����С����������Զ������á�
, ��Ĵҽҩ
��1 ������VEGF����ת�ƺ����������ܲⶨ(
 ��s) ���
��s) �������
������ת��ø
(U/L)
�춬����ת��ø
(U/L)
�ܵ�����
(��mol/L)
���ص�
(mmol/L)
����
, ��Ĵҽҩ
(��mol/L)
������
5
74��9
296��70
0.93��0.25
7.7��0.7
68.3��0.6
VEGF��
5
68��9
220��18*
, http://www.100md.com
1.10��0.43*
7.0��1.4*
67.6��4.2*
������Ƚ� *P>0.05
��2 ������תVEGF������ѪҺ����ָ��ⶨ(
 ��s) ʱ��
��s) ʱ������
ALT
(U/L)
AST
(U/L)
, http://www.100md.com
L
(mmol/L)
TG
(mmol/L)
Ѫ��
(mmol/L)
����
(��mol/L)
���ص�
(mmol/L)
0��
5
14.5��7.8
, ��Ĵҽҩ
29.5��2.2
2.4��0.3
0.58��0.64
4.2��1.0
79��14
6.55��0.07
2��
5
11.8��3.8
33.3��17.5
3.1��0.8
0.49��0.10
, ��Ĵҽҩ
4.1��0.8
73��28
6.03��1.20
1��
5
12.5��0.7
30.0��10.5
2.4��1.0
0.44��0.07
3.3��1.4
78��18
6.90��1.40
, ��Ĵҽҩ
6��
5
18.0��4.2
34.5�� 2.1
3.4��0.6
0.67��0.10
3.4��0.7
84��14
6.55��1.06
2.�����Ŵ�ѧ������ѧ��������1�ܡ�2�ܡ�1�¡�2�¡�4�¾����ڷ��ߴ������ڼ���Դ��VEGF����ķֲ��������ڸ�������δ�����иû���ķֲ������ELISA���ⶨ��ʾ��ת�����ͬʱ�ڣ�Ѫ��VEGF�����Ϊ����(ͼ4)��

, ��Ĵҽҩ
ע����ͼΪת����2�ܣ���ͼΪת����4�£�0Ϊ���Զ��գ�MΪDNA����1���⣻2�ģ�3�Σ�4����5�Σ�6�ԣ�7غ��
ͼ4 תpcD2/VEGF���������VEGF����ķֲ�
�� ��
֫�嶯�������������ƣ��ٴ�����Ҫ����Ѫ�ܳ���������ƴ����������մ���֢�࣬��Ч������������������Ϊ�俪����һ���µ�;��������Isner��[2]��phVEGF165����Ķ�����ˮ�������ҵ��ܽ��л���ת�ƣ����Ƽ���֫��Ѫ�ܱ���֢��óɹ������ѻ������ٴ����飬ȡ���˳�����Ч[3��4]����ˮ�����ױ�Ѫ����ɢ���ڶ�������Ӳ��Ѫ���ڵ�ת��Ч�ʼ��͡���������Bupivacaine�̼����������������ת�Ƶ�Ч��[5]�����ü����ڻ�����߷������������㣬�ҿɴﵽ��Ч������Ŀ�ġ�
, http://www.100md.com
��������֫�嶯�������Ĵ����Ȯģ���ϣ�Ӧ��pcDNA3/VEGF165���оֲ����������ߣ���������������ٽ���֫������Ѫ�ܺͲ�֧ѭ��������֫�廵������֮Ϊ�����Ӵ�������[6��7]��Ϊ�˽�һ�����VEGF�ı���Ч�ʣ���pcDNA3/VEGF�����ϣ������¹�����pcD2/VEGF121������������CMV�������⣬�����ں��ӣ�������������ӵ����ã�����V1��V2Ƭ�Σ��Ӷ����������ӵ����á�Ѫ��ƽ����ϸ��תȾ�Ľ����ʾ��pcD2/VEGF�ı���Ч�ʸ���pcDNA3/VEGF(������)���øû��������Զ��������ĺ�ģ�ͽ��������ƣ��ɴٽ�����Ѫ���γɺͲ�֧ѭ���Ľ�����������6���¹۲죬δ������Ѫ��������������ʵ��֤����ͨ��������ߣ���ȱѪ��λת��VEGF����ʹѪ��Ѹ�ٻָ������ƾֲ�Ѫ������ֹ��֯������
��С����Ӻﶾ�����ù۲죬����Ѫ����ָ�����֯���������쳣����ʾ��VEGF�����ڶ������ڵİ�ȫ�ԡ��ɴ˿ɼ���VEGF�����֫�嶯������֢�ɴﵽ��ȫ��Ч������Ŀ�ģ���Ϊ����ȱѪ��֯�ָ�Ѫ������;����
, http://www.100md.com
������Ϊ���ҡ����������ƻ����\��������Ŀ(BH-03)
����� 1 European Working Group on Critical Ischemia. Second European consensus document on chronic critical leg ischemia. Circulation, 1991,84(suppl IV):IV1-IV26.
2 Isner JM, Walsh K, Symes J, et al. Clinical protocol: Arterial gene transfer for therapeutic angiogenesis in patients with peripheral artery disease. Hum Gene Ther 1996,7:959-988.
3 Isner JM, Pieczek A, Schainfeld R, et al. Clinical evidence of angiogenesis after arterial gene transfer of phVEGF165 in patient with ischemic limb. Lancet, 1996,348:370-374.
, http://www.100md.com
4 Baumgartner I, Pieczek A, Manor O, et al. Constitutive expression of phVEGF165 after intramuscular gene transfer promotes collateral vessel development in patients with critical limb ischemia. Circulation, 1998,97:1114-1123.
5 Danko I, Fritz JD, Jiao S, et al. Pharmacological enhancement of in vivo foreign gene expression in muscle. Gene Ther,1994,1:114-121.
6 �ܰ���,֣��,�ϵ���,��.���Ӵ�����-VEGF�������ƴ��������Ѫ�ܲ���ʵ���о�,�л�ҽѧ��־,1996��76:662-666.
7 ֣��,����,�ϵ���,��.Ѫ����Ƥ�������ӻ�������Ȯ������Ѫ�ܲ��ij����о�,�л���Ѫ�ܲ���־��1998��26:62-64.
(�ո壺1998-02-19 �أ�1998-11-28), ��Ĵҽҩ