对尿毒症毒素的新认识
作者:赵素梅
单位:赵素梅 首都医科大学附属北京红十字朝阳医院肾内科
关键词:慢性肾功能衰竭;尿毒症毒素;发病机制
赵素梅 综述 郑法雷 审校赵素梅 综述 郑法雷 审校
在慢性肾功能不全进行性加重后,体内有200种以上物质的水平比正常人增高,其中有些物质具有毒性作用。这些具有毒性作用的物质在体内积聚,是引起尿毒症症状、代谢紊乱和多个系统功能失调的主要原因之一。近二十年来关于大、中分子尿毒症毒素的研究进展相对迟缓,但近年来有关学者在这方面的研究已有某些新发现,有些毒素蛋白已被分离出,通过体内、外实验对其性质及毒性有了一定的认识,对以前已知毒素的作用也有了新的了解。
1 被认为是“新毒素”的主要物质
, 百拇医药
凡被称为“尿毒症毒素”的物质应具备以下条件:①在尿毒症患者体内该物质的浓度显著高于正常;②该物质的化学结构和理化性质明确;③高浓度的该物质与特异的尿毒症临床表现相关;④动物试验或体外实验证实该物质在其浓度与尿毒症患者体内浓度相似时,可出现类似毒性作用;⑤体液内该物质浓度下降与尿毒症症状、体征改善相伴随[1]。
据近年有关文献报告,目前被认为可能是“新”尿毒症毒素的物质约有20种左右(表1)。
表1 近年报告的具有尿毒症毒素作用的物质
1 粒细胞抑制蛋白Ⅰ(GIP-Ⅰ)和粒细胞抑制蛋白Ⅱ(GIP-Ⅱ)
2 趋化抑制蛋白(CIP)
3 中性粒细胞脱颗粒抑制蛋白Ⅰ(DIP-Ⅰ)和中性粒细胞脱颗粒抑制蛋白Ⅱ(DIP-Ⅱ)
, 百拇医药
4 同型半胱氨酸(Homocysteine,Hcy)
5 晚期糖基化终末产物(AGEs)和终末氧化蛋白产物(AOPP)
6 氨甲酰化的氨基酸和蛋白质
7 瘦素(Leptin)
8 活性维生素D抑制物
9 影响一氧化氮合成的毒素
10 其它:硫酸吲哚酚,癌原性杂环胺,马尿酸,假尿嘧啶核苷,免疫球蛋白轻链,3-羧-4-甲-5-丙基呋喃戊酮酸(CMPF)
2 具有抑制免疫细胞活性作用的毒素
这类毒素包括粒细胞抑制蛋白Ⅰ(GIP-Ⅰ)、粒细胞抑制蛋白Ⅱ(GIP-Ⅱ)、趋化抑制蛋白(CIP)、中性粒细胞脱颗粒抑制蛋白Ⅰ(DIP-Ⅰ)、中性粒细胞脱颗粒抑制蛋白Ⅱ(DIP-Ⅱ)、免疫球蛋白轻链等。GIP-Ⅰ和GIP-Ⅱ都是从规律血透患者的血浆中分离出来的[2]。GIP-Ⅰ分子量为28000,电离点位于4.0~4.5,属于免疫球蛋白轻链类,其中80%与κ轻链同类,40%与λ轻链同类。GIP-Ⅱ分子量为9500,与β2微球蛋白(β2-MG)同一类。
, 百拇医药
GIP-Ⅰ和GIP-Ⅱ具有抑制多核粒细胞(PMN)对糖摄取的作用。GIP-Ⅰ是通过抑制趋化性肽(甲酰-甲硫氨酰-亮氨酰-苯丙氨酸)而影响PMN的功能,抑制PMN的趋化性、氧化代谢及细胞内的杀菌作用。GIP-Ⅱ则抑制由佛波醇酯(phorbolester)刺激的糖摄取;此外它也可刺激人体单核细胞分泌IL-1β和IL-6[3]。
DIP-Ⅰ和DIP-Ⅱ均为尿毒症规律血透患者的血浆超滤液中提出。DIP-Ⅰ分子量为14400,与血管生成素(Angiogenin)属同一类物质,在尿毒症时比正常人高2~3倍,而在CAPD患者的腹透液中DIP-Ⅰ浓度可高达正常人的1000倍,提示DIP-Ⅰ是由腹腔中的细胞合成。DIP-Ⅰ可抑制自发性及刺激后的PMN脱颗粒[4],而应用人重组血管生成素多克隆抗体可消除DIP-Ⅰ对PMN的这种抑制作用。DIP-Ⅰ不仅抑制PMN的乳肝褐质(Lactoferrin)、胶原酶、明胶酶的释放,而且也抑制弹性硬蛋白酶释放。含有血管生成素片段中的二硫化物C39~C92,对PMN的抑制作用与DIP-Ⅰ作用相同,但要弱得多。这表明DIP-Ⅰ在PMN细胞上有一个新的、生物学活性位置,而与血管生成素的活性部位有所不同。DIP-Ⅱ分子量为24 000,这种蛋白质可能为补体D,在血透患者中补体D比正常人高约10倍,补体D可引起刺激后的剂量依赖性的乳肝褐质脱颗粒约减少到正常对照的34%[5]。
, 百拇医药
CIP是从腹透患者的腹透液中分离所得,在体外实验中,它抑制PMN的趋化呈浓度依赖性,且不可逆转。氨基酸序列测定显示这种多肽与泛素有着相同的氨基末端,但比泛素电离点更偏酸性,而泛素本身对PMN的趋化性无影响。由此看来CIP很可能是被修饰的泛素,其分子量为8500[6]。
免疫球蛋白轻链κ和λ的单体和二聚体在体外很小的浓度即可抑制PMN的糖摄取和趋化性,由B淋巴细胞产生的免疫球蛋白轻链多于重链,因此有少量的轻链以自由形式存在于血液中,严重肾功能减退患者其血中自由轻链的水平增高5倍[7]。
3 氨甲酰化氨基酸和蛋白质
正常时人体内的尿素可转变为氰酸盐,氰酸盐分子通过氨甲酰化被清除。而尿毒症时,氨甲酰化氰酸盐不能被有效清除,造成积聚,从而引起血液中氨基酸和蛋白质氨甲酰化(附图)。氨甲酰化的氨基酸称为C-AA,没有氨甲酰化的氨基酸为F-AA。由于C-AA没有自由的氨基与另一个氨基酸的羧基结合,引起蛋白质合成障碍,因而是造成尿毒症患者的营养不良的因素之一[8],也可引起某些物质代谢的障碍,甚至影响组织、器官的功能(表2)。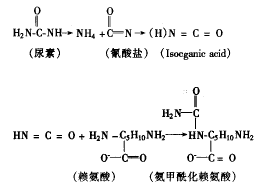
, 百拇医药
附图 氨基酸的氨甲酰化(以赖氨酸为例)
表2 氨甲酰化蛋白质、氨基酸的毒性
1 蛋白质合成↓ 蛋白质分解↑
2 蛋白质功能变化
如血红蛋白氨甲酰化→血红蛋白释放氧减少
3 酶功能变化
纤溶酶、G6PD、ALP、RNase、胃蛋白酶、糜蛋白酶
4 组织-器官功能的变化:如大脑皮质功能、周围神经功能障碍
5 药物生物利用度的变化:氨甲酰化蛋白质与药物结合↓
血红蛋白中缬氨酸的氨基端被氨甲酰化时,形成了与氧高亲和力的氨甲酰血红蛋白,使氧离曲线左移,减少氧的释放,造成组织缺氧[9]。尿毒症时,由于天门冬酰胺的氨甲酰化,且呈剂量依赖方式,损害胰岛素敏感的糖转运系统,是造成胰岛素抵抗的原因之一,因而使CRF患者体内组织的葡萄糖摄取量减少[10]。
, 百拇医药
体内结构蛋白、胞浆蛋白、内质网蛋白的氨甲酰化,可影响器官的正常功能。白蛋白在结合和转运酸性药物中起重要的作用,氨甲酰化的白蛋白可使药物的生物度利用降低[11]。在神经系统,酶和结构蛋白的氨甲酰化,对大脑皮质功能、学习和记忆造成不利影响,也可引起外周神经病变。
氨甲酰化可使多种激素和酶活性降低,如胰岛素、催产素、葡萄糖-6-磷酸脱氢酶、纤溶酶、谷氨酸脱氢酶、磷酸化酶a和b、丙酮酸激酶、碱性磷酸酶、核糖核酸酶、糜蛋白酶、胃蛋白酶等,从而影响多种物质的代谢和某些器官的功能。
4 晚期糖基化终末产物(AGE)和终末氧化蛋白产物(AOPP)
有人认为AGE可代表尿毒症中分子物质毒性的“现代形式”,多肽AGE分子量多数均小于10 000。AGE是蛋白质的氨基组、脂质和脂蛋白非酶糖基化反应的终产物,反应早期产物仍有可逆性,而其晚期产物(AGE)则较稳定,已失去可逆性。慢性肾衰时,由于肾脏清除障碍及其他尚不清楚的原因,体内一些短半衰期的血浆蛋白如β2-MG被AGE修饰并导致蓄积。高流量透析可显著降低由AGE修饰的小分子,在糖尿病肾衰患者中可使其降低47.4%,在非糖尿病肾衰患者中可使其降低60.6%,然而3h后其浓度又回到治疗前水平。CAPD患者虽然与葡萄糖持续接触,但血中AGE水平并不比血透者高;然而腹膜组织中的蛋白质可发生糖基化。此外,某些食物中含有的AGE在小肠吸收,故食物的摄取也可增加尿毒症患者的血AGE水平。高AGE水平是尿毒症患者心血管并发症原因之一,实验发现血透患者冠状动脉壁AGE积聚[12],AGE修饰的β2-MG是透析相关性淀粉样变性的淀粉样物质的主要成分,它能刺激巨噬细胞增加分泌TNF-α和IL-1β,也能增加人单核细胞的趋化性,故淀粉样物质沉积处出现单核/巨噬细胞聚集及原发性炎症反应,导致骨和关节损害。这些效应是由AGE受体(RAGE)即AGE结合蛋白所介导的,AGE和RAGE相互作用,可引起氧化应激反应,导致血管通透性增加,血管壁增厚[13]。
, 百拇医药
在尿毒症时血中存在着氧化损伤的蛋白产物,称为终末氧化蛋白产物(Advanced oxidation protein products,AOPP)。由活性中性粒细胞产生的氧化物增多,或这些氧化物的清除减少,均可导致AOPP增加。氧化物是吞噬细胞尤其是中性粒细胞在呼吸爆裂时产生的大量的反应性氧类(ractive oxygen species)物质,为氧分子被单价还原成过氧离子(O-2)、原始羟基(OH0)、单价氧(1O2)和含氯氧化物(HOCl),它们可杀死病原菌,但当宿主的抗氧化系统被抑制时,它也造成组织损伤[14]。氧化应激时氧化物前体与抗氧化物的平衡被打破,而前者偏高,使DNA、蛋白和脂质等人体基本成分的氧化增多;此外,氧化物被认为是炎症介质,可导致氧化性结构损伤和细胞的功能紊乱。氧化物对蛋白质水解的敏感度依赖于氧化应激的强度[15]。
据报告尿毒症患者AOPP水平可高出正常人3倍。AOPP的积聚可反映尿毒症时清除受损伤蛋白的能力下降。高分子量的AOPP为600 000,是蛋白质的集合体;低分子量的AOPP为80 000左右,白蛋白是其主要成分。AOPP是一组“奇特”的毒素和(或)前炎症介质,在尿毒症时AOPP可引起免疫紊乱和炎症损伤[16]。
, http://www.100md.com
5 同型半胱氨酸(Hcy)
在肾功能不全时,Hcy水平升高,并与血肌酐水平呈正相关,与肌酐清除率呈负相关。Hcy升高的机制尚不完全清楚。仅有小部分Hcy从肾脏排泄,故肾脏排泄率降低并不能完全解释CRF时的高同型半胱氨酸血症。在CRF时,肾小管摄取Hcy减少;此外正常人的Hcy可通过分解代谢而变成半胱氨酸,也可甲基化成为蛋氨酸。尿毒症时肾小管功能减退,Hcy的分解和(或)甲基化受抑制[17]。有人报告,尿毒症患者甲基四氢叶酸还原酶缺陷是由于其纯合子基因突变发生率(677C被T代替)比健康人增高所致[18]。血Hcy是叶酸盐缺乏的一个敏感的生物标记物。当叶酸盐缺乏时,血中Hcy水平增高。叶酸的活性形式是5-甲-四氢叶酸,在Hcy转变为蛋氨酸时,它作为联合底物。
高Hcy血症是心血管疾病的一个独立的危险因素,随着血中Hcy水平增高,颈动脉狭窄、颈动脉内膜增厚、冠状动脉疾病、心肌梗塞[19]和深静脉血栓的发病率升高。高Hcy血症致血管疾病的机制,主要与引起内皮产生的松弛因子(NO)减少、刺激平滑肌细胞增殖[20]、增加血栓调节素(thrombomodulin)的表达及蛋白酶C的活性、抑制内皮细胞生长等作用有关。Hcy也可通过使低密度脂蛋白氧化而促进动脉硬化的发生与发展。
, 百拇医药
有人报告,尿毒症患者血中Hcy水平可比健康人高4倍,而在有过动脉闭塞病史的尿毒症患者中更高。通过透析可部分(11%~50%)将Hcy清除[21]。血中总Hcy浓度由自由Hcy及与蛋白结合的Hcy组成,血中大多以结合形式存在,因此透析只能清除体内部分Hcy,而难以将Hcy水平降至正常。据报道,正常人每天饮食中摄入叶酸盐400μg时,血中Hcy水平可维持在相对较低水平;尿毒症患者每天服叶酸5~10mg,即可明显降低血中Hcy的水平[22]。
6 瘦素(Leptin)
瘦素是由肥胖基因编码,脂肪细胞分泌的肽类激素,它由167个氨基酸组成,分子量16 000。非肥胖尿毒症患者血中瘦素水平明显升高,其原因与瘦素的排泄障碍及某些因素如高胰岛素血症、C反应蛋白升高及TNF-α、IL-1增多等刺激其合成增加有关。瘦素可引起食欲下降,使蛋白质、热量摄入减少,并增加能量消耗,很可能是引起CRF患者食欲减退、营养不良的原因之一。透析治疗前后,血清瘦素水平变化较小,透析治疗难以纠正尿毒症患者的高瘦素血症。据报告,给尿毒症患者胰岛素样生长因子-1治疗,其血瘦素水平可明显降低[23]。
, http://www.100md.com
7 其 它
NO合成抑制物、活性维生素D抑制物等也具有潜在的毒性作用。NO是L-精氨酸合成酶在内皮细胞中形成的,NO有松弛血管的作用,抑制血小板粘附和聚集,是神经传导和神经毒性介质。NO能杀死或抑制许多病原体,包括细菌、真菌、寄生虫、结核杆菌等。尿毒症时有几种毒素影响NO的合成,如不对称的二甲-L-精氨酸(ADMA)可作为抑制剂。NO的合成受抑制可导致隐静脉和肠系膜血管收缩、高血压、肾小球局部缺血、神经病变。在大脑中,ADMA引起血管收缩及抑制乙酰胆碱诱导的血管松弛[24]。
用尿毒症的超滤液灌注正常大鼠,可抑制1,25(OH)2D3的合成,也可使其小肠钙三醇受体浓度明显降低。肾衰时,钙三醇受体的合成在转录部位被抑制,并有明显的钙三醇抵抗。肾功能正常时,钙三醇诱导的单核细胞CD14表达是升高的,而尿毒症患者的超滤液不仅能抑制基本的CD14的表达,也可使钙三醇诱导的单核细胞CD14表达明显受到抑制。实验研究已发现尿酸、黄嘌呤、次黄嘌呤等物质具有这种抑制作用[25]。
, 百拇医药
CMPF及硫酸吲哚酚均为与蛋白结合的有机酸,结合率分别高达98%、90%,其毒性作用抑制药物与蛋白结合,CMPF可抑制红细胞生成,抑制肝内谷胱甘肽-S-转移酶及线粒体呼吸。硫酸吲哚酚的重要作用之一是加速肾小球硬化,降低肝细胞内甲状腺素的转移。
结语 近年新发现的某些尿毒症毒素的作用,使人们加深了对尿毒症发病机制的认识。加强尿毒症毒素的清除途径的研究,包括应用血液吸附剂、口服吸附剂、高效的透析器和某些药物等,将可能进一步改善CRF患者尿毒症症状和患者预后。
作者单位:郑法雷 中国医学科学院,中国协和医科大学北京协和医院肾内科(北京,100730)
参考文献
1 Massry SG.Is parathyroid hormone a uremic toxin?Nephron,1977,19:125
, http://www.100md.com
2 Horl WH,Haag-Weber M,Georgopoulos A et al. Physicochemical characterization of a polypeptide present in uremic serum that inhibits the biological activity of polymorphon-uclear cells.Proc Natl Acad Sci USA,1990,87:6353
3 Haag-Weber M,Mai B,Horl WH.Impaired cellular host defence in peritoneal dialysis by two granulocyte inhibitory proteins.Nephrol Dial Transplant,1994,9:1769
4 Tschesche H,Kopp C,Horl WH et al.Inhibition of degranulation of polymorphonuclear leukocytes by angiogenin and tryptic fragment.J Biol Chem,1994,269:30274
, 百拇医药
5 Balke N,Holtkamp U,Horl WH et al.Inhibition of degranulation of human polymorphonuclear leukocytes by complement factor D.FEBS Letters,1995,371:300
6 Cohen G,Rudnicki M,Horl WH et al.Isolation of modified ubiquition as a neutrophil chemotaxis inhibitor from uremic patients.J Am Soc Nephrol,1998,9:451
7 Cohen G,Haag-Weber M,Mai B et al.Effect of immunoglobulin light chains from hemodialysis and CAPD patients on PMNL functions.J Am Soc Nephrol,1995,6:1592
, 百拇医药
8 Stim J,Shaykh M,Anwar F et al.Factors determining hemoglobin carbamylation in renal failture.Kidney Int,1995,48:1605
9 Balion CM,Draisey TF,Thibert RJ.Carbamylated hemoglubin and carbamylated plasmaprotein in hemodialyzed patients.Kidney Int,1998,53:488
10 Kraus LM,Traxinger R.N-carbamyl-asparagine inhibits insulin sensitive glucosw uptake in ray adipocytes.The 7th International Congress on Nutrition and Metabolism in Renal Disease.Stockholm:Sweden,1994.194-195A
, 百拇医药
11 Erill S,Calvo R,Carlos R.Plasma protein caramylation and decreased acidic druk protein binding in ureamia.Clin Pharm Ther,1980,27:612
12 Yoshida S,Yamada K,Hamaguchi et al. Growth factors in cardiac tissues of patient on maintence dialysis and with kidney transplantation.Clin Nephrol,1998,49:273
13 Makita Z,Bucala R,Rayfield EJ et al.Reactive glycosylation endproducts in diabetic ureamia and treatment of renal failure.Lancet,1994,343:1519
, 百拇医药
14 Davies KJ.Protein damage and degradation by oxygen redicals.General ascepts.J Biol Chem,1987,262:9895
15 Gurne T,Reinhecker T,Joshi M et al.Proteolysis in cultured liver epithelial cells during oxidative stress.Role of the multicatalytic proteinase complex,proteasome.J Biol Chem,1995,270:2344
16 Descamps-Latscha B,Herbelin A,Nguyen AT et al.Balance between IL-1β,TNF-α and their specific inhibitors in chronic renal failture and maintance dialysis.Relationships with activation markers of T cells,B cells,and monocytes.J Immunol,1995,154:882
17 Hultberg B,Andersson A,Sterner G.Plasma homocysteine in renal failure.Clin Nephrol,1993,4:, http://www.100md.com
单位:赵素梅 首都医科大学附属北京红十字朝阳医院肾内科
关键词:慢性肾功能衰竭;尿毒症毒素;发病机制
赵素梅 综述 郑法雷 审校赵素梅 综述 郑法雷 审校
在慢性肾功能不全进行性加重后,体内有200种以上物质的水平比正常人增高,其中有些物质具有毒性作用。这些具有毒性作用的物质在体内积聚,是引起尿毒症症状、代谢紊乱和多个系统功能失调的主要原因之一。近二十年来关于大、中分子尿毒症毒素的研究进展相对迟缓,但近年来有关学者在这方面的研究已有某些新发现,有些毒素蛋白已被分离出,通过体内、外实验对其性质及毒性有了一定的认识,对以前已知毒素的作用也有了新的了解。
1 被认为是“新毒素”的主要物质
, 百拇医药
凡被称为“尿毒症毒素”的物质应具备以下条件:①在尿毒症患者体内该物质的浓度显著高于正常;②该物质的化学结构和理化性质明确;③高浓度的该物质与特异的尿毒症临床表现相关;④动物试验或体外实验证实该物质在其浓度与尿毒症患者体内浓度相似时,可出现类似毒性作用;⑤体液内该物质浓度下降与尿毒症症状、体征改善相伴随[1]。
据近年有关文献报告,目前被认为可能是“新”尿毒症毒素的物质约有20种左右(表1)。
表1 近年报告的具有尿毒症毒素作用的物质
1 粒细胞抑制蛋白Ⅰ(GIP-Ⅰ)和粒细胞抑制蛋白Ⅱ(GIP-Ⅱ)
2 趋化抑制蛋白(CIP)
3 中性粒细胞脱颗粒抑制蛋白Ⅰ(DIP-Ⅰ)和中性粒细胞脱颗粒抑制蛋白Ⅱ(DIP-Ⅱ)
, 百拇医药
4 同型半胱氨酸(Homocysteine,Hcy)
5 晚期糖基化终末产物(AGEs)和终末氧化蛋白产物(AOPP)
6 氨甲酰化的氨基酸和蛋白质
7 瘦素(Leptin)
8 活性维生素D抑制物
9 影响一氧化氮合成的毒素
10 其它:硫酸吲哚酚,癌原性杂环胺,马尿酸,假尿嘧啶核苷,免疫球蛋白轻链,3-羧-4-甲-5-丙基呋喃戊酮酸(CMPF)
2 具有抑制免疫细胞活性作用的毒素
这类毒素包括粒细胞抑制蛋白Ⅰ(GIP-Ⅰ)、粒细胞抑制蛋白Ⅱ(GIP-Ⅱ)、趋化抑制蛋白(CIP)、中性粒细胞脱颗粒抑制蛋白Ⅰ(DIP-Ⅰ)、中性粒细胞脱颗粒抑制蛋白Ⅱ(DIP-Ⅱ)、免疫球蛋白轻链等。GIP-Ⅰ和GIP-Ⅱ都是从规律血透患者的血浆中分离出来的[2]。GIP-Ⅰ分子量为28000,电离点位于4.0~4.5,属于免疫球蛋白轻链类,其中80%与κ轻链同类,40%与λ轻链同类。GIP-Ⅱ分子量为9500,与β2微球蛋白(β2-MG)同一类。
, 百拇医药
GIP-Ⅰ和GIP-Ⅱ具有抑制多核粒细胞(PMN)对糖摄取的作用。GIP-Ⅰ是通过抑制趋化性肽(甲酰-甲硫氨酰-亮氨酰-苯丙氨酸)而影响PMN的功能,抑制PMN的趋化性、氧化代谢及细胞内的杀菌作用。GIP-Ⅱ则抑制由佛波醇酯(phorbolester)刺激的糖摄取;此外它也可刺激人体单核细胞分泌IL-1β和IL-6[3]。
DIP-Ⅰ和DIP-Ⅱ均为尿毒症规律血透患者的血浆超滤液中提出。DIP-Ⅰ分子量为14400,与血管生成素(Angiogenin)属同一类物质,在尿毒症时比正常人高2~3倍,而在CAPD患者的腹透液中DIP-Ⅰ浓度可高达正常人的1000倍,提示DIP-Ⅰ是由腹腔中的细胞合成。DIP-Ⅰ可抑制自发性及刺激后的PMN脱颗粒[4],而应用人重组血管生成素多克隆抗体可消除DIP-Ⅰ对PMN的这种抑制作用。DIP-Ⅰ不仅抑制PMN的乳肝褐质(Lactoferrin)、胶原酶、明胶酶的释放,而且也抑制弹性硬蛋白酶释放。含有血管生成素片段中的二硫化物C39~C92,对PMN的抑制作用与DIP-Ⅰ作用相同,但要弱得多。这表明DIP-Ⅰ在PMN细胞上有一个新的、生物学活性位置,而与血管生成素的活性部位有所不同。DIP-Ⅱ分子量为24 000,这种蛋白质可能为补体D,在血透患者中补体D比正常人高约10倍,补体D可引起刺激后的剂量依赖性的乳肝褐质脱颗粒约减少到正常对照的34%[5]。
, 百拇医药
CIP是从腹透患者的腹透液中分离所得,在体外实验中,它抑制PMN的趋化呈浓度依赖性,且不可逆转。氨基酸序列测定显示这种多肽与泛素有着相同的氨基末端,但比泛素电离点更偏酸性,而泛素本身对PMN的趋化性无影响。由此看来CIP很可能是被修饰的泛素,其分子量为8500[6]。
免疫球蛋白轻链κ和λ的单体和二聚体在体外很小的浓度即可抑制PMN的糖摄取和趋化性,由B淋巴细胞产生的免疫球蛋白轻链多于重链,因此有少量的轻链以自由形式存在于血液中,严重肾功能减退患者其血中自由轻链的水平增高5倍[7]。
3 氨甲酰化氨基酸和蛋白质
正常时人体内的尿素可转变为氰酸盐,氰酸盐分子通过氨甲酰化被清除。而尿毒症时,氨甲酰化氰酸盐不能被有效清除,造成积聚,从而引起血液中氨基酸和蛋白质氨甲酰化(附图)。氨甲酰化的氨基酸称为C-AA,没有氨甲酰化的氨基酸为F-AA。由于C-AA没有自由的氨基与另一个氨基酸的羧基结合,引起蛋白质合成障碍,因而是造成尿毒症患者的营养不良的因素之一[8],也可引起某些物质代谢的障碍,甚至影响组织、器官的功能(表2)。

, 百拇医药
附图 氨基酸的氨甲酰化(以赖氨酸为例)
表2 氨甲酰化蛋白质、氨基酸的毒性
1 蛋白质合成↓ 蛋白质分解↑
2 蛋白质功能变化
如血红蛋白氨甲酰化→血红蛋白释放氧减少
3 酶功能变化
纤溶酶、G6PD、ALP、RNase、胃蛋白酶、糜蛋白酶
4 组织-器官功能的变化:如大脑皮质功能、周围神经功能障碍
5 药物生物利用度的变化:氨甲酰化蛋白质与药物结合↓
血红蛋白中缬氨酸的氨基端被氨甲酰化时,形成了与氧高亲和力的氨甲酰血红蛋白,使氧离曲线左移,减少氧的释放,造成组织缺氧[9]。尿毒症时,由于天门冬酰胺的氨甲酰化,且呈剂量依赖方式,损害胰岛素敏感的糖转运系统,是造成胰岛素抵抗的原因之一,因而使CRF患者体内组织的葡萄糖摄取量减少[10]。
, 百拇医药
体内结构蛋白、胞浆蛋白、内质网蛋白的氨甲酰化,可影响器官的正常功能。白蛋白在结合和转运酸性药物中起重要的作用,氨甲酰化的白蛋白可使药物的生物度利用降低[11]。在神经系统,酶和结构蛋白的氨甲酰化,对大脑皮质功能、学习和记忆造成不利影响,也可引起外周神经病变。
氨甲酰化可使多种激素和酶活性降低,如胰岛素、催产素、葡萄糖-6-磷酸脱氢酶、纤溶酶、谷氨酸脱氢酶、磷酸化酶a和b、丙酮酸激酶、碱性磷酸酶、核糖核酸酶、糜蛋白酶、胃蛋白酶等,从而影响多种物质的代谢和某些器官的功能。
4 晚期糖基化终末产物(AGE)和终末氧化蛋白产物(AOPP)
有人认为AGE可代表尿毒症中分子物质毒性的“现代形式”,多肽AGE分子量多数均小于10 000。AGE是蛋白质的氨基组、脂质和脂蛋白非酶糖基化反应的终产物,反应早期产物仍有可逆性,而其晚期产物(AGE)则较稳定,已失去可逆性。慢性肾衰时,由于肾脏清除障碍及其他尚不清楚的原因,体内一些短半衰期的血浆蛋白如β2-MG被AGE修饰并导致蓄积。高流量透析可显著降低由AGE修饰的小分子,在糖尿病肾衰患者中可使其降低47.4%,在非糖尿病肾衰患者中可使其降低60.6%,然而3h后其浓度又回到治疗前水平。CAPD患者虽然与葡萄糖持续接触,但血中AGE水平并不比血透者高;然而腹膜组织中的蛋白质可发生糖基化。此外,某些食物中含有的AGE在小肠吸收,故食物的摄取也可增加尿毒症患者的血AGE水平。高AGE水平是尿毒症患者心血管并发症原因之一,实验发现血透患者冠状动脉壁AGE积聚[12],AGE修饰的β2-MG是透析相关性淀粉样变性的淀粉样物质的主要成分,它能刺激巨噬细胞增加分泌TNF-α和IL-1β,也能增加人单核细胞的趋化性,故淀粉样物质沉积处出现单核/巨噬细胞聚集及原发性炎症反应,导致骨和关节损害。这些效应是由AGE受体(RAGE)即AGE结合蛋白所介导的,AGE和RAGE相互作用,可引起氧化应激反应,导致血管通透性增加,血管壁增厚[13]。
, 百拇医药
在尿毒症时血中存在着氧化损伤的蛋白产物,称为终末氧化蛋白产物(Advanced oxidation protein products,AOPP)。由活性中性粒细胞产生的氧化物增多,或这些氧化物的清除减少,均可导致AOPP增加。氧化物是吞噬细胞尤其是中性粒细胞在呼吸爆裂时产生的大量的反应性氧类(ractive oxygen species)物质,为氧分子被单价还原成过氧离子(O-2)、原始羟基(OH0)、单价氧(1O2)和含氯氧化物(HOCl),它们可杀死病原菌,但当宿主的抗氧化系统被抑制时,它也造成组织损伤[14]。氧化应激时氧化物前体与抗氧化物的平衡被打破,而前者偏高,使DNA、蛋白和脂质等人体基本成分的氧化增多;此外,氧化物被认为是炎症介质,可导致氧化性结构损伤和细胞的功能紊乱。氧化物对蛋白质水解的敏感度依赖于氧化应激的强度[15]。
据报告尿毒症患者AOPP水平可高出正常人3倍。AOPP的积聚可反映尿毒症时清除受损伤蛋白的能力下降。高分子量的AOPP为600 000,是蛋白质的集合体;低分子量的AOPP为80 000左右,白蛋白是其主要成分。AOPP是一组“奇特”的毒素和(或)前炎症介质,在尿毒症时AOPP可引起免疫紊乱和炎症损伤[16]。
, http://www.100md.com
5 同型半胱氨酸(Hcy)
在肾功能不全时,Hcy水平升高,并与血肌酐水平呈正相关,与肌酐清除率呈负相关。Hcy升高的机制尚不完全清楚。仅有小部分Hcy从肾脏排泄,故肾脏排泄率降低并不能完全解释CRF时的高同型半胱氨酸血症。在CRF时,肾小管摄取Hcy减少;此外正常人的Hcy可通过分解代谢而变成半胱氨酸,也可甲基化成为蛋氨酸。尿毒症时肾小管功能减退,Hcy的分解和(或)甲基化受抑制[17]。有人报告,尿毒症患者甲基四氢叶酸还原酶缺陷是由于其纯合子基因突变发生率(677C被T代替)比健康人增高所致[18]。血Hcy是叶酸盐缺乏的一个敏感的生物标记物。当叶酸盐缺乏时,血中Hcy水平增高。叶酸的活性形式是5-甲-四氢叶酸,在Hcy转变为蛋氨酸时,它作为联合底物。
高Hcy血症是心血管疾病的一个独立的危险因素,随着血中Hcy水平增高,颈动脉狭窄、颈动脉内膜增厚、冠状动脉疾病、心肌梗塞[19]和深静脉血栓的发病率升高。高Hcy血症致血管疾病的机制,主要与引起内皮产生的松弛因子(NO)减少、刺激平滑肌细胞增殖[20]、增加血栓调节素(thrombomodulin)的表达及蛋白酶C的活性、抑制内皮细胞生长等作用有关。Hcy也可通过使低密度脂蛋白氧化而促进动脉硬化的发生与发展。
, 百拇医药
有人报告,尿毒症患者血中Hcy水平可比健康人高4倍,而在有过动脉闭塞病史的尿毒症患者中更高。通过透析可部分(11%~50%)将Hcy清除[21]。血中总Hcy浓度由自由Hcy及与蛋白结合的Hcy组成,血中大多以结合形式存在,因此透析只能清除体内部分Hcy,而难以将Hcy水平降至正常。据报道,正常人每天饮食中摄入叶酸盐400μg时,血中Hcy水平可维持在相对较低水平;尿毒症患者每天服叶酸5~10mg,即可明显降低血中Hcy的水平[22]。
6 瘦素(Leptin)
瘦素是由肥胖基因编码,脂肪细胞分泌的肽类激素,它由167个氨基酸组成,分子量16 000。非肥胖尿毒症患者血中瘦素水平明显升高,其原因与瘦素的排泄障碍及某些因素如高胰岛素血症、C反应蛋白升高及TNF-α、IL-1增多等刺激其合成增加有关。瘦素可引起食欲下降,使蛋白质、热量摄入减少,并增加能量消耗,很可能是引起CRF患者食欲减退、营养不良的原因之一。透析治疗前后,血清瘦素水平变化较小,透析治疗难以纠正尿毒症患者的高瘦素血症。据报告,给尿毒症患者胰岛素样生长因子-1治疗,其血瘦素水平可明显降低[23]。
, http://www.100md.com
7 其 它
NO合成抑制物、活性维生素D抑制物等也具有潜在的毒性作用。NO是L-精氨酸合成酶在内皮细胞中形成的,NO有松弛血管的作用,抑制血小板粘附和聚集,是神经传导和神经毒性介质。NO能杀死或抑制许多病原体,包括细菌、真菌、寄生虫、结核杆菌等。尿毒症时有几种毒素影响NO的合成,如不对称的二甲-L-精氨酸(ADMA)可作为抑制剂。NO的合成受抑制可导致隐静脉和肠系膜血管收缩、高血压、肾小球局部缺血、神经病变。在大脑中,ADMA引起血管收缩及抑制乙酰胆碱诱导的血管松弛[24]。
用尿毒症的超滤液灌注正常大鼠,可抑制1,25(OH)2D3的合成,也可使其小肠钙三醇受体浓度明显降低。肾衰时,钙三醇受体的合成在转录部位被抑制,并有明显的钙三醇抵抗。肾功能正常时,钙三醇诱导的单核细胞CD14表达是升高的,而尿毒症患者的超滤液不仅能抑制基本的CD14的表达,也可使钙三醇诱导的单核细胞CD14表达明显受到抑制。实验研究已发现尿酸、黄嘌呤、次黄嘌呤等物质具有这种抑制作用[25]。
, 百拇医药
CMPF及硫酸吲哚酚均为与蛋白结合的有机酸,结合率分别高达98%、90%,其毒性作用抑制药物与蛋白结合,CMPF可抑制红细胞生成,抑制肝内谷胱甘肽-S-转移酶及线粒体呼吸。硫酸吲哚酚的重要作用之一是加速肾小球硬化,降低肝细胞内甲状腺素的转移。
结语 近年新发现的某些尿毒症毒素的作用,使人们加深了对尿毒症发病机制的认识。加强尿毒症毒素的清除途径的研究,包括应用血液吸附剂、口服吸附剂、高效的透析器和某些药物等,将可能进一步改善CRF患者尿毒症症状和患者预后。
作者单位:郑法雷 中国医学科学院,中国协和医科大学北京协和医院肾内科(北京,100730)
参考文献
1 Massry SG.Is parathyroid hormone a uremic toxin?Nephron,1977,19:125
, http://www.100md.com
2 Horl WH,Haag-Weber M,Georgopoulos A et al. Physicochemical characterization of a polypeptide present in uremic serum that inhibits the biological activity of polymorphon-uclear cells.Proc Natl Acad Sci USA,1990,87:6353
3 Haag-Weber M,Mai B,Horl WH.Impaired cellular host defence in peritoneal dialysis by two granulocyte inhibitory proteins.Nephrol Dial Transplant,1994,9:1769
4 Tschesche H,Kopp C,Horl WH et al.Inhibition of degranulation of polymorphonuclear leukocytes by angiogenin and tryptic fragment.J Biol Chem,1994,269:30274
, 百拇医药
5 Balke N,Holtkamp U,Horl WH et al.Inhibition of degranulation of human polymorphonuclear leukocytes by complement factor D.FEBS Letters,1995,371:300
6 Cohen G,Rudnicki M,Horl WH et al.Isolation of modified ubiquition as a neutrophil chemotaxis inhibitor from uremic patients.J Am Soc Nephrol,1998,9:451
7 Cohen G,Haag-Weber M,Mai B et al.Effect of immunoglobulin light chains from hemodialysis and CAPD patients on PMNL functions.J Am Soc Nephrol,1995,6:1592
, 百拇医药
8 Stim J,Shaykh M,Anwar F et al.Factors determining hemoglobin carbamylation in renal failture.Kidney Int,1995,48:1605
9 Balion CM,Draisey TF,Thibert RJ.Carbamylated hemoglubin and carbamylated plasmaprotein in hemodialyzed patients.Kidney Int,1998,53:488
10 Kraus LM,Traxinger R.N-carbamyl-asparagine inhibits insulin sensitive glucosw uptake in ray adipocytes.The 7th International Congress on Nutrition and Metabolism in Renal Disease.Stockholm:Sweden,1994.194-195A
, 百拇医药
11 Erill S,Calvo R,Carlos R.Plasma protein caramylation and decreased acidic druk protein binding in ureamia.Clin Pharm Ther,1980,27:612
12 Yoshida S,Yamada K,Hamaguchi et al. Growth factors in cardiac tissues of patient on maintence dialysis and with kidney transplantation.Clin Nephrol,1998,49:273
13 Makita Z,Bucala R,Rayfield EJ et al.Reactive glycosylation endproducts in diabetic ureamia and treatment of renal failure.Lancet,1994,343:1519
, 百拇医药
14 Davies KJ.Protein damage and degradation by oxygen redicals.General ascepts.J Biol Chem,1987,262:9895
15 Gurne T,Reinhecker T,Joshi M et al.Proteolysis in cultured liver epithelial cells during oxidative stress.Role of the multicatalytic proteinase complex,proteasome.J Biol Chem,1995,270:2344
16 Descamps-Latscha B,Herbelin A,Nguyen AT et al.Balance between IL-1β,TNF-α and their specific inhibitors in chronic renal failture and maintance dialysis.Relationships with activation markers of T cells,B cells,and monocytes.J Immunol,1995,154:882
17 Hultberg B,Andersson A,Sterner G.Plasma homocysteine in renal failure.Clin Nephrol,1993,4:, http://www.100md.com
参见:首页 > 医疗版 > 疾病专题 > 肾脏内科 > 肾病信息 > 尿毒症