异常结肠上皮细胞增生与分化的低脂制乳食品调节随机对照实验
作者:王宏宇
单位:
关键词:
美国医学会杂志中文版990306 Modulation of Abnormal Colonic Epithelial Cell
Proliferation and Differentiation by Low-Fat Dairy Foods
A Randomized Controlled Trial
Peter R. Holt, MD; Evren O. Atillasoy, MD; Jody Gilman, RD; Janet Guss, MS;
Steven F. Moss, MD; Harold Newmark, MS; Kunhua Fan, MD; Kan Yang, MD; Martin Lipkin, MD Janet Guss, MS;
, http://www.100md.com
Steven F. Moss, MD; Harold Newmark, MS; Kunhua Fan, MD; Kan Yang, MD; Martin Lipkin, MD
背景——人类结肠肿瘤发生前,结肠上皮细胞显示生长和分化的变异。这种具有癌变危险的变异被称为癌的中间生物标志(intermediate biomarkers of risk)。通过营养素或药物调节使粘膜恢复正常是化学预防结肠癌的手段之一。
目的——确定通过奶制品增加钙的摄入是否可使结肠生物标志正常化。
设计——随机、单盲、对照研究。
地点——门诊。
研究对象——70例因结肠腺瘤性息肉而有息肉切除病史的患者。
, 百拇医药 干预——钙含量为1 200 mg/d的低脂奶制品。根据饮食(对照组、高钙组)和年龄(<60岁、≥60岁)将患者随机分为4组。
主要观察指标——全结肠上皮细胞以及胸腺嘧啶脱氧核苷标记的上皮细胞数量和位置的变化;硫粘蛋白(主要由远侧结直肠上皮细胞分泌)与涎粘蛋白(sialomucins)比例以及细胞角蛋白(cytokeractin) AE1表达的变化。
结果——在6和12个月的治疗期间,结肠上皮细胞增生减弱(P<0.05),增生腔隙减小(P<0.05),酸性粘蛋白(P<0.02)、细胞角蛋白AE1的分布(P<0.05)以及细胞核大小(P<0.05)有恢复正常倾向。对照组在6个月和12个月时增生指标与基线无差异(P>0.05)。
结论——对于有结肠肿瘤危险的患者,通过低脂奶制品将钙摄入量增加至1 200 mg/d,可减弱结肠上皮细胞增生,使细胞分化标志恢复正常。
, 百拇医药
美国大约有134 000例结肠癌患者,每年因此死亡者约55 000例1。为此,寻找可能的化学预防营养疗法是肿瘤研究的重要目标之一。有关流行病学证据显示,饮食钙和维生素D水平与结肠癌的发生呈负相关关系2-4。加钙饮食可抑制啮齿动物和人6-8结肠上皮细胞增生降低粪水的细胞毒性5,抑制啮齿动物结肠肿瘤形成9。在人结肠癌预防研究中,通常用细胞增生与分化作为评价化学预防效果的生物标志5。
本文患者既往均有结肠腺瘤病史,与正常人群相比,属结肠肿瘤高危人群10。患者随机分为两组,实验组接受奶制品,对照组饮食照旧。随访观察1年,了解直肠乙状结肠粘膜上皮细胞的变化,描述细胞增生、分化、成熟状况。
方 法
患 者
, 百拇医药
本文患者年龄均大于18岁,均有结肠腺瘤性息肉病史。有下列情况者除外:结肠癌病史,阑尾切除术以外的肠道手术史,吸收障碍,炎性肠病,明显的内分泌或代谢疾病,乳糖不耐受症,总钙摄入量超过1 000 mg/d,补充钙超过400 mg/d或补充维生素D的摄入。用随机排列区组法将患者分组11。按性别和年龄(≥60,<60岁)将患者分为4组,产生一种独立的治疗分配方案。每个方案均有相同数量的患者在2、4或6区中被随机分至各治疗组。区组顺序在每个方案是随机的。采用SAS程序执行随机化排序。
从医院记录中共筛选出350例有近期腺瘤性息肉病史的患者。患者的保健医生允许我们与其中230例进行有关接触。这些可能的志愿者基本是健康的。实际接触180例,65例因饮食原因、补钙或乳糖酶缺乏症史而被排除;25例由于医疗原因不能参加试验;另外20例不愿参加试验。最后有70例进入本试验,对照组33例,实验组37例(图1)。对患者医院体检、4次营养面试、4次活检造成的不便和花费予以补偿。此研究为单盲的。受试者知道进行的是一种特殊饮食试验,然而他们不知道该饮食与所得资料关系的意义。样本大小估计以我们以往有关钙调节减低增生标志指数的研究为依据12。试验要求每组25~30例,以便检出试验组与对照组间的显著差异。维持I类误差在5%,检出显著差异的把握度为80%,采用双尾检验。本研究于1993年开始,于1995年6月完成。
, 百拇医药
营养的评估与监控
营养摄入水平由一位专门的营养学家采用24小时食物回忆和3天饮食记录(两次)进行评估。两次基线评估间隔1个月。以后按6个月的间隔进行。特别注意有关奶制食品资料的收集。食物回忆还按3个月的间隔进行,并对其变化进行研究。由于食物成分及其添加剂经常发生变化,故对食品的标签和品牌均做出相应要求。
实验组患者每日钙摄入总量增加至1 200 mg,维持恒定的脂肪、热卡和纤维摄入(建议每天减少糖45 g,蛋白质30 g,脂肪5 g)。我们为实验组提供了一种脱脂奶酪,同时要求增加其他低脂奶制品的摄入。不补钙对照组饮食如常,每3个月随访一次。3天饮食记录的多记录计算分析采用明尼苏达营养指标系统软件,版本2.7(Nutrition Coordinating Center, University of Minnesota, Minneapolis)。
直肠乙状结肠活检
, 百拇医药
直肠乙状结肠活检标本取自内镜检查表现正常的“扁平”粘膜。基线2次(间隔1个月),然后在6个月及12个月时各1次。自来水灌肠后于上午8~10点行纤维乙状结肠镜检,并于距肛缘10~15 cm处4个象限用Jumbo钳取6~8个活体标本。活检标本用0.185 MBq[3H]胸腺嘧啶脱氧核苷孵育后12用10%缓冲福尔马林液固定,以便进行[3H]胸腺嘧啶脱氧核苷掺入增生细胞的研究;或者用95%乙醇固定,以便观察细胞分化标志。
细胞增生与分化的研究
1.细胞增生:在15~25个完整的陷窝腺管(crypts),按以前的描述,对细胞增生进行了研究12。记录每个陷窝腺管上皮细胞的总数以及有胸腺嘧啶脱氧核苷标记的上皮细胞的数量和位置;用计算机系统进行自动处理13。
2.分化标志研究:在10~12个完整的陷窝腺管,用高铁二胺溶液对酸性粘蛋白进行染色14。硫粘蛋白主要由结直肠远侧上皮细胞分泌。根据硫粘蛋白与涎粘蛋白的比例可确定粘蛋白是否有异常14。
, 百拇医药
使用一种细胞角蛋白AE1单克隆抗体,用免疫组化法研究细胞角蛋白AE1的表达。在10~12个完整的腺管测定了上皮细胞内AE1的表达。在正常结直肠粘膜,细胞角蛋白AE1的表达局限于粘膜表面和腺管上部,因此细胞角蛋白AE1表达积分很少。当抗原向腺管下部扩增时,细胞角蛋白AE1的表达增加。
3.细胞核的形态测量:切片(3 μm)苏木素和伊红染色后用计算机辅助的细胞形态分析仪测定结直肠上皮细胞的大小,并在平均10个完整的腺管中,测定胞核的面积、周径和直径。
4.统计学分析:对两组患者各时间点(基线、6个月及12个月)24小时营养消耗进行了比较。将两个基线值的平均数作为每例患者的数值。两组各时间点结果的比较用Student t检验。此外,我们还对两组3个时间点不同营养、生物标志进行了方差分析,以便确定饮食改变或生物标志的时间效果。时间为重复量数(repeated measure),饮食或生物标志为组间因素。然后,对两组所有具显著作用的影响因素进行Post hoc Duncan multiple range检验,以便检出各时间点有关均值的差异(P<0.05)。以每日脂肪总摄入量作为协变量对生物标志进行协方差分析,结果显示生物标志的时间变化显著。对两组间最小校正均方值亦进行了比较。
, 百拇医药
结 果
总共对70例患者进行了观察,实验组37例,对照组33例,两组患者人口统计学及息肉切除史匹配(表1)。有11例患者退出研究(实验组7例,对照组4例),退出者或为个人原因或为医疗原因所致,但两组无差异(图1)。
表1 患者的特征 特征
对照组
实验组
例数
33
37
年龄,mean(SE),岁
66(2)
, http://www.100md.com
67(3)
≥65
19
25
<65
14
12
性别
男
22
22
女
11
15
, 百拇医药
种族
黑人
8
12
白人
19
21
拉丁美洲人
5
4
其他
1
0
体重,mean(SE),kg
, 百拇医药
76.5(2.7)
79.4(3.6)
腺瘤距最后一次息肉
切除术的时间,mean(SE),月
7.2(3)
8.6(2)
多发的息肉
切除术,%
14
16

, http://www.100md.com
图1 随机研究流程。对照组4例退出,因个人原因和医疗原因退出者各2例。实验组7例退出,其中2例为个人原因,1例为医疗原因,2例不服从试验,2例对牛奶增加不耐受
基线时对照组和实验组营养摄入近似(表2)。研究期间对照组维持基线营养摄入,包括钙的摄入。实验组每日钙摄入量从730 mg增至810 mg。基线食物钙分析显示,53%~60%的钙来自奶制品(35%来自奶,6%来自酸奶,16%来自奶酪)。实验组增加的食物钙83%来自奶制品(31%来自奶,11%来自酸奶和冰激淋,41%来自奶酪制品)。实验组能量摄入较对照组高1%~5%。
表2 每日营养物摄入计算*
对照组
乳类组
P值
, http://www.100md.com
能量,kJ
基线
6745(77)
7459(84)
>0.10
6个月
6686(74)
7001(78)
>0.10
12个月
7279(96)
7371(73)
, 百拇医药 >0.10
蛋白质,g
基线
70.2(4.3)
74.9(3.3)
>0.10
6个月
70.2(3.5)
82.1(3.5)
<0.02
12个月
74.7(4.7)
, 百拇医药 86.0(4.0)
0.07
脂肪,g
基线
49.9(3.1)
60.0(4.1)
0.06
6个月
49.5(3.5)
45.7(3.8)
>0.10
12个月
56.0(6.3)
, 百拇医药
45.2(3.2)
>0.10
钙,mg
基线
642(48)
608(29)
>0.10
6个月
725(60)
1421(76)
<0.001
12个月
685(31)
, 百拇医药
1538(103)
<0.001
磷酸盐,mg
基线
1082(59)
1073(47)
>0.10
6个月
1106(63)
1767(100)
<0.001
12个月
, 百拇医药
1192(104)
1915(131)
<0.001
维生素D,mg
基线
5.2(0.9)
4.4(0.5)
>0.10
6个月
4.9(0.6)
5.4(0.4)
>0.10
, 百拇医药
12个月
4.7(0.6)
5.8(0.6)
>0.10
纤维素,g
基线
16.8(1.7)
16.4(1.0)
>0.10
6个月
17.2(1.4)
16.0(1.2)
, 百拇医药
>0.10
12个月
20.5(2.4)
17.1(1.1)
>0.10
其他
基线
10.8(1.2)
10.3(0.7)
>0.10
6个月
11.0(1.0)
, http://www.100md.com 10.1(0.8)
>0.10
12个月
13.4(1.8)
10.9(0.8)
>0.10
* 两组总的平均每日营养摄入用3天食物日记计算,详见方法所述 对照组:基线时33例;6个月时29例;12个月时29例
对照组:基线时33例;6个月时29例;12个月时29例 实验组:基线时37例;6个月时29例;12个月时30例
实验组:基线时37例;6个月时29例;12个月时30例
评价两组基线直肠活检标本可计算生物标志的重复性,有助于确定研究期间有统计学显著性的变化。除一个腺管亚腔隙(腔隙3)标志指数外(P=0.05),两组在增生动力学方面无差异。两组基线活检数值的变异系数,细胞角蛋白AEAE为12.4%,酸性粘蛋白为10%,形态学测量胞核总面积为10.8%。观察者内重复测定结果如下:AE1,r2=0.969;酸性粘蛋白,r2=0.945;胞核的形态学测量,r2=0.865;增生指数,r2=0.966。
, http://www.100md.com
基线时,两组所有增生参数均无明显差异。在6个月和12个月时,对照组与基线相比增生参数无变化,亦未见有何变化趋向。与此相反,实验组则发生显著改变。在6个月时,整个腺管增生细胞的数目减少。由于[3H]胸腺嘧啶脱氧核苷标记细胞(靠近腔面的腺管上部40% Phi h)减少,因此增生的腔隙亦较小,5腔隙的标记指数降低。在12个月时,实验组整个腺管的增生活性仍有减低(表3,图2),Phi h亦较对照组为小。在研究期间(基线至12个月),与对照组相比,实验组每个腺管中的标记细胞数以及整个腺管的标记指数均显著下降。





, http://www.100md.com
图2 补充牛奶对结直肠粘膜细胞增生的影响。各时间点资料均为mean(SE)。星号表示此时两组比较P<0.05。C为结肠腺管近腔面5间隙的标记指数。D为Phi h,结肠腺管近腔面上部40%中的增生细胞数
表3 上皮细胞增生指标* 变量
总LI,%
5.5(0.4)
7.1(0.7)
6.6(0.6)
6.0(0.3)
6.3(0.4)
, 百拇医药
5.1(0.2)
LI 4,%
4.0(0.6)
3.4(0.7)
3.5(0.9)
3.5(0.6)
3.6(0.8)
1.9(0.4)
LI 5,%
0.6(0.1)
1.0(0.4)
, http://www.100md.com
0.5(0.2)
0.8(0.2)
0.3(0.1)
0.2(0.1)
标记细胞,No
2.8(0.2)
3.6(0.3)
3.6(0.4)
2.9(0.1)
3.1(0.2)
2.6(0.2)
, 百拇医药
Phi h×10-1
1.6(0.2)
1.5(0.4)
1.2(0.2)
1.5(0.2)
1.2(0.2)
0.9(0.2)
* LI:标记指数;Phi h:腺管中增生细胞分布的测量。时间反应显著的为:总LI,1年时P<0.02;<25%,6个月时P<0.02;标记细胞,1年时P<0.01;Phi h,1年时P<0.01 与对照组比较P<0.05表4 奶钙治疗对结肠腺管中分化标记表达的影响 标记
与对照组比较P<0.05表4 奶钙治疗对结肠腺管中分化标记表达的影响 标记
, 百拇医药
对照组mean(SE)
治疗组mean(SE)
%
P值
细胞角蛋白AE1
基线
3.89(0.15)
4.39(0.16)
+12.9
0.02
6个月
4.36(0.14)
, http://www.100md.com
3.81(0.14)
-12.6
<0.05
12个月
3.97(0.16)
3.06(0.11)
-22.9
<0.05
酸性粘蛋白*
基线
10.25(0.5)
10.52(0.3)
, http://www.100md.com
+ 2.6
>0.10
6个月
9.78(0.6)
11.61(0.6)
+18.7
<0.05
12个月
7.23(0.4)
9.2 (0.4)
+27.2
<0.02
, 百拇医药
*为硫粘蛋白和涎酸粘蛋白的相对含量
实验组基线结直肠粘膜细胞角蛋白AE1表达略高于对照组(P=0.02);对照组始终无变化(表4)。实验组在6个月和12个月时AE1表达分别减少13%和23%(图3A)。实验组AE1表达的位置与正常结肠相同,亦位于结肠粘膜腔表面14,15。两组间组对时间(group vs time)差异显著(P<0.01)。
基线时,两组患者酸性粘蛋白的免疫反应性无显著差异。研究期间,对照组始终无明显变化。然而,实验组在6个月、12个月时酸性粘蛋白积分显著降低(表4,图3B)14,16。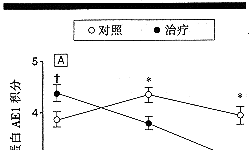


, http://www.100md.com
图3 补充牛奶对细胞角蛋白AE1和粘蛋白表达的影响。各时间点数据均为mean(SE)单位。星号表示此时两组P<0.05;剑号为Student t检验的基线水平
基线时,两组细胞核形态学测量无差异。在6个月时,与对照组比较,实验组胞核面积、最大直径和周径均显著下降,但是这种差异在12个月时未能维持(表5)。变化主要发生在直肠腺管底部处于增生周期的细胞。
实验组生物标志的显著改变并未因去除脂肪而减弱,提示食物消费变化对两组间的差异并无影响。
表5 胞核的形态测定结果* 变量
核面积,μm2
16.78(0.36)
, 百拇医药
17.99(0.59)
16.80(0.45)
17.45(0.38)
16.50(0.40)*
17.49(0.39)
最大直径,μm
7.70(0.10)
7.93(0.01)
7.77(0.11)
7.77(0.10)
7.52(0.13)*
, http://www.100md.com
7.97(0.12)
最小直径,μm
3.24(0.05)
3.36(0.08)
3.20(0.04)
3.34(0.04)
3.27(0.04)
3.24(0.04)
周径,μm
19.97(0.26)
20.71(0.31)
, http://www.100md.com
19.95(0.30)
20.29(0.26)
19.86(0.27)*
20.40(0.28)
*与对照组比较,P<0.05
结 论
饮食结构对结直肠癌的发生具有重要作用17。大量动物实验证实钙有保护结肠不致癌变的作用5。游离胆酸和脂肪酸可刺激细胞增生,激惹或损伤结肠上皮细胞。钙可与之结合形成不溶性复合物,从而减弱它们对结肠细胞增生与分化的干扰6,7。在体外,钙还能直接减弱结肠和其他细胞增生并诱导最终分化(terminal differentiation)2。食入的钙和维生素D主要来自奶和奶制品。研究显示脱脂奶粉中的钙可保护小鼠免发结肠癌18。
, http://www.100md.com
本文对照组食物摄入基本保持恒定,因此能量、蛋白质、脂肪、钙、磷酸盐、维生素D和其他微量营养素的摄入变化不大。实验组钙摄入平均增加872 mg,钙总摄入量达1 500 mg/d。在基线时,蛋白和脂肪的摄入两组近似。在6个月时,实验组蛋白质摄入因奶制品的增加而有适量增加。
研究显示,实验组在6个月和12个月时,细胞增生动力学呈持续的改变,其结果与腺瘤患者补钙的随机抽样研究类似5,19,20。然而,并非所有补钙研究均获如此恒定的结果5。奶制品还含有其他可减少动物肿瘤数目的成分,包括维生素D、丁酸盐21,22、鞘磷脂23、结合亚油酸24。奶制品还能降低粪水的细胞毒性25。补钙期间,粪二酰基甘油的浓度亦有降低26。艾姆斯试验27显示奶制品具有抗突变作用。
我们还检测了一系列可确定上皮细胞增生活力的生物标志以及某些与细胞分化、成熟相关的指标(例如:细胞角蛋白、酸性粘蛋白)。研究证实,外观正常的结肠上皮细胞,其增生活性与结肠癌的危险相关28,29。细胞角蛋白为上皮细胞的结构蛋白,在细胞分化、成熟和转化期间这种蛋白可发生相应的变化30-33。在正常结肠粘膜,细胞角蛋白AE1的表达局限于上皮表面和腺管上部,腺管下部细胞无此反应14,15。与此相反,家族性息肉病患者的扁平结肠粘膜以及结肠腺瘤和癌症患者,细胞角蛋白AE1反应性则扩展至整个腺管。本文患者基线时扁平结肠粘膜亦有很强的细胞角蛋白AE1反应性,可延及腺管底部,这也是患病粘膜的特征。然而,随着奶制食品的补充,细胞角蛋白AE1减少并局限于正常粘膜腺管的上部。
, 百拇医药
糖蛋白(例如粘蛋白)在维持细胞结构和功能方面具有重要作用。配糖体改变在结直肠癌发生早期即已出现34。发生结肠癌时,粘蛋白的表达失常35。在人和啮齿动物正常结肠粘膜远侧,硫粘蛋白是占优势的酸性粘蛋白,涎粘蛋白不能测及或水平很低14,16。与之相反,在腺瘤和腺癌上皮细胞,涎粘蛋白增加。因而在这些肿瘤,硫粘蛋白与涎粘蛋白的比例较正常偏低16。本文患者在给予奶制食品前,结肠粘膜涎粘蛋白水平异常升高。给予奶制食品后,涎粘蛋白水平降低,硫粘蛋白与涎粘蛋白比例升高恢复正常。
计算机辅助的细胞形态分析为定量分析细胞核形态特征提供了一种新的方法。与正常结肠上皮细胞比较,癌前上皮细胞和肿瘤组织胞核体积增大36-38。在我们的研究中,治疗6个月后胞核变小,但12个月时未见改变。本研究首次采用计算机辅助细胞形态分析对直肠活检标本胞核的组织形态改变进行评价。
我们对已知结肠癌危险较高患者的饮食习惯进行了研究。结果显示这些患者基线每日能量摄入水平很低,约7 140 kJ,其中27%的能量由脂肪提供,钙的摄入为655 mg/d,维生素D摄入为202 IU/d。这些指标不同于一般美国人,但与那些有保健意识的人群接近。
, 百拇医药
研究显示:结肠癌易感者饮食中增加低脂奶食品可减少结肠上皮细胞增生,使结肠粘膜中正常分化成熟的上皮细胞增加。饮食中最大的变化是钙的摄入,从600~700 mg/d增至1 500 mg/d。初步资料显示:补钙可减少腺瘤复发40。由于实验例数太少,实验时间过短,因此本试验不能对食疗能否改变结肠腺瘤的复发作出确切评价。本文资料不能证实饮食钙含量为有关生物标志发生变化的唯一原因。
国立卫生研究院共识会议建议,为了降低骨质疏松症的危险,65岁以上的成年人应每天摄入钙1 200~1 500 mg钙41。本文实验组(平均66~67岁)每天钙摄入量为1 500 mg,结果证实可减少结肠发生肿瘤的危险。因此我们认为:补钙不仅有益于骨质疏松的预防,而且也是一种预防结肠肿瘤的措施。
参考文献
1. Parker SL, TongT, Bolden 8, Wmgu PA. Cancer statistics. CA J Ciin. 1997f47:527.
, 百拇医药
2. Lipkin M, Newmark H, Kelloff G. Cairium,tamin D and Coio n Canser. Boca Raton, Fla: CRC Press inc) 1991.
3. Garland CF, Shekelle RB, Barrett-Comior E Criqui MH, RossofAH, Paul O. Dietary vitamin Daiid calauni and ofcolorectal cancer: a 19-year prospective study in men. bencet 1985i8424:307-309.
4. SlatteryM, SorensonA, FordM. Uietazycalcium intake as a mitigating factor in colon cancer. Am J 1988il28:504-514.
, 百拇医药
5. Lipkin M, Newniark H. Develc chemoprevention trials. J Natl Canser inst. 1995,87:1275-1277.
6. LapreJA, DeVries HT, Van derMeerR. Dietai calcium phospliate inhihite crtotokicity wa-ter. Am J Physwi. 1991261:G907G913.
7. Lapre JA, De Vries HT, Terniont DSML, et al,Mecliamsrn ofthe proteotive effect ofsupplementai dietary calciuni on cytolytic activity offecal water.Res. 1993,53:248-253.
8. WelbergJWM, KleibeulcerJH, Vazi der Meer R et al. Effeots ofotal calciuzn supplementation on in testinai bile acids and cytolytic activity offecal ter in patients with adenomatous polyl)s of the co-lon. Eur J Clin invest. 1993pe:63-68.
, 百拇医药
9. Pence BC, Buddingh F. Inhjbition ofdietary fat-promoted oolon ca.rcinogenesis in rats by supple-mental calcium orvitaniin Ds. Carrinsgenssis. 19te,9:187190.
10. Moi`son BC. The polyl)-cancer sequence in the large bowel. Proc R Soc Med 1974,67A51.
ll. Fleiss J. The Desig?z and Anaiysis ofCiinical New York, NY: John Wiley k Sons Inc, 1986:49-51.
12. Lipkin M, Newnlark H. Effeet ofadded dieti-calcinmoncolonicepithelial-cellpr sub-jects at high risk for familial colonic cancer. NEngi J Med. 1985)313:1381-1384. .
, 百拇医药
13. Richter F, Newniark HL, Richter A, et al. In-hibitionofWesterndiet-induced hyl)erproliferation azid hyperplasia in mouse colon by two sources of calcium. Carcinsgenssis. 1995,16:26852689.
14. YangK, Fan K, NewniarkH, etai. Cytokeratin lectin, aiid acidic mucin modulation in differentiat-ingcolonicepitheliaicellsofmiceait ern-style diets. Cancer Res. 1996i5(3:46444648.IS. Garin-Chesa P, Teting WJ, Melazned MR. Ex-pression of crtokeratins in noriziai and neoplastic colomc epithelial cells: implications for cellular dif ferentiation and carcinogenesis. Am JSurgpathol.1986,10:829-835.
, http://www.100md.com
16. Filipo MT, Bndoot BM. Abnormal 1)atterns of mucus secretion in apparently normai mucosa of largeintestinewtthcarcinoma Canser. 1974j34M-290.
17. WeisbargerJ, Horii C. The causes ofc HollebA, FinkD, MurphyG,eds.Ansan Soczety Textbook ofCiinseai Oncologu. Atlanta, Ga:American Cancer Society, 1991.
18. Pence BC, Dunn DM, Zhao C, et al. Protertive effects of caicium hom nonfat dried milk against colon carcinogenesis in rats. Nutr 199625:35-45.
, 百拇医药
19. Bostick RM, Fosdick L, WoodJR, et al. Calciiim norinalizes distribution of proliferating colls in cca lorectalmucosaofspoi`adicadenoma aran-domized double-blinded, placebrveontrolled clinical trial. J Natl Cancer inst. 1995,87:13071315.
20. Duris i, Hruby D, Pakarkova B, et al. Caicium chemoprevention in colorectal cancer. Hel,'ztogas-boenterotoW. 1996`f43:152-154.
21. Newniark H, Young C. Butyrate and phenylac-etate as differentiating agents: practicai problems and opportunities. JCill Bioc}iem. 1995,22:247-253.
, 百拇医药
22. D'Argenio G, Cosenza V, Delle Cave M, et al.Butyrate enemas in exporimental colitis and pro-tection aguinst large bowel cancer in a rat model.GastroenteroioW. 1996;ll0:17271734.
23. schmelz E, Dillehay D, Webb S, et al. Sphingo-myelin consumption suppresses aberrant colonic cryl)tfoci azid increases the prol)ortion ofadenomas versus adenocarcinomas in CFI mice treated with 1,2dimethylhydrazine: implications for dietar sphingolipidsandcoloncarcinogene CanserRes.1996i56:4936-4941.
, http://www.100md.com
24. LiewC, Schut HAf, Chin SF, ParizaMW, Dash-wooi] RH. Protectinn of coNuguted linoleic acid against 2-azninrv3-methylimidazo[4,5-fl quinoline- induce doolon car cinogenesisinthe F344rat:astudy ofinhibitory mecliamsms.30373043.
25. Govere WAP,TermontDSML, LapreJA, etal.Calcium in milk products precipitates intestinal fattyacidsandsecondarybileacidsand colonic cytotoxicity in humans. Res. 1996,56:3270-3275.
26. Holt PR, Moss SF, Wlielan R, et al. Fecal and rectalmucosaldiacyglycerolconcen
, http://www.100md.com
theliaiproliferativekinetics. CanserEpboioiBio-1996i5.`937-940.
27. Abdelali H, Cassand P, Soussotte V, et al. An-timutagenicity of components of dairy products.Mutat Res. 1995i331:133-141.Xi. Lipkin M. Biomakers ofincreased susceptibility to gastrointestinal cazicer: new application to stud-ies ofcancer prevention in humazi subjects. Res. 1988;48:235-245.
29. Lipkln M, Newniark H. Deve10 chemoprevention trials. J Natl Inst 1995,87:1275-1277.
, 百拇医药
30. Arends JW, Bosman FT, Hilgers J. Tissue an-tigens in Inye-bowel carcinoma. Bfocdem Biophgs Res Commun. 1985)7ed:1-19.
31. Sunwr, EichnerR, SchermerA, CooperD, Nel-son WG, Weiss RA. Classificatii possiblemechanismsofevohitionofma epi-thelial keratins:aunifyingmodel. In: LevineA,Topp G, Vande Woide G, Watson JD, eds. Celts:The Transfond Phenstgpe. Cold Spnzig Harbor,NY: Cold Spring Harbor Laboratory Press, 1984.
32. Cooper D, Schermer A, Sun mp. Classificatfon of human epithelial cells and their neoplasms us-ing monoclonal antibodies to keratins: strate applications azid liznitations. Lab invest. 1985i52:243256.
, 百拇医药
33. Mof1R,FrankeWW, SchillerDL,GeigerB, Kre-pler R. The catalogue of human cytokeratins: pat-teriis ofexpression in normal epithelial tuniors and cultured cells. Ceii. 1982f31:llAs.
34. sams JS, Lynch HT, Burt RW, Lanspa gy, Bo-lazid CR. Abnormalities of lectin histochemistry in farnilial polyposis coli azid hereditai7 nonpolypoais colorectal cancer. Cancer 1990,66:502-508.
35. Hanski C, Sheehan J, Kiehntopf M, Stolze B Stein H, Riecken EO. Incre sible sugar epitopes defined with monoclonal anti-body AM3 on colomc mucins is associated with ma-lignant transformation of colonic mui Res. 1991;51:53425347.
, 百拇医药
36. Verhest A, Kiss R, d'Olne D, et al. Charecten ization ofhumazi colorectalmuoosa, polyps, and can-cers by means of computerized morphonuclear im-age analysis. CaaseerlWe,65204T2054.
37. Ainbros RA, Pawel BR, Meshcheryakov i,Kotrosios J, Lanibet WC, Trost RC. Nucle
pbometryas aprognosticindicatorincolorectal cinoma dissected forcare. Anal Qi`ant Cgto Histol.1990,12:172-176.
38. MelingGI, Rognum TO, Clausen OPF, etal. As-sociation between DNA ploidy pattern and cellular atyl)iain oolorectal carcinonias: a new cfinical appli-cation ofDNA flow cytometric study. 1991 67:1642-1649.
, 百拇医药
39. VitaJ and Heaith Statistics of the Centere for Disease Control and Prevention/National Center for Health Statistics.National Health and Nutritioti Examination Suree)!I, Ph,z.se 1, 1988-91.Data. Atlanta, Ga: Centers for D Control and Prevention; 1994:255.
40. Baron JA, Beach M. A randon cinm supplementation to prevent colorectal adeno-mas [abstract]. Gastroenterotopp. 1998ill4:A563.
41. National institutes ofHealth. optimal calmum intake. In: NIH Co?i.sooi'.s Statement. Bethesda,Md: National institutes ofHealth,1994;12:l-31.
王宏宇 译 黄志强 校
JAMA 1998;280:1074~1079, 百拇医药
单位:
关键词:
美国医学会杂志中文版990306 Modulation of Abnormal Colonic Epithelial Cell
Proliferation and Differentiation by Low-Fat Dairy Foods
A Randomized Controlled Trial
Peter R. Holt, MD; Evren O. Atillasoy, MD; Jody Gilman, RD; Janet Guss, MS;
Steven F. Moss, MD; Harold Newmark, MS; Kunhua Fan, MD; Kan Yang, MD; Martin Lipkin, MD Janet Guss, MS;
, http://www.100md.com
Steven F. Moss, MD; Harold Newmark, MS; Kunhua Fan, MD; Kan Yang, MD; Martin Lipkin, MD
背景——人类结肠肿瘤发生前,结肠上皮细胞显示生长和分化的变异。这种具有癌变危险的变异被称为癌的中间生物标志(intermediate biomarkers of risk)。通过营养素或药物调节使粘膜恢复正常是化学预防结肠癌的手段之一。
目的——确定通过奶制品增加钙的摄入是否可使结肠生物标志正常化。
设计——随机、单盲、对照研究。
地点——门诊。
研究对象——70例因结肠腺瘤性息肉而有息肉切除病史的患者。
, 百拇医药 干预——钙含量为1 200 mg/d的低脂奶制品。根据饮食(对照组、高钙组)和年龄(<60岁、≥60岁)将患者随机分为4组。
主要观察指标——全结肠上皮细胞以及胸腺嘧啶脱氧核苷标记的上皮细胞数量和位置的变化;硫粘蛋白(主要由远侧结直肠上皮细胞分泌)与涎粘蛋白(sialomucins)比例以及细胞角蛋白(cytokeractin) AE1表达的变化。
结果——在6和12个月的治疗期间,结肠上皮细胞增生减弱(P<0.05),增生腔隙减小(P<0.05),酸性粘蛋白(P<0.02)、细胞角蛋白AE1的分布(P<0.05)以及细胞核大小(P<0.05)有恢复正常倾向。对照组在6个月和12个月时增生指标与基线无差异(P>0.05)。
结论——对于有结肠肿瘤危险的患者,通过低脂奶制品将钙摄入量增加至1 200 mg/d,可减弱结肠上皮细胞增生,使细胞分化标志恢复正常。
, 百拇医药
美国大约有134 000例结肠癌患者,每年因此死亡者约55 000例1。为此,寻找可能的化学预防营养疗法是肿瘤研究的重要目标之一。有关流行病学证据显示,饮食钙和维生素D水平与结肠癌的发生呈负相关关系2-4。加钙饮食可抑制啮齿动物和人6-8结肠上皮细胞增生降低粪水的细胞毒性5,抑制啮齿动物结肠肿瘤形成9。在人结肠癌预防研究中,通常用细胞增生与分化作为评价化学预防效果的生物标志5。
本文患者既往均有结肠腺瘤病史,与正常人群相比,属结肠肿瘤高危人群10。患者随机分为两组,实验组接受奶制品,对照组饮食照旧。随访观察1年,了解直肠乙状结肠粘膜上皮细胞的变化,描述细胞增生、分化、成熟状况。
方 法
患 者
, 百拇医药
本文患者年龄均大于18岁,均有结肠腺瘤性息肉病史。有下列情况者除外:结肠癌病史,阑尾切除术以外的肠道手术史,吸收障碍,炎性肠病,明显的内分泌或代谢疾病,乳糖不耐受症,总钙摄入量超过1 000 mg/d,补充钙超过400 mg/d或补充维生素D的摄入。用随机排列区组法将患者分组11。按性别和年龄(≥60,<60岁)将患者分为4组,产生一种独立的治疗分配方案。每个方案均有相同数量的患者在2、4或6区中被随机分至各治疗组。区组顺序在每个方案是随机的。采用SAS程序执行随机化排序。
从医院记录中共筛选出350例有近期腺瘤性息肉病史的患者。患者的保健医生允许我们与其中230例进行有关接触。这些可能的志愿者基本是健康的。实际接触180例,65例因饮食原因、补钙或乳糖酶缺乏症史而被排除;25例由于医疗原因不能参加试验;另外20例不愿参加试验。最后有70例进入本试验,对照组33例,实验组37例(图1)。对患者医院体检、4次营养面试、4次活检造成的不便和花费予以补偿。此研究为单盲的。受试者知道进行的是一种特殊饮食试验,然而他们不知道该饮食与所得资料关系的意义。样本大小估计以我们以往有关钙调节减低增生标志指数的研究为依据12。试验要求每组25~30例,以便检出试验组与对照组间的显著差异。维持I类误差在5%,检出显著差异的把握度为80%,采用双尾检验。本研究于1993年开始,于1995年6月完成。
, 百拇医药
营养的评估与监控
营养摄入水平由一位专门的营养学家采用24小时食物回忆和3天饮食记录(两次)进行评估。两次基线评估间隔1个月。以后按6个月的间隔进行。特别注意有关奶制食品资料的收集。食物回忆还按3个月的间隔进行,并对其变化进行研究。由于食物成分及其添加剂经常发生变化,故对食品的标签和品牌均做出相应要求。
实验组患者每日钙摄入总量增加至1 200 mg,维持恒定的脂肪、热卡和纤维摄入(建议每天减少糖45 g,蛋白质30 g,脂肪5 g)。我们为实验组提供了一种脱脂奶酪,同时要求增加其他低脂奶制品的摄入。不补钙对照组饮食如常,每3个月随访一次。3天饮食记录的多记录计算分析采用明尼苏达营养指标系统软件,版本2.7(Nutrition Coordinating Center, University of Minnesota, Minneapolis)。
直肠乙状结肠活检
, 百拇医药
直肠乙状结肠活检标本取自内镜检查表现正常的“扁平”粘膜。基线2次(间隔1个月),然后在6个月及12个月时各1次。自来水灌肠后于上午8~10点行纤维乙状结肠镜检,并于距肛缘10~15 cm处4个象限用Jumbo钳取6~8个活体标本。活检标本用0.185 MBq[3H]胸腺嘧啶脱氧核苷孵育后12用10%缓冲福尔马林液固定,以便进行[3H]胸腺嘧啶脱氧核苷掺入增生细胞的研究;或者用95%乙醇固定,以便观察细胞分化标志。
细胞增生与分化的研究
1.细胞增生:在15~25个完整的陷窝腺管(crypts),按以前的描述,对细胞增生进行了研究12。记录每个陷窝腺管上皮细胞的总数以及有胸腺嘧啶脱氧核苷标记的上皮细胞的数量和位置;用计算机系统进行自动处理13。
2.分化标志研究:在10~12个完整的陷窝腺管,用高铁二胺溶液对酸性粘蛋白进行染色14。硫粘蛋白主要由结直肠远侧上皮细胞分泌。根据硫粘蛋白与涎粘蛋白的比例可确定粘蛋白是否有异常14。
, 百拇医药
使用一种细胞角蛋白AE1单克隆抗体,用免疫组化法研究细胞角蛋白AE1的表达。在10~12个完整的腺管测定了上皮细胞内AE1的表达。在正常结直肠粘膜,细胞角蛋白AE1的表达局限于粘膜表面和腺管上部,因此细胞角蛋白AE1表达积分很少。当抗原向腺管下部扩增时,细胞角蛋白AE1的表达增加。
3.细胞核的形态测量:切片(3 μm)苏木素和伊红染色后用计算机辅助的细胞形态分析仪测定结直肠上皮细胞的大小,并在平均10个完整的腺管中,测定胞核的面积、周径和直径。
4.统计学分析:对两组患者各时间点(基线、6个月及12个月)24小时营养消耗进行了比较。将两个基线值的平均数作为每例患者的数值。两组各时间点结果的比较用Student t检验。此外,我们还对两组3个时间点不同营养、生物标志进行了方差分析,以便确定饮食改变或生物标志的时间效果。时间为重复量数(repeated measure),饮食或生物标志为组间因素。然后,对两组所有具显著作用的影响因素进行Post hoc Duncan multiple range检验,以便检出各时间点有关均值的差异(P<0.05)。以每日脂肪总摄入量作为协变量对生物标志进行协方差分析,结果显示生物标志的时间变化显著。对两组间最小校正均方值亦进行了比较。
, 百拇医药
结 果
总共对70例患者进行了观察,实验组37例,对照组33例,两组患者人口统计学及息肉切除史匹配(表1)。有11例患者退出研究(实验组7例,对照组4例),退出者或为个人原因或为医疗原因所致,但两组无差异(图1)。
表1 患者的特征 特征
对照组
实验组
例数
33
37
年龄,mean(SE),岁
66(2)
, http://www.100md.com
67(3)
≥65
19
25
<65
14
12
性别
男
22
22
女
11
15
, 百拇医药
种族
黑人
8
12
白人
19
21
拉丁美洲人
5
4
其他
1
0
体重,mean(SE),kg
, 百拇医药
76.5(2.7)
79.4(3.6)
腺瘤距最后一次息肉
切除术的时间,mean(SE),月
7.2(3)
8.6(2)
多发的息肉
切除术,%
14
16


, http://www.100md.com
图1 随机研究流程。对照组4例退出,因个人原因和医疗原因退出者各2例。实验组7例退出,其中2例为个人原因,1例为医疗原因,2例不服从试验,2例对牛奶增加不耐受
基线时对照组和实验组营养摄入近似(表2)。研究期间对照组维持基线营养摄入,包括钙的摄入。实验组每日钙摄入量从730 mg增至810 mg。基线食物钙分析显示,53%~60%的钙来自奶制品(35%来自奶,6%来自酸奶,16%来自奶酪)。实验组增加的食物钙83%来自奶制品(31%来自奶,11%来自酸奶和冰激淋,41%来自奶酪制品)。实验组能量摄入较对照组高1%~5%。
表2 每日营养物摄入计算*
对照组
乳类组
P值
, http://www.100md.com
能量,kJ
基线
6745(77)
7459(84)
>0.10
6个月
6686(74)
7001(78)
>0.10
12个月
7279(96)
7371(73)
, 百拇医药 >0.10
蛋白质,g
基线
70.2(4.3)
74.9(3.3)
>0.10
6个月
70.2(3.5)
82.1(3.5)
<0.02
12个月
74.7(4.7)
, 百拇医药 86.0(4.0)
0.07
脂肪,g
基线
49.9(3.1)
60.0(4.1)
0.06
6个月
49.5(3.5)
45.7(3.8)
>0.10
12个月
56.0(6.3)
, 百拇医药
45.2(3.2)
>0.10
钙,mg
基线
642(48)
608(29)
>0.10
6个月
725(60)
1421(76)
<0.001
12个月
685(31)
, 百拇医药
1538(103)
<0.001
磷酸盐,mg
基线
1082(59)
1073(47)
>0.10
6个月
1106(63)
1767(100)
<0.001
12个月
, 百拇医药
1192(104)
1915(131)
<0.001
维生素D,mg
基线
5.2(0.9)
4.4(0.5)
>0.10
6个月
4.9(0.6)
5.4(0.4)
>0.10
, 百拇医药
12个月
4.7(0.6)
5.8(0.6)
>0.10
纤维素,g
基线
16.8(1.7)
16.4(1.0)
>0.10
6个月
17.2(1.4)
16.0(1.2)
, 百拇医药
>0.10
12个月
20.5(2.4)
17.1(1.1)
>0.10
其他
基线
10.8(1.2)
10.3(0.7)
>0.10
6个月
11.0(1.0)
, http://www.100md.com 10.1(0.8)
>0.10
12个月
13.4(1.8)
10.9(0.8)
>0.10
* 两组总的平均每日营养摄入用3天食物日记计算,详见方法所述
 对照组:基线时33例;6个月时29例;12个月时29例
对照组:基线时33例;6个月时29例;12个月时29例 实验组:基线时37例;6个月时29例;12个月时30例
实验组:基线时37例;6个月时29例;12个月时30例评价两组基线直肠活检标本可计算生物标志的重复性,有助于确定研究期间有统计学显著性的变化。除一个腺管亚腔隙(腔隙3)标志指数外(P=0.05),两组在增生动力学方面无差异。两组基线活检数值的变异系数,细胞角蛋白AEAE为12.4%,酸性粘蛋白为10%,形态学测量胞核总面积为10.8%。观察者内重复测定结果如下:AE1,r2=0.969;酸性粘蛋白,r2=0.945;胞核的形态学测量,r2=0.865;增生指数,r2=0.966。
, http://www.100md.com
基线时,两组所有增生参数均无明显差异。在6个月和12个月时,对照组与基线相比增生参数无变化,亦未见有何变化趋向。与此相反,实验组则发生显著改变。在6个月时,整个腺管增生细胞的数目减少。由于[3H]胸腺嘧啶脱氧核苷标记细胞(靠近腔面的腺管上部40% Phi h)减少,因此增生的腔隙亦较小,5腔隙的标记指数降低。在12个月时,实验组整个腺管的增生活性仍有减低(表3,图2),Phi h亦较对照组为小。在研究期间(基线至12个月),与对照组相比,实验组每个腺管中的标记细胞数以及整个腺管的标记指数均显著下降。






, http://www.100md.com
图2 补充牛奶对结直肠粘膜细胞增生的影响。各时间点资料均为mean(SE)。星号表示此时两组比较P<0.05。C为结肠腺管近腔面5间隙的标记指数。D为Phi h,结肠腺管近腔面上部40%中的增生细胞数
表3 上皮细胞增生指标* 变量
总LI,%
5.5(0.4)
7.1(0.7)
6.6(0.6)
6.0(0.3)
6.3(0.4)
, 百拇医药
5.1(0.2)
LI 4,%
4.0(0.6)
3.4(0.7)
3.5(0.9)
3.5(0.6)
3.6(0.8)
1.9(0.4)
LI 5,%
0.6(0.1)
1.0(0.4)
, http://www.100md.com
0.5(0.2)
0.8(0.2)
0.3(0.1)
0.2(0.1)
标记细胞,No
2.8(0.2)
3.6(0.3)
3.6(0.4)
2.9(0.1)
3.1(0.2)
2.6(0.2)
, 百拇医药
Phi h×10-1
1.6(0.2)
1.5(0.4)
1.2(0.2)
1.5(0.2)
1.2(0.2)
0.9(0.2)
* LI:标记指数;Phi h:腺管中增生细胞分布的测量。时间反应显著的为:总LI,1年时P<0.02;<25%,6个月时P<0.02;标记细胞,1年时P<0.01;Phi h,1年时P<0.01
 与对照组比较P<0.05表4 奶钙治疗对结肠腺管中分化标记表达的影响 标记
与对照组比较P<0.05表4 奶钙治疗对结肠腺管中分化标记表达的影响 标记, 百拇医药
对照组mean(SE)
治疗组mean(SE)
%
P值
细胞角蛋白AE1
基线
3.89(0.15)
4.39(0.16)
+12.9
0.02
6个月
4.36(0.14)
, http://www.100md.com
3.81(0.14)
-12.6
<0.05
12个月
3.97(0.16)
3.06(0.11)
-22.9
<0.05
酸性粘蛋白*
基线
10.25(0.5)
10.52(0.3)
, http://www.100md.com
+ 2.6
>0.10
6个月
9.78(0.6)
11.61(0.6)
+18.7
<0.05
12个月
7.23(0.4)
9.2 (0.4)
+27.2
<0.02
, 百拇医药
*为硫粘蛋白和涎酸粘蛋白的相对含量
实验组基线结直肠粘膜细胞角蛋白AE1表达略高于对照组(P=0.02);对照组始终无变化(表4)。实验组在6个月和12个月时AE1表达分别减少13%和23%(图3A)。实验组AE1表达的位置与正常结肠相同,亦位于结肠粘膜腔表面14,15。两组间组对时间(group vs time)差异显著(P<0.01)。
基线时,两组患者酸性粘蛋白的免疫反应性无显著差异。研究期间,对照组始终无明显变化。然而,实验组在6个月、12个月时酸性粘蛋白积分显著降低(表4,图3B)14,16。



, http://www.100md.com
图3 补充牛奶对细胞角蛋白AE1和粘蛋白表达的影响。各时间点数据均为mean(SE)单位。星号表示此时两组P<0.05;剑号为Student t检验的基线水平
基线时,两组细胞核形态学测量无差异。在6个月时,与对照组比较,实验组胞核面积、最大直径和周径均显著下降,但是这种差异在12个月时未能维持(表5)。变化主要发生在直肠腺管底部处于增生周期的细胞。
实验组生物标志的显著改变并未因去除脂肪而减弱,提示食物消费变化对两组间的差异并无影响。
表5 胞核的形态测定结果* 变量

核面积,μm2
16.78(0.36)
, 百拇医药
17.99(0.59)
16.80(0.45)
17.45(0.38)
16.50(0.40)*
17.49(0.39)
最大直径,μm
7.70(0.10)
7.93(0.01)
7.77(0.11)
7.77(0.10)
7.52(0.13)*
, http://www.100md.com
7.97(0.12)
最小直径,μm
3.24(0.05)
3.36(0.08)
3.20(0.04)
3.34(0.04)
3.27(0.04)
3.24(0.04)
周径,μm
19.97(0.26)
20.71(0.31)
, http://www.100md.com
19.95(0.30)
20.29(0.26)
19.86(0.27)*
20.40(0.28)
*与对照组比较,P<0.05
结 论
饮食结构对结直肠癌的发生具有重要作用17。大量动物实验证实钙有保护结肠不致癌变的作用5。游离胆酸和脂肪酸可刺激细胞增生,激惹或损伤结肠上皮细胞。钙可与之结合形成不溶性复合物,从而减弱它们对结肠细胞增生与分化的干扰6,7。在体外,钙还能直接减弱结肠和其他细胞增生并诱导最终分化(terminal differentiation)2。食入的钙和维生素D主要来自奶和奶制品。研究显示脱脂奶粉中的钙可保护小鼠免发结肠癌18。
, http://www.100md.com
本文对照组食物摄入基本保持恒定,因此能量、蛋白质、脂肪、钙、磷酸盐、维生素D和其他微量营养素的摄入变化不大。实验组钙摄入平均增加872 mg,钙总摄入量达1 500 mg/d。在基线时,蛋白和脂肪的摄入两组近似。在6个月时,实验组蛋白质摄入因奶制品的增加而有适量增加。
研究显示,实验组在6个月和12个月时,细胞增生动力学呈持续的改变,其结果与腺瘤患者补钙的随机抽样研究类似5,19,20。然而,并非所有补钙研究均获如此恒定的结果5。奶制品还含有其他可减少动物肿瘤数目的成分,包括维生素D、丁酸盐21,22、鞘磷脂23、结合亚油酸24。奶制品还能降低粪水的细胞毒性25。补钙期间,粪二酰基甘油的浓度亦有降低26。艾姆斯试验27显示奶制品具有抗突变作用。
我们还检测了一系列可确定上皮细胞增生活力的生物标志以及某些与细胞分化、成熟相关的指标(例如:细胞角蛋白、酸性粘蛋白)。研究证实,外观正常的结肠上皮细胞,其增生活性与结肠癌的危险相关28,29。细胞角蛋白为上皮细胞的结构蛋白,在细胞分化、成熟和转化期间这种蛋白可发生相应的变化30-33。在正常结肠粘膜,细胞角蛋白AE1的表达局限于上皮表面和腺管上部,腺管下部细胞无此反应14,15。与此相反,家族性息肉病患者的扁平结肠粘膜以及结肠腺瘤和癌症患者,细胞角蛋白AE1反应性则扩展至整个腺管。本文患者基线时扁平结肠粘膜亦有很强的细胞角蛋白AE1反应性,可延及腺管底部,这也是患病粘膜的特征。然而,随着奶制食品的补充,细胞角蛋白AE1减少并局限于正常粘膜腺管的上部。
, 百拇医药
糖蛋白(例如粘蛋白)在维持细胞结构和功能方面具有重要作用。配糖体改变在结直肠癌发生早期即已出现34。发生结肠癌时,粘蛋白的表达失常35。在人和啮齿动物正常结肠粘膜远侧,硫粘蛋白是占优势的酸性粘蛋白,涎粘蛋白不能测及或水平很低14,16。与之相反,在腺瘤和腺癌上皮细胞,涎粘蛋白增加。因而在这些肿瘤,硫粘蛋白与涎粘蛋白的比例较正常偏低16。本文患者在给予奶制食品前,结肠粘膜涎粘蛋白水平异常升高。给予奶制食品后,涎粘蛋白水平降低,硫粘蛋白与涎粘蛋白比例升高恢复正常。
计算机辅助的细胞形态分析为定量分析细胞核形态特征提供了一种新的方法。与正常结肠上皮细胞比较,癌前上皮细胞和肿瘤组织胞核体积增大36-38。在我们的研究中,治疗6个月后胞核变小,但12个月时未见改变。本研究首次采用计算机辅助细胞形态分析对直肠活检标本胞核的组织形态改变进行评价。
我们对已知结肠癌危险较高患者的饮食习惯进行了研究。结果显示这些患者基线每日能量摄入水平很低,约7 140 kJ,其中27%的能量由脂肪提供,钙的摄入为655 mg/d,维生素D摄入为202 IU/d。这些指标不同于一般美国人,但与那些有保健意识的人群接近。
, 百拇医药
研究显示:结肠癌易感者饮食中增加低脂奶食品可减少结肠上皮细胞增生,使结肠粘膜中正常分化成熟的上皮细胞增加。饮食中最大的变化是钙的摄入,从600~700 mg/d增至1 500 mg/d。初步资料显示:补钙可减少腺瘤复发40。由于实验例数太少,实验时间过短,因此本试验不能对食疗能否改变结肠腺瘤的复发作出确切评价。本文资料不能证实饮食钙含量为有关生物标志发生变化的唯一原因。
国立卫生研究院共识会议建议,为了降低骨质疏松症的危险,65岁以上的成年人应每天摄入钙1 200~1 500 mg钙41。本文实验组(平均66~67岁)每天钙摄入量为1 500 mg,结果证实可减少结肠发生肿瘤的危险。因此我们认为:补钙不仅有益于骨质疏松的预防,而且也是一种预防结肠肿瘤的措施。
参考文献
1. Parker SL, TongT, Bolden 8, Wmgu PA. Cancer statistics. CA J Ciin. 1997f47:527.
, 百拇医药
2. Lipkin M, Newmark H, Kelloff G. Cairium,tamin D and Coio n Canser. Boca Raton, Fla: CRC Press inc) 1991.
3. Garland CF, Shekelle RB, Barrett-Comior E Criqui MH, RossofAH, Paul O. Dietary vitamin Daiid calauni and ofcolorectal cancer: a 19-year prospective study in men. bencet 1985i8424:307-309.
4. SlatteryM, SorensonA, FordM. Uietazycalcium intake as a mitigating factor in colon cancer. Am J 1988il28:504-514.
, 百拇医药
5. Lipkin M, Newniark H. Develc chemoprevention trials. J Natl Canser inst. 1995,87:1275-1277.
6. LapreJA, DeVries HT, Van derMeerR. Dietai calcium phospliate inhihite crtotokicity wa-ter. Am J Physwi. 1991261:G907G913.
7. Lapre JA, De Vries HT, Terniont DSML, et al,Mecliamsrn ofthe proteotive effect ofsupplementai dietary calciuni on cytolytic activity offecal water.Res. 1993,53:248-253.
8. WelbergJWM, KleibeulcerJH, Vazi der Meer R et al. Effeots ofotal calciuzn supplementation on in testinai bile acids and cytolytic activity offecal ter in patients with adenomatous polyl)s of the co-lon. Eur J Clin invest. 1993pe:63-68.
, 百拇医药
9. Pence BC, Buddingh F. Inhjbition ofdietary fat-promoted oolon ca.rcinogenesis in rats by supple-mental calcium orvitaniin Ds. Carrinsgenssis. 19te,9:187190.
10. Moi`son BC. The polyl)-cancer sequence in the large bowel. Proc R Soc Med 1974,67A51.
ll. Fleiss J. The Desig?z and Anaiysis ofCiinical New York, NY: John Wiley k Sons Inc, 1986:49-51.
12. Lipkin M, Newnlark H. Effeet ofadded dieti-calcinmoncolonicepithelial-cellpr sub-jects at high risk for familial colonic cancer. NEngi J Med. 1985)313:1381-1384. .
, 百拇医药
13. Richter F, Newniark HL, Richter A, et al. In-hibitionofWesterndiet-induced hyl)erproliferation azid hyperplasia in mouse colon by two sources of calcium. Carcinsgenssis. 1995,16:26852689.
14. YangK, Fan K, NewniarkH, etai. Cytokeratin lectin, aiid acidic mucin modulation in differentiat-ingcolonicepitheliaicellsofmiceait ern-style diets. Cancer Res. 1996i5(3:46444648.IS. Garin-Chesa P, Teting WJ, Melazned MR. Ex-pression of crtokeratins in noriziai and neoplastic colomc epithelial cells: implications for cellular dif ferentiation and carcinogenesis. Am JSurgpathol.1986,10:829-835.
, http://www.100md.com
16. Filipo MT, Bndoot BM. Abnormal 1)atterns of mucus secretion in apparently normai mucosa of largeintestinewtthcarcinoma Canser. 1974j34M-290.
17. WeisbargerJ, Horii C. The causes ofc HollebA, FinkD, MurphyG,eds.Ansan Soczety Textbook ofCiinseai Oncologu. Atlanta, Ga:American Cancer Society, 1991.
18. Pence BC, Dunn DM, Zhao C, et al. Protertive effects of caicium hom nonfat dried milk against colon carcinogenesis in rats. Nutr 199625:35-45.
, 百拇医药
19. Bostick RM, Fosdick L, WoodJR, et al. Calciiim norinalizes distribution of proliferating colls in cca lorectalmucosaofspoi`adicadenoma aran-domized double-blinded, placebrveontrolled clinical trial. J Natl Cancer inst. 1995,87:13071315.
20. Duris i, Hruby D, Pakarkova B, et al. Caicium chemoprevention in colorectal cancer. Hel,'ztogas-boenterotoW. 1996`f43:152-154.
21. Newniark H, Young C. Butyrate and phenylac-etate as differentiating agents: practicai problems and opportunities. JCill Bioc}iem. 1995,22:247-253.
, 百拇医药
22. D'Argenio G, Cosenza V, Delle Cave M, et al.Butyrate enemas in exporimental colitis and pro-tection aguinst large bowel cancer in a rat model.GastroenteroioW. 1996;ll0:17271734.
23. schmelz E, Dillehay D, Webb S, et al. Sphingo-myelin consumption suppresses aberrant colonic cryl)tfoci azid increases the prol)ortion ofadenomas versus adenocarcinomas in CFI mice treated with 1,2dimethylhydrazine: implications for dietar sphingolipidsandcoloncarcinogene CanserRes.1996i56:4936-4941.
, http://www.100md.com
24. LiewC, Schut HAf, Chin SF, ParizaMW, Dash-wooi] RH. Protectinn of coNuguted linoleic acid against 2-azninrv3-methylimidazo[4,5-fl quinoline- induce doolon car cinogenesisinthe F344rat:astudy ofinhibitory mecliamsms.30373043.
25. Govere WAP,TermontDSML, LapreJA, etal.Calcium in milk products precipitates intestinal fattyacidsandsecondarybileacidsand colonic cytotoxicity in humans. Res. 1996,56:3270-3275.
26. Holt PR, Moss SF, Wlielan R, et al. Fecal and rectalmucosaldiacyglycerolconcen
, http://www.100md.com
theliaiproliferativekinetics. CanserEpboioiBio-1996i5.`937-940.
27. Abdelali H, Cassand P, Soussotte V, et al. An-timutagenicity of components of dairy products.Mutat Res. 1995i331:133-141.Xi. Lipkin M. Biomakers ofincreased susceptibility to gastrointestinal cazicer: new application to stud-ies ofcancer prevention in humazi subjects. Res. 1988;48:235-245.
29. Lipkln M, Newniark H. Deve10 chemoprevention trials. J Natl Inst 1995,87:1275-1277.
, 百拇医药
30. Arends JW, Bosman FT, Hilgers J. Tissue an-tigens in Inye-bowel carcinoma. Bfocdem Biophgs Res Commun. 1985)7ed:1-19.
31. Sunwr, EichnerR, SchermerA, CooperD, Nel-son WG, Weiss RA. Classificatii possiblemechanismsofevohitionofma epi-thelial keratins:aunifyingmodel. In: LevineA,Topp G, Vande Woide G, Watson JD, eds. Celts:The Transfond Phenstgpe. Cold Spnzig Harbor,NY: Cold Spring Harbor Laboratory Press, 1984.
32. Cooper D, Schermer A, Sun mp. Classificatfon of human epithelial cells and their neoplasms us-ing monoclonal antibodies to keratins: strate applications azid liznitations. Lab invest. 1985i52:243256.
, 百拇医药
33. Mof1R,FrankeWW, SchillerDL,GeigerB, Kre-pler R. The catalogue of human cytokeratins: pat-teriis ofexpression in normal epithelial tuniors and cultured cells. Ceii. 1982f31:llAs.
34. sams JS, Lynch HT, Burt RW, Lanspa gy, Bo-lazid CR. Abnormalities of lectin histochemistry in farnilial polyposis coli azid hereditai7 nonpolypoais colorectal cancer. Cancer 1990,66:502-508.
35. Hanski C, Sheehan J, Kiehntopf M, Stolze B Stein H, Riecken EO. Incre sible sugar epitopes defined with monoclonal anti-body AM3 on colomc mucins is associated with ma-lignant transformation of colonic mui Res. 1991;51:53425347.
, 百拇医药
36. Verhest A, Kiss R, d'Olne D, et al. Charecten ization ofhumazi colorectalmuoosa, polyps, and can-cers by means of computerized morphonuclear im-age analysis. CaaseerlWe,65204T2054.
37. Ainbros RA, Pawel BR, Meshcheryakov i,Kotrosios J, Lanibet WC, Trost RC. Nucle
pbometryas aprognosticindicatorincolorectal cinoma dissected forcare. Anal Qi`ant Cgto Histol.1990,12:172-176.
38. MelingGI, Rognum TO, Clausen OPF, etal. As-sociation between DNA ploidy pattern and cellular atyl)iain oolorectal carcinonias: a new cfinical appli-cation ofDNA flow cytometric study. 1991 67:1642-1649.
, 百拇医药
39. VitaJ and Heaith Statistics of the Centere for Disease Control and Prevention/National Center for Health Statistics.National Health and Nutritioti Examination Suree)!I, Ph,z.se 1, 1988-91.Data. Atlanta, Ga: Centers for D Control and Prevention; 1994:255.
40. Baron JA, Beach M. A randon cinm supplementation to prevent colorectal adeno-mas [abstract]. Gastroenterotopp. 1998ill4:A563.
41. National institutes ofHealth. optimal calmum intake. In: NIH Co?i.sooi'.s Statement. Bethesda,Md: National institutes ofHealth,1994;12:l-31.
王宏宇 译 黄志强 校
JAMA 1998;280:1074~1079, 百拇医药