卵巢癌药物敏感基因治疗实验研究——(Ⅰ)体外实验
作者:徐丛剑 张惜阴 许秀兰 金志军 丰有吉 姚 明 顾 峻 曹斌融 顾健人
单位:徐丛剑 张惜阴 丰有吉 曹斌融(上海医科大学妇产科医院(上海 200011);许秀兰 姚 明 顾 峻 顾健人(上海市肿瘤研究所);金志军(第二军医大学长征医院妇产科)
关键词:卵巢肿瘤;细胞,培养的;基因治疗;逆转录病毒载体;单纯疱疹病毒;胸腺嘧啶核苷激酶基因;羟甲基无环鸟苷
肿瘤990321 为探索Ⅰ型单纯疱疹病毒胸腺嘧啶核苷激酶基因/羟甲基无环鸟苷(HSV1-tk/GCV)药物敏感基因治疗系统应用于卵巢癌,本文进行了一系列实验研究,这里先介绍体外实验结果。
材料与方法
1.卵巢上皮癌细胞系AO来自中国科学院上海细胞库;病毒生产细胞(VPC)由上海市肿瘤研究所癌基因及相关基因国家重点实验室顾健人院士提供,包括:(1)VPC/x:可产生不含目的基因的逆转录病毒(RV);(2)VPC/HSV1-tkc:可产生带有HVS1-tkc的RV颗粒(HSV1-tkc系由HSV1中国株扩增而获得的HSV1-tk基因)。两种RV中均带有新霉素抗性(NeoR)基因。
, 百拇医药
2.以RV介导的方法向AO细胞内导入HSV1-tkc,以400 μg/ml G418(Sigma)筛选阳性克隆,并以PCR、Southern blot、Northern blot及羟甲基无环鸟苷(GCV)克隆杀伤试验鉴定基因转导,并证实AO细胞内HSV1-tkc为阴性。所用扩增引物为上游:5’AACTGGCGTGAAACTCCCGCACC3’,下游:5’GAGGTATTGTCTCCTTCCGAGTT3’;HSV1-tkc探针为HSV1-tkc完整cDNA,全长1.25 kb,由pSKtkc重组质粒DNA经EcoRⅠ和XholⅠ酶切获得;GCV由Roch Syntex公司惠赠。
3.测定GCV、ACV(无环鸟苷)杀伤AO/HSV1-tkc细胞的半数抑制浓度IC50,并以光镜及电镜观察细胞形态及集落形成;以FACS检测细胞周期及DNA倍体分析;以PI(碘化丙锭)染色观察细胞核形态变化。
, http://www.100md.com
4.以含RV的细胞培养液重复感染卵巢癌细胞2~8次,分别计数克隆或给予GCV,观察重复感染是否能提高RV的感染效率。并以HSV1-tkc+的卵巢癌细胞及VPC与HSV1-tkc-的卵巢癌细胞AO混合培养,并对分离培养及混合培养的细胞分别给予GCV(10μg/ml),观察“旁观者”效应及重复感染对系统作用的影响。
结 果
1.基因转导及阳性克隆筛选、鉴定 VPC/HSV1-tkc培养液对AO细胞的感染滴度为9.3×105集落形成单位(cfu)/ml。感染复数(MOI)为4.6。
PCR产物凝胶电泳结果显示,AO及AO/x基因组DNA的HSV1-tkc扩增均呈阴性,而AO/HSV1-tkc,VPC/HSV1-tkc组DNA及pSKtkc DNA均显示长度约1.25 kb的阳性条带,且此条带Southern 杂交也呈阳性。而上述HSV1-tkc扩增呈阳性的细胞,所提取的mRNA作Northern杂交,其结果也呈阳性。
, http://www.100md.com
GCV杀伤AO/HSV1-tkc克隆 1号孔细胞于G-418筛选18天后全部死亡;2,3号孔阳性克隆数分别为46个和52个;2号孔在以后的培养中克隆发生融合,细胞呈复层生长;3号孔在加用GCV后第5天仅剩2个克隆尚有细胞存活,其中一个于第8天死亡脱落,另一个克隆则于第15天细胞全部死亡。
2.GCV、ACV对AO系列细胞的体外生长抑制作用 GCV,ACV对各细胞的半数抑制浓度IC50值见表1。
表1 GCV、ACV对AO系列细胞的生长抑制作用(IC50,μg)
AO
AO/x
AO/HSV1-tkc
, http://www.100md.com
GCV
1.585
1.431
0.010
ACV
58.43
54.72
3.09
电镜下,未经GCV作用的AO/HSV1-tkc细胞与AO细胞形态相似,而经GCV作用后AO/HSV1-tkc细胞则有明显改变,其中,贴壁的细胞核内均一淡染,也可见核仁固缩之细胞,胞浆变化不明显;而已悬浮的细胞核呈棉絮状,胞浆内细胞器明显肿胀。多数细胞核膜及细胞膜尚完整。少数细胞核膜及细胞膜消失,未找到明确的凋亡小体。
, http://www.100md.com
DNA荧光染色 在GCV作用下,AO/HSV1-tkc细胞有部分呈凋亡形态表现,在GCV 1 μg/ml组中占6.2%,GCV 10 μg/ml组中占11.3 %;而在对照组中仅占1.8%(分别计数1000个细胞)。A0峰细胞比例分析: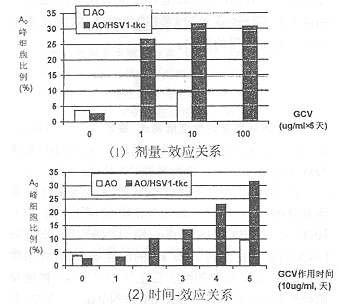
图1 A0峰细胞比例分析
图1显示各组细胞中A0峰细胞比例,可见GCV杀伤AO/HSV1-tkc细胞存在明确的剂量依赖性和时间依赖性。
细胞周期分析 结果显示,GCV作用后各期细胞比例均有明显改变;尤以10 μg/ml GCV作用3~4天最为显著,S期细胞占90%以上,G1期和G2+M期细胞比例则明显降低,但第5天S期细胞比例有所下降,代之以G2+M期细胞比例则明显升高;而在100 μg/ml GCV作用5天后,G2+M期细胞比例仍维持低水平,未经GCV作用的AO/HSV1-tkc细胞的周期分布每日无明显变化。
, http://www.100md.com
3.HSV1-tk/GCV基因治疗系统对卵巢癌细胞的体外作用 旁观者效应观察 结果显示,当AO/HSV1-tkc细胞在AO+AO/HSV1-tkc细胞群体中所占比例在70%以下时,旁观者效应不明显,当其比例达80%时,GCV对该细胞群体的生长抑制率可达95.2%;当其比例为90%时,在加用GCV后,该细胞群体几乎不形成集落(3个孔中仅见1个克隆)。
重复感染试验 随着感染次数的增多,AO细胞对GCV的敏感性有所增加,G418筛选所获得的阳性克隆数也逐渐增多(见表2)。
表2 重复感染后G418筛选阳性克隆数及GCV对细胞的生长抑制率 感染次数
1
2
4
, 百拇医药
6
8
G418筛选阳性克隆数(x±s)
48±7
93±12
145±12
185±9
226±28
GCV对细胞的生长抑制率(%)
5.8
8.3
14.3
, 百拇医药 23.1
33.9
混合培养试验:与VPC/HSV1-tkc细胞混合培养后,AO细胞对GCV的敏感性见图2,可见随着与之混合培养的VPC/HSV1-tkc细胞比例的增高,AO细胞对GCV的敏感性也逐渐增高,当VPC/HSV1-tkc细胞与AO细胞之比为8:2时,GCV对AO细胞的生长抑制率可达96.6%。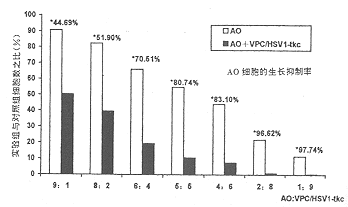
图2 GCV对与VPC/HSV1-tkc细胞混育后的AO细胞的生长抑制率
讨 论
1.关于药物敏感基因治疗 药物敏感基因治疗(又称自杀基因治疗)作为一种最有希望的肿瘤基因治疗策略已引起广泛关注[1]。其主要治疗原理为:应用逆转录病毒介导等方法将单纯疱疹病毒胸腺嘧啶核苷激酶基因(HSV1-tk)导入肿瘤细胞,使其表达HSV1特有的胸腺嘧啶核苷激酶(HSV1-TK),然后再给予HSV1-TK的底物羟甲基无环鸟苷(GCV)进行治疗。GCV磷酸化产物具有高度细胞毒性,可阻断肿瘤细胞的DNA合成,从而导致肿瘤细胞死亡,并对其周围的肿瘤细胞具有“旁观者效应”、达到治疗肿瘤的目的。这一治疗策略更适用于治疗象卵巢癌这样相对较为隔离(主要存在于腹腔内)的肿瘤。
, 百拇医药
2.GCV、ACV对AO/HSV1-tkc的生长抑制效应
资料表明[2],GCV对HSV1-tk阳性的鼠成纤维细胞生长的半数抑制浓度(IC50)比HSV1-tk阴性者低120余倍,而ACV对二者的IC50仅相差约20倍。哺乳动物细胞的tk存在与否对IC50无明显影响。这点正是设计HSV1-tk/GCV基因治疗系统的基础与前提。本文的实验结果与此相似,且显微镜下跟踪观察也提示在10μg/ml以上的GCV作用下,HSV1-tk阳性的AO细胞所形成的集落较小或不形成集落,进一步证实了GCV对HSV1-tkc+的卵巢癌细胞有强力的杀伤和/或抑制生长效应,其作用明显优于ACV。从而为将HSV1-tk/GCV系统应用于卵巢癌提供了理论基础。
, 百拇医药
肿瘤组织病理学检查进一步提示,虽然GCV未能在治疗期内将AO/HSV1-tk细胞完全消灭,但其残留细胞形态上已发生明显变化,大部分细胞处于变性、裂解状态。
3.GCV抑制AO/HSV1-tkc生长的机理
早在1977年,Elion等[3]报告ACV可抑制HSV1复制,并提示其作用过程需要HSV1-tk酶的参与。其后,多位学者证实,ACV可抑制转导有HSV1-tk的细胞生长,其作用机制为HSV1-tk可将ACV磷酸化为毒性产物,终止DNA合成,从而导致细胞死亡。
本研究结果表明,AO/HSV1-tkc细胞在GCV作用下,S期细胞比例明显升高,且呈一定的剂量依赖性。在药物作用时间上,经用药后3~4天S期细胞比例最高,达90%以上,第5天有所回降。
, 百拇医药
另外,体外实验研究中G2+M期细胞比例的变化也较为明显,总的说来,在GCV作用下,AO/HSV1-tkc细胞中的G2+M期细胞比例维持在一个较低的水平,但是在10 μg/ml GCV作用第5天,G2+M期细胞比例呈现明显“反跳”,达25.0%。当GCV浓度为100 μg/ml时无此“反跳”现象,但S期细胞比例又较低剂量组高。作者认为有以下几种可能的解释:
(1)GCV在HSV1-tk酶的催化下磷酸化为毒性产物,终止了正处于S期的细胞的DNA合成,从而使细胞阻滞于S期,造成S期细胞大量堆积;
(2)部分细胞未能导入HSV1-tk而仅导入了neo基因,因而仍呈G418抗性;或是在GCV作用的压力下,部分细胞可能丢失HSV1-tk或关闭其表达,或通过其它机制对GCV产生耐药性,这样当大量的表达HSV1-tk的细胞被杀伤后,通过某种途径刺激这部分细胞大量增殖,进入S期,并占主导地位,从而导致S期细胞比例增加。
, 百拇医药
(3)某些细胞尽管在S期受到损伤,但通过某种机制能够加以“修复”,从而在中量(10 μg/ml)GCV作用的后期(第5天)跨越S期,进入G2、M期。但在大剂量(100 μg/ml)GCV作用时则无法修复,因而G2+M期比例仍较低。
上述三种情况是否能确立,尚有待于进一步研究,但S期细胞比例增加这一现象本身就可能提示正负两方面的效应:其一,GCV停药后可能会出现肿瘤加速生长的反跳现象。既往文献就曾报道[4],以HSV1-tk/GCV系统治疗实验性大鼠脑胶质瘤后,近期效果非常显著,肿瘤体积缩小28倍,大鼠生存时间延长4倍,但远期有复发。这一现象支持本文的推断;其二,残存肿瘤可能对S期特异的化疗药物更为敏感,提示联合应用HSV1-tk/GCV系统和常规化疗可能有协同效应。Kim等人[5]曾报道,ACV可以选择性地提高HSV1-tk+的神经胶质瘤细胞的放射敏感性。这对于本文的这一推断可能是一个佐证。
, http://www.100md.com
此外,有学者报道,GCV可诱导携有HSV1-tk的细胞发生凋亡(Apoptosis)[6]。本实验中以PI作DNA荧光染色,显示经10 μg/ml GCV作用后部分细胞呈现凋亡细胞的形态表现,即核呈颗粒状裂解,FACS检测也提示GCV作用后A0峰细胞(有人认为即为凋亡细胞)比例明显升高,且呈一定的剂量依赖性与时间依赖性;
4.关于旁观者效应
前文所示,GCV可以高效杀伤携有HSV1-tk的细胞,或抑制其生长,而在体内体外实验中,人们还发现GCV不仅可以诱使携有HSV1-tk的细胞本身死亡(即“自杀),还可影响邻近的HSV1-tk-细胞,产生杀伤效果,此即所谓“旁观者效应”(Bystander Effect),而且,这种经GCV作用的HSV1-tk+细胞仍能发挥对周围细胞的杀伤作用。Freeman等据此提出,将卵巢癌细胞自病人体内取出后,体外转导HSV1-tk,并以致死剂量的放射线照射,将其作为肿瘤疫苗回植入病人体内,再给予GCV治疗。这一方案已获得NIH的批准[7]。
, http://www.100md.com
至于这种“旁观者效应”的机理,目前说法不一,主要包括:(1)细胞之间通过间隙连接(gap junction)或桥粒传送有毒物质的颗粒而产生邻近杀伤;(2)“旁观”细胞主动摄取凋亡碎片,而碎片中含有磷酸化的GCV,从而致使“旁观”细胞死亡;(3)已发生自杀的细胞及其碎片引发机体免疫反应,由于“旁观”肿瘤细胞与其有较一致的抗原性,从而被免疫效应细胞杀伤、清除;(4)肿瘤血管内皮细胞转导了HSV1-tk,并被GCV杀伤,导致肿瘤缺血,细胞死亡。有学者提出,这种“旁观”细胞的死亡方式为凋亡,bcl-2基因表达可抑制凋亡的发生。
本文在体外实验中证实HSV1-tkc/GCV系统对卵巢癌AO细胞确有一定的“旁观者效应”,这也说明免疫及/或血管机制至少不是“旁观者效应”的唯一途径。但本研究中这种效应不如国外报道的体内实验中明显,则可能是由于缺乏免疫及/或血管机制的作用,也可能是由于接种细胞密度较低,细胞不能密切接触所致。
, http://www.100md.com 5.关于重复RV感染
由于GCV对携有HSV1-tk的卵巢癌细胞有较强的杀伤作用或明显的抑制生长的作用,因此转基因效率的提高已成为制约基因治疗应用效果的关键问题。逆转录病毒转染肿瘤的效率除受许多因素影响,如温度、感染液中逆转录病毒浓度及载体本身的构建和VPC生长状态等,此外,还受到感染时进入分裂期的细胞数量的制约。卵巢癌与其它肿瘤一样,每个细胞的细胞周期处于无序的非同步状态,这样一次性感染只能是少数细胞获得基因转导。在本实验中也观察到随着感染次数的增多,所获得的转染阳性克隆数明显提高,转染后肿瘤细胞对GCV的敏感性也有所提高,提示重复逆转录病毒感染可能是提高基因转导效率的有效途径之一。与降温、浓缩及离心等目前国外常用的方法相比,重复感染可以应用于体内感染试验,因此具有一定的优越性。当然,从本实验中也可看出,即使重复感染8次,其感染率仍然很低。与临床应用的要求还相距甚远。
6.关于VPC/HSV1-tkc细胞与AO细胞的混合培养
, 百拇医药
动物实验证实,将VPC注射到脑胶质瘤部位,使其在生长期间不断释放新生的RV颗粒,从而产生对肿瘤细胞的连续的重复感染,从而提高了对肿瘤的治疗作有。这一方面目前已进入Ⅲ期临床试验[8]。由于“旁观者效应”并非细胞特异性的表现。它在不同细胞系之间也有作用,因此在这一方法的总体效应中也不能除外“旁观者效应”的作用。本文实验中证实,这一方法对卵巢癌细胞同样有效。
总之,HSV1-tk/GCV基因治疗系统在体外对卵巢癌细胞具有高效的杀伤作用。但其应用方法尚需进一步研究。
第一作者简介 徐丛剑,男,博士,主治医师。
参 考 文 献
1 Stone R.Molecular surgery for brain tumors.Science,1992,256:1513
, 百拇医药
2 Oliver S,Bubley G,Crumpacker C.Inhibition of HSV1-transformed murine cells by nucleoside analogs,2'-NDG and 2'-nor-cGMP:Mechanisms of inhibition and reversal by exogenous nucleosides.Virology,1985,145:84
3 Elion GB,Furman PA,Fyfe JA,et al.Selectivity of action of an antiheptic agent,9-(2-hydroxyethoxymethyl)guanine.Proc Natl Acad Sci USA,1977,74:5716
4 Maron A,Gustin T,Le Roux A,et al.Gene therapy of rat C6 glioma using adenovirus-mediated transfer of the herpes simplex virus thymidine kinase gene:long-term follow-up by magnetic resonance imaging.Gene-Ther,1996,3(4):315
, 百拇医药
5 Kim JH,Kim SH,Kolozsvary A,et al.Selective enhancement of radiation response of herpes simplex virus thymidine kinase transduced 9L gliosarcoma cells in vitro and in vivo by antiviral agents.Int J Radiat Oncol Biol Phys,1995,33(4):861
6 Freeman SM,Abboud CN,Whartenby KA,et al.The “bystander effect”:Tumor regression when a fraction of the tumor mass is genetically modified.Cancer Res,1993,53:5274
7 Freeman SM,McCune C,Angel C,et al.Treatment of ovarian cancer using HSV1-tk gene modified vaccine-regulatory issues.Hum Gene Ther,1992,3:342
8 Wivel N.Sandoz plans first large phase Ⅲ gene therapy trial.Biotechnology News,1996,16(12):1
(收稿:1998-11-12 修回:1999-03-24), http://www.100md.com
单位:徐丛剑 张惜阴 丰有吉 曹斌融(上海医科大学妇产科医院(上海 200011);许秀兰 姚 明 顾 峻 顾健人(上海市肿瘤研究所);金志军(第二军医大学长征医院妇产科)
关键词:卵巢肿瘤;细胞,培养的;基因治疗;逆转录病毒载体;单纯疱疹病毒;胸腺嘧啶核苷激酶基因;羟甲基无环鸟苷
肿瘤990321 为探索Ⅰ型单纯疱疹病毒胸腺嘧啶核苷激酶基因/羟甲基无环鸟苷(HSV1-tk/GCV)药物敏感基因治疗系统应用于卵巢癌,本文进行了一系列实验研究,这里先介绍体外实验结果。
材料与方法
1.卵巢上皮癌细胞系AO来自中国科学院上海细胞库;病毒生产细胞(VPC)由上海市肿瘤研究所癌基因及相关基因国家重点实验室顾健人院士提供,包括:(1)VPC/x:可产生不含目的基因的逆转录病毒(RV);(2)VPC/HSV1-tkc:可产生带有HVS1-tkc的RV颗粒(HSV1-tkc系由HSV1中国株扩增而获得的HSV1-tk基因)。两种RV中均带有新霉素抗性(NeoR)基因。
, 百拇医药
2.以RV介导的方法向AO细胞内导入HSV1-tkc,以400 μg/ml G418(Sigma)筛选阳性克隆,并以PCR、Southern blot、Northern blot及羟甲基无环鸟苷(GCV)克隆杀伤试验鉴定基因转导,并证实AO细胞内HSV1-tkc为阴性。所用扩增引物为上游:5’AACTGGCGTGAAACTCCCGCACC3’,下游:5’GAGGTATTGTCTCCTTCCGAGTT3’;HSV1-tkc探针为HSV1-tkc完整cDNA,全长1.25 kb,由pSKtkc重组质粒DNA经EcoRⅠ和XholⅠ酶切获得;GCV由Roch Syntex公司惠赠。
3.测定GCV、ACV(无环鸟苷)杀伤AO/HSV1-tkc细胞的半数抑制浓度IC50,并以光镜及电镜观察细胞形态及集落形成;以FACS检测细胞周期及DNA倍体分析;以PI(碘化丙锭)染色观察细胞核形态变化。
, http://www.100md.com
4.以含RV的细胞培养液重复感染卵巢癌细胞2~8次,分别计数克隆或给予GCV,观察重复感染是否能提高RV的感染效率。并以HSV1-tkc+的卵巢癌细胞及VPC与HSV1-tkc-的卵巢癌细胞AO混合培养,并对分离培养及混合培养的细胞分别给予GCV(10μg/ml),观察“旁观者”效应及重复感染对系统作用的影响。
结 果
1.基因转导及阳性克隆筛选、鉴定 VPC/HSV1-tkc培养液对AO细胞的感染滴度为9.3×105集落形成单位(cfu)/ml。感染复数(MOI)为4.6。
PCR产物凝胶电泳结果显示,AO及AO/x基因组DNA的HSV1-tkc扩增均呈阴性,而AO/HSV1-tkc,VPC/HSV1-tkc组DNA及pSKtkc DNA均显示长度约1.25 kb的阳性条带,且此条带Southern 杂交也呈阳性。而上述HSV1-tkc扩增呈阳性的细胞,所提取的mRNA作Northern杂交,其结果也呈阳性。
, http://www.100md.com
GCV杀伤AO/HSV1-tkc克隆 1号孔细胞于G-418筛选18天后全部死亡;2,3号孔阳性克隆数分别为46个和52个;2号孔在以后的培养中克隆发生融合,细胞呈复层生长;3号孔在加用GCV后第5天仅剩2个克隆尚有细胞存活,其中一个于第8天死亡脱落,另一个克隆则于第15天细胞全部死亡。
2.GCV、ACV对AO系列细胞的体外生长抑制作用 GCV,ACV对各细胞的半数抑制浓度IC50值见表1。
表1 GCV、ACV对AO系列细胞的生长抑制作用(IC50,μg)
AO
AO/x
AO/HSV1-tkc
, http://www.100md.com
GCV
1.585
1.431
0.010
ACV
58.43
54.72
3.09
电镜下,未经GCV作用的AO/HSV1-tkc细胞与AO细胞形态相似,而经GCV作用后AO/HSV1-tkc细胞则有明显改变,其中,贴壁的细胞核内均一淡染,也可见核仁固缩之细胞,胞浆变化不明显;而已悬浮的细胞核呈棉絮状,胞浆内细胞器明显肿胀。多数细胞核膜及细胞膜尚完整。少数细胞核膜及细胞膜消失,未找到明确的凋亡小体。
, http://www.100md.com
DNA荧光染色 在GCV作用下,AO/HSV1-tkc细胞有部分呈凋亡形态表现,在GCV 1 μg/ml组中占6.2%,GCV 10 μg/ml组中占11.3 %;而在对照组中仅占1.8%(分别计数1000个细胞)。A0峰细胞比例分析:

图1 A0峰细胞比例分析
图1显示各组细胞中A0峰细胞比例,可见GCV杀伤AO/HSV1-tkc细胞存在明确的剂量依赖性和时间依赖性。
细胞周期分析 结果显示,GCV作用后各期细胞比例均有明显改变;尤以10 μg/ml GCV作用3~4天最为显著,S期细胞占90%以上,G1期和G2+M期细胞比例则明显降低,但第5天S期细胞比例有所下降,代之以G2+M期细胞比例则明显升高;而在100 μg/ml GCV作用5天后,G2+M期细胞比例仍维持低水平,未经GCV作用的AO/HSV1-tkc细胞的周期分布每日无明显变化。
, http://www.100md.com
3.HSV1-tk/GCV基因治疗系统对卵巢癌细胞的体外作用 旁观者效应观察 结果显示,当AO/HSV1-tkc细胞在AO+AO/HSV1-tkc细胞群体中所占比例在70%以下时,旁观者效应不明显,当其比例达80%时,GCV对该细胞群体的生长抑制率可达95.2%;当其比例为90%时,在加用GCV后,该细胞群体几乎不形成集落(3个孔中仅见1个克隆)。
重复感染试验 随着感染次数的增多,AO细胞对GCV的敏感性有所增加,G418筛选所获得的阳性克隆数也逐渐增多(见表2)。
表2 重复感染后G418筛选阳性克隆数及GCV对细胞的生长抑制率 感染次数
1
2
4
, 百拇医药
6
8
G418筛选阳性克隆数(x±s)
48±7
93±12
145±12
185±9
226±28
GCV对细胞的生长抑制率(%)
5.8
8.3
14.3
, 百拇医药 23.1
33.9
混合培养试验:与VPC/HSV1-tkc细胞混合培养后,AO细胞对GCV的敏感性见图2,可见随着与之混合培养的VPC/HSV1-tkc细胞比例的增高,AO细胞对GCV的敏感性也逐渐增高,当VPC/HSV1-tkc细胞与AO细胞之比为8:2时,GCV对AO细胞的生长抑制率可达96.6%。

图2 GCV对与VPC/HSV1-tkc细胞混育后的AO细胞的生长抑制率
讨 论
1.关于药物敏感基因治疗 药物敏感基因治疗(又称自杀基因治疗)作为一种最有希望的肿瘤基因治疗策略已引起广泛关注[1]。其主要治疗原理为:应用逆转录病毒介导等方法将单纯疱疹病毒胸腺嘧啶核苷激酶基因(HSV1-tk)导入肿瘤细胞,使其表达HSV1特有的胸腺嘧啶核苷激酶(HSV1-TK),然后再给予HSV1-TK的底物羟甲基无环鸟苷(GCV)进行治疗。GCV磷酸化产物具有高度细胞毒性,可阻断肿瘤细胞的DNA合成,从而导致肿瘤细胞死亡,并对其周围的肿瘤细胞具有“旁观者效应”、达到治疗肿瘤的目的。这一治疗策略更适用于治疗象卵巢癌这样相对较为隔离(主要存在于腹腔内)的肿瘤。
, 百拇医药
2.GCV、ACV对AO/HSV1-tkc的生长抑制效应
资料表明[2],GCV对HSV1-tk阳性的鼠成纤维细胞生长的半数抑制浓度(IC50)比HSV1-tk阴性者低120余倍,而ACV对二者的IC50仅相差约20倍。哺乳动物细胞的tk存在与否对IC50无明显影响。这点正是设计HSV1-tk/GCV基因治疗系统的基础与前提。本文的实验结果与此相似,且显微镜下跟踪观察也提示在10μg/ml以上的GCV作用下,HSV1-tk阳性的AO细胞所形成的集落较小或不形成集落,进一步证实了GCV对HSV1-tkc+的卵巢癌细胞有强力的杀伤和/或抑制生长效应,其作用明显优于ACV。从而为将HSV1-tk/GCV系统应用于卵巢癌提供了理论基础。
, 百拇医药
肿瘤组织病理学检查进一步提示,虽然GCV未能在治疗期内将AO/HSV1-tk细胞完全消灭,但其残留细胞形态上已发生明显变化,大部分细胞处于变性、裂解状态。
3.GCV抑制AO/HSV1-tkc生长的机理
早在1977年,Elion等[3]报告ACV可抑制HSV1复制,并提示其作用过程需要HSV1-tk酶的参与。其后,多位学者证实,ACV可抑制转导有HSV1-tk的细胞生长,其作用机制为HSV1-tk可将ACV磷酸化为毒性产物,终止DNA合成,从而导致细胞死亡。
本研究结果表明,AO/HSV1-tkc细胞在GCV作用下,S期细胞比例明显升高,且呈一定的剂量依赖性。在药物作用时间上,经用药后3~4天S期细胞比例最高,达90%以上,第5天有所回降。
, 百拇医药
另外,体外实验研究中G2+M期细胞比例的变化也较为明显,总的说来,在GCV作用下,AO/HSV1-tkc细胞中的G2+M期细胞比例维持在一个较低的水平,但是在10 μg/ml GCV作用第5天,G2+M期细胞比例呈现明显“反跳”,达25.0%。当GCV浓度为100 μg/ml时无此“反跳”现象,但S期细胞比例又较低剂量组高。作者认为有以下几种可能的解释:
(1)GCV在HSV1-tk酶的催化下磷酸化为毒性产物,终止了正处于S期的细胞的DNA合成,从而使细胞阻滞于S期,造成S期细胞大量堆积;
(2)部分细胞未能导入HSV1-tk而仅导入了neo基因,因而仍呈G418抗性;或是在GCV作用的压力下,部分细胞可能丢失HSV1-tk或关闭其表达,或通过其它机制对GCV产生耐药性,这样当大量的表达HSV1-tk的细胞被杀伤后,通过某种途径刺激这部分细胞大量增殖,进入S期,并占主导地位,从而导致S期细胞比例增加。
, 百拇医药
(3)某些细胞尽管在S期受到损伤,但通过某种机制能够加以“修复”,从而在中量(10 μg/ml)GCV作用的后期(第5天)跨越S期,进入G2、M期。但在大剂量(100 μg/ml)GCV作用时则无法修复,因而G2+M期比例仍较低。
上述三种情况是否能确立,尚有待于进一步研究,但S期细胞比例增加这一现象本身就可能提示正负两方面的效应:其一,GCV停药后可能会出现肿瘤加速生长的反跳现象。既往文献就曾报道[4],以HSV1-tk/GCV系统治疗实验性大鼠脑胶质瘤后,近期效果非常显著,肿瘤体积缩小28倍,大鼠生存时间延长4倍,但远期有复发。这一现象支持本文的推断;其二,残存肿瘤可能对S期特异的化疗药物更为敏感,提示联合应用HSV1-tk/GCV系统和常规化疗可能有协同效应。Kim等人[5]曾报道,ACV可以选择性地提高HSV1-tk+的神经胶质瘤细胞的放射敏感性。这对于本文的这一推断可能是一个佐证。
, http://www.100md.com
此外,有学者报道,GCV可诱导携有HSV1-tk的细胞发生凋亡(Apoptosis)[6]。本实验中以PI作DNA荧光染色,显示经10 μg/ml GCV作用后部分细胞呈现凋亡细胞的形态表现,即核呈颗粒状裂解,FACS检测也提示GCV作用后A0峰细胞(有人认为即为凋亡细胞)比例明显升高,且呈一定的剂量依赖性与时间依赖性;
4.关于旁观者效应
前文所示,GCV可以高效杀伤携有HSV1-tk的细胞,或抑制其生长,而在体内体外实验中,人们还发现GCV不仅可以诱使携有HSV1-tk的细胞本身死亡(即“自杀),还可影响邻近的HSV1-tk-细胞,产生杀伤效果,此即所谓“旁观者效应”(Bystander Effect),而且,这种经GCV作用的HSV1-tk+细胞仍能发挥对周围细胞的杀伤作用。Freeman等据此提出,将卵巢癌细胞自病人体内取出后,体外转导HSV1-tk,并以致死剂量的放射线照射,将其作为肿瘤疫苗回植入病人体内,再给予GCV治疗。这一方案已获得NIH的批准[7]。
, http://www.100md.com
至于这种“旁观者效应”的机理,目前说法不一,主要包括:(1)细胞之间通过间隙连接(gap junction)或桥粒传送有毒物质的颗粒而产生邻近杀伤;(2)“旁观”细胞主动摄取凋亡碎片,而碎片中含有磷酸化的GCV,从而致使“旁观”细胞死亡;(3)已发生自杀的细胞及其碎片引发机体免疫反应,由于“旁观”肿瘤细胞与其有较一致的抗原性,从而被免疫效应细胞杀伤、清除;(4)肿瘤血管内皮细胞转导了HSV1-tk,并被GCV杀伤,导致肿瘤缺血,细胞死亡。有学者提出,这种“旁观”细胞的死亡方式为凋亡,bcl-2基因表达可抑制凋亡的发生。
本文在体外实验中证实HSV1-tkc/GCV系统对卵巢癌AO细胞确有一定的“旁观者效应”,这也说明免疫及/或血管机制至少不是“旁观者效应”的唯一途径。但本研究中这种效应不如国外报道的体内实验中明显,则可能是由于缺乏免疫及/或血管机制的作用,也可能是由于接种细胞密度较低,细胞不能密切接触所致。
, http://www.100md.com 5.关于重复RV感染
由于GCV对携有HSV1-tk的卵巢癌细胞有较强的杀伤作用或明显的抑制生长的作用,因此转基因效率的提高已成为制约基因治疗应用效果的关键问题。逆转录病毒转染肿瘤的效率除受许多因素影响,如温度、感染液中逆转录病毒浓度及载体本身的构建和VPC生长状态等,此外,还受到感染时进入分裂期的细胞数量的制约。卵巢癌与其它肿瘤一样,每个细胞的细胞周期处于无序的非同步状态,这样一次性感染只能是少数细胞获得基因转导。在本实验中也观察到随着感染次数的增多,所获得的转染阳性克隆数明显提高,转染后肿瘤细胞对GCV的敏感性也有所提高,提示重复逆转录病毒感染可能是提高基因转导效率的有效途径之一。与降温、浓缩及离心等目前国外常用的方法相比,重复感染可以应用于体内感染试验,因此具有一定的优越性。当然,从本实验中也可看出,即使重复感染8次,其感染率仍然很低。与临床应用的要求还相距甚远。
6.关于VPC/HSV1-tkc细胞与AO细胞的混合培养
, 百拇医药
动物实验证实,将VPC注射到脑胶质瘤部位,使其在生长期间不断释放新生的RV颗粒,从而产生对肿瘤细胞的连续的重复感染,从而提高了对肿瘤的治疗作有。这一方面目前已进入Ⅲ期临床试验[8]。由于“旁观者效应”并非细胞特异性的表现。它在不同细胞系之间也有作用,因此在这一方法的总体效应中也不能除外“旁观者效应”的作用。本文实验中证实,这一方法对卵巢癌细胞同样有效。
总之,HSV1-tk/GCV基因治疗系统在体外对卵巢癌细胞具有高效的杀伤作用。但其应用方法尚需进一步研究。
第一作者简介 徐丛剑,男,博士,主治医师。
参 考 文 献
1 Stone R.Molecular surgery for brain tumors.Science,1992,256:1513
, 百拇医药
2 Oliver S,Bubley G,Crumpacker C.Inhibition of HSV1-transformed murine cells by nucleoside analogs,2'-NDG and 2'-nor-cGMP:Mechanisms of inhibition and reversal by exogenous nucleosides.Virology,1985,145:84
3 Elion GB,Furman PA,Fyfe JA,et al.Selectivity of action of an antiheptic agent,9-(2-hydroxyethoxymethyl)guanine.Proc Natl Acad Sci USA,1977,74:5716
4 Maron A,Gustin T,Le Roux A,et al.Gene therapy of rat C6 glioma using adenovirus-mediated transfer of the herpes simplex virus thymidine kinase gene:long-term follow-up by magnetic resonance imaging.Gene-Ther,1996,3(4):315
, 百拇医药
5 Kim JH,Kim SH,Kolozsvary A,et al.Selective enhancement of radiation response of herpes simplex virus thymidine kinase transduced 9L gliosarcoma cells in vitro and in vivo by antiviral agents.Int J Radiat Oncol Biol Phys,1995,33(4):861
6 Freeman SM,Abboud CN,Whartenby KA,et al.The “bystander effect”:Tumor regression when a fraction of the tumor mass is genetically modified.Cancer Res,1993,53:5274
7 Freeman SM,McCune C,Angel C,et al.Treatment of ovarian cancer using HSV1-tk gene modified vaccine-regulatory issues.Hum Gene Ther,1992,3:342
8 Wivel N.Sandoz plans first large phase Ⅲ gene therapy trial.Biotechnology News,1996,16(12):1
(收稿:1998-11-12 修回:1999-03-24), http://www.100md.com