Η–»Ψ–‘–ίΩΥ―–ΨΩœ÷Ή¥
Ής’ΏΘΚΝθΜ≥«μ
ΒΞΈΜΘΚΝθΜ≥«μ ΒΎ»ΐΨϋ“Ϋ¥σ―ߥσΤΚ“Ϋ‘Κ ÷Ί«λ 630000
ΙΊΦϋ¥ ΘΚ
“Ϋ―ß–¬÷Σ‘”÷Ψ990401 ’Σ“Σ ‘Ύ¥σ σΡ‘»±―Σ‘ΌΙύΉΔΥπ…Υ Β―ιΡΘ–Ά…œΘ§Ιέ≤λΓΔ≤βΕ®‘ΎΡ‘»±―ΣΚσΕ‘ΚΘ¬μΉι÷·ΒΡ–ΥΖή–‘Α±ΜυΥαΦΑ―θΉ‘”…ΜυΒΡ”ΑœλΓΘΫαΙϊœ‘ Ψ»±―ΣΚσGM1œ‘÷χΦθ…ΌΘ§”’ΖΔΤδœΗΑϊΆβΙ»Α±ΥαΚΆΧλΟ≈Ε§Α±Υα‘ωΗΏΓΘ±μΟςΡ‘»±―Σ‘ΌΙύΉΔΥπ…Υ”κEAAΒΡΙΐΕ» ΆΖ≈ΚΆ―θΉ‘”…ΜυΒΡ≤ζ…ζΟή«–œύΙΊΘ§ΕχGM1Ε‘¥σ σΡ‘»±―ΣΨΏ”–±ΘΜΛΉς”Ο(P<0.01)ΓΘ
Effect of EAA and Oxygen Free Radical
of Hippocampus on Experimental
Rat Ischemic Reperfusion Injury
, ΑΌΡ¥“Ϋ“©
Huan Huaijun Xu Renshi Liu Yumin et al
Department of Neurology, the Second Affiliated hospital of
Hubei Medical University, Wuhan 430071
Abstract The effect of excitatory amino acid (EAA) and oxygen free radical on ischemic reperfusion injury was investigated by measuring hippocampus glutamate (Glu), aspartate (Asp) and malonaldehyde (MDA) contents on sham operated. NS-treated and GM1-treated group in 4-vessel occlusion model. We found that the MDA contents significantly increased and the EAA content significatly decreased in NStreated group as compared with the sham operated group respectively (P<0.01). In GM1-treated group, the changes significantly improved (P<0.01). The results suggested that EAA excitotoxin is closely related with the cerebral ischemic reperfusion damage.
, http://www.100md.com
Key words Cerebral ischemic damage; Oxygen free radical;EAA Ganglioside
ΫϋΡξ Β―ι―–ΨΩ±μΟςΘΚ–ΥΖή–‘Α±ΜυΥα(Excitatory Amino Acid, EAA)ΒΡ…ώΨ≠ΕΨ–‘Ής”Ο”–―θΉ‘”…Μυ≤Έ”κΤδΙΐ≥Χ[1]ΓΘΒΪ―θΉ‘”…Μυ”κEAAΒΡΙΊœΒ…–≤Μ«ε≥ΰΓΘ‘χ”–±®Βά[2]‘Ύ…≥ΆΝ σΝΫ≤ύΨ±ΉήΕ·¬ωΉηΕœΒΡΡΘ–Ά…œΘ§Ιέ≤λΒΫ…ώΨ≠ΫΎΏΑ÷§(Ganglioside M1Θ§GM1)Ω…œ‘÷χΦθ…Ό»±―Σ”’ΖΔΒΡœΗΑϊΆβ–ΥΖή–‘Α±ΜυΥα(Ι»Α±ΥαΚΆΧλΟ≈Ε§Α±Υα)Υ°ΤΫ‘ωΗΏΓΘ“ρ¥ΥΘ§Έ“Ο«Ά®Ιΐ”Π”ΟGM1Φθ…Ό¥σ σ»ΪΡ‘»±―Σ‘ΌΙύΉΔΤΎEAAΒΡΙΐΕ» ΆΖ≈ά¥Ιέ≤λ±ϊΕΰ»©(MDA)Κ§ΝΩΒΡ±δΜ·Θ§“‘ΧΫΧ÷EAA”κ―θΉ‘”…Μυ‘Ύ»±―Σ‘ΌΙύΉΔΥπ…Υ÷–ΒΡΙΊœΒΘ§ΈΣΝΌ¥≤Ρ‘»±―ΣΥπ…ΥΒΡ÷ΈΝΤΧαΙ©“άΨίΓΘ
1 ≤ΡΝœ”κΖΫΖ®
1.1 Ε·ΈοΖ÷ΉιΦΑ»±―Σ‘ΌΙύΉΔΡΘ–Ά ≥… λΫΓΩΒ–έ–‘Wistar¥σ σ24÷ΜΘ§Χε÷Ί200ΓΪ250 gΓΘΥφΜζΖ÷ΈΣΦΌ ÷ θΉι(ΩΊ÷ΤΉι)Θ§Ζ«GM1÷ΈΝΤΉι(»±―Σ30 min‘ΌΙύΉΔ60 min NS)ΚΆ÷ΈΝΤΉι(»±―Σ30 min‘ΌΙύΉΔ60 min NSΦΑGM1¥Πάμ)Θ§ΟΩΉι8÷ΜΓΘ»±―Σ(Ψ±ΡΎΥΡ―ΣΙήΉηΕœ)‘ΌΙύΉΔΡΘ–Ά‘ΎPulsinelliΒ»[3]Ζ®Μυ¥Γ…œ…‘ΉςΗΡΫχΓΘ
, http://www.100md.com
1.2 Ρ‘ΚΘ¬μΉι÷·EAAΦΑMDAΚ§ΝΩ≤βΕ® Α¥ΗςΉι…ηΦΤ“Σ«σ”Ύ Β―ιΆξ≥… ±Θ§―ΗΥΌΕœΆΖ»ΓΡ‘Θ§±υ≈Χ÷–Ζ÷άκΥΪ≤ύΚΘ¬μΘ§ΒΆΈ¬‘»Ϋ§Θ§EAA≤…«Α”ΟΗΏ–ß“Κœύ…ΪΤΉ“«―ή…ζ…ΪΤΉΖ®≤βΕ®Θ§MDA≤…”ΟΝρ¥ζΑΆ±»ΆΉœ‘…ΪΖ®(TBA)[4]≤βΕ®ΓΘ
GM1¥ΠάμΉι‘Ύ»±―ΣΚσ5 minΗχ“©Θ§Α¥10 mg/kgΗΙ«ΜΡΎΉΔ…δGM1ΓΘ
1.3 Ά≥ΦΤ―ß¥Πάμ ΐΨί“‘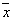 Γάs±μ ΨΓΘΉιΦδ±»Ϋœ≤…”ΟtΦλ―ιΘ§ΠΝ=0.05ΓΘEAAΚ§ΝΩ”κMDAΚ§ΝΩΉςΦρΒΞ÷±œΏœύΙΊΖ÷ΈωΓΘ
Γάs±μ ΨΓΘΉιΦδ±»Ϋœ≤…”ΟtΦλ―ιΘ§ΠΝ=0.05ΓΘEAAΚ§ΝΩ”κMDAΚ§ΝΩΉςΦρΒΞ÷±œΏœύΙΊΖ÷ΈωΓΘ
2 ΫαΙϊ
»±―ΣΦΑ‘ΌΙύΉΔEAAΓΔMDAΚ§ΝΩ±δΜ·ΦΑGM1ΒΡ”ΑœλΫαΙϊΦϊΗΫ±μΓΘ
, ΑΌΡ¥“Ϋ“© ΗΫ±μ »±―Σ‘ΌΙύΉΔEAAΓΔMDAΚ§ΝΩ±δΜ·ΦΑGM1ΒΡ”Αœλ(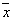 Γάs) Ιέ≤β÷Η±ξ
Γάs) Ιέ≤β÷Η±ξ
ΩΊ÷ΤΉι
Ρ‘»±―ΣΚσ30 min ‘ΌΙύΉΔΚσ60 min
Ζ«GM1÷ΈΝΤΉι
GM1÷ΈΝΤΉι
Ι» Α± Υα
7.51 Γά 1.05
5.48 Γά 0.84*
6.85 Γά 0.93
, http://www.100md.com
ΧλΟ≈Ε§Α±Υα
5.16 Γά 0.55
4.04Γά 0.31*
4.79 Γά 0.24
±ϊΕΰ»©Υα
82.99Γά13.33
158.68Γά14.68*
93.06Γά18.98Γς
”κΩΊ÷ΤΉιΓΔGM1÷ΈΝΤΉι±»ΫœΘ§*P<0.01ΘΜ”κΩΊ÷ΤΉι±»ΫœΘ§ΓςP>0.053 Χ÷¬έ
ΡΩ«ΑΒΡ―–ΨΩ±μΟςΘ§―θΉ‘”…Μυ―ßΥΒ‘ΎΡ‘»±―Σ‘ΌΙύΉΔΥπ…ΥΜζάμ÷–’Φ”–÷Ί“ΣΒΡΒΊΈΜ[5]ΓΘΡ‘»±―Σ‘ΌΙύΉΔ‘γΤΎΘ§œΗΑϊΆβEAA≈®Ε»œ‘÷χ‘ωΗΏΘ§EAAΤτΕ·NMDA ήΧεΟ≈ΩΊ–‘ΗΤάκΉ”Ά®ΒάΘ§ ΙœΗΑϊΡΎ”ΈάκΗΤΕ―Ψέ≥ωœ÷ΗΤ≥§‘ΊΓΘΗΤ≥§‘ΊΩ…“‘ΦΛΜνΝΉ÷§ΟΗ≤ζ…ζΉ‘”…ΜυΘ§Ή‘”…Μυ”÷ΗΡ±δ…ζΈοΡΛΒΡΫαΙΙΚΆΙΠΡήΘ§ΗΤΆ®ΒάΩΣΖ≈Θ§Φ”÷ΊΗΤ≥§‘ΊΓΘ≥÷–χΖ≈ΒγCa++ΡΎΝς”÷ΡήΫχ“Μ≤ΫΒΦ÷¬EAA ΆΖ≈ΒΡ‘ωΦ”Θ§Ά§ ± Ι÷Ί…ψ»Γ ήΉηΘ§ΫχΕχΦ”÷ΊEAA‘ΎœΗΑϊΆβΕ―Ψέ[6]ΓΘ’β÷÷≤ΓάμΙΐ≥ΧΉν÷’ΒΦ÷¬–ΥΖή–‘Υπ…ΥΒΡΖΔ…ζΓΘΉ‘”…ΜυΕ‘œΗΑϊΒΡΥπ…ΥΉς”Ο÷ς“Σ «“ΐΤπ…ζΈοΡΛ≤Μ±ΞΚΆ÷§ΖΨΥαΖΔ…ζ÷§÷ Ιΐ―θΜ·ΈοΘ§ΤδΚ§ΝΩΒΡ±δΜ·ΦδΫ”ΒΊΖ¥”ΠΝΥΉι÷·÷–―θΉ‘”…ΜυΚ§ΝΩΒΡ±δΜ·ΓΘ“ρ¥ΥΘ§Ά®Ιΐ≤βΕ®MDAΚ§ΝΩΒΡ±δΜ·ΦδΫ”ΒΊΙάΦΤΡ‘Ήι÷·÷–―θΉ‘”…ΜυΥ°ΤΫΚΆ÷§÷ Ιΐ―θΜ·Ζ¥”ΠΒΡ«Ω»θΓΘ―–ΨΩΫαΙϊ ΨΚΘ¬μΉι÷·÷–EAA‘Ύ»±―Σ30 min‘ΌΙύΉΔ60 min ±œ‘÷χΫœΦΌ ÷ θΉιœ¬ΫΒ(P<0.01)Θ§ΕχMDA‘ρœ‘÷χ…ΐΗΏ(P<0.01)ΓΘΒ±”ΟGM1¥Πάμ»±―Σ‘ΌΙύΉΔ¥σ σΚσΘ§ΥφΉ≈EAAœ¬ΫΒΒΡΗΡ…ΤΘ§MDAΚ§ΝΩœύ”ΠΒΊΫΒΒΆ(P<0.01)Θ§«“Ά§ΦΌ ÷ θΉιΟΜ”–œ‘÷χ–‘≤ν“λ(P>0.05)ΓΘΦρΒΞ÷±œΏœύΙΊΖ÷ΈωΫαΙϊ±μΟςΘΚΧλΟ≈Ε§Α±ΥαΆ§MDAΚ§ΝΩ”–œ‘÷χΗΚœύΙΊ–‘(r=-0.494)ΓΘ“ρ¥ΥΘ§Έ“Ο«»œΈΣΡ‘»±―Σ‘ΌΙύΉΔΥπ…ΥΙΐ≥Χ÷–―θΉ‘”…ΜυΒΡ≤ζ…ζΚΆEAAΒΡΙΐΕ» ΆΖ≈÷°Φδ”–Ή≈œύΜΞ–≠Ά§ΓΔΜΞΈΣ“ρΙϊΒΡΙΊœΒΘ§Ρ‘»±―ΣΥπ…Υ÷–EAAΒΡ–ΥΖήΕΨ–‘Ής”ΟΩ…ΡήΆ§―θΉ‘”…ΜυΒΡΫιΒΦ”–Ή≈≤ΜΩ…Ζ÷ΗνΒΡΙΊœΒΓΘ
, ΑΌΡ¥“Ϋ“©
≤ΈΩΦΈΡœΉ
1 Barth A, Barth L, Newell D W. Combination therapy of MK801 and ΠΝ phenyltertbutylnitrone enhances protection against ischemic neuronal damage in organotypic hippcampal slice cultures. Exp Neurol, 1996,141(2):330
2 ΒΥ–ΓΟςΘ§÷λ≥œΘ§’≈ΙβωΪ.ΒΞΆΌ“ΚΥα…ώΨ≠ΫΎή’”κ»±―Σ–‘Ρ‘Υπ…Υ(Ήέ ω).ΙζΆβ“Ϋ―ß(Ρ‘―ΣΙήΦ≤≤ΓΖ÷≤α)Θ§1994Θ§2(2)ΘΚ69
3 Pulsinelli W A, Brierley J B. A new model of bilateral the unanesthatized rat hemispheric ischemia. Stroke, 1997,10(2):267
, ΑΌΡ¥“Ϋ“©
4 Χο―«ΨϋΘ§…ρΈΡΟΖ.―Σ«εΉήTBAΖ¥”ΠΈοΓΔLPOΦΑMDA―υΈο÷ ΒΡΝΣΚœ≤βΕ®.ΫβΖ≈Ψϋ“Ϋ―ß«ι±®Θ§1990Θ§(4):322ΓΪ323
5 Traystman R J,Kirsch J R, Koehler R C. oxygen radical mechanisms of brain injury following ischemia and reperfusion. J Appl Physiol, 1991,71(4):1185
6 Thomas W, Furlow J R. Cerebral ischemia produced by four-vessel occlusion in the rat: a quantitative evaluation of cerebral blood flow. J Appl physiol, 1982,13(6):852
’Ηε»’ΤΎΘΚ1999-04-0, ΑΌΡ¥“Ϋ“©
ΒΞΈΜΘΚΝθΜ≥«μ ΒΎ»ΐΨϋ“Ϋ¥σ―ߥσΤΚ“Ϋ‘Κ ÷Ί«λ 630000
ΙΊΦϋ¥ ΘΚ
“Ϋ―ß–¬÷Σ‘”÷Ψ990401 ’Σ“Σ ‘Ύ¥σ σΡ‘»±―Σ‘ΌΙύΉΔΥπ…Υ Β―ιΡΘ–Ά…œΘ§Ιέ≤λΓΔ≤βΕ®‘ΎΡ‘»±―ΣΚσΕ‘ΚΘ¬μΉι÷·ΒΡ–ΥΖή–‘Α±ΜυΥαΦΑ―θΉ‘”…ΜυΒΡ”ΑœλΓΘΫαΙϊœ‘ Ψ»±―ΣΚσGM1œ‘÷χΦθ…ΌΘ§”’ΖΔΤδœΗΑϊΆβΙ»Α±ΥαΚΆΧλΟ≈Ε§Α±Υα‘ωΗΏΓΘ±μΟςΡ‘»±―Σ‘ΌΙύΉΔΥπ…Υ”κEAAΒΡΙΐΕ» ΆΖ≈ΚΆ―θΉ‘”…ΜυΒΡ≤ζ…ζΟή«–œύΙΊΘ§ΕχGM1Ε‘¥σ σΡ‘»±―ΣΨΏ”–±ΘΜΛΉς”Ο(P<0.01)ΓΘ
Effect of EAA and Oxygen Free Radical
of Hippocampus on Experimental
Rat Ischemic Reperfusion Injury
, ΑΌΡ¥“Ϋ“©
Huan Huaijun Xu Renshi Liu Yumin et al
Department of Neurology, the Second Affiliated hospital of
Hubei Medical University, Wuhan 430071
Abstract The effect of excitatory amino acid (EAA) and oxygen free radical on ischemic reperfusion injury was investigated by measuring hippocampus glutamate (Glu), aspartate (Asp) and malonaldehyde (MDA) contents on sham operated. NS-treated and GM1-treated group in 4-vessel occlusion model. We found that the MDA contents significantly increased and the EAA content significatly decreased in NStreated group as compared with the sham operated group respectively (P<0.01). In GM1-treated group, the changes significantly improved (P<0.01). The results suggested that EAA excitotoxin is closely related with the cerebral ischemic reperfusion damage.
, http://www.100md.com
Key words Cerebral ischemic damage; Oxygen free radical;EAA Ganglioside
ΫϋΡξ Β―ι―–ΨΩ±μΟςΘΚ–ΥΖή–‘Α±ΜυΥα(Excitatory Amino Acid, EAA)ΒΡ…ώΨ≠ΕΨ–‘Ής”Ο”–―θΉ‘”…Μυ≤Έ”κΤδΙΐ≥Χ[1]ΓΘΒΪ―θΉ‘”…Μυ”κEAAΒΡΙΊœΒ…–≤Μ«ε≥ΰΓΘ‘χ”–±®Βά[2]‘Ύ…≥ΆΝ σΝΫ≤ύΨ±ΉήΕ·¬ωΉηΕœΒΡΡΘ–Ά…œΘ§Ιέ≤λΒΫ…ώΨ≠ΫΎΏΑ÷§(Ganglioside M1Θ§GM1)Ω…œ‘÷χΦθ…Ό»±―Σ”’ΖΔΒΡœΗΑϊΆβ–ΥΖή–‘Α±ΜυΥα(Ι»Α±ΥαΚΆΧλΟ≈Ε§Α±Υα)Υ°ΤΫ‘ωΗΏΓΘ“ρ¥ΥΘ§Έ“Ο«Ά®Ιΐ”Π”ΟGM1Φθ…Ό¥σ σ»ΪΡ‘»±―Σ‘ΌΙύΉΔΤΎEAAΒΡΙΐΕ» ΆΖ≈ά¥Ιέ≤λ±ϊΕΰ»©(MDA)Κ§ΝΩΒΡ±δΜ·Θ§“‘ΧΫΧ÷EAA”κ―θΉ‘”…Μυ‘Ύ»±―Σ‘ΌΙύΉΔΥπ…Υ÷–ΒΡΙΊœΒΘ§ΈΣΝΌ¥≤Ρ‘»±―ΣΥπ…ΥΒΡ÷ΈΝΤΧαΙ©“άΨίΓΘ
1 ≤ΡΝœ”κΖΫΖ®
1.1 Ε·ΈοΖ÷ΉιΦΑ»±―Σ‘ΌΙύΉΔΡΘ–Ά ≥… λΫΓΩΒ–έ–‘Wistar¥σ σ24÷ΜΘ§Χε÷Ί200ΓΪ250 gΓΘΥφΜζΖ÷ΈΣΦΌ ÷ θΉι(ΩΊ÷ΤΉι)Θ§Ζ«GM1÷ΈΝΤΉι(»±―Σ30 min‘ΌΙύΉΔ60 min NS)ΚΆ÷ΈΝΤΉι(»±―Σ30 min‘ΌΙύΉΔ60 min NSΦΑGM1¥Πάμ)Θ§ΟΩΉι8÷ΜΓΘ»±―Σ(Ψ±ΡΎΥΡ―ΣΙήΉηΕœ)‘ΌΙύΉΔΡΘ–Ά‘ΎPulsinelliΒ»[3]Ζ®Μυ¥Γ…œ…‘ΉςΗΡΫχΓΘ
, http://www.100md.com
1.2 Ρ‘ΚΘ¬μΉι÷·EAAΦΑMDAΚ§ΝΩ≤βΕ® Α¥ΗςΉι…ηΦΤ“Σ«σ”Ύ Β―ιΆξ≥… ±Θ§―ΗΥΌΕœΆΖ»ΓΡ‘Θ§±υ≈Χ÷–Ζ÷άκΥΪ≤ύΚΘ¬μΘ§ΒΆΈ¬‘»Ϋ§Θ§EAA≤…«Α”ΟΗΏ–ß“Κœύ…ΪΤΉ“«―ή…ζ…ΪΤΉΖ®≤βΕ®Θ§MDA≤…”ΟΝρ¥ζΑΆ±»ΆΉœ‘…ΪΖ®(TBA)[4]≤βΕ®ΓΘ
GM1¥ΠάμΉι‘Ύ»±―ΣΚσ5 minΗχ“©Θ§Α¥10 mg/kgΗΙ«ΜΡΎΉΔ…δGM1ΓΘ
1.3 Ά≥ΦΤ―ß¥Πάμ ΐΨί“‘
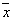 Γάs±μ ΨΓΘΉιΦδ±»Ϋœ≤…”ΟtΦλ―ιΘ§ΠΝ=0.05ΓΘEAAΚ§ΝΩ”κMDAΚ§ΝΩΉςΦρΒΞ÷±œΏœύΙΊΖ÷ΈωΓΘ
Γάs±μ ΨΓΘΉιΦδ±»Ϋœ≤…”ΟtΦλ―ιΘ§ΠΝ=0.05ΓΘEAAΚ§ΝΩ”κMDAΚ§ΝΩΉςΦρΒΞ÷±œΏœύΙΊΖ÷ΈωΓΘ2 ΫαΙϊ
»±―ΣΦΑ‘ΌΙύΉΔEAAΓΔMDAΚ§ΝΩ±δΜ·ΦΑGM1ΒΡ”ΑœλΫαΙϊΦϊΗΫ±μΓΘ
, ΑΌΡ¥“Ϋ“© ΗΫ±μ »±―Σ‘ΌΙύΉΔEAAΓΔMDAΚ§ΝΩ±δΜ·ΦΑGM1ΒΡ”Αœλ(
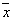 Γάs) Ιέ≤β÷Η±ξ
Γάs) Ιέ≤β÷Η±ξΩΊ÷ΤΉι
Ρ‘»±―ΣΚσ30 min ‘ΌΙύΉΔΚσ60 min
Ζ«GM1÷ΈΝΤΉι
GM1÷ΈΝΤΉι
Ι» Α± Υα
7.51 Γά 1.05
5.48 Γά 0.84*
6.85 Γά 0.93
, http://www.100md.com
ΧλΟ≈Ε§Α±Υα
5.16 Γά 0.55
4.04Γά 0.31*
4.79 Γά 0.24
±ϊΕΰ»©Υα
82.99Γά13.33
158.68Γά14.68*
93.06Γά18.98Γς
”κΩΊ÷ΤΉιΓΔGM1÷ΈΝΤΉι±»ΫœΘ§*P<0.01ΘΜ”κΩΊ÷ΤΉι±»ΫœΘ§ΓςP>0.053 Χ÷¬έ
ΡΩ«ΑΒΡ―–ΨΩ±μΟςΘ§―θΉ‘”…Μυ―ßΥΒ‘ΎΡ‘»±―Σ‘ΌΙύΉΔΥπ…ΥΜζάμ÷–’Φ”–÷Ί“ΣΒΡΒΊΈΜ[5]ΓΘΡ‘»±―Σ‘ΌΙύΉΔ‘γΤΎΘ§œΗΑϊΆβEAA≈®Ε»œ‘÷χ‘ωΗΏΘ§EAAΤτΕ·NMDA ήΧεΟ≈ΩΊ–‘ΗΤάκΉ”Ά®ΒάΘ§ ΙœΗΑϊΡΎ”ΈάκΗΤΕ―Ψέ≥ωœ÷ΗΤ≥§‘ΊΓΘΗΤ≥§‘ΊΩ…“‘ΦΛΜνΝΉ÷§ΟΗ≤ζ…ζΉ‘”…ΜυΘ§Ή‘”…Μυ”÷ΗΡ±δ…ζΈοΡΛΒΡΫαΙΙΚΆΙΠΡήΘ§ΗΤΆ®ΒάΩΣΖ≈Θ§Φ”÷ΊΗΤ≥§‘ΊΓΘ≥÷–χΖ≈ΒγCa++ΡΎΝς”÷ΡήΫχ“Μ≤ΫΒΦ÷¬EAA ΆΖ≈ΒΡ‘ωΦ”Θ§Ά§ ± Ι÷Ί…ψ»Γ ήΉηΘ§ΫχΕχΦ”÷ΊEAA‘ΎœΗΑϊΆβΕ―Ψέ[6]ΓΘ’β÷÷≤ΓάμΙΐ≥ΧΉν÷’ΒΦ÷¬–ΥΖή–‘Υπ…ΥΒΡΖΔ…ζΓΘΉ‘”…ΜυΕ‘œΗΑϊΒΡΥπ…ΥΉς”Ο÷ς“Σ «“ΐΤπ…ζΈοΡΛ≤Μ±ΞΚΆ÷§ΖΨΥαΖΔ…ζ÷§÷ Ιΐ―θΜ·ΈοΘ§ΤδΚ§ΝΩΒΡ±δΜ·ΦδΫ”ΒΊΖ¥”ΠΝΥΉι÷·÷–―θΉ‘”…ΜυΚ§ΝΩΒΡ±δΜ·ΓΘ“ρ¥ΥΘ§Ά®Ιΐ≤βΕ®MDAΚ§ΝΩΒΡ±δΜ·ΦδΫ”ΒΊΙάΦΤΡ‘Ήι÷·÷–―θΉ‘”…ΜυΥ°ΤΫΚΆ÷§÷ Ιΐ―θΜ·Ζ¥”ΠΒΡ«Ω»θΓΘ―–ΨΩΫαΙϊ ΨΚΘ¬μΉι÷·÷–EAA‘Ύ»±―Σ30 min‘ΌΙύΉΔ60 min ±œ‘÷χΫœΦΌ ÷ θΉιœ¬ΫΒ(P<0.01)Θ§ΕχMDA‘ρœ‘÷χ…ΐΗΏ(P<0.01)ΓΘΒ±”ΟGM1¥Πάμ»±―Σ‘ΌΙύΉΔ¥σ σΚσΘ§ΥφΉ≈EAAœ¬ΫΒΒΡΗΡ…ΤΘ§MDAΚ§ΝΩœύ”ΠΒΊΫΒΒΆ(P<0.01)Θ§«“Ά§ΦΌ ÷ θΉιΟΜ”–œ‘÷χ–‘≤ν“λ(P>0.05)ΓΘΦρΒΞ÷±œΏœύΙΊΖ÷ΈωΫαΙϊ±μΟςΘΚΧλΟ≈Ε§Α±ΥαΆ§MDAΚ§ΝΩ”–œ‘÷χΗΚœύΙΊ–‘(r=-0.494)ΓΘ“ρ¥ΥΘ§Έ“Ο«»œΈΣΡ‘»±―Σ‘ΌΙύΉΔΥπ…ΥΙΐ≥Χ÷–―θΉ‘”…ΜυΒΡ≤ζ…ζΚΆEAAΒΡΙΐΕ» ΆΖ≈÷°Φδ”–Ή≈œύΜΞ–≠Ά§ΓΔΜΞΈΣ“ρΙϊΒΡΙΊœΒΘ§Ρ‘»±―ΣΥπ…Υ÷–EAAΒΡ–ΥΖήΕΨ–‘Ής”ΟΩ…ΡήΆ§―θΉ‘”…ΜυΒΡΫιΒΦ”–Ή≈≤ΜΩ…Ζ÷ΗνΒΡΙΊœΒΓΘ
, ΑΌΡ¥“Ϋ“©
≤ΈΩΦΈΡœΉ
1 Barth A, Barth L, Newell D W. Combination therapy of MK801 and ΠΝ phenyltertbutylnitrone enhances protection against ischemic neuronal damage in organotypic hippcampal slice cultures. Exp Neurol, 1996,141(2):330
2 ΒΥ–ΓΟςΘ§÷λ≥œΘ§’≈ΙβωΪ.ΒΞΆΌ“ΚΥα…ώΨ≠ΫΎή’”κ»±―Σ–‘Ρ‘Υπ…Υ(Ήέ ω).ΙζΆβ“Ϋ―ß(Ρ‘―ΣΙήΦ≤≤ΓΖ÷≤α)Θ§1994Θ§2(2)ΘΚ69
3 Pulsinelli W A, Brierley J B. A new model of bilateral the unanesthatized rat hemispheric ischemia. Stroke, 1997,10(2):267
, ΑΌΡ¥“Ϋ“©
4 Χο―«ΨϋΘ§…ρΈΡΟΖ.―Σ«εΉήTBAΖ¥”ΠΈοΓΔLPOΦΑMDA―υΈο÷ ΒΡΝΣΚœ≤βΕ®.ΫβΖ≈Ψϋ“Ϋ―ß«ι±®Θ§1990Θ§(4):322ΓΪ323
5 Traystman R J,Kirsch J R, Koehler R C. oxygen radical mechanisms of brain injury following ischemia and reperfusion. J Appl Physiol, 1991,71(4):1185
6 Thomas W, Furlow J R. Cerebral ischemia produced by four-vessel occlusion in the rat: a quantitative evaluation of cerebral blood flow. J Appl physiol, 1982,13(6):852
’Ηε»’ΤΎΘΚ1999-04-0, ΑΌΡ¥“Ϋ“©