皮肤再生膜的生物相容性系列研究
宁丽 薛淼 黄海宁 孙皎 李亦文 顾国珍 钱云芳 孟爱英 李昌本 赵寿元
摘 要:目的 对医用丝素蛋白皮肤再生膜进行一系列生物学试验和生物相容性研究。方法 将医用丝素蛋白皮肤再生膜材料按国际标准化组织标准要求制备浸提液,进行急性全身毒性试验、皮肤原发刺激试验、细胞毒性试验,以及Ⅰ型胶原、纤维连接蛋白mRNA基因表达等试验。综合分析评价其生物相容性。结果 医用丝素蛋白皮肤再生膜的急性全身毒性试验、皮肤原发刺激试验、细胞毒性试验,以及Ⅰ型胶原、纤维连接蛋白mRNA基因表达等试验,都显示阴性结果。结论 从整体、细胞和分子生物学水平研究提示:医用丝素蛋白皮肤再生膜具有良好的生物相容性。
关键词:皮肤再生膜 基因表达 生物相容性 组织工程
近30年来,国际上医用生物材料和人工器官的研究与生产迅速掘起,为临床医学的发展开辟了新的途径,作为新兴的、边缘性学科而受到关注,获得飞速的发展。如人工心脏瓣膜、人工血管、人工肾、人工肺、人工肝辅助装置、人工关节和骨、人工乳房等整形材料,口腔材料,计划生育材料等已在临床上广泛使用。医用丝素蛋白皮肤再生膜就是我国新近研制的生物材料。对于生物材料用于人体安全性的研究和对其生物学性能的评价在国内外早就引起了重视。自70年代起就加强了对生物材料及其制品的安全性检测方法研究,并建立了有关生物学性能的评价标准。80年代,国际标准化组织(ISO)、国际牙医联盟(FDI)制定了有关材料的生物学性能评价标准。我国根据国情和以上标准制定了适合于我国的具体实施措施。但是这些标准中所有的生物学性能评价标准都只是在整体水平和细胞水平上的评价,尚未深入到分子生物学水平。
, 百拇医药
1 材料与方法
1.1 生物材料试样浸提液制备[1]
已消毒包装的医用丝素蛋白皮肤再生膜,以及其它生物材料试样:用于面部整形的植入性硅橡胶,制作义眼、义齿基托的热凝塑料,人工骨水泥,制取口腔印模的国产硅橡胶和进口口腔印模硅橡胶等材料,在无菌条件下用培养液浸提(试样表面积/浸体介质=3 cm2/ml),37 ℃、120小时,用于培养细胞的试验;用生理盐水浸提,高压(121 ℃)灭菌1小时,用于急性全身毒性试验。阳性对照:0.64%苯酚。阴性对照:生理盐水。
1.2 试剂及试验方法
1.2.1 皮肤原发刺激试验[2] 医用丝素蛋白皮肤再生膜2.5 cm×2.5 cm/块。阴性对照:生理盐水0.5 ml/滤纸块。阳性对照:5%甲醛0.5 ml/滤纸块。试验动物:新西兰大白兔,体重2.0~2.5 kg,雌雄均可,每组3只,背部斑贴区备皮。
, 百拇医药
试验步骤:完整和损伤皮肤各贴一块材料,24小时后去除。去除后1、24、48及72小时观察皮肤反应。皮肤刺激试验反应记分标准见表1[1]。刺激反应总评判定:0分为无刺激;≤1.9分为轻度刺激;2.0~4.9分为中度刺激;5.0~8.0为强刺激。
表1 皮肤刺激试验反应记分标准
Tab. 1 Evaluation criteria of skin irritatant test
记分
Score
红斑反应
Erythema reaction
记分
, 百拇医药
Score
水肿反应
Edema reaction
0
无红斑
No erythema
0
无水肿
No edema
1
极轻微红斑(隐约可见)
Tiny erythema(faintly visible)
, 百拇医药
1
极轻微水肿
Tiny edema
2
边界清晰红斑(淡红色)
Erythema with clear boundary(light red)
2
轻度水肿(可见边缘略高)
Mild edema(higher edge)
3
中毒红斑(红色、界清)
, 百拇医药
Toxic erythema (red, clear boundary)
3
中度水肿(高出1 mm)
Moderate edema(more than 1 mm)
4
严重红斑(紫红色、焦痂形成)
Severe erythema(purplish red, eschar formation)
4
严重水肿(高出1 mm,面积扩出)
Severe edema(more than 1 mm,expansion)
, 百拇医药
1.2.2 急性全身毒性试验 健康小白鼠,体重20 g左右,随机分组,每组5只。记录初始体重。通过小鼠尾静脉分别注射医用丝素蛋白皮肤再生膜浸提液和生理盐水1 ml/只,分别于注射后24、48和72小时称量,观察反应,记录结果。
1.2.3 细胞毒性试验 细胞相对增殖率(relative growth rate,RGR)的检测:医用丝素蛋白皮肤再生膜浸提液(浸提原液100%、50%、25%、10%),L-929细胞在RPMI 1640培养液中贴壁培养。加样后分别于2、4和7天,细胞固定、染色,用分光光度仪588 nm波长测其吸光度值(A),取平均值。计算RGR和细胞毒性分级[3]。结果见表2。 RGR(%)=试样A值-空白A值/阴性A值-空白A值
表2 计算RGR和细胞毒性分级
Tab. 2 RGR evaluation and cytotoxicity stage
, 百拇医药
细胞相对增殖率(%)
Cellular relative growth rate(%)
细胞毒性分级
Cytotoxicity stage
≥100
0
75~99
1
50~74
2
25~49
3
, 百拇医药
1~24
4
<1
5
1.2.4 细胞毒性试验 四唑盐(MTT)比色法[4]:用96板培养L-929细胞,其细胞浓度为5×103/ml,加样同上。分别于24及48小时,经5 mg/ml MTT和酸化异丙醇处理后,用酶联仪(BIO-RAD 450型)在490 nm波长测其吸光度值,取平均值。计算RGR和细胞毒性分析。
1.2.5 抽提细胞总RNA[5] 用7 cm×4 cm培养瓶播种L-929细胞,其细胞浓度为1×104/ml,加入医用丝素蛋白皮肤再生膜浸提液,浓度为浸提原液的10%和阴、阳性对照,每组重复4瓶。加样继续培养48小时后,异硫氰酸胍一步法抽提细胞总RNA。
, http://www.100md.com
1.2.6 细胞Ⅰ型胶原基因表达 采用RNA印迹分子杂交法(Northern Blot)[6]。细胞培养、加样和抽提细胞总RNA方法同上。走RNA电泳,转RNA尼龙膜。抽质粒,酶切,回收Ⅰ型胶原DNA目的片段。用[α-32P]dAPT标记DNA模板,纯化探针,尼龙膜在杂交炉中42 ℃预杂交4小时,加入Ⅰ型胶原cDNA探针,杂交20小时,放射自显影1周见结果。
1.2.7 细胞纤维连接蛋白mRNA基因表达 采用PCR法+RNA印迹分子杂交法(Northern Blot)。细胞培养、加样和抽提细胞总RNA方法同上。走RNA电泳,转RNA尼龙膜。查找鼠细胞纤维连接蛋白的DNA序列,设计合成引物:①5′-GTGCTATGACGATGGGAAGACC-3′;②5′-ATCTAG-CGGCATGAAGCACT-3′。
以L-929细胞的RNA经反转录(Promage试剂盒)得到cDNA模板,Taq酶+纤维连接蛋白的引物+PCR试剂+[α-32P]dAPT,用PCR仪(PTC-100TM)经94 ℃60秒,60 ℃45秒,72 ℃45秒,35个循环,PCR扩增DNA标记探针[7]。纯化探针,尼龙膜在杂交炉中42 ℃预杂交4小时,加入纤维连接蛋白cDNA探针,杂交20小时,放射自显影1周见结果。
, 百拇医药
2 结果
2.1 医用丝素蛋白皮肤再生膜的急性全身毒性试验
医用丝素蛋白皮肤再生膜浸提液注射后24、48及72小时,小鼠体重均呈增长趋势,未发现死亡和中毒反应,与阴性对照无差别。表明该材料在急性全身毒性试验中均呈阴性反应。
2.2 皮肤原发刺激试验
医用丝素蛋白皮肤再生膜材料对皮肤无刺激性。结果见表3。
表3 皮肤再生膜的皮肤原发刺激试验结果
Tab. 3 Primary skin irrtant test of skin reproductive
组别
, 百拇医药
Groups
破损皮肤刺激反应记分
Score of irritant reaction
in defected skin
完整皮肤刺激反应记分
Score of irritant reaction
in normal skin
1 h
24 h
48 h
1 h
, 百拇医药
24 h
48 h
72 h
红斑
Erythema
水肿
Edema
红斑
Erythema
水肿
Edema
红斑
Erythema
, 百拇医药
水肿
Edema
红斑
Erythema
水肿
Edema
红斑
Erythema
水肿
Edema
红斑
Erythema
水肿
, 百拇医药
Edema
红斑
Erythema
水肿
Edema
实验组
Experimen-
tal
group
0
0
0
0
, http://www.100md.com
0
0
0
0
0
0
0
0
0
0
阴性对照组
Negative
control
group
, http://www.100md.com
0
0
0
0
0
0
0
0
0
0
0
0
0
0
, http://www.100md.com
阳性对照组
Positive
control
group
2
1
3
1
1
0
2
0
1
, 百拇医药 0
0
0
0
0
2.3 细胞相对增殖度法试验和MTT比色法试验
按ISO/TC194文件规定,细胞毒性0~1级为合格。细胞相对增殖度法试验和MTT比色法试验的结果见表4、表5。表4 皮肤再生膜细胞毒性试验结果
Tab. 4 Cytotoxicity test of skin reproductive membrane
时间(天)
Time(days)
, http://www.100md.com
组别
Groups
吸光度值
Value of
absorption
细胞增殖率(%)
Cellular
proliferative
rate(%)
细胞毒性分级
Cytotoxicity
stage
, 百拇医药
2
实验组
Experimental group
0.918
0.905
1.275
1.235
1.261
1.281
118
0
对照组
Control group
, 百拇医药
0.868
0.943
0.778
1.033
1.153
1.041
4
实验组
Experimental group
0.970
1.129
1.047
0.892
, 百拇医药
0.806
0.854
86
1
对照组
Control group
1.052
1.085
1.196
1.200
1.332
1.100
7
, http://www.100md.com
实验组
Experimental group
1.327
1.576
1.160
1.186
1.090
1.259
88
1
对照组
Control group
, http://www.100md.com 1.487
1.459
1.269
1.380
1.543
1.455
表5 皮肤再生膜细胞毒性试验结果
Tab. 5 Cytotoxicity test of skin reproductive membrane
浸提浓度
Extract
concentration
, 百拇医药
吸光度值
Value of absorption
细胞增殖率(%)
Cellular
proliferative
rate(%)
细胞毒性分级
Cytotoxicity stage
(-)
0.890
0.825
0.848
, 百拇医药
100.0
0
1%
0.767
1.298
0.683
107.0
0
10%
0.833
0.734
0.692
88.2
, http://www.100md.com
1
25%
0.715
0.717
0.679
82.3
1
50%
0.663
0.645
0.685
77.7
1
, 百拇医药
100%
0.667
0.660
0.674
77.1
1
(+)
0.391
0.322
0.351
41.5
3
2.4 细胞Ⅰ型胶原和纤维连接蛋白mRNA基因表达
, 百拇医药
医用丝素蛋白皮肤再生膜不影响细胞Ⅰ型胶原及纤维连接蛋白mRNA的基因表达。与阴性对照试验结果相似,见附图。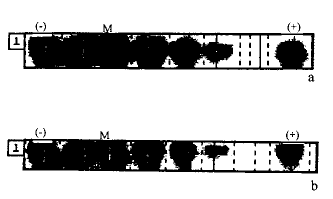
附图 医用丝素蛋白皮肤再生膜(M)的10%浸提原液和阴性、阳性对照液与L-929细胞共同培养48小时后,细胞Ⅰ型胶原(a)
和纤维连接蛋白(b)基因表达结果(原倍数)
Fig. Gene expression of type Ⅰ collagen
(a) and fibronectin (b) after 48 hours of
combined culture of 10% extract solution
, http://www.100md.com
of skin reproductive membrane, negative
and positive control solution with L-929 cells(orginal size)
3 讨论
在国家自然科学基金委召开的“面向21世纪新材料的科学问题交叉领域研讨会”中指出,21世纪材料科学的发展趋势是:“生物材料成为材料科学的重要领域,并将为人工器官和人体替代材料提供物质基础”。因此,国家优先资助遴选的领域包括:“生物材料生物相容性分子设计基础理论和方法的研究,其表征和评价方法的研究。重视评价标准统一化、规范化”。为了使生物材料能健康蓬勃地迅速发展,必须要坚持“两条腿走路”的方针,一方面支持鼓励生物材料的研制开发和生产,另一方面要重视生物材料的安全性评价方法和标准化的研究,使生物材料安全有效地应用于医学临床。生物材料与其他新兴的学科和工业发展的初始阶段一样,也出现了在早期的“管理无归口、质量无标准”的较混乱局面。60年代初期,人们对生物和人工器官应用在体内所产生的生物反应认识不足,对所用的生物材料也未进行严格的筛选和安全有效的评价,因而在临床的实际应用中出现了一些医疗事故。例如,近十年来经研究发现人工乳房的硅凝胶扩散和渗透到组织中与乳房癌的发生有密切的相关关系。因此,1992年美国食品药品管理署(FDA)决定停止使用含硅凝胶的人工乳房。而我国仍在使用这类产品。我国在1995年对一次性输液器全面检测发现其合格率仅为50%左右。还有某些人工髋关节的材料碎屑引起植入失败。有些室温硫化硅橡胶的催化剂具有一定的细胞毒性。如何把握生物材料的质量,保证其对人体的安全性问题越来越受到各国政府和有关学术界的重视。
, http://www.100md.com
在美国FDA和欧洲联盟(EU)的有关生物材料和医疗器械的管理立法中,将1 800多种生物材料和医疗装置根据其对人体潜在的危险程度不同分为三类,进行不同层次的管理(Ⅰ类材料:一般性管理,Ⅱ类材料:实施标准性管理,Ⅲ类材料:售前批准管理)。施行的分类标准涉及到这些生物材料和器械是否与人体相接触或相互反应,是否通过人的体腔或以手术方式进入人体,使用的时间长短,接触部位是否与重要器官如心脏、循环系统、脑组织或肝脏等相接触,是否可被能量激活等。由于有些生物材料要与人体血液、粘膜、骨骼、肌肉等组织接触,因此,对生物材料要做一系列的生物学安全性试验,以确保生物材料安全合理地用于人体。
90年代该领域的学者们提出了分子生物相容性的概念[8]。当前,对临床上广泛应用的生物材料开展分子水平生物相容性研究,特别是系统地开展整体、细胞和分子生物学试验的相关性研究,是该领域前沿研究内容和首要任务。生物材料特别是植入人体软组织的材料,会与成纤维细胞直接接触,植入人体硬组织的材料,会与成骨细胞直接接触。经研究已证明,成骨细胞可合成与骨形成相关的骨钙蛋白(osteocalcin)、骨粘连蛋白(osteonectin)和骨桥蛋白(osteopontin),以及大量的Ⅰ型胶原蛋白。成纤维细胞可合成作用于细胞增殖的组蛋白(histone),作用于细胞粘着的纤维连接蛋白,作用于细胞构架的肌动蛋白(actin)和波形蛋白(vimentin),以及大量与细胞外基质有关的Ⅰ型和Ⅲ型胶原[9]。遗传物质的主要活性是能够指导蛋白质的合成,但它必须基于RNA和DNA,特别是mRNA作为模板才能起作用。通过对基因表达的观察,可提示生物材料在分子水平上是否干扰和影响遗传物质的转译。mRNA占细胞内总RNA的1%~5%,若生物材料对细胞的增殖分化已在整体水平和细胞水平产生影响,可能在分子水平的基因表达方面也会造成影响,并且会极灵敏地反映出来。近几年的前瞻性研究已证实了这一点[10]。为了确保医用生物材料特别是植入体内的材料和组织工程材料的安全性,还需要进行较全面地观察和深入地研究。
, 百拇医药
我们的研究是对医用丝素蛋白皮肤再生膜进行急性全身毒性试验、皮肤原发刺激试验、细胞毒性试验,以及Ⅰ型胶原纤维连接蛋白mRNA基因表达等试验。综合分析评价其生物相容性。结果提示:医用丝素蛋白皮肤再生膜具有良好的生物相容性。我们的研究结果将为我国高新技术新材料领域的医用生物材料研究提供生物相容性试验数据、理论基础和临床应用依据。■
基金项目:国家八六三计划新材料领域基金资助(863-715-002-022)
作者单位:宁丽(上海第二医科大学生物材料研究测试中心(上海,200023))
薛淼(上海第二医科大学生物材料研究测试中心(上海,200023))
黄海宁(上海第二医科大学生物材料研究测试中心(上海,200023))
孙皎(上海第二医科大学生物材料研究测试中心(上海,200023))
, http://www.100md.com
李亦文(上海第二医科大学生物材料研究测试中心(上海,200023))
顾国珍(上海第二医科大学生物材料研究测试中心(上海,200023))
钱云芳(上海第二医科大学生物材料研究测试中心(上海,200023))
孟爱英(上海第二医科大学生物材料研究测试中心(上海,200023))
李昌本(复旦大学遗传研究所遗传工程国家重点实验室)
赵寿元(复旦大学遗传研究所遗传工程国家重点实验室)
参考文献:
[1]中国GB/16886.1-1997.生物材料和医疗器材生物学评价技术要求.1997:1~30
, http://www.100md.com
[2]中国对卫生部标准.WS 5-1-87医用热硫化甲基乙烯基硅橡胶.1987:1~15
[3]张彩霞.应用细胞培养法对复合树脂充填材料的毒性研究.口腔医学,1982;2(1):40
[4]吕晓迎,Kappert HF.牙科材料细胞毒性评定的新方法(MTT试验).中华口腔医学杂志,1995;30(6):377
[5]J.萨姆布鲁克.分子克隆实验指南.第三版.北京:科学出版社,1996:96~98
[6]陈诗书,汤雪明.医学细胞与分子生物学.上海:上海医科大学出版社,1995:2~4
[7]Sambrook J.Molecular Cloning.第三版.北京:科学出版社,1996:6~8
, 百拇医药
[8]Chou L.Molecular Biocompatibility. J Dent Res, 1995;74:190
[9]Mostafa Raif EL.Molecular interface characterization on human bone matrix. Biomaterials,1993;14(13):978
[10]Veron MH.Selective inhibition of collagen synthesis by fluoride in human pulp fibroblast in vitro. Calcified Tissue, 1993;53:38, 百拇医药
摘 要:目的 对医用丝素蛋白皮肤再生膜进行一系列生物学试验和生物相容性研究。方法 将医用丝素蛋白皮肤再生膜材料按国际标准化组织标准要求制备浸提液,进行急性全身毒性试验、皮肤原发刺激试验、细胞毒性试验,以及Ⅰ型胶原、纤维连接蛋白mRNA基因表达等试验。综合分析评价其生物相容性。结果 医用丝素蛋白皮肤再生膜的急性全身毒性试验、皮肤原发刺激试验、细胞毒性试验,以及Ⅰ型胶原、纤维连接蛋白mRNA基因表达等试验,都显示阴性结果。结论 从整体、细胞和分子生物学水平研究提示:医用丝素蛋白皮肤再生膜具有良好的生物相容性。
关键词:皮肤再生膜 基因表达 生物相容性 组织工程
近30年来,国际上医用生物材料和人工器官的研究与生产迅速掘起,为临床医学的发展开辟了新的途径,作为新兴的、边缘性学科而受到关注,获得飞速的发展。如人工心脏瓣膜、人工血管、人工肾、人工肺、人工肝辅助装置、人工关节和骨、人工乳房等整形材料,口腔材料,计划生育材料等已在临床上广泛使用。医用丝素蛋白皮肤再生膜就是我国新近研制的生物材料。对于生物材料用于人体安全性的研究和对其生物学性能的评价在国内外早就引起了重视。自70年代起就加强了对生物材料及其制品的安全性检测方法研究,并建立了有关生物学性能的评价标准。80年代,国际标准化组织(ISO)、国际牙医联盟(FDI)制定了有关材料的生物学性能评价标准。我国根据国情和以上标准制定了适合于我国的具体实施措施。但是这些标准中所有的生物学性能评价标准都只是在整体水平和细胞水平上的评价,尚未深入到分子生物学水平。
, 百拇医药
1 材料与方法
1.1 生物材料试样浸提液制备[1]
已消毒包装的医用丝素蛋白皮肤再生膜,以及其它生物材料试样:用于面部整形的植入性硅橡胶,制作义眼、义齿基托的热凝塑料,人工骨水泥,制取口腔印模的国产硅橡胶和进口口腔印模硅橡胶等材料,在无菌条件下用培养液浸提(试样表面积/浸体介质=3 cm2/ml),37 ℃、120小时,用于培养细胞的试验;用生理盐水浸提,高压(121 ℃)灭菌1小时,用于急性全身毒性试验。阳性对照:0.64%苯酚。阴性对照:生理盐水。
1.2 试剂及试验方法
1.2.1 皮肤原发刺激试验[2] 医用丝素蛋白皮肤再生膜2.5 cm×2.5 cm/块。阴性对照:生理盐水0.5 ml/滤纸块。阳性对照:5%甲醛0.5 ml/滤纸块。试验动物:新西兰大白兔,体重2.0~2.5 kg,雌雄均可,每组3只,背部斑贴区备皮。
, 百拇医药
试验步骤:完整和损伤皮肤各贴一块材料,24小时后去除。去除后1、24、48及72小时观察皮肤反应。皮肤刺激试验反应记分标准见表1[1]。刺激反应总评判定:0分为无刺激;≤1.9分为轻度刺激;2.0~4.9分为中度刺激;5.0~8.0为强刺激。
表1 皮肤刺激试验反应记分标准
Tab. 1 Evaluation criteria of skin irritatant test
记分
Score
红斑反应
Erythema reaction
记分
, 百拇医药
Score
水肿反应
Edema reaction
0
无红斑
No erythema
0
无水肿
No edema
1
极轻微红斑(隐约可见)
Tiny erythema(faintly visible)
, 百拇医药
1
极轻微水肿
Tiny edema
2
边界清晰红斑(淡红色)
Erythema with clear boundary(light red)
2
轻度水肿(可见边缘略高)
Mild edema(higher edge)
3
中毒红斑(红色、界清)
, 百拇医药
Toxic erythema (red, clear boundary)
3
中度水肿(高出1 mm)
Moderate edema(more than 1 mm)
4
严重红斑(紫红色、焦痂形成)
Severe erythema(purplish red, eschar formation)
4
严重水肿(高出1 mm,面积扩出)
Severe edema(more than 1 mm,expansion)
, 百拇医药
1.2.2 急性全身毒性试验 健康小白鼠,体重20 g左右,随机分组,每组5只。记录初始体重。通过小鼠尾静脉分别注射医用丝素蛋白皮肤再生膜浸提液和生理盐水1 ml/只,分别于注射后24、48和72小时称量,观察反应,记录结果。
1.2.3 细胞毒性试验 细胞相对增殖率(relative growth rate,RGR)的检测:医用丝素蛋白皮肤再生膜浸提液(浸提原液100%、50%、25%、10%),L-929细胞在RPMI 1640培养液中贴壁培养。加样后分别于2、4和7天,细胞固定、染色,用分光光度仪588 nm波长测其吸光度值(A),取平均值。计算RGR和细胞毒性分级[3]。结果见表2。 RGR(%)=试样A值-空白A值/阴性A值-空白A值
表2 计算RGR和细胞毒性分级
Tab. 2 RGR evaluation and cytotoxicity stage
, 百拇医药
细胞相对增殖率(%)
Cellular relative growth rate(%)
细胞毒性分级
Cytotoxicity stage
≥100
0
75~99
1
50~74
2
25~49
3
, 百拇医药
1~24
4
<1
5
1.2.4 细胞毒性试验 四唑盐(MTT)比色法[4]:用96板培养L-929细胞,其细胞浓度为5×103/ml,加样同上。分别于24及48小时,经5 mg/ml MTT和酸化异丙醇处理后,用酶联仪(BIO-RAD 450型)在490 nm波长测其吸光度值,取平均值。计算RGR和细胞毒性分析。
1.2.5 抽提细胞总RNA[5] 用7 cm×4 cm培养瓶播种L-929细胞,其细胞浓度为1×104/ml,加入医用丝素蛋白皮肤再生膜浸提液,浓度为浸提原液的10%和阴、阳性对照,每组重复4瓶。加样继续培养48小时后,异硫氰酸胍一步法抽提细胞总RNA。
, http://www.100md.com
1.2.6 细胞Ⅰ型胶原基因表达 采用RNA印迹分子杂交法(Northern Blot)[6]。细胞培养、加样和抽提细胞总RNA方法同上。走RNA电泳,转RNA尼龙膜。抽质粒,酶切,回收Ⅰ型胶原DNA目的片段。用[α-32P]dAPT标记DNA模板,纯化探针,尼龙膜在杂交炉中42 ℃预杂交4小时,加入Ⅰ型胶原cDNA探针,杂交20小时,放射自显影1周见结果。
1.2.7 细胞纤维连接蛋白mRNA基因表达 采用PCR法+RNA印迹分子杂交法(Northern Blot)。细胞培养、加样和抽提细胞总RNA方法同上。走RNA电泳,转RNA尼龙膜。查找鼠细胞纤维连接蛋白的DNA序列,设计合成引物:①5′-GTGCTATGACGATGGGAAGACC-3′;②5′-ATCTAG-CGGCATGAAGCACT-3′。
以L-929细胞的RNA经反转录(Promage试剂盒)得到cDNA模板,Taq酶+纤维连接蛋白的引物+PCR试剂+[α-32P]dAPT,用PCR仪(PTC-100TM)经94 ℃60秒,60 ℃45秒,72 ℃45秒,35个循环,PCR扩增DNA标记探针[7]。纯化探针,尼龙膜在杂交炉中42 ℃预杂交4小时,加入纤维连接蛋白cDNA探针,杂交20小时,放射自显影1周见结果。
, 百拇医药
2 结果
2.1 医用丝素蛋白皮肤再生膜的急性全身毒性试验
医用丝素蛋白皮肤再生膜浸提液注射后24、48及72小时,小鼠体重均呈增长趋势,未发现死亡和中毒反应,与阴性对照无差别。表明该材料在急性全身毒性试验中均呈阴性反应。
2.2 皮肤原发刺激试验
医用丝素蛋白皮肤再生膜材料对皮肤无刺激性。结果见表3。
表3 皮肤再生膜的皮肤原发刺激试验结果
Tab. 3 Primary skin irrtant test of skin reproductive
组别
, 百拇医药
Groups
破损皮肤刺激反应记分
Score of irritant reaction
in defected skin
完整皮肤刺激反应记分
Score of irritant reaction
in normal skin
1 h
24 h
48 h
1 h
, 百拇医药
24 h
48 h
72 h
红斑
Erythema
水肿
Edema
红斑
Erythema
水肿
Edema
红斑
Erythema
, 百拇医药
水肿
Edema
红斑
Erythema
水肿
Edema
红斑
Erythema
水肿
Edema
红斑
Erythema
水肿
, 百拇医药
Edema
红斑
Erythema
水肿
Edema
实验组
Experimen-
tal
group
0
0
0
0
, http://www.100md.com
0
0
0
0
0
0
0
0
0
0
阴性对照组
Negative
control
group
, http://www.100md.com
0
0
0
0
0
0
0
0
0
0
0
0
0
0
, http://www.100md.com
阳性对照组
Positive
control
group
2
1
3
1
1
0
2
0
1
, 百拇医药 0
0
0
0
0
2.3 细胞相对增殖度法试验和MTT比色法试验
按ISO/TC194文件规定,细胞毒性0~1级为合格。细胞相对增殖度法试验和MTT比色法试验的结果见表4、表5。表4 皮肤再生膜细胞毒性试验结果
Tab. 4 Cytotoxicity test of skin reproductive membrane
时间(天)
Time(days)
, http://www.100md.com
组别
Groups
吸光度值
Value of
absorption
细胞增殖率(%)
Cellular
proliferative
rate(%)
细胞毒性分级
Cytotoxicity
stage
, 百拇医药
2
实验组
Experimental group
0.918
0.905
1.275
1.235
1.261
1.281
118
0
对照组
Control group
, 百拇医药
0.868
0.943
0.778
1.033
1.153
1.041
4
实验组
Experimental group
0.970
1.129
1.047
0.892
, 百拇医药
0.806
0.854
86
1
对照组
Control group
1.052
1.085
1.196
1.200
1.332
1.100
7
, http://www.100md.com
实验组
Experimental group
1.327
1.576
1.160
1.186
1.090
1.259
88
1
对照组
Control group
, http://www.100md.com 1.487
1.459
1.269
1.380
1.543
1.455
表5 皮肤再生膜细胞毒性试验结果
Tab. 5 Cytotoxicity test of skin reproductive membrane
浸提浓度
Extract
concentration
, 百拇医药
吸光度值
Value of absorption
细胞增殖率(%)
Cellular
proliferative
rate(%)
细胞毒性分级
Cytotoxicity stage
(-)
0.890
0.825
0.848
, 百拇医药
100.0
0
1%
0.767
1.298
0.683
107.0
0
10%
0.833
0.734
0.692
88.2
, http://www.100md.com
1
25%
0.715
0.717
0.679
82.3
1
50%
0.663
0.645
0.685
77.7
1
, 百拇医药
100%
0.667
0.660
0.674
77.1
1
(+)
0.391
0.322
0.351
41.5
3
2.4 细胞Ⅰ型胶原和纤维连接蛋白mRNA基因表达
, 百拇医药
医用丝素蛋白皮肤再生膜不影响细胞Ⅰ型胶原及纤维连接蛋白mRNA的基因表达。与阴性对照试验结果相似,见附图。

附图 医用丝素蛋白皮肤再生膜(M)的10%浸提原液和阴性、阳性对照液与L-929细胞共同培养48小时后,细胞Ⅰ型胶原(a)
和纤维连接蛋白(b)基因表达结果(原倍数)
Fig. Gene expression of type Ⅰ collagen
(a) and fibronectin (b) after 48 hours of
combined culture of 10% extract solution
, http://www.100md.com
of skin reproductive membrane, negative
and positive control solution with L-929 cells(orginal size)
3 讨论
在国家自然科学基金委召开的“面向21世纪新材料的科学问题交叉领域研讨会”中指出,21世纪材料科学的发展趋势是:“生物材料成为材料科学的重要领域,并将为人工器官和人体替代材料提供物质基础”。因此,国家优先资助遴选的领域包括:“生物材料生物相容性分子设计基础理论和方法的研究,其表征和评价方法的研究。重视评价标准统一化、规范化”。为了使生物材料能健康蓬勃地迅速发展,必须要坚持“两条腿走路”的方针,一方面支持鼓励生物材料的研制开发和生产,另一方面要重视生物材料的安全性评价方法和标准化的研究,使生物材料安全有效地应用于医学临床。生物材料与其他新兴的学科和工业发展的初始阶段一样,也出现了在早期的“管理无归口、质量无标准”的较混乱局面。60年代初期,人们对生物和人工器官应用在体内所产生的生物反应认识不足,对所用的生物材料也未进行严格的筛选和安全有效的评价,因而在临床的实际应用中出现了一些医疗事故。例如,近十年来经研究发现人工乳房的硅凝胶扩散和渗透到组织中与乳房癌的发生有密切的相关关系。因此,1992年美国食品药品管理署(FDA)决定停止使用含硅凝胶的人工乳房。而我国仍在使用这类产品。我国在1995年对一次性输液器全面检测发现其合格率仅为50%左右。还有某些人工髋关节的材料碎屑引起植入失败。有些室温硫化硅橡胶的催化剂具有一定的细胞毒性。如何把握生物材料的质量,保证其对人体的安全性问题越来越受到各国政府和有关学术界的重视。
, http://www.100md.com
在美国FDA和欧洲联盟(EU)的有关生物材料和医疗器械的管理立法中,将1 800多种生物材料和医疗装置根据其对人体潜在的危险程度不同分为三类,进行不同层次的管理(Ⅰ类材料:一般性管理,Ⅱ类材料:实施标准性管理,Ⅲ类材料:售前批准管理)。施行的分类标准涉及到这些生物材料和器械是否与人体相接触或相互反应,是否通过人的体腔或以手术方式进入人体,使用的时间长短,接触部位是否与重要器官如心脏、循环系统、脑组织或肝脏等相接触,是否可被能量激活等。由于有些生物材料要与人体血液、粘膜、骨骼、肌肉等组织接触,因此,对生物材料要做一系列的生物学安全性试验,以确保生物材料安全合理地用于人体。
90年代该领域的学者们提出了分子生物相容性的概念[8]。当前,对临床上广泛应用的生物材料开展分子水平生物相容性研究,特别是系统地开展整体、细胞和分子生物学试验的相关性研究,是该领域前沿研究内容和首要任务。生物材料特别是植入人体软组织的材料,会与成纤维细胞直接接触,植入人体硬组织的材料,会与成骨细胞直接接触。经研究已证明,成骨细胞可合成与骨形成相关的骨钙蛋白(osteocalcin)、骨粘连蛋白(osteonectin)和骨桥蛋白(osteopontin),以及大量的Ⅰ型胶原蛋白。成纤维细胞可合成作用于细胞增殖的组蛋白(histone),作用于细胞粘着的纤维连接蛋白,作用于细胞构架的肌动蛋白(actin)和波形蛋白(vimentin),以及大量与细胞外基质有关的Ⅰ型和Ⅲ型胶原[9]。遗传物质的主要活性是能够指导蛋白质的合成,但它必须基于RNA和DNA,特别是mRNA作为模板才能起作用。通过对基因表达的观察,可提示生物材料在分子水平上是否干扰和影响遗传物质的转译。mRNA占细胞内总RNA的1%~5%,若生物材料对细胞的增殖分化已在整体水平和细胞水平产生影响,可能在分子水平的基因表达方面也会造成影响,并且会极灵敏地反映出来。近几年的前瞻性研究已证实了这一点[10]。为了确保医用生物材料特别是植入体内的材料和组织工程材料的安全性,还需要进行较全面地观察和深入地研究。
, 百拇医药
我们的研究是对医用丝素蛋白皮肤再生膜进行急性全身毒性试验、皮肤原发刺激试验、细胞毒性试验,以及Ⅰ型胶原纤维连接蛋白mRNA基因表达等试验。综合分析评价其生物相容性。结果提示:医用丝素蛋白皮肤再生膜具有良好的生物相容性。我们的研究结果将为我国高新技术新材料领域的医用生物材料研究提供生物相容性试验数据、理论基础和临床应用依据。■
基金项目:国家八六三计划新材料领域基金资助(863-715-002-022)
作者单位:宁丽(上海第二医科大学生物材料研究测试中心(上海,200023))
薛淼(上海第二医科大学生物材料研究测试中心(上海,200023))
黄海宁(上海第二医科大学生物材料研究测试中心(上海,200023))
孙皎(上海第二医科大学生物材料研究测试中心(上海,200023))
, http://www.100md.com
李亦文(上海第二医科大学生物材料研究测试中心(上海,200023))
顾国珍(上海第二医科大学生物材料研究测试中心(上海,200023))
钱云芳(上海第二医科大学生物材料研究测试中心(上海,200023))
孟爱英(上海第二医科大学生物材料研究测试中心(上海,200023))
李昌本(复旦大学遗传研究所遗传工程国家重点实验室)
赵寿元(复旦大学遗传研究所遗传工程国家重点实验室)
参考文献:
[1]中国GB/16886.1-1997.生物材料和医疗器材生物学评价技术要求.1997:1~30
, http://www.100md.com
[2]中国对卫生部标准.WS 5-1-87医用热硫化甲基乙烯基硅橡胶.1987:1~15
[3]张彩霞.应用细胞培养法对复合树脂充填材料的毒性研究.口腔医学,1982;2(1):40
[4]吕晓迎,Kappert HF.牙科材料细胞毒性评定的新方法(MTT试验).中华口腔医学杂志,1995;30(6):377
[5]J.萨姆布鲁克.分子克隆实验指南.第三版.北京:科学出版社,1996:96~98
[6]陈诗书,汤雪明.医学细胞与分子生物学.上海:上海医科大学出版社,1995:2~4
[7]Sambrook J.Molecular Cloning.第三版.北京:科学出版社,1996:6~8
, 百拇医药
[8]Chou L.Molecular Biocompatibility. J Dent Res, 1995;74:190
[9]Mostafa Raif EL.Molecular interface characterization on human bone matrix. Biomaterials,1993;14(13):978
[10]Veron MH.Selective inhibition of collagen synthesis by fluoride in human pulp fibroblast in vitro. Calcified Tissue, 1993;53:38, 百拇医药