银屑病皮损内酪氨酸蛋白激酶活性的初步研究
银屑病皮损内酪氨酸蛋白激酶活性的初步研究
吕根法 李文维 伍津津
摘要 目的:探讨酪氨酸蛋白激酶(TPK)在银屑病表皮异常增生中的作用。方法:通过外源性底物磷酸化的方法,测定银屑病进行期皮损角质形成细胞的TPK活性。结果:①银屑病进行期皮损角质形成细胞基础TPK活性显著增高,且对于转化生长因子-α的刺激,反应性明显增强;②增高的基础TPK活性与角质形成细胞膜表皮生长因子受体的表达量呈明显正相关;同时银屑病角质形成细胞表皮生长因子受体的自磷酸化水平亦显著增高。结论:TPK活性增高,以及对有丝分裂信号刺激的反应增强,可能在表皮的增生中起到重要作用,TPK活性的改变可能主要是由于表皮生长因子受体的表达异常所致,表皮生长因子受体可能在银屑病表皮的异常增生中发挥着重要作用。
, http://www.100md.com
关键词:银屑病 蛋白质酪氨酸激酶 受体,表皮生长因子-尿抑胃素 转化生长因子α
银屑病是一种常见的炎性增生性皮肤病,其病因、发病机制目前尚不清楚。角质形成细胞(KC)的增生、分化与细胞表面表皮生长因子受体(EGFR)的表达具有明显的关系[1]。EGFR的相对分子质量为170000的单链多肽,胞内区具有特异的酪氨酸蛋白激酶(TPK)活性,TPK激活是EGFR生物学功能发挥的关键步骤,且是细胞生长所必需的。本实验通过对皮损KC的TPK活性的研究,以探讨TPK在银屑病表皮增生中的作用。
材料和方法
一、材料
(一)标本来源:寻常型进行期银屑病患者22例,年龄16~58岁,平均28.4岁,男13例,女9例;正常对照组16例,男9例,女7例。年龄17~45岁,平均25.7岁,皮损标本取自2周内未内服及外用过任何药物的斑块性损害,银屑病组和正常对照组年龄、性别差异无显著性。皮肤取材厚度:银屑病组约0.4~0.6cm,正常人对照组约0.3~0.5cm。标本迅速用冰冷PBS冲洗3次除去血污,立即放入液氮瓶内。
, 百拇医药
(二)主要试剂:多聚谷酪氨酸(PolyGlu∶Tyr)(4∶1),Sigma公司;转化生长因子-α(TGF-α),Promega公司;[γ-32P]-ATP(>5000Ci/mmol),北京亚辉公司。
二、方法
(一)KC膜制备:冷冻保存的皮肤组织剪碎后于50mmol/LTris-HCl,pH7.4,1.0mmol/LPMSF混合液内(0.5mL/100mg组织),冰水浴内匀浆破膜,1000g离心5min,上清液再置低温超高速离心机100000g、4℃离心60min,分装放入-70℃冰箱内贮存,2个月内测定TPK活性。
(二)皮肤标本TPK活性的测定:
1.外源性底物磷酸化TPK活性的测定[2]:混合反应体系含终浓度为:10mmol/LHepers,pH7.4,10mmol/LMgCl2,1mmol/L正矾酸钠,0.1%TritonX100,PolyGlu∶Tyr(4∶1)1mg/mL,膜蛋白50μg。反应以加入[γ-32P]-ATP(0.5μCi/管)起动,37℃水浴反应5min;10μL0.5mol/LEDTA,pH8.0,终止反应。取40μL反应液点样于0.22μm微孔滤膜,以10%三氯醋酸负压抽滤,LKB-1275型液体闪烁机计数。TPK活性以每毫克膜蛋白每分钟催化32P转入到PolyGlu∶Tyr(4∶1)的fmol数减去自磷酸化的受体TPK活性值来表示。
, 百拇医药
2.TGF-α对EGFRTPK活性的影响:反应体系和实验方法基本同外源性底物磷酸化;分别加入不同浓度的TGF-α(0、101、102、103ng/mL)。在22℃水浴中保温30min。刺激后TPK活性以每毫克膜蛋白每分钟催化32P转入到PolyGlu∶Tyr(4∶1)的fmol数减去基础状态下的TPK活性值来表示。
(三)表皮生长因子受体自身磷酸化分析[3]:反应体系含终浓度为0.1%TritonX100,2mmol/LMgCl2,10μmol/L正矾酸钠,0.25mg/mL牛血清白蛋白,20mmol/LHepers,pH7.4,1μCi[γ-32P]-ATP,TGF-α10ng/mL;反应以加入100mg膜蛋白起动,4℃反应10min。10%的SDS-PAGE,干胶,-70℃的冰箱曝光72h作放射性自显影。
(四)采用ABC法染色分析表皮生长因子受体的分布:阳性染色显示KC膜上出现黄色颗粒。用半定量计分,染色强度用0~3级计分:0为无染色,1为轻度染色;2为中度染色;3为强度染色。染色范围采用表皮细胞阳性染色的百分数分0~4级;无染色为0;25%为1;25%~50%为2;50%~75%为3;>75%为4。染色总评分为染色强度+染色范围。
, 百拇医药
表1 表皮生长因子受体在银屑病皮损和正常人皮肤的表达(x±s)
组 别
例数
基底层
棘 层
颗粒层+角质层
银屑病
11
4.41±1.25
5.33±0.75
4.08±1.13
正常人
, 百拇医药
8
5.06±1.48
2.85±0.64
0.60±0.96
t值*
1.42
12.43*
12.82*
P值
>0.05
<0.01
<0.01
, 百拇医药
*与正常对照组比较表2 不同浓度转化生长因子α与表皮生长因子刺激后角质形成细胞酪氨酸蛋白激酶活性(fmol.min-1.mg-1)
组 别
基 础
转化生长因子α浓度(ng/mL)
表皮生长因子(ng/mL)
101
102
103
101
, 百拇医药
102
103
正常人对照
1.84±0.42
2.27±0.54
2.95±1.42
2.97±1.13
2.25±0.96
2.72±1.67
2.87±0.78
银屑病
3.04±1.61
, 百拇医药
3.83±1.35
5.05±1.07
4.96±1.32
4.21±1.07
5.12±1.39
5.18±1.45
t值
2.23
3.32
4.04
4.05
3.43
, http://www.100md.com
4.17
4.15
P值
<0.05
<0.05
<0.01
<0.01
<0.05
<0.01
<0.01
结果
一、免疫组化
, 百拇医药 正常皮肤EGFR阳性染色主要位于基底层的细胞膜上,银屑病皮损阳性染色可见于表皮的全层细胞膜上。基底层的细胞膜染色较正常对照组弱,但增厚的棘层细胞膜染色明显增强,角质层的细胞膜上亦可见阳性染色;自棘细胞层以上细胞膜阳性染色显著高于正常人对照组。约为正常人组的5~6倍。
二、表皮生长
因子受体自身磷酸化的改变通过放射性自显影的方法,观察到银屑病和正常人对照组EGFR的自磷酸化存在明显差异,见图1。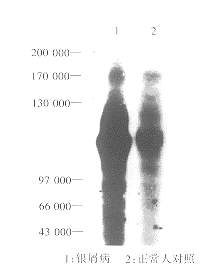
图1 银屑病和正常人角质形成细胞膜表皮生长因子受体170000放射性自显影
三、KC基础TPK活性和TGF-α刺激后TPK活性的变化
, 百拇医药
在无外源性刺激时,TPK活性在正常人对照组为(1.36±0.55)fmol.min-1.mg-1;银屑病组为(3.01±1.05)fmol.min-1.mg-1,两组比较差异有显著性,基础TPK活性与细胞膜EGFR的表达量之间具有显著相关性(r=0.65,P<0.01,n=24)。不同浓度TGF-α刺激后,KC膜的TPK活性呈剂量依赖性增高,但银屑病组的反应明显高于正常人对照组(表2)。测定不同浓度(101、102、103ng/mL)EGF刺激下KC的TPK活性(见表2),结果说明,在激活KC的EGFR的TPK活性方面,EGF和TGF-α是等效的。
讨论
, http://www.100md.com
EGFR数量的变化及功能异常是KC过度增殖及异常分化的重要原因。银屑病基底层细胞膜染色较弱,可能是处于增生池的细胞相对较少,或由于基底层细胞的快速分裂更新,新生细胞相对幼稚,一些细胞功能蛋白合成不足;随着细胞进入棘层逐步成熟,以及皮损局部增高的TGF-α、IFN-γ对EGFR转录和降解水平的影响,造成了棘层细胞EGFR的表达增高,这也可能是造成棘层细胞过度增殖和分化不全的重要原因。颗粒层和角质层EGFR的表达可能是因为快速分裂的棘细胞推移进入外层,致使EGFR不能完全消退所致。
TPK的激活是EGFR生长因子信息传递的关键步骤。银屑病KC膜基础TPK活性明显增高,且与细胞膜上EGFR的表达量呈明显正相关。但EGFR的表达银屑病组约为对照组的5~6倍,而基础TPK的活性仅为正常组的2~3倍,因此:①部分阳性染色可能是EGFR的前体或降解形式等,它们不具有内在的TPK活性;②可能仍存在其它具有内在TPK活性的生长因子受体;③通过自显影结果发现除相对分子质量为170000的EGFR显影增强外,许多具有催化32P渗入的激酶活性均增高。关于银屑病TPK活性升高的分子机理目前尚不清楚。
, http://www.100md.com
作者单位:吕根法(400038 重庆,第三军医大学大坪医院)
吕根法(现在河南洛阳解放军第五三四医院皮肤科,471003)
李文维(400038 重庆,第三军医大学大坪医院)
伍津津(400038 重庆,第三军医大学大坪医院)
参考文献
1,Threadgill DW,Dlugosz AA,Hansen LA,et al.Targeted disruption of mouse EGF receptor:effect of genetic background on mutant phenotype.Science, 1995,269:230- 234.
, 百拇医药
2,Meyer T,Regenass U,Fabbro D,et al.A derivative of staurosporine(cGP41 251) shows selectivity for protein kinase C inhibition and in vitro anti proliferation as well as in vivo antitumor activity.Int J Cancer, 1989,43:851- 856.
3,Chen WS,Lazar CS,Poenie M,et al.Requirement for intrinsic protein tyrosine kinase in the immediate and late actions of the EGF receptor. Nature, 1987,328:820- 823., 百拇医药
吕根法 李文维 伍津津
摘要 目的:探讨酪氨酸蛋白激酶(TPK)在银屑病表皮异常增生中的作用。方法:通过外源性底物磷酸化的方法,测定银屑病进行期皮损角质形成细胞的TPK活性。结果:①银屑病进行期皮损角质形成细胞基础TPK活性显著增高,且对于转化生长因子-α的刺激,反应性明显增强;②增高的基础TPK活性与角质形成细胞膜表皮生长因子受体的表达量呈明显正相关;同时银屑病角质形成细胞表皮生长因子受体的自磷酸化水平亦显著增高。结论:TPK活性增高,以及对有丝分裂信号刺激的反应增强,可能在表皮的增生中起到重要作用,TPK活性的改变可能主要是由于表皮生长因子受体的表达异常所致,表皮生长因子受体可能在银屑病表皮的异常增生中发挥着重要作用。
, http://www.100md.com
关键词:银屑病 蛋白质酪氨酸激酶 受体,表皮生长因子-尿抑胃素 转化生长因子α
银屑病是一种常见的炎性增生性皮肤病,其病因、发病机制目前尚不清楚。角质形成细胞(KC)的增生、分化与细胞表面表皮生长因子受体(EGFR)的表达具有明显的关系[1]。EGFR的相对分子质量为170000的单链多肽,胞内区具有特异的酪氨酸蛋白激酶(TPK)活性,TPK激活是EGFR生物学功能发挥的关键步骤,且是细胞生长所必需的。本实验通过对皮损KC的TPK活性的研究,以探讨TPK在银屑病表皮增生中的作用。
材料和方法
一、材料
(一)标本来源:寻常型进行期银屑病患者22例,年龄16~58岁,平均28.4岁,男13例,女9例;正常对照组16例,男9例,女7例。年龄17~45岁,平均25.7岁,皮损标本取自2周内未内服及外用过任何药物的斑块性损害,银屑病组和正常对照组年龄、性别差异无显著性。皮肤取材厚度:银屑病组约0.4~0.6cm,正常人对照组约0.3~0.5cm。标本迅速用冰冷PBS冲洗3次除去血污,立即放入液氮瓶内。
, 百拇医药
(二)主要试剂:多聚谷酪氨酸(PolyGlu∶Tyr)(4∶1),Sigma公司;转化生长因子-α(TGF-α),Promega公司;[γ-32P]-ATP(>5000Ci/mmol),北京亚辉公司。
二、方法
(一)KC膜制备:冷冻保存的皮肤组织剪碎后于50mmol/LTris-HCl,pH7.4,1.0mmol/LPMSF混合液内(0.5mL/100mg组织),冰水浴内匀浆破膜,1000g离心5min,上清液再置低温超高速离心机100000g、4℃离心60min,分装放入-70℃冰箱内贮存,2个月内测定TPK活性。
(二)皮肤标本TPK活性的测定:
1.外源性底物磷酸化TPK活性的测定[2]:混合反应体系含终浓度为:10mmol/LHepers,pH7.4,10mmol/LMgCl2,1mmol/L正矾酸钠,0.1%TritonX100,PolyGlu∶Tyr(4∶1)1mg/mL,膜蛋白50μg。反应以加入[γ-32P]-ATP(0.5μCi/管)起动,37℃水浴反应5min;10μL0.5mol/LEDTA,pH8.0,终止反应。取40μL反应液点样于0.22μm微孔滤膜,以10%三氯醋酸负压抽滤,LKB-1275型液体闪烁机计数。TPK活性以每毫克膜蛋白每分钟催化32P转入到PolyGlu∶Tyr(4∶1)的fmol数减去自磷酸化的受体TPK活性值来表示。
, 百拇医药
2.TGF-α对EGFRTPK活性的影响:反应体系和实验方法基本同外源性底物磷酸化;分别加入不同浓度的TGF-α(0、101、102、103ng/mL)。在22℃水浴中保温30min。刺激后TPK活性以每毫克膜蛋白每分钟催化32P转入到PolyGlu∶Tyr(4∶1)的fmol数减去基础状态下的TPK活性值来表示。
(三)表皮生长因子受体自身磷酸化分析[3]:反应体系含终浓度为0.1%TritonX100,2mmol/LMgCl2,10μmol/L正矾酸钠,0.25mg/mL牛血清白蛋白,20mmol/LHepers,pH7.4,1μCi[γ-32P]-ATP,TGF-α10ng/mL;反应以加入100mg膜蛋白起动,4℃反应10min。10%的SDS-PAGE,干胶,-70℃的冰箱曝光72h作放射性自显影。
(四)采用ABC法染色分析表皮生长因子受体的分布:阳性染色显示KC膜上出现黄色颗粒。用半定量计分,染色强度用0~3级计分:0为无染色,1为轻度染色;2为中度染色;3为强度染色。染色范围采用表皮细胞阳性染色的百分数分0~4级;无染色为0;25%为1;25%~50%为2;50%~75%为3;>75%为4。染色总评分为染色强度+染色范围。
, 百拇医药
表1 表皮生长因子受体在银屑病皮损和正常人皮肤的表达(x±s)
组 别
例数
基底层
棘 层
颗粒层+角质层
银屑病
11
4.41±1.25
5.33±0.75
4.08±1.13
正常人
, 百拇医药
8
5.06±1.48
2.85±0.64
0.60±0.96
t值*
1.42
12.43*
12.82*
P值
>0.05
<0.01
<0.01
, 百拇医药
*与正常对照组比较表2 不同浓度转化生长因子α与表皮生长因子刺激后角质形成细胞酪氨酸蛋白激酶活性(fmol.min-1.mg-1)
组 别
基 础
转化生长因子α浓度(ng/mL)
表皮生长因子(ng/mL)
101
102
103
101
, 百拇医药
102
103
正常人对照
1.84±0.42
2.27±0.54
2.95±1.42
2.97±1.13
2.25±0.96
2.72±1.67
2.87±0.78
银屑病
3.04±1.61
, 百拇医药
3.83±1.35
5.05±1.07
4.96±1.32
4.21±1.07
5.12±1.39
5.18±1.45
t值
2.23
3.32
4.04
4.05
3.43
, http://www.100md.com
4.17
4.15
P值
<0.05
<0.05
<0.01
<0.01
<0.05
<0.01
<0.01
结果
一、免疫组化
, 百拇医药 正常皮肤EGFR阳性染色主要位于基底层的细胞膜上,银屑病皮损阳性染色可见于表皮的全层细胞膜上。基底层的细胞膜染色较正常对照组弱,但增厚的棘层细胞膜染色明显增强,角质层的细胞膜上亦可见阳性染色;自棘细胞层以上细胞膜阳性染色显著高于正常人对照组。约为正常人组的5~6倍。
二、表皮生长
因子受体自身磷酸化的改变通过放射性自显影的方法,观察到银屑病和正常人对照组EGFR的自磷酸化存在明显差异,见图1。

图1 银屑病和正常人角质形成细胞膜表皮生长因子受体170000放射性自显影
三、KC基础TPK活性和TGF-α刺激后TPK活性的变化
, 百拇医药
在无外源性刺激时,TPK活性在正常人对照组为(1.36±0.55)fmol.min-1.mg-1;银屑病组为(3.01±1.05)fmol.min-1.mg-1,两组比较差异有显著性,基础TPK活性与细胞膜EGFR的表达量之间具有显著相关性(r=0.65,P<0.01,n=24)。不同浓度TGF-α刺激后,KC膜的TPK活性呈剂量依赖性增高,但银屑病组的反应明显高于正常人对照组(表2)。测定不同浓度(101、102、103ng/mL)EGF刺激下KC的TPK活性(见表2),结果说明,在激活KC的EGFR的TPK活性方面,EGF和TGF-α是等效的。
讨论
, http://www.100md.com
EGFR数量的变化及功能异常是KC过度增殖及异常分化的重要原因。银屑病基底层细胞膜染色较弱,可能是处于增生池的细胞相对较少,或由于基底层细胞的快速分裂更新,新生细胞相对幼稚,一些细胞功能蛋白合成不足;随着细胞进入棘层逐步成熟,以及皮损局部增高的TGF-α、IFN-γ对EGFR转录和降解水平的影响,造成了棘层细胞EGFR的表达增高,这也可能是造成棘层细胞过度增殖和分化不全的重要原因。颗粒层和角质层EGFR的表达可能是因为快速分裂的棘细胞推移进入外层,致使EGFR不能完全消退所致。
TPK的激活是EGFR生长因子信息传递的关键步骤。银屑病KC膜基础TPK活性明显增高,且与细胞膜上EGFR的表达量呈明显正相关。但EGFR的表达银屑病组约为对照组的5~6倍,而基础TPK的活性仅为正常组的2~3倍,因此:①部分阳性染色可能是EGFR的前体或降解形式等,它们不具有内在的TPK活性;②可能仍存在其它具有内在TPK活性的生长因子受体;③通过自显影结果发现除相对分子质量为170000的EGFR显影增强外,许多具有催化32P渗入的激酶活性均增高。关于银屑病TPK活性升高的分子机理目前尚不清楚。
, http://www.100md.com
作者单位:吕根法(400038 重庆,第三军医大学大坪医院)
吕根法(现在河南洛阳解放军第五三四医院皮肤科,471003)
李文维(400038 重庆,第三军医大学大坪医院)
伍津津(400038 重庆,第三军医大学大坪医院)
参考文献
1,Threadgill DW,Dlugosz AA,Hansen LA,et al.Targeted disruption of mouse EGF receptor:effect of genetic background on mutant phenotype.Science, 1995,269:230- 234.
, 百拇医药
2,Meyer T,Regenass U,Fabbro D,et al.A derivative of staurosporine(cGP41 251) shows selectivity for protein kinase C inhibition and in vitro anti proliferation as well as in vivo antitumor activity.Int J Cancer, 1989,43:851- 856.
3,Chen WS,Lazar CS,Poenie M,et al.Requirement for intrinsic protein tyrosine kinase in the immediate and late actions of the EGF receptor. Nature, 1987,328:820- 823., 百拇医药