丁型肝炎病人肝组织HDAg与HBsAg/HBcAg和HBV DNA表达及关系
丁型肝炎病人肝组织HDAg与HBsAg/HBcAg和HBV DNA表达及关系
顾小红 李奇芬 王宇明
摘 要 目的:探讨丁型肝炎病人肝组织中HDAg与HBsAg/HBcAg和HBVDNA表达及关系。方法:应用免疫组化双重染色和原位杂交,检测79例丁型肝炎病人肝组织HDAg、HBsAg、HBcAg和HBVDNA表达,以52例乙型肝炎作对照。结果:丁型肝炎HBsAg、HBcAg检出率(81%、71%)较乙型肝炎(94%、92%)低(P< 0.05或0.01)。HDAg以肝细胞核表达为主,HBsAg以肝细胞浆表达为主,HDAg和HBsAg表达强度及阳性细胞分布呈一致性,且与肝组织的炎症活动和病理损害程度相关(P< 0.01)。HBcAg以肝细胞核表达为主,阳性细胞主要呈单个细胞或点状分布,且HBcAg阳性细胞明显少于HDAg阳性细胞。HDAg表达强度与HBVDNA表达呈负相关(P< 0.05)。结论:HDV感染会抑制HBV DNA复制或病毒抗原表达;在HDV致病机制中既有HDV的直接细胞毒性作用,也有HBV和HDV的协同作用。
, http://www.100md.com
关键词:丁型肝炎;丁肝病毒抗原;乙肝病毒表面抗原;乙肝病毒核心抗原;乙肝病毒脱氧核糖酸
自1977年Rizzetto等[1]发现 Delta抗原(δ-Ag)以来,有关HDV的分子生物学特性等研究取得了很大成就,但丁型肝炎的发病机理并不十分肯定。本研究应用免疫组化双重染色和原位杂交技术,分析了79例丁型肝炎病人肝组织HDAg表达与HBsAg/HBcAg和HBVDNA表达及关系,以期了解HDV和HBV在丁型肝炎发病机制中作用和意义,现报道如下。
1 材料与方法
1.1 研究对象
79病例均为西南医院感染病专科中心1990~1998年住院的血清HDV阳性乙型肝炎患者,其中急性肝炎(Acute hepatitis, AH)8例,慢性肝炎轻度(Mild-chronic hepatitis, mild-CH)23例,慢性肝炎中度(Moderate-chroonic,mode-CH)27例,重型肝炎(Severe hepatitis, SH)21例(包括慢性肝炎重度6例)。以52例乙型肝炎作对照,其中AH 8例,Mild-CH 12例,Mode-CH 27例,SH 5例(包括2例重度慢性肝炎)所有病例均经肝组织病理学检查确诊,诊断标准以1995年《病毒性肝炎防治方案(试行)》为依据[2]。
, 百拇医药
1.2 主要试剂及来源
免疫组化SP试剂盒和鼠抗HBsAg、HBcAg试剂盒购自福州迈新公司(Maxim biotech,inc产品)。双重染色试剂盒购自北京中山生物技术公司(美国Zymed公司产品)。丁型肝炎多克隆抗体由本科自行选定的HDV合成肽抗原经免疫家兔制备[3],工作浓度1∶160。HBV DNA试剂盒购置华西医科大学附一院肝病研究室。
1.3 操作步骤
操作步骤均按试剂盒说明书进行。
1.4 对照
阳性对照为预试中HBsAg、HBcAg和HBV DNA阳性乙型肝炎肝组织切片和HDAg阳性丁型肝炎肝组织切片。阴性对照选自正常人肝组织。此外,分别用鼠血清和PBS代替第一抗体作为替代实验,每例切片先分别检测HBsAg、HBcAg和HDAg,然后进行双重染色。
, http://www.100md.com
1.5 结果判断标准
双重染色HBsAg、HBcAg阳性颗粒NBT显色为紫黑色,HDAg阳性颗粒AEC显色为深红色。免疫组化半定量判断:未见阳性细胞(-),阳性细胞占肝小叶全部肝细胞的1/3以下(+),1/3~2/3为( ),2/3以上为(
),2/3以上为( )。
)。
1.6 统计学处理
采用计数资料的χ2检验和秩相关分析。
2 结果
, 百拇医药
2.1 丁型肝炎患者肝组织中HDAg表达
HDAg以肝细胞核型表达为主,其次是胞浆型表达。阳性细胞呈弥散型、灶状或片簇状分布于肝小叶内,尤其在门脉周围、坏死灶处较密集。在坏死灶边缘和气球样变性的肝细胞浆内有大量的HDAg表达,还观察到HDAg呈眉弓状分布在有病变的肝细胞膜下。慢肝中度和重型肝炎肝组织中,HDAg阳性细胞主要呈弥散型、片簇状分布于肝小叶内,在坏死灶处及其周围较多,有时可见HDAg阳性细胞以门脉为中心沿肝索分布整个肝小叶,见图1。在急性肝炎和慢肝轻度肝组织中,HDAg阳性细胞多呈单个或小灶状稀疏分布。秩相关分析发现重型肝炎和慢性肝炎中度HDAg表达强于急性肝炎和慢性肝炎轻度,且有显著差异(P<0.05),见表1。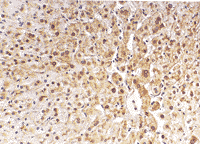
图1 慢性中度丁型肝炎患者肝组织HDAg表达 (S-P×200)
, 百拇医药
Fig 1 Expression of HDAg in liver tissue of the patient
with chronic moderate HD (S-P×200)
表1 丁型肝炎患者肚组织HDAg表达
Tab1 Expression of HDAg in the liver tissue of the patients with hepatitis D
HDAg expression
AH
Mild-Ch
Mode-Ch*
, http://www.100md.com
SH*
-
2
5
4
2
+
4
13
4
1
, http://www.100md.com
2
5
11
8
0
0
8
10
Total
8
23
, http://www.100md.com
27
21
Ridit analysis;*:P<0.05 vs AH
2.2 丁型肝炎患者肝组织中HBsAg、HBcAg表达
HBsAg阳性率为81%(64/79),HBsAg主要表达于肝细胞浆,有的呈包涵体型。在慢肝中度和重型肝炎,阳性细胞呈灶状或片簇状分布于肝小叶周边,在门脉周围及碎屑状坏死区较密集,还可见HBsAg呈岛屿状分布。在慢肝轻度和急性肝炎,阳性细胞较少且分散,表达强度也较弱;乙型肝炎HBsAg阳性率为94%(49/52),HBsAg表达及阳性细胞分布基本与丁型肝炎一致,但片簇状分布更多见,表达程度也较强,两组比较差异显著(P<0.05)。HBsAg表达强度和阳性细胞分布均与肝组织炎症活动度和病理损害相关(P<0.01),见表2。HBcAg阳性率为71%(56/79),HBcAg以肝细胞核表达为主。阳性细胞分布主要呈单个细胞或点状(3~5个细胞)分布,见图2;乙型肝炎HBcAg阳性率为94%(49/52),阳性细胞分布主要在门脉周围、碎屑状坏死区较明显,HBcAg表达程度较强,两组比较有显著差异(P< 0.01),见表2。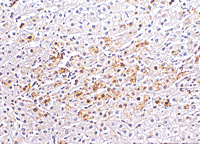
, http://www.100md.com
图2 慢性丁型肝炎患者肝组织HBcAg表达 (S-P×200)
Fig 2 The expression of HBcAg in liver tissue of the
patient with HD (S-P×200)
表2 丁型肚炎及乙型肝炎病人肝组织HBsAg、HBcAg表达(%)
Tab2 Expression of HBsAg in liver tissue of the
patients with hepatits D and hepatitis B(%)
Clincal type
Hepatitis D
, http://www.100md.com
Hepatitis B
n
HBsAg(%)*
HBcAg(%)#
n
HBsAg(%)
HBcAg(%)
-
+

, 百拇医药
Total
positive
-
+

Total
positive
-
+

, 百拇医药
Total
positive
-
+

Total
positive
AH
8
, http://www.100md.com
3
4
1
0
5(63)
5
2
1
0
3(38)
8
2
4
2
, 百拇医药
0
6(75)
1
5
2
0
7(86)
Mild-CH
23
6
10
7
0
17(74)
, 百拇医药
7
13
3
0
16(70)
12
1
8
3
0
11(92)
1
8
3
, 百拇医药
0
11(92)
Mode-CH
27
3
5
12
7
24(89)
6
8
10
3
, http://www.100md.com 21(78)
27
0
5
19
3
27(100)
2
2
18
5
25(93)
SH
21
, 百拇医药
3
0
9
9
18(86)
5
6
7
3
16(76)
5
0
0
2
, 百拇医药
3
5(100)
0
0
2
3
5(100)
total
79
15
19
29
16
, http://www.100md.com 64(81)
23
29
21
6
56(71)
52
3
17
26
6
49(94)
4
15
, 百拇医药
25
8
48(92)
χ2 test;*:P<0.05 vs HBsAg expression of hepatitis B;#:P<0.01 vs HBcAg expression of hepatitis B
2.3 HDAg与HBsAg、HBcAg表达关系
双标记检测发现HBsAg、HDAg两抗原多同时表达在同一肝细胞,单独表达的细胞也有,但数量明显少于双抗原表达的肝细胞,且二抗原阳性细胞分布比较一致,其间也可见二抗原均阴性的肝细胞。HBcAg和HDAg阳性细胞分布关系不密切,HBcAg阳性细胞明显少于HDAg阳性细胞,有时可见众多HDAg阳性细胞周围或之中仅一个或3~5个HBcAg阳性细胞。
, http://www.100md.com
2.4 HBV DNA在丁型肝炎患者肝组织表达
丁型肝炎患者肝组织HBV DNA阳性率为27%(21/79),HBV DNA阳性颗粒呈稀疏散在分布在肝细胞浆或核内以细胞核内分布为主,着色浅淡。秩相关分析发现HBV DNA阴性组HDAg表达明显强于HBV DNA阳性组,两者有统计学差异,即HBV DNA表达与HDAg表达强度呈负相关,见表3;而对照组HBV DNA阳性率为44%(23/52),阳性颗粒主要密集分布于肝细胞浆内,有时可集中在细胞核周围,个别细胞核内亦可见少数浅染的阳性颗粒,着色较深,表明乙型肝炎组HBV复制活跃而且HBV DNA的基因拷贝数较多,两者比较差异显著(P< 0.05)。
表3 79例丁型肝炎患者肝组织HDAg表达
与HBV DNA表达关系
Tab 3 Relationship between the expressions of HDAg
, http://www.100md.com
and HBV DNA in liver tissues of 79 patients with hepatitis D
HDAg expression
n
HBV DNA expression
+
-
Positive rate(%)
-
13
7
6
, 百拇医药
54
+
22
9
13
41
26
5
21
19 +
+
, http://www.100md.com
18
0
18
0
Total
79
21(27)
58(73)
Ridit analysis;P<0.05 vs HB DNA(-)
3 讨论
HDV感染对HBV存在依赖关系,但慢性乙型肝炎重叠感染HDV后,HDV会抑制HBV DNA复制或HBcAg表达[4],不少学者检测了HDV感染者血清HBV标记物的变化,甚至观察了血清和肝组织HBV DNA含量(Southern blot法)[5],得出类似的结果。本研究发现丁型肝炎肝组织HBsAg、HBcAg和HBV DNA阳性率及表达强度均低于单纯HBV感染者,且HBcAg主要呈核型表达,表达强度也较弱,表明HBV DNA基因呈低水平复制,而且HDAg表达强度与HBV DNA表达呈负性相关,这一结果表明HDV感染有抑制HBV基因复制或病毒抗原表达的作用,特别是在HDV复制活跃的阶段,即HDAg大量表达时,HBV复制受到的抑制最为明显。当抗HD阳性时,HDAg表达受抑制,HBV复制受到的抑制就减少,因此仍有HBV DNA被检出。此表明HBV复制的受抑制可能是一过性的,一旦HDAg转阴,HBV复制又可重新开始,即HDV感染时HBV的抑制状况,因HDV感染的不同阶段而异,这与Rizzetto等[6]动物实验结果亦相一致。本实验也发现HBsAg和HDAg表达及分布有一致关系,提示HDV对HBsAg的依赖,HDV和HBV可共同存在;同时,丁型肝炎有较高率的HBcAg检出,呈浆型或混合型表达,这些提示有HBV呈活动性复制状态,为HDV复制提供HBsAg创造有利条件,这与HDV感染时HBV的抑制状况,因HDV感染的不同阶段而异不相矛盾。
, 百拇医药
丁型肝炎发病机制中,有的认为是HDAg或HDV RNA对肝细胞的直接细胞毒性作用,有的认为是CTL为主的免疫调节机制在肝损害中起主导作用,也有的认为是HDV和HBV之间相互作用的结果。实验观察到HDAg阳性细胞呈弥散型、灶状和片簇状分布于肝小叶内,尤其是在门脉周围和坏死灶处,HDAg表达强度及阳性细胞分布均与肝组织炎症活动度及病理损害程度正有关。在坏死灶边缘肝细胞和气球样变性肝细胞浆内有大量的HDAg强阳性表达,证实有大量HDV堆积在病变肝细胞内,可以直接损害肝细胞,还观察到HDAg呈眉弓状分布在病变肝细胞膜下,这可能预示有大量HDV从该细胞释放而感染邻近细胞;有学者认为丁型肝炎病理学致变和临床表现可因原来感染的HBV或伴随的HBV感染而不同,通过对肝移植病人的研究,此观点也得到证实,因为移植肝脏原来的HDV感染常常不引起任何可见病理学改变或临床表现,只有发生HBV重叠感染时,才出现肝组织大块性炎症活动。有研究证实具有HBV活动性复制的丁型肝炎比没有HBV活动复制的病人有更严重的肝脏疾病和临床结果。也有可能HBV复制帮助了HDV的扩散,或HBV和HDV的协同作用加速了肝脏损害,因此认为HBV感染的本质在与已经加深了HDV致病效能。
, 百拇医药
作者简介:顾小红(1968.6),女,四川省绵阳市人,硕士,主治医师,现附属大坪医院野战外科研究所消化内科工作,主要从事病毒性肝炎发病机制方面的研究, 发表论文 6 篇。
顾小红(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
李奇芬(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
王宇明(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
参考文献
[1] Rizztto M, Canese M G, Arico O, et al. Immunofluorescence detection of a new antigenantibody system (delta/antidelta) associated to the hepatitis B virus in the liver and the serum of HBsAg carriers[J]. Gut, 1977, 18(11): 997-1 003.
, 百拇医药
[2] 病毒性肝炎防治方案(试行)[J].中华内科杂志, 1995, 34(11):788-791.
[3] 郑 红,李奇芬,林小红,等. 人工合成丁型肝炎病毒抗原多肽片段的特征与临床应用[J].中华医学杂志, 1993, 77(5):273-275.
[4] Rizzetto M. The delta agent[J]. Hepatology, 1983, 3(5):729-937.
[5] Hadziyannis S J, Sherman M, Lieberman H M,et al. Liver disease activity and hepatitis B virus replication in chronic Delta antigen positive hepatitis B virus carriers[J]. Hepatology,1985, 5(4): 544-547.
[6] Rizzetto M, Rosina F, Saracco G,et al. Treat of chronic Delta hepatitis with alpha2recombiant interferon[J]. J Hepatol,1986,3(Suppl 2):5 229-5 233., http://www.100md.com
顾小红 李奇芬 王宇明
摘 要 目的:探讨丁型肝炎病人肝组织中HDAg与HBsAg/HBcAg和HBVDNA表达及关系。方法:应用免疫组化双重染色和原位杂交,检测79例丁型肝炎病人肝组织HDAg、HBsAg、HBcAg和HBVDNA表达,以52例乙型肝炎作对照。结果:丁型肝炎HBsAg、HBcAg检出率(81%、71%)较乙型肝炎(94%、92%)低(P< 0.05或0.01)。HDAg以肝细胞核表达为主,HBsAg以肝细胞浆表达为主,HDAg和HBsAg表达强度及阳性细胞分布呈一致性,且与肝组织的炎症活动和病理损害程度相关(P< 0.01)。HBcAg以肝细胞核表达为主,阳性细胞主要呈单个细胞或点状分布,且HBcAg阳性细胞明显少于HDAg阳性细胞。HDAg表达强度与HBVDNA表达呈负相关(P< 0.05)。结论:HDV感染会抑制HBV DNA复制或病毒抗原表达;在HDV致病机制中既有HDV的直接细胞毒性作用,也有HBV和HDV的协同作用。
, http://www.100md.com
关键词:丁型肝炎;丁肝病毒抗原;乙肝病毒表面抗原;乙肝病毒核心抗原;乙肝病毒脱氧核糖酸
自1977年Rizzetto等[1]发现 Delta抗原(δ-Ag)以来,有关HDV的分子生物学特性等研究取得了很大成就,但丁型肝炎的发病机理并不十分肯定。本研究应用免疫组化双重染色和原位杂交技术,分析了79例丁型肝炎病人肝组织HDAg表达与HBsAg/HBcAg和HBVDNA表达及关系,以期了解HDV和HBV在丁型肝炎发病机制中作用和意义,现报道如下。
1 材料与方法
1.1 研究对象
79病例均为西南医院感染病专科中心1990~1998年住院的血清HDV阳性乙型肝炎患者,其中急性肝炎(Acute hepatitis, AH)8例,慢性肝炎轻度(Mild-chronic hepatitis, mild-CH)23例,慢性肝炎中度(Moderate-chroonic,mode-CH)27例,重型肝炎(Severe hepatitis, SH)21例(包括慢性肝炎重度6例)。以52例乙型肝炎作对照,其中AH 8例,Mild-CH 12例,Mode-CH 27例,SH 5例(包括2例重度慢性肝炎)所有病例均经肝组织病理学检查确诊,诊断标准以1995年《病毒性肝炎防治方案(试行)》为依据[2]。
, 百拇医药
1.2 主要试剂及来源
免疫组化SP试剂盒和鼠抗HBsAg、HBcAg试剂盒购自福州迈新公司(Maxim biotech,inc产品)。双重染色试剂盒购自北京中山生物技术公司(美国Zymed公司产品)。丁型肝炎多克隆抗体由本科自行选定的HDV合成肽抗原经免疫家兔制备[3],工作浓度1∶160。HBV DNA试剂盒购置华西医科大学附一院肝病研究室。
1.3 操作步骤
操作步骤均按试剂盒说明书进行。
1.4 对照
阳性对照为预试中HBsAg、HBcAg和HBV DNA阳性乙型肝炎肝组织切片和HDAg阳性丁型肝炎肝组织切片。阴性对照选自正常人肝组织。此外,分别用鼠血清和PBS代替第一抗体作为替代实验,每例切片先分别检测HBsAg、HBcAg和HDAg,然后进行双重染色。
, http://www.100md.com
1.5 结果判断标准
双重染色HBsAg、HBcAg阳性颗粒NBT显色为紫黑色,HDAg阳性颗粒AEC显色为深红色。免疫组化半定量判断:未见阳性细胞(-),阳性细胞占肝小叶全部肝细胞的1/3以下(+),1/3~2/3为(
1.6 统计学处理
采用计数资料的χ2检验和秩相关分析。
2 结果
, 百拇医药
2.1 丁型肝炎患者肝组织中HDAg表达
HDAg以肝细胞核型表达为主,其次是胞浆型表达。阳性细胞呈弥散型、灶状或片簇状分布于肝小叶内,尤其在门脉周围、坏死灶处较密集。在坏死灶边缘和气球样变性的肝细胞浆内有大量的HDAg表达,还观察到HDAg呈眉弓状分布在有病变的肝细胞膜下。慢肝中度和重型肝炎肝组织中,HDAg阳性细胞主要呈弥散型、片簇状分布于肝小叶内,在坏死灶处及其周围较多,有时可见HDAg阳性细胞以门脉为中心沿肝索分布整个肝小叶,见图1。在急性肝炎和慢肝轻度肝组织中,HDAg阳性细胞多呈单个或小灶状稀疏分布。秩相关分析发现重型肝炎和慢性肝炎中度HDAg表达强于急性肝炎和慢性肝炎轻度,且有显著差异(P<0.05),见表1。

图1 慢性中度丁型肝炎患者肝组织HDAg表达 (S-P×200)
, 百拇医药
Fig 1 Expression of HDAg in liver tissue of the patient
with chronic moderate HD (S-P×200)
表1 丁型肝炎患者肚组织HDAg表达
Tab1 Expression of HDAg in the liver tissue of the patients with hepatitis D
HDAg expression
AH
Mild-Ch
Mode-Ch*
, http://www.100md.com
SH*
-
2
5
4
2
+
4
13
4
1
, http://www.100md.com
2
5
11
8
0
0
8
10
Total
8
23
, http://www.100md.com
27
21
Ridit analysis;*:P<0.05 vs AH
2.2 丁型肝炎患者肝组织中HBsAg、HBcAg表达
HBsAg阳性率为81%(64/79),HBsAg主要表达于肝细胞浆,有的呈包涵体型。在慢肝中度和重型肝炎,阳性细胞呈灶状或片簇状分布于肝小叶周边,在门脉周围及碎屑状坏死区较密集,还可见HBsAg呈岛屿状分布。在慢肝轻度和急性肝炎,阳性细胞较少且分散,表达强度也较弱;乙型肝炎HBsAg阳性率为94%(49/52),HBsAg表达及阳性细胞分布基本与丁型肝炎一致,但片簇状分布更多见,表达程度也较强,两组比较差异显著(P<0.05)。HBsAg表达强度和阳性细胞分布均与肝组织炎症活动度和病理损害相关(P<0.01),见表2。HBcAg阳性率为71%(56/79),HBcAg以肝细胞核表达为主。阳性细胞分布主要呈单个细胞或点状(3~5个细胞)分布,见图2;乙型肝炎HBcAg阳性率为94%(49/52),阳性细胞分布主要在门脉周围、碎屑状坏死区较明显,HBcAg表达程度较强,两组比较有显著差异(P< 0.01),见表2。

, http://www.100md.com
图2 慢性丁型肝炎患者肝组织HBcAg表达 (S-P×200)
Fig 2 The expression of HBcAg in liver tissue of the
patient with HD (S-P×200)
表2 丁型肚炎及乙型肝炎病人肝组织HBsAg、HBcAg表达(%)
Tab2 Expression of HBsAg in liver tissue of the
patients with hepatits D and hepatitis B(%)
Clincal type
Hepatitis D
, http://www.100md.com
Hepatitis B
n
HBsAg(%)*
HBcAg(%)#
n
HBsAg(%)
HBcAg(%)
-
+
, 百拇医药
Total
positive
-
+
Total
positive
-
+
, 百拇医药
Total
positive
-
+
Total
positive
AH
8
, http://www.100md.com
3
4
1
0
5(63)
5
2
1
0
3(38)
8
2
4
2
, 百拇医药
0
6(75)
1
5
2
0
7(86)
Mild-CH
23
6
10
7
0
17(74)
, 百拇医药
7
13
3
0
16(70)
12
1
8
3
0
11(92)
1
8
3
, 百拇医药
0
11(92)
Mode-CH
27
3
5
12
7
24(89)
6
8
10
3
, http://www.100md.com 21(78)
27
0
5
19
3
27(100)
2
2
18
5
25(93)
SH
21
, 百拇医药
3
0
9
9
18(86)
5
6
7
3
16(76)
5
0
0
2
, 百拇医药
3
5(100)
0
0
2
3
5(100)
total
79
15
19
29
16
, http://www.100md.com 64(81)
23
29
21
6
56(71)
52
3
17
26
6
49(94)
4
15
, 百拇医药
25
8
48(92)
χ2 test;*:P<0.05 vs HBsAg expression of hepatitis B;#:P<0.01 vs HBcAg expression of hepatitis B
2.3 HDAg与HBsAg、HBcAg表达关系
双标记检测发现HBsAg、HDAg两抗原多同时表达在同一肝细胞,单独表达的细胞也有,但数量明显少于双抗原表达的肝细胞,且二抗原阳性细胞分布比较一致,其间也可见二抗原均阴性的肝细胞。HBcAg和HDAg阳性细胞分布关系不密切,HBcAg阳性细胞明显少于HDAg阳性细胞,有时可见众多HDAg阳性细胞周围或之中仅一个或3~5个HBcAg阳性细胞。
, http://www.100md.com
2.4 HBV DNA在丁型肝炎患者肝组织表达
丁型肝炎患者肝组织HBV DNA阳性率为27%(21/79),HBV DNA阳性颗粒呈稀疏散在分布在肝细胞浆或核内以细胞核内分布为主,着色浅淡。秩相关分析发现HBV DNA阴性组HDAg表达明显强于HBV DNA阳性组,两者有统计学差异,即HBV DNA表达与HDAg表达强度呈负相关,见表3;而对照组HBV DNA阳性率为44%(23/52),阳性颗粒主要密集分布于肝细胞浆内,有时可集中在细胞核周围,个别细胞核内亦可见少数浅染的阳性颗粒,着色较深,表明乙型肝炎组HBV复制活跃而且HBV DNA的基因拷贝数较多,两者比较差异显著(P< 0.05)。
表3 79例丁型肝炎患者肝组织HDAg表达
与HBV DNA表达关系
Tab 3 Relationship between the expressions of HDAg
, http://www.100md.com
and HBV DNA in liver tissues of 79 patients with hepatitis D
HDAg expression
n
HBV DNA expression
+
-
Positive rate(%)
-
13
7
6
, 百拇医药
54
+
22
9
13
41
26
5
21
19
, http://www.100md.com
18
0
18
0
Total
79
21(27)
58(73)
Ridit analysis;P<0.05 vs HB DNA(-)
3 讨论
HDV感染对HBV存在依赖关系,但慢性乙型肝炎重叠感染HDV后,HDV会抑制HBV DNA复制或HBcAg表达[4],不少学者检测了HDV感染者血清HBV标记物的变化,甚至观察了血清和肝组织HBV DNA含量(Southern blot法)[5],得出类似的结果。本研究发现丁型肝炎肝组织HBsAg、HBcAg和HBV DNA阳性率及表达强度均低于单纯HBV感染者,且HBcAg主要呈核型表达,表达强度也较弱,表明HBV DNA基因呈低水平复制,而且HDAg表达强度与HBV DNA表达呈负性相关,这一结果表明HDV感染有抑制HBV基因复制或病毒抗原表达的作用,特别是在HDV复制活跃的阶段,即HDAg大量表达时,HBV复制受到的抑制最为明显。当抗HD阳性时,HDAg表达受抑制,HBV复制受到的抑制就减少,因此仍有HBV DNA被检出。此表明HBV复制的受抑制可能是一过性的,一旦HDAg转阴,HBV复制又可重新开始,即HDV感染时HBV的抑制状况,因HDV感染的不同阶段而异,这与Rizzetto等[6]动物实验结果亦相一致。本实验也发现HBsAg和HDAg表达及分布有一致关系,提示HDV对HBsAg的依赖,HDV和HBV可共同存在;同时,丁型肝炎有较高率的HBcAg检出,呈浆型或混合型表达,这些提示有HBV呈活动性复制状态,为HDV复制提供HBsAg创造有利条件,这与HDV感染时HBV的抑制状况,因HDV感染的不同阶段而异不相矛盾。
, 百拇医药
丁型肝炎发病机制中,有的认为是HDAg或HDV RNA对肝细胞的直接细胞毒性作用,有的认为是CTL为主的免疫调节机制在肝损害中起主导作用,也有的认为是HDV和HBV之间相互作用的结果。实验观察到HDAg阳性细胞呈弥散型、灶状和片簇状分布于肝小叶内,尤其是在门脉周围和坏死灶处,HDAg表达强度及阳性细胞分布均与肝组织炎症活动度及病理损害程度正有关。在坏死灶边缘肝细胞和气球样变性肝细胞浆内有大量的HDAg强阳性表达,证实有大量HDV堆积在病变肝细胞内,可以直接损害肝细胞,还观察到HDAg呈眉弓状分布在病变肝细胞膜下,这可能预示有大量HDV从该细胞释放而感染邻近细胞;有学者认为丁型肝炎病理学致变和临床表现可因原来感染的HBV或伴随的HBV感染而不同,通过对肝移植病人的研究,此观点也得到证实,因为移植肝脏原来的HDV感染常常不引起任何可见病理学改变或临床表现,只有发生HBV重叠感染时,才出现肝组织大块性炎症活动。有研究证实具有HBV活动性复制的丁型肝炎比没有HBV活动复制的病人有更严重的肝脏疾病和临床结果。也有可能HBV复制帮助了HDV的扩散,或HBV和HDV的协同作用加速了肝脏损害,因此认为HBV感染的本质在与已经加深了HDV致病效能。
, 百拇医药
作者简介:顾小红(1968.6),女,四川省绵阳市人,硕士,主治医师,现附属大坪医院野战外科研究所消化内科工作,主要从事病毒性肝炎发病机制方面的研究, 发表论文 6 篇。
顾小红(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
李奇芬(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
王宇明(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
参考文献
[1] Rizztto M, Canese M G, Arico O, et al. Immunofluorescence detection of a new antigenantibody system (delta/antidelta) associated to the hepatitis B virus in the liver and the serum of HBsAg carriers[J]. Gut, 1977, 18(11): 997-1 003.
, 百拇医药
[2] 病毒性肝炎防治方案(试行)[J].中华内科杂志, 1995, 34(11):788-791.
[3] 郑 红,李奇芬,林小红,等. 人工合成丁型肝炎病毒抗原多肽片段的特征与临床应用[J].中华医学杂志, 1993, 77(5):273-275.
[4] Rizzetto M. The delta agent[J]. Hepatology, 1983, 3(5):729-937.
[5] Hadziyannis S J, Sherman M, Lieberman H M,et al. Liver disease activity and hepatitis B virus replication in chronic Delta antigen positive hepatitis B virus carriers[J]. Hepatology,1985, 5(4): 544-547.
[6] Rizzetto M, Rosina F, Saracco G,et al. Treat of chronic Delta hepatitis with alpha2recombiant interferon[J]. J Hepatol,1986,3(Suppl 2):5 229-5 233., http://www.100md.com