高效液相色谱衍生化法测定红参及生脉注射液中人参二醇和人参三醇的含量
作者:李章万 徐秀荣 冯春琼 刘三康 钱广生
单位:华西医科大学药学院 成都 610041
关键词:人参二醇;人参三醇;衍生化;高效液相色谱
高效液相色谱衍生化法测定红参及生脉注射液 中人参二醇和人参三醇的含量 提要 用3,5-二硝基苯甲酰氯(3,5-DNB)为衍生化剂,高效液相色谱法测定了红参和生脉注射液中人参二醇及人参三醇的含量。以C18硅烷键合相为填料,甲醇-水(95∶5)为流动相,检测波长230 nm,进行反相高效液相色法测定。供试品经提取、水解和衍生化等操作处理后,测得红参中人参二醇及人参三醇的含量约为0.9%和0.5%;生脉注射液中分别约为0.7 mg/ml和0.5 mg/ml。
DETERMINATION OF PANAXADIOL AND PANAXATRIOL
, 百拇医药
IN PANAX GINSENG C.A.MEY AND SHENGMAI
INJECTION BY HPLC WITH DERIVATION
Li Zhangwan Xu Xiurong Feng Chunqiong Liu Sankang Qian Guangsheng
(School of Pharmacy,West China University of Medical Sciences Chengdu 610041)
ABSTRACT The use of 3,5-dinitrobenzoyl(3,5-DNB) chloride to form an ultaviolet absorbing derivative was attempted to determine panaxadiol and panaxatriol in Panax ginseng C.A. Mey and Shengmai injection by RP-HPLC. The HPLC of the derivatives was performed on an ODS column, using MeOH-H2O (95∶5) solvent system and ultraviolet detection (230 nm).The samples were treated by extraction, hydrolysis and derivation. The contents of panaxadiol and panaxatriol in Panax ginseng C.A.Mey were about 0.9% and 0.5%, and in Shengmai injection were about 0.7mg/ml and 0.5mg/ml,respectively. Key Words Panaxadiol Panaxatriol Derivation RP-HPLC
, 百拇医药
红参是人参(Panax ginseng C.A.Mey)的栽培品,名贵中药之一,也是生脉注射液的君药。红参中主要成分的人参皂苷,经强酸水解得人参二醇(panaxadiol,PD)和人参三醇(panaxatriol, PT)等[1]。国内外有各种有关人参的含量测定方法报道,比色法[2]、薄层扫描法[3]、高效液相色谱法[4]以及超临界流体色谱法[5]。由于人参皂苷及其水解产物均无特征紫外吸收,上述方法在灵敏度或分离度等方面都不尽人意。采用3,5-二硝基苯甲酰氯为衍生化剂,反相HPLC法对红参和生脉注射液中人参二醇和人参三醇含量测定方法进行了研究。
1 实验部分
1.1 仪器与试剂
日本岛津LC-6A高效液相色谱仪,SPD-6AV紫外检测器,C-R4A数据处理机;Shimpack CLC-ODS(150 mm×6 mm)分析柱,自填国产YWG C18(10 mm×4.6 mm)保护柱。人参二醇和人参三醇对照品(中国药品生物制品检定所);红参(市售,华西医科大学生药教研室鉴定);生脉注射液(华西医大制药厂)。3,5-二硝基苯甲酰氯(3,5-DNB)自制(mp 68.5~69.5℃),其它试剂皆为分析纯。
, 百拇医药
1.2 测定方法和结果
1.2.1 色谱条件 以甲醇-水(95∶5)为流动相,流速1 ml/min,色谱柱温35℃,检测波长230 nm。在此条件下测得人参二醇及人参三醇DNB衍生物的保留时间分别约为12 min和25 min。
1.2.2 对照品溶液的制备 精密称取人参二醇和人参三醇对照品约10 mg,分别置25 ml量瓶中,用甲醇溶解并稀释至刻度,摇匀,得对照品贮备液。精密吸取对照品贮备液1.00 ml,置同一具塞试管中,减压下用氮气流吹干,加3,5-DNB 20 mg,无水吡啶0.3 ml,置75℃水浴上回流1 h,取出后减压下用氮气流吹干。残渣用四氢呋喃溶解,并转入5 ml量瓶中,稀释至刻度,摇匀,即得。
1.2.3 供试品溶液的制备 红参药材打成细粉,过4号筛。精密称取红参粉约0.1 g,加45%乙醇10 ml,超声提取1 h,转入15 ml离心管中离心(4000 r/min)5 min,残渣用45%乙醇各5 ml洗涤二次。合并上清液于50 ml烧瓶中,加浓硫酸2.0 ml,置75℃水浴上回流4 h,转入蒸发皿中,浓缩至约10 ml,取下,于冷水浴上滴加6 mol/L NaOH中和至pH6~7,转入分液漏斗中,用环己烷提取三次,每次15 ml。合并环己烷层,加无水Na2SO4约2 g,脱水滤过,用少许环己烷洗涤滤渣,浓缩至近干,转入具塞试管中,用少许环己烷洗涤蒸发皿,洗液并入试管中,减压下用氮气流吹干,加3,5-DNB约20 mg,无水吡啶0.3 ml,置75℃水浴上回流1 h,取出后,减压下用氮气流吹干。残渣用四氢呋喃溶解,并转入5 ml量瓶中,稀释至刻度,摇匀,即得。
, 百拇医药
精密吸取生脉注射液1 ml,加水9 ml,无水乙醇9 ml,再加入浓硫酸2.0 ml,置75℃水浴上回流水解,其余操作与红参供试品溶液制备相同,即得。
1.2.4 线性关系 分别精密吸取对照品溶液5.0、10.0、15.0、20.0 μl注入色谱仪,测定PD及PT峰的峰面积,每个体积各进样三次;以进样量(μg)对峰面积积分值进行线性回归,得回归方程分别为:A=-421+95872X,r=0.9966(PD)和A=-310+249177X,r=0.9997(PT)。可见在(0.4~1.6) μg范围内,二者色谱峰面积积分值与进样量成线性关系。
1.2.5 衍生化条件 文献[6]曾用3,5-DNB衍生化测定强心苷。据此,进一步考察了PD及PT衍生化反应的3,5-DNB用量、反应温度与时间和无水吡啶用量等。用一定量PD和PT对照品进行单因素变化的实验,其它操作条件不变。通过测定PD及PT峰面积进行比较。结果发现加入3,5-DNB的量是PD或PT的摩尔数的20倍后,色谱峰峰面积基本不变;反应温度75℃、时间1 h时为宜。当温度过高或过低时,峰面积明显减少。无水吡啶为0.3 ml足以维持反应需要;吡啶量增加,挥干费时。
, 百拇医药
1.2.6 水解条件 文献[5]报道,人参皂苷在15%硫酸乙醇-水(1∶1)溶液中,75℃回流4 h较好。用同一批红参提取液,分别进行不同硫酸量,不同水解温度的考察,结果与文献报道基本相同。硫酸量的增加或减少,水解时间的延长都会导致含量偏低。水解产物易溶于氯仿,但萃取时乳化严重,改用环己烷萃取,结果较好。
1.2.7 回收率试验 精密称取红参细粉或生脉注射液适量,加入一定量的混合对照品溶液,按“1.2.3”项下处理,测定PD和PT的含量,并计算回收率。红参中PD及PT的回收率分别为93.7%和90.5%,RSD分别为4.9%和4%;生脉注液中分别为92.6%和93.3%,RSD分别为5.4%和3.6%。
1.2.8 测定结果 将对照品溶液和供试溶液各5~10 μl分别注入色谱仪,测定峰面积,按外标法计算。测得红参药材及生脉注射液中PD及PT的含量(表1,图1)。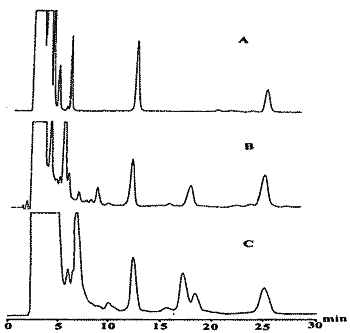
, 百拇医药
Fig 1 Chromatograms of the DNB-derivatives of PD and PT
A Standard B Panax ginseng C.A.Mey C Shengmai injection
Table 1 The contents of panaxadiol ane panaxatriol in Panax ginseng C.A.Mey and in Shengmai injection (n=3)
Sample
Panaxadiol
(RSD%
Panaxatriol
, 百拇医药 (RSD%)
Panax ginseng
0.892%(5.3)
0.498%(6.2)
Shengmai of injection
970201
0.675mg/ml(5.6)
0.551mg/ml(5.6)
970206
0.668mg/ml(3.8)
0.542mg/ml(4.3)
, 百拇医药
970209
0.672mg/ml(2.9)
0.540mg/ml(6.1)
2 讨论
2.1 PD和PT的3,5-DNB衍生物有很强的紫外吸收,230 nm处有最大吸收。在色谱条件下,以信噪比为3∶1计算,人参二醇的最小检测量为2.4×10-11g,人参三醇的最小检测量为8.2×10-12g。
2.2 PD和PT的3,5-DNB衍生物保留时间分别约为12 min和25 min。这种流出次序与Fujii等人[6]所研究的强心苷3,5-DNB衍生物流出次序相同,即RP-HPLC中,3,5-DNB衍生物分子中3,5-DNB基团越少,保留时间越小。这间接说明PD和PT与3,5-DNB的反应分别是与甾环上的二个羟基和三个羟基发生的。采用改变流动相组成的办法,可使PD和PT衍生物峰保留值大约相等,相同摩尔数的人参二醇和人参三醇得到的峰面积比约为2/3。
, 百拇医药
2.3 研究中曾试图采用内标法,因未找到合适内标而采用外标法。如胆固醇的3,5-DNB衍生物保留时间约30 min,麦角甾醇衍生物约21 min例如。前者保留时间过长,后者有干扰而未采用。欲使外标法有较好的精密度,操作中注意各步的一致性,如提取时间、水解时间、酸的用量、衍生化时间和温度等因素都应严格控制,在样品转移、吹干等操作中,需谨防丢失。
作者简介:冯春琼:华西医科大学药学院1991届学生
参考文献
1 中国医学科学院药物研究所编.中草药现代研究(第二卷).北京:北京医科大学中国协和医科大学联合出版社,1996.430
2 谢刚林.参麦注射液中人参总皂苷含量测定.中草药,1990,21(11)∶16
3 王宝 .薄层扫描法测定复方人参酊中人参皂苷Re的含量.中成药,1991,13(4)∶15
.薄层扫描法测定复方人参酊中人参皂苷Re的含量.中成药,1991,13(4)∶15
4 周志华,章观德.人参的分析.Ⅳ人参皂苷HPLC测定.药学学报,1988,23(2)∶137
5 李云华,李修禄,虹岚等.超临界流体色谱法测定三七及云南白药中人参二醇和人参三醇的含量.药学学报,1991,26(10)∶764
6 Fujii Y, Dguri R, Mitsuashi A, et al. Micro HPLC separation of 3,5-dinitrobengoyl derivatives of cardiac glycosides and their metabolites. J Chromatogs Science, 1983, 21∶495, http://www.100md.com
单位:华西医科大学药学院 成都 610041
关键词:人参二醇;人参三醇;衍生化;高效液相色谱
高效液相色谱衍生化法测定红参及生脉注射液 中人参二醇和人参三醇的含量 提要 用3,5-二硝基苯甲酰氯(3,5-DNB)为衍生化剂,高效液相色谱法测定了红参和生脉注射液中人参二醇及人参三醇的含量。以C18硅烷键合相为填料,甲醇-水(95∶5)为流动相,检测波长230 nm,进行反相高效液相色法测定。供试品经提取、水解和衍生化等操作处理后,测得红参中人参二醇及人参三醇的含量约为0.9%和0.5%;生脉注射液中分别约为0.7 mg/ml和0.5 mg/ml。
DETERMINATION OF PANAXADIOL AND PANAXATRIOL
, 百拇医药
IN PANAX GINSENG C.A.MEY AND SHENGMAI
INJECTION BY HPLC WITH DERIVATION
Li Zhangwan Xu Xiurong Feng Chunqiong Liu Sankang Qian Guangsheng
(School of Pharmacy,West China University of Medical Sciences Chengdu 610041)
ABSTRACT The use of 3,5-dinitrobenzoyl(3,5-DNB) chloride to form an ultaviolet absorbing derivative was attempted to determine panaxadiol and panaxatriol in Panax ginseng C.A. Mey and Shengmai injection by RP-HPLC. The HPLC of the derivatives was performed on an ODS column, using MeOH-H2O (95∶5) solvent system and ultraviolet detection (230 nm).The samples were treated by extraction, hydrolysis and derivation. The contents of panaxadiol and panaxatriol in Panax ginseng C.A.Mey were about 0.9% and 0.5%, and in Shengmai injection were about 0.7mg/ml and 0.5mg/ml,respectively. Key Words Panaxadiol Panaxatriol Derivation RP-HPLC
, 百拇医药
红参是人参(Panax ginseng C.A.Mey)的栽培品,名贵中药之一,也是生脉注射液的君药。红参中主要成分的人参皂苷,经强酸水解得人参二醇(panaxadiol,PD)和人参三醇(panaxatriol, PT)等[1]。国内外有各种有关人参的含量测定方法报道,比色法[2]、薄层扫描法[3]、高效液相色谱法[4]以及超临界流体色谱法[5]。由于人参皂苷及其水解产物均无特征紫外吸收,上述方法在灵敏度或分离度等方面都不尽人意。采用3,5-二硝基苯甲酰氯为衍生化剂,反相HPLC法对红参和生脉注射液中人参二醇和人参三醇含量测定方法进行了研究。
1 实验部分
1.1 仪器与试剂
日本岛津LC-6A高效液相色谱仪,SPD-6AV紫外检测器,C-R4A数据处理机;Shimpack CLC-ODS(150 mm×6 mm)分析柱,自填国产YWG C18(10 mm×4.6 mm)保护柱。人参二醇和人参三醇对照品(中国药品生物制品检定所);红参(市售,华西医科大学生药教研室鉴定);生脉注射液(华西医大制药厂)。3,5-二硝基苯甲酰氯(3,5-DNB)自制(mp 68.5~69.5℃),其它试剂皆为分析纯。
, 百拇医药
1.2 测定方法和结果
1.2.1 色谱条件 以甲醇-水(95∶5)为流动相,流速1 ml/min,色谱柱温35℃,检测波长230 nm。在此条件下测得人参二醇及人参三醇DNB衍生物的保留时间分别约为12 min和25 min。
1.2.2 对照品溶液的制备 精密称取人参二醇和人参三醇对照品约10 mg,分别置25 ml量瓶中,用甲醇溶解并稀释至刻度,摇匀,得对照品贮备液。精密吸取对照品贮备液1.00 ml,置同一具塞试管中,减压下用氮气流吹干,加3,5-DNB 20 mg,无水吡啶0.3 ml,置75℃水浴上回流1 h,取出后减压下用氮气流吹干。残渣用四氢呋喃溶解,并转入5 ml量瓶中,稀释至刻度,摇匀,即得。
1.2.3 供试品溶液的制备 红参药材打成细粉,过4号筛。精密称取红参粉约0.1 g,加45%乙醇10 ml,超声提取1 h,转入15 ml离心管中离心(4000 r/min)5 min,残渣用45%乙醇各5 ml洗涤二次。合并上清液于50 ml烧瓶中,加浓硫酸2.0 ml,置75℃水浴上回流4 h,转入蒸发皿中,浓缩至约10 ml,取下,于冷水浴上滴加6 mol/L NaOH中和至pH6~7,转入分液漏斗中,用环己烷提取三次,每次15 ml。合并环己烷层,加无水Na2SO4约2 g,脱水滤过,用少许环己烷洗涤滤渣,浓缩至近干,转入具塞试管中,用少许环己烷洗涤蒸发皿,洗液并入试管中,减压下用氮气流吹干,加3,5-DNB约20 mg,无水吡啶0.3 ml,置75℃水浴上回流1 h,取出后,减压下用氮气流吹干。残渣用四氢呋喃溶解,并转入5 ml量瓶中,稀释至刻度,摇匀,即得。
, 百拇医药
精密吸取生脉注射液1 ml,加水9 ml,无水乙醇9 ml,再加入浓硫酸2.0 ml,置75℃水浴上回流水解,其余操作与红参供试品溶液制备相同,即得。
1.2.4 线性关系 分别精密吸取对照品溶液5.0、10.0、15.0、20.0 μl注入色谱仪,测定PD及PT峰的峰面积,每个体积各进样三次;以进样量(μg)对峰面积积分值进行线性回归,得回归方程分别为:A=-421+95872X,r=0.9966(PD)和A=-310+249177X,r=0.9997(PT)。可见在(0.4~1.6) μg范围内,二者色谱峰面积积分值与进样量成线性关系。
1.2.5 衍生化条件 文献[6]曾用3,5-DNB衍生化测定强心苷。据此,进一步考察了PD及PT衍生化反应的3,5-DNB用量、反应温度与时间和无水吡啶用量等。用一定量PD和PT对照品进行单因素变化的实验,其它操作条件不变。通过测定PD及PT峰面积进行比较。结果发现加入3,5-DNB的量是PD或PT的摩尔数的20倍后,色谱峰峰面积基本不变;反应温度75℃、时间1 h时为宜。当温度过高或过低时,峰面积明显减少。无水吡啶为0.3 ml足以维持反应需要;吡啶量增加,挥干费时。
, 百拇医药
1.2.6 水解条件 文献[5]报道,人参皂苷在15%硫酸乙醇-水(1∶1)溶液中,75℃回流4 h较好。用同一批红参提取液,分别进行不同硫酸量,不同水解温度的考察,结果与文献报道基本相同。硫酸量的增加或减少,水解时间的延长都会导致含量偏低。水解产物易溶于氯仿,但萃取时乳化严重,改用环己烷萃取,结果较好。
1.2.7 回收率试验 精密称取红参细粉或生脉注射液适量,加入一定量的混合对照品溶液,按“1.2.3”项下处理,测定PD和PT的含量,并计算回收率。红参中PD及PT的回收率分别为93.7%和90.5%,RSD分别为4.9%和4%;生脉注液中分别为92.6%和93.3%,RSD分别为5.4%和3.6%。
1.2.8 测定结果 将对照品溶液和供试溶液各5~10 μl分别注入色谱仪,测定峰面积,按外标法计算。测得红参药材及生脉注射液中PD及PT的含量(表1,图1)。

, 百拇医药
Fig 1 Chromatograms of the DNB-derivatives of PD and PT
A Standard B Panax ginseng C.A.Mey C Shengmai injection
Table 1 The contents of panaxadiol ane panaxatriol in Panax ginseng C.A.Mey and in Shengmai injection (n=3)
Sample
Panaxadiol
(RSD%
Panaxatriol
, 百拇医药 (RSD%)
Panax ginseng
0.892%(5.3)
0.498%(6.2)
Shengmai of injection
970201
0.675mg/ml(5.6)
0.551mg/ml(5.6)
970206
0.668mg/ml(3.8)
0.542mg/ml(4.3)
, 百拇医药
970209
0.672mg/ml(2.9)
0.540mg/ml(6.1)
2 讨论
2.1 PD和PT的3,5-DNB衍生物有很强的紫外吸收,230 nm处有最大吸收。在色谱条件下,以信噪比为3∶1计算,人参二醇的最小检测量为2.4×10-11g,人参三醇的最小检测量为8.2×10-12g。
2.2 PD和PT的3,5-DNB衍生物保留时间分别约为12 min和25 min。这种流出次序与Fujii等人[6]所研究的强心苷3,5-DNB衍生物流出次序相同,即RP-HPLC中,3,5-DNB衍生物分子中3,5-DNB基团越少,保留时间越小。这间接说明PD和PT与3,5-DNB的反应分别是与甾环上的二个羟基和三个羟基发生的。采用改变流动相组成的办法,可使PD和PT衍生物峰保留值大约相等,相同摩尔数的人参二醇和人参三醇得到的峰面积比约为2/3。
, 百拇医药
2.3 研究中曾试图采用内标法,因未找到合适内标而采用外标法。如胆固醇的3,5-DNB衍生物保留时间约30 min,麦角甾醇衍生物约21 min例如。前者保留时间过长,后者有干扰而未采用。欲使外标法有较好的精密度,操作中注意各步的一致性,如提取时间、水解时间、酸的用量、衍生化时间和温度等因素都应严格控制,在样品转移、吹干等操作中,需谨防丢失。
作者简介:冯春琼:华西医科大学药学院1991届学生
参考文献
1 中国医学科学院药物研究所编.中草药现代研究(第二卷).北京:北京医科大学中国协和医科大学联合出版社,1996.430
2 谢刚林.参麦注射液中人参总皂苷含量测定.中草药,1990,21(11)∶16
3 王宝
4 周志华,章观德.人参的分析.Ⅳ人参皂苷HPLC测定.药学学报,1988,23(2)∶137
5 李云华,李修禄,虹岚等.超临界流体色谱法测定三七及云南白药中人参二醇和人参三醇的含量.药学学报,1991,26(10)∶764
6 Fujii Y, Dguri R, Mitsuashi A, et al. Micro HPLC separation of 3,5-dinitrobengoyl derivatives of cardiac glycosides and their metabolites. J Chromatogs Science, 1983, 21∶495, http://www.100md.com