含稳定整合pMCLacI/Neo质粒的NIH3T3细胞体外突变研究模型的建立
作者:卢洋 黎怀星 傅继梁
单位:卢洋(200433 上海,第二军医大学医学遗传学教研室);黎怀星(200433 上海,第二军医大学医学遗传学教研室);傅继梁(200433 上海,第二军医大学医学遗传学教研室)
关键词:基因突变;lacI基因;NIH3T3细胞;转录;质粒
New Page 1 【摘要】 目的 建立一个用于比较研究哺乳动物细胞内表达基因和沉默基因的突变机理的实验模型。方法 以脂质体转染法将线性化的pMCLacI/Neo质粒导入NIH3T3细胞,用G418筛选,选择一个药物抗性细胞克隆进行扩增,用基因组Southern杂交,RT-PCR及RT-PCR Southern杂交进行分子鉴定。结果 (1)在此细胞克隆的基因组中整合有pMCLacI/Neo质粒;(2)该质粒上的两个lacI靶基因中,有一个在NIH3T3细胞内处于转录表达状态;(3)可以通过酶切环化的方法从阳性细胞克隆的基因组DNA中回收出结构完整、功能正常的pMCLacI/Neo质粒。结论 建立了在基因组中整合有pMCLacI/Neo质粒的NIH3T3细胞系;两个lacI靶基因可分别模拟哺乳动物细胞内表达基因和沉默基因的功能状态;可以将该细胞系用作研究哺乳动物细胞内表达基因和沉默基因的不同突变机理的实验模型。
, http://www.100md.com
Development of a mouse cell line containing stably integrated copies of pMCLacI/Neo plasmid: a model for studying mutations in vitro*
LU Yang LI Huaixing FU Jiliang
(Department of Medical Genetics, Second Military Medical University, Shanghai, 200433 P.R. China. E-mail:Huaixing@bigfoot.com)
【Abstract】 Objective To establish a suitable model for studying the different mechanisms of mutation between expressed and non-expressed genes in mammalian cells. Methods The NIH3T3 cells were transfected with the linearized pMCLacI/Neo DNAs by liposome-mediated transfection,and grew in the presence of G418. One drug resistant cell clone was selected to proliferate and to be analyzed with Southern blot and RT-PCR analyses on its genomic DNAs. Results (1)Multiple copies of pMCLacI/Neo plasmid DNA were intactly integrated in the genomic DNAs of the cell clone. (2) One of lac Ⅰ target genes in the integrated plasmid could be transcribed in the NIH3T3 cells while the other could not. (3) The pMCLacI/Neo plasmid DNA could be efficiently rescued from the genomic DNAs of the cell clone with the average rescue efficiency of 410 cfu/μg DNA. Conclusion The NIH3T3 cell line containing copies of a stably integrated pMCLacI/Neo has been established. The two lacI target genes in the cell line could imitate the functional states of expressed and non-expressed genes in mammalian cells respectively. The cell line will be a useful model for studying the different mechanisms of mutation between expressed and non-expressed genes in mammalian cells.
, 百拇医药
【Key words】 mutagenesis; lacI gene; NIH3T3 cells; transcription; plasmid
迄今为止,已建立了多种体外、体内突变检测系统。在这些系统中,突变靶基因都是在哺乳动物组织细胞内不转录和表达的,而人和哺乳动物细胞内许多重要的功能基因都是处于被转录和表达的活性状态。大量的研究结果表明体内被转录和表达的功能基因的DNA损伤将被优先修复。因此,在这些突变检测系统中,通过一些不表达的中性靶基因所检测到的突变规律是否代表体内一些重要的功能基因的真实情况,目前尚不清楚[1-3]。我们通过脂质体转染法建立了在基因组DNA中稳定整合有pMCLacI/Neo质粒的NIH3T3细胞系[4]。该质粒中含有两个lacI突变靶基因,其中一个在NIH3T3细胞中处于转录表达状态,而另一个则处于非转录表达状态,从而起到了模拟哺乳动物细胞内表达基因和沉默基因的功能状态的作用。该细胞系的建立为比较研究人和哺乳动物体内表达基因和沉默基因的不同突变机理提供了一个有效的实验模型。
, http://www.100md.com
1 材料和方法
1.1 主要材料 pMCLacI/Neo质粒由本室构建保种;DNA凝胶回收试剂盒(QIAquick Gel Extract Kit)购自QIAgene公司;NIH3T3源自ATCC库;DH10B宿主菌,DMEM培养基,胎牛血清(FCS),脂质体(Lipofectamin),RNA抽提试剂(TrizolTm reagent)和RT-PCR试剂盒(SuperscriptTm Preamplification system)均为GIBCO公司产品;G418是Calbiochem产品;α-32P dCTP购自北京亚辉生物技术公司。lacI基因的特异性PCR引物由Sangon生物工程公司合成,其序列为:P1:5′-AGCTTCCACAG-CAATGGCATCCTGG-3′;P2:5′-CTTTCGCGGTA-TGGCATGATAGCGC-3′能扩增出468bp长的DNA片段。
, 百拇医药 1.2 基因转染用DNA的准备 将pMCLacI/Neo质粒(图1)以Xho I酶切后进行电泳,并用QIAquick Gel Extract Kit从凝胶中回收、纯化线性化的该质粒DNA,以500 ng/μl的浓度溶于双蒸水中待用。
图1 pMCLacI/Neo质粒的结构示意图
Fig 1 Map of pMCLacI/Neo plasmid
1.3 NIH3T3细胞的转染和药物筛选[5] 将对数生长期的NIH3T3细胞以1×105~3×105个细胞/孔的密度接种至6孔培养板中,将1~2 μg线性化的pMCLacI/Neo质粒DNA通过脂质体转染入NIH3T3细胞。转染后48 h,将细胞传代培养至含G418(300 μg/ml)的DMEM培养基中,经过10 d后,未被转染的NIH3T3细胞已全部死亡,而抗性细胞开始呈集落性生长。至21 d时,抗性细胞克隆长成肉眼可见的细胞团。按照文献[6]推荐的方法挑取抗性细胞克隆并进一步扩增培养(10代以上)。
, http://www.100md.com
1.4 细胞基因组DNA的Southern杂交 收集108~109个抗性细胞用蛋白酶K法提取基因组DNA[7],取20~30 μg基因组DNA,用80U Cla I于37℃酶切16 h,按常规方法电泳、转膜后,置于68℃杂交液(7% SDS,0.5mol/L NaH2PO4,0.5mol/L Na2HPO4,10 mmol/L EDTA,1% BSA)中预杂交6 h,然后加入探针继续杂交16 h(取25 ng线性化的pMCLacI/Neo DNA作模板,采用Rediprime DNA Labeling System制备α-32P dCTP标记的探针),分别用加和未加pMCLacI/Neo质粒DNA的正常NIH3T3细胞基因组DNA作阳性和阴性对照。用洗膜液A(0.5% BSA,5% SDS,1 mmol/L EDTA,40 mmol/L Na2HPO4,40 mmol/L NaH2PO4)于室温洗膜两次共30 min,再用洗膜液B(1% SDS,1 mmol/L EDTA,40 mmol/L Na2HPO4,40 mmol/L NaH2PO4)于68℃洗30 min,最后用0.1×SSC漂洗,按常规进行压片和放射自显影。
, http://www.100md.com
1.5 细胞RT-PCR鉴定 将经以上Southern杂交鉴定呈阳性的细胞克隆接种到6孔培养板上扩增培养至细胞数量达106~107,一半细胞冻存留种,另一半采用GIBCO公司的TRIZOL试剂抽提细胞总RNA。再采用SuperscriptTm Preamplification System进行RT-PCR分析,PCR扩增按94℃ 30 s,65℃ 45 s,72℃ 1 min的条件进行循环,扩增产物经电泳观察后进行Southern杂交鉴定(其电泳、转膜和杂交过程与以上相同)。
1.6 pMCLacI/Neo质粒的回收 取10 μg经Cla I完全酶切的细胞基因组DNA,75℃处理10 min后,用双蒸水稀释至449 μl,加入50 μl 10×Buffer,1 μl(3U) T4 DNA连接酶,于16℃连接12 h。取5 μl连接环化的DNA液转化100 μl DH10B感受态细胞,涂布含X-gal并呈Ampr的LB平板,于37℃培养16~24 h后,计数平板上的菌落数并观察有无蓝色突变子出现,以确定回收效率。此外每次还随机挑取5个单菌落进行以下鉴定:一是扩增后抽取质粒DNA进行酶切鉴定;二是用X-gal和IPTG来鉴定菌落内lacI基因的功能。
, http://www.100md.com
2 结果和讨论
我们采用脂质体转染法将经Xho I酶切成线状的pMCLacI/Neo质粒导入NIH3T3细胞并加入G418进行筛选,然后将抗性细胞克隆采用Southern杂交鉴定基因组中是否整合有pMCLacI/Neo质粒。图2是其中一个呈G418抗性的细胞克隆C1的基因组DNA的Southern杂交结果,从图中可看出整合于C1细胞克隆基因组DNA中的pMCLacI/Neo质粒与阳性对照大小相同,表明该质粒没有出现明显的缺失和插入突变,并且质粒在基因组中是以多拷贝首尾串联的方式进行排列的。
图2 细胞基因组DNA的Southern杂交结果 1:正常NIH3T3
2:LC1细胞克隆;3:pMCLacI/Neo阳性对照
, 百拇医药
Fig 2 Southern blot result of C1 cell clone genomic DNAs lane 1: negative control(NIH3T3 cell genomic DNAs); lane 2:C1 cell clone; lane 3:positive control(10 μg genomic DNAs of NIH3T3 cells+10 pg pMCLacI/Neo DNAs)
图3 C1细胞克隆RT-PCR(a)和RT-PCR Southern杂交(b)结果 1:经逆转录的C1 RNA;2:未经逆转录的C1 RNA;3:系统对照mRNA; 4:正常NIH3T3 RNA; M:λ/EcoRI+HindⅢ DNA分子量标准
, http://www.100md.com
Fig 3 RT-PCR(a) and RT-PCR Southern blot(b) results of C1 cell clone lane 1:reverse transcribed; lane 2:not reverse transcribed; lane 3:system control mRNA; lane 4: negative control (NIH3T3 cell RNA);M:λ/EcoRI+HindⅢ DNA standards
为了鉴定pMCLacI/Neo质粒中受CMV启动子驱动的lacI靶基因是否在C1细胞克隆内处于表达状态,我们提取了C1细胞克隆的总RNA,并进行了RT-PCR分析,其结果见图3a。从图3a可以看出:lacI基因特异性的引物从经过逆转录的C1细胞克隆的总RNA中扩增出了468 bp长的条带,而从未经过逆转录的C1细胞克隆的总RNA以及经过逆转录的正常NIH3T3细胞的总RNA中却未扩增出任何条带(图1a)。这排除了在总RNA中有C1细胞克隆基因组DNA或其它带有lacI靶基因的DNA污染的可能,证明了在C1细胞克隆的总RNA中含有lacI靶基因的转录产物(图1a3是由该RT-PCR系统为了检测其反应效率而提供的引物和mRNA所进行的RT-PCR结果,表明整个RT-PCR体系是灵敏和有效的)。对RT-PCR扩增产物的进一步Southern杂交的结果(图3b)表明:仅C1克隆的RT-PCR扩增产物能和lacI基因的序列特异性探针杂交,进一步证实了该RT-PCR产物来源于lacI基因转录的RNA。由于该质粒在基因组DNA中的整合位点是随机的,因此确保该RNA产物只来源于受CMV启动子驱动的lacI是关系到本研究成败的一个关键性问题。由于在经Xho I酶线性化的pMCLacI/Neo质粒内,不受CMV启动子驱动的lacI靶基因编码区的5′末端是SV40A转录终止信号,而在其3′末端方向则具有来源于tk基因的转录终止信号(tkA),它们能分别终止来源于CMV启动子、tk启动子或其它内源启动子的转录,因此即使该质粒插入NIH3T3细胞内的一个内源表达基因的启动子下游,质粒上不受CMV启动子驱动的lacI靶基因也不会被转录表达,即该RNA产物只可能来源于受CMV启动子驱动的lacI靶基因。因此,在整合于C1细胞克隆基因组DNA的pMCLacI/Neo质粒内的两个lacI靶基因中,只有受CMV启动子驱动的lacI靶基因在NIH3T3细胞内处于转录表达状态,而另一个lacI靶基因则未被转录表达。
, http://www.100md.com
能否从C1细胞克隆的基因组DNA中回收出结构完整、功能正常的pMCLacI/Neo质粒,将决定该C1细胞克隆能否用于突变检测分析。我们采用了酶切环化的方法从C1细胞克隆的基因组DNA中进行了pMCLacI/Neo质粒的回收,并进行了限制性内切酶酶切结构分析和lacI靶基因在原核系统内的功能鉴定,其结果见表1、表2和图4。从表1可看出:我们成功地从/μg C1细胞克隆的基因组DNA中回收出了410个质粒;对该质粒进行限制性酶切分析发现,该质粒的结构大小和酶切图谱与pMCLacI/Neo质粒完全相同(图4);最后将该质粒转入DH10B宿主菌后涂布到LB平板上培养,并加入IPTG和X-gal进行lacI靶基因的功能鉴定,结果表明位于该质粒上的lacI基因能正确地调节lacZα基因的表达(表2),由于lacI靶基因的突变型对其野生型呈显 性,因此可以认为该质粒上两个lacI靶基因的功能都是正常的。
表1 C1细胞克隆基因组DNA中pMCLacI/Neo载体的回收效率
, 百拇医药
Table 1 Efficiency of rescuing plasmids from C1 cell clone
Origin of
DNAs
(DNA来源)
Amount of
DNAs
(DNA量)
No.of
assay
(实验次数)
Clonies
, 百拇医药
(回收菌落数)
Rescue
efficiency
(回收效率)
No.of
mutants
(突变子数)
C1 clone
100ng
2
45,37
410
, 百拇医药 0
NIH3T3
100ng
2
0,0
0
0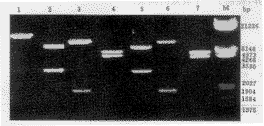
图4 从C1细胞克隆基因组DNA中回收的质粒的酶切鉴定结果 1:pMCLacI/Neo质粒DNA;2:pMCLacI/Neo/XhoI+HindⅢ;3:pMCLacI/Neo/Xba I+HindⅢ;4:pMCLacI/Neo/Rca I;5:回收质粒/XhoI+HindⅢ;6:回收质粒/Xba I+HindⅢ;7:回收质粒/Rca I;M:λ/EcoRI+HindⅢ DNA分子量标准
, 百拇医药
Fig 4 Restriction map of plasmids rescued from C1 cell clone genomic DNA M:λ/EcoR I+Hind Ⅲ DNA markers; lane 1:pMCLacI/Neo plasmids; lane 2:pMCLacI/Neo/Xho I+Hind Ⅲ; lane 3:pMCLacI/Neo/Xba I+Hind Ⅲ; lane 4:pMCLacI/Neo/Rca I; lane 5:rescued plasmids/Xho I+Hind Ⅲ; lane 6:rescued plasmids/Xha I+Hind Ⅲ; lane 7:rescued plasmids/Rca I
表2 回收质粒中lacI靶基因的功能鉴定结果
Table 2 Functional analysis of lacI target genes in the rescued plasmid
, 百拇医药
Plasmid
(质粒)
IPTG
X-gal
AmpR
Color of colonies
(菌落的颜色)
rescued plasmids/DH10B
+
+
+
blue
, http://www.100md.com
rescued plasmids/DH10B
-
+
+
white
pMCLacI/Neo/DH10B
+
+
+
blue
pMCLacI/Neo/DH10B
-
, http://www.100md.com +
+
white
blue(蓝色);white(白色)
综上所述,可以认为本研究已经成功地获得了一个在基因组中稳定整合有pMCLacI/Neo质粒的NIH3T3细胞克隆,而且从该细胞克隆的基因组DNA中回收出了结构、功能完整的pMCLacI/Neo质粒,该质粒上的一个lacI靶基因在NIH3T3细胞内处于转录表达状态,而另一个处于非转录表达状态,从而起到了模拟哺乳动物细胞内表达基因和沉默基因功能状态的作用。它的建立为研究哺乳动物细胞内表达基因和沉默基因在DNA损伤、修复、突变和癌变等方面的差异,提供了一个有效的模型。
基金项目:国家自然科学基金(39570400)
参考文献
, 百拇医药
[1]Fiedberg EC.Relationships between DNA repair and transcription. Annu Rev Biochem, 1996,65∶1-16.
[2]Wassermann K. Intragenomic heterogeneity of DNA damage formation and repair:a review of cellular responses to covalent drug DNA interaction. Crit Rev Toxicol,1994,24∶281-288.
[3]Chen RH, Maher VM.Preferential repair and strand-specific repair of Benzo[α] pyrene diol epoxide adducts in the HPRT gene of diploid human fibroblasts. Proc Natl Acad Sci U S A,1992,89∶5413-5419.
, 百拇医药
[4]Lu Y, Li HX, Fu JL. Construction of pMCLacⅠ/Neo plasmid and a new strategy for studing gene mutation. Acad J Sec Mil Med Univ, 1999,20(8)∶509-512.〔卢洋,黎怀星,傅继梁.pMCLacI/Neo质粒的构建和基因突变研究的新策略.第二军医大学学报,1999,20(8)∶509-512.〕
[5]Shih PJ, Evansta K, Schifferli K, et al.High efficiency transfection with minimal optimization using the lipofectamin plusTM reagent. Focus, 1997,19(3)∶52-56.
[6]Jiang B, Zhang YL, Zhou DY, eds. Common exprimental protocol of molecular biology, 1st. ed. Beijing:People Militury Medicine Press,1996.152-161.〔姜泊,张亚历,周殿元主编.分子生物学常用实验方法.第1版.北京:人民军医出版社,1996.152-161.〕
[7]Sambrook J, Fritsch EF, Maniatis T. eds. Molecular Cloning:A Laboratory Manual. 2nd ed.Isolation of DNA Fragments from ployaerylamide Gels.Cold Spring Harber,New York:CSH Laboratory Press,1989.6.46-6.48.〔J.萨姆布鲁克,E.F.弗里奇,T.曼尼阿蒂斯著.金冬雁,黎孟枫译.从哺乳动物细胞中分离高分子量DNA分子克隆实验指南.第2版.北京:科学出版社,1992.463-468.〕
收稿日期:1999-06-08, 百拇医药
单位:卢洋(200433 上海,第二军医大学医学遗传学教研室);黎怀星(200433 上海,第二军医大学医学遗传学教研室);傅继梁(200433 上海,第二军医大学医学遗传学教研室)
关键词:基因突变;lacI基因;NIH3T3细胞;转录;质粒
New Page 1 【摘要】 目的 建立一个用于比较研究哺乳动物细胞内表达基因和沉默基因的突变机理的实验模型。方法 以脂质体转染法将线性化的pMCLacI/Neo质粒导入NIH3T3细胞,用G418筛选,选择一个药物抗性细胞克隆进行扩增,用基因组Southern杂交,RT-PCR及RT-PCR Southern杂交进行分子鉴定。结果 (1)在此细胞克隆的基因组中整合有pMCLacI/Neo质粒;(2)该质粒上的两个lacI靶基因中,有一个在NIH3T3细胞内处于转录表达状态;(3)可以通过酶切环化的方法从阳性细胞克隆的基因组DNA中回收出结构完整、功能正常的pMCLacI/Neo质粒。结论 建立了在基因组中整合有pMCLacI/Neo质粒的NIH3T3细胞系;两个lacI靶基因可分别模拟哺乳动物细胞内表达基因和沉默基因的功能状态;可以将该细胞系用作研究哺乳动物细胞内表达基因和沉默基因的不同突变机理的实验模型。
, http://www.100md.com
Development of a mouse cell line containing stably integrated copies of pMCLacI/Neo plasmid: a model for studying mutations in vitro*
LU Yang LI Huaixing FU Jiliang
(Department of Medical Genetics, Second Military Medical University, Shanghai, 200433 P.R. China. E-mail:Huaixing@bigfoot.com)
【Abstract】 Objective To establish a suitable model for studying the different mechanisms of mutation between expressed and non-expressed genes in mammalian cells. Methods The NIH3T3 cells were transfected with the linearized pMCLacI/Neo DNAs by liposome-mediated transfection,and grew in the presence of G418. One drug resistant cell clone was selected to proliferate and to be analyzed with Southern blot and RT-PCR analyses on its genomic DNAs. Results (1)Multiple copies of pMCLacI/Neo plasmid DNA were intactly integrated in the genomic DNAs of the cell clone. (2) One of lac Ⅰ target genes in the integrated plasmid could be transcribed in the NIH3T3 cells while the other could not. (3) The pMCLacI/Neo plasmid DNA could be efficiently rescued from the genomic DNAs of the cell clone with the average rescue efficiency of 410 cfu/μg DNA. Conclusion The NIH3T3 cell line containing copies of a stably integrated pMCLacI/Neo has been established. The two lacI target genes in the cell line could imitate the functional states of expressed and non-expressed genes in mammalian cells respectively. The cell line will be a useful model for studying the different mechanisms of mutation between expressed and non-expressed genes in mammalian cells.
, 百拇医药
【Key words】 mutagenesis; lacI gene; NIH3T3 cells; transcription; plasmid
迄今为止,已建立了多种体外、体内突变检测系统。在这些系统中,突变靶基因都是在哺乳动物组织细胞内不转录和表达的,而人和哺乳动物细胞内许多重要的功能基因都是处于被转录和表达的活性状态。大量的研究结果表明体内被转录和表达的功能基因的DNA损伤将被优先修复。因此,在这些突变检测系统中,通过一些不表达的中性靶基因所检测到的突变规律是否代表体内一些重要的功能基因的真实情况,目前尚不清楚[1-3]。我们通过脂质体转染法建立了在基因组DNA中稳定整合有pMCLacI/Neo质粒的NIH3T3细胞系[4]。该质粒中含有两个lacI突变靶基因,其中一个在NIH3T3细胞中处于转录表达状态,而另一个则处于非转录表达状态,从而起到了模拟哺乳动物细胞内表达基因和沉默基因的功能状态的作用。该细胞系的建立为比较研究人和哺乳动物体内表达基因和沉默基因的不同突变机理提供了一个有效的实验模型。
, http://www.100md.com
1 材料和方法
1.1 主要材料 pMCLacI/Neo质粒由本室构建保种;DNA凝胶回收试剂盒(QIAquick Gel Extract Kit)购自QIAgene公司;NIH3T3源自ATCC库;DH10B宿主菌,DMEM培养基,胎牛血清(FCS),脂质体(Lipofectamin),RNA抽提试剂(TrizolTm reagent)和RT-PCR试剂盒(SuperscriptTm Preamplification system)均为GIBCO公司产品;G418是Calbiochem产品;α-32P dCTP购自北京亚辉生物技术公司。lacI基因的特异性PCR引物由Sangon生物工程公司合成,其序列为:P1:5′-AGCTTCCACAG-CAATGGCATCCTGG-3′;P2:5′-CTTTCGCGGTA-TGGCATGATAGCGC-3′能扩增出468bp长的DNA片段。
, 百拇医药 1.2 基因转染用DNA的准备 将pMCLacI/Neo质粒(图1)以Xho I酶切后进行电泳,并用QIAquick Gel Extract Kit从凝胶中回收、纯化线性化的该质粒DNA,以500 ng/μl的浓度溶于双蒸水中待用。

图1 pMCLacI/Neo质粒的结构示意图
Fig 1 Map of pMCLacI/Neo plasmid
1.3 NIH3T3细胞的转染和药物筛选[5] 将对数生长期的NIH3T3细胞以1×105~3×105个细胞/孔的密度接种至6孔培养板中,将1~2 μg线性化的pMCLacI/Neo质粒DNA通过脂质体转染入NIH3T3细胞。转染后48 h,将细胞传代培养至含G418(300 μg/ml)的DMEM培养基中,经过10 d后,未被转染的NIH3T3细胞已全部死亡,而抗性细胞开始呈集落性生长。至21 d时,抗性细胞克隆长成肉眼可见的细胞团。按照文献[6]推荐的方法挑取抗性细胞克隆并进一步扩增培养(10代以上)。
, http://www.100md.com
1.4 细胞基因组DNA的Southern杂交 收集108~109个抗性细胞用蛋白酶K法提取基因组DNA[7],取20~30 μg基因组DNA,用80U Cla I于37℃酶切16 h,按常规方法电泳、转膜后,置于68℃杂交液(7% SDS,0.5mol/L NaH2PO4,0.5mol/L Na2HPO4,10 mmol/L EDTA,1% BSA)中预杂交6 h,然后加入探针继续杂交16 h(取25 ng线性化的pMCLacI/Neo DNA作模板,采用Rediprime DNA Labeling System制备α-32P dCTP标记的探针),分别用加和未加pMCLacI/Neo质粒DNA的正常NIH3T3细胞基因组DNA作阳性和阴性对照。用洗膜液A(0.5% BSA,5% SDS,1 mmol/L EDTA,40 mmol/L Na2HPO4,40 mmol/L NaH2PO4)于室温洗膜两次共30 min,再用洗膜液B(1% SDS,1 mmol/L EDTA,40 mmol/L Na2HPO4,40 mmol/L NaH2PO4)于68℃洗30 min,最后用0.1×SSC漂洗,按常规进行压片和放射自显影。
, http://www.100md.com
1.5 细胞RT-PCR鉴定 将经以上Southern杂交鉴定呈阳性的细胞克隆接种到6孔培养板上扩增培养至细胞数量达106~107,一半细胞冻存留种,另一半采用GIBCO公司的TRIZOL试剂抽提细胞总RNA。再采用SuperscriptTm Preamplification System进行RT-PCR分析,PCR扩增按94℃ 30 s,65℃ 45 s,72℃ 1 min的条件进行循环,扩增产物经电泳观察后进行Southern杂交鉴定(其电泳、转膜和杂交过程与以上相同)。
1.6 pMCLacI/Neo质粒的回收 取10 μg经Cla I完全酶切的细胞基因组DNA,75℃处理10 min后,用双蒸水稀释至449 μl,加入50 μl 10×Buffer,1 μl(3U) T4 DNA连接酶,于16℃连接12 h。取5 μl连接环化的DNA液转化100 μl DH10B感受态细胞,涂布含X-gal并呈Ampr的LB平板,于37℃培养16~24 h后,计数平板上的菌落数并观察有无蓝色突变子出现,以确定回收效率。此外每次还随机挑取5个单菌落进行以下鉴定:一是扩增后抽取质粒DNA进行酶切鉴定;二是用X-gal和IPTG来鉴定菌落内lacI基因的功能。
, http://www.100md.com
2 结果和讨论
我们采用脂质体转染法将经Xho I酶切成线状的pMCLacI/Neo质粒导入NIH3T3细胞并加入G418进行筛选,然后将抗性细胞克隆采用Southern杂交鉴定基因组中是否整合有pMCLacI/Neo质粒。图2是其中一个呈G418抗性的细胞克隆C1的基因组DNA的Southern杂交结果,从图中可看出整合于C1细胞克隆基因组DNA中的pMCLacI/Neo质粒与阳性对照大小相同,表明该质粒没有出现明显的缺失和插入突变,并且质粒在基因组中是以多拷贝首尾串联的方式进行排列的。

图2 细胞基因组DNA的Southern杂交结果 1:正常NIH3T3
2:LC1细胞克隆;3:pMCLacI/Neo阳性对照
, 百拇医药
Fig 2 Southern blot result of C1 cell clone genomic DNAs lane 1: negative control(NIH3T3 cell genomic DNAs); lane 2:C1 cell clone; lane 3:positive control(10 μg genomic DNAs of NIH3T3 cells+10 pg pMCLacI/Neo DNAs)

图3 C1细胞克隆RT-PCR(a)和RT-PCR Southern杂交(b)结果 1:经逆转录的C1 RNA;2:未经逆转录的C1 RNA;3:系统对照mRNA; 4:正常NIH3T3 RNA; M:λ/EcoRI+HindⅢ DNA分子量标准
, http://www.100md.com
Fig 3 RT-PCR(a) and RT-PCR Southern blot(b) results of C1 cell clone lane 1:reverse transcribed; lane 2:not reverse transcribed; lane 3:system control mRNA; lane 4: negative control (NIH3T3 cell RNA);M:λ/EcoRI+HindⅢ DNA standards
为了鉴定pMCLacI/Neo质粒中受CMV启动子驱动的lacI靶基因是否在C1细胞克隆内处于表达状态,我们提取了C1细胞克隆的总RNA,并进行了RT-PCR分析,其结果见图3a。从图3a可以看出:lacI基因特异性的引物从经过逆转录的C1细胞克隆的总RNA中扩增出了468 bp长的条带,而从未经过逆转录的C1细胞克隆的总RNA以及经过逆转录的正常NIH3T3细胞的总RNA中却未扩增出任何条带(图1a)。这排除了在总RNA中有C1细胞克隆基因组DNA或其它带有lacI靶基因的DNA污染的可能,证明了在C1细胞克隆的总RNA中含有lacI靶基因的转录产物(图1a3是由该RT-PCR系统为了检测其反应效率而提供的引物和mRNA所进行的RT-PCR结果,表明整个RT-PCR体系是灵敏和有效的)。对RT-PCR扩增产物的进一步Southern杂交的结果(图3b)表明:仅C1克隆的RT-PCR扩增产物能和lacI基因的序列特异性探针杂交,进一步证实了该RT-PCR产物来源于lacI基因转录的RNA。由于该质粒在基因组DNA中的整合位点是随机的,因此确保该RNA产物只来源于受CMV启动子驱动的lacI是关系到本研究成败的一个关键性问题。由于在经Xho I酶线性化的pMCLacI/Neo质粒内,不受CMV启动子驱动的lacI靶基因编码区的5′末端是SV40A转录终止信号,而在其3′末端方向则具有来源于tk基因的转录终止信号(tkA),它们能分别终止来源于CMV启动子、tk启动子或其它内源启动子的转录,因此即使该质粒插入NIH3T3细胞内的一个内源表达基因的启动子下游,质粒上不受CMV启动子驱动的lacI靶基因也不会被转录表达,即该RNA产物只可能来源于受CMV启动子驱动的lacI靶基因。因此,在整合于C1细胞克隆基因组DNA的pMCLacI/Neo质粒内的两个lacI靶基因中,只有受CMV启动子驱动的lacI靶基因在NIH3T3细胞内处于转录表达状态,而另一个lacI靶基因则未被转录表达。
, http://www.100md.com
能否从C1细胞克隆的基因组DNA中回收出结构完整、功能正常的pMCLacI/Neo质粒,将决定该C1细胞克隆能否用于突变检测分析。我们采用了酶切环化的方法从C1细胞克隆的基因组DNA中进行了pMCLacI/Neo质粒的回收,并进行了限制性内切酶酶切结构分析和lacI靶基因在原核系统内的功能鉴定,其结果见表1、表2和图4。从表1可看出:我们成功地从/μg C1细胞克隆的基因组DNA中回收出了410个质粒;对该质粒进行限制性酶切分析发现,该质粒的结构大小和酶切图谱与pMCLacI/Neo质粒完全相同(图4);最后将该质粒转入DH10B宿主菌后涂布到LB平板上培养,并加入IPTG和X-gal进行lacI靶基因的功能鉴定,结果表明位于该质粒上的lacI基因能正确地调节lacZα基因的表达(表2),由于lacI靶基因的突变型对其野生型呈显 性,因此可以认为该质粒上两个lacI靶基因的功能都是正常的。
表1 C1细胞克隆基因组DNA中pMCLacI/Neo载体的回收效率
, 百拇医药
Table 1 Efficiency of rescuing plasmids from C1 cell clone
Origin of
DNAs
(DNA来源)
Amount of
DNAs
(DNA量)
No.of
assay
(实验次数)
Clonies
, 百拇医药
(回收菌落数)
Rescue
efficiency
(回收效率)
No.of
mutants
(突变子数)
C1 clone
100ng
2
45,37
410
, 百拇医药 0
NIH3T3
100ng
2
0,0
0
0

图4 从C1细胞克隆基因组DNA中回收的质粒的酶切鉴定结果 1:pMCLacI/Neo质粒DNA;2:pMCLacI/Neo/XhoI+HindⅢ;3:pMCLacI/Neo/Xba I+HindⅢ;4:pMCLacI/Neo/Rca I;5:回收质粒/XhoI+HindⅢ;6:回收质粒/Xba I+HindⅢ;7:回收质粒/Rca I;M:λ/EcoRI+HindⅢ DNA分子量标准
, 百拇医药
Fig 4 Restriction map of plasmids rescued from C1 cell clone genomic DNA M:λ/EcoR I+Hind Ⅲ DNA markers; lane 1:pMCLacI/Neo plasmids; lane 2:pMCLacI/Neo/Xho I+Hind Ⅲ; lane 3:pMCLacI/Neo/Xba I+Hind Ⅲ; lane 4:pMCLacI/Neo/Rca I; lane 5:rescued plasmids/Xho I+Hind Ⅲ; lane 6:rescued plasmids/Xha I+Hind Ⅲ; lane 7:rescued plasmids/Rca I
表2 回收质粒中lacI靶基因的功能鉴定结果
Table 2 Functional analysis of lacI target genes in the rescued plasmid
, 百拇医药
Plasmid
(质粒)
IPTG
X-gal
AmpR
Color of colonies
(菌落的颜色)
rescued plasmids/DH10B
+
+
+
blue
, http://www.100md.com
rescued plasmids/DH10B
-
+
+
white
pMCLacI/Neo/DH10B
+
+
+
blue
pMCLacI/Neo/DH10B
-
, http://www.100md.com +
+
white
blue(蓝色);white(白色)
综上所述,可以认为本研究已经成功地获得了一个在基因组中稳定整合有pMCLacI/Neo质粒的NIH3T3细胞克隆,而且从该细胞克隆的基因组DNA中回收出了结构、功能完整的pMCLacI/Neo质粒,该质粒上的一个lacI靶基因在NIH3T3细胞内处于转录表达状态,而另一个处于非转录表达状态,从而起到了模拟哺乳动物细胞内表达基因和沉默基因功能状态的作用。它的建立为研究哺乳动物细胞内表达基因和沉默基因在DNA损伤、修复、突变和癌变等方面的差异,提供了一个有效的模型。
基金项目:国家自然科学基金(39570400)
参考文献
, 百拇医药
[1]Fiedberg EC.Relationships between DNA repair and transcription. Annu Rev Biochem, 1996,65∶1-16.
[2]Wassermann K. Intragenomic heterogeneity of DNA damage formation and repair:a review of cellular responses to covalent drug DNA interaction. Crit Rev Toxicol,1994,24∶281-288.
[3]Chen RH, Maher VM.Preferential repair and strand-specific repair of Benzo[α] pyrene diol epoxide adducts in the HPRT gene of diploid human fibroblasts. Proc Natl Acad Sci U S A,1992,89∶5413-5419.
, 百拇医药
[4]Lu Y, Li HX, Fu JL. Construction of pMCLacⅠ/Neo plasmid and a new strategy for studing gene mutation. Acad J Sec Mil Med Univ, 1999,20(8)∶509-512.〔卢洋,黎怀星,傅继梁.pMCLacI/Neo质粒的构建和基因突变研究的新策略.第二军医大学学报,1999,20(8)∶509-512.〕
[5]Shih PJ, Evansta K, Schifferli K, et al.High efficiency transfection with minimal optimization using the lipofectamin plusTM reagent. Focus, 1997,19(3)∶52-56.
[6]Jiang B, Zhang YL, Zhou DY, eds. Common exprimental protocol of molecular biology, 1st. ed. Beijing:People Militury Medicine Press,1996.152-161.〔姜泊,张亚历,周殿元主编.分子生物学常用实验方法.第1版.北京:人民军医出版社,1996.152-161.〕
[7]Sambrook J, Fritsch EF, Maniatis T. eds. Molecular Cloning:A Laboratory Manual. 2nd ed.Isolation of DNA Fragments from ployaerylamide Gels.Cold Spring Harber,New York:CSH Laboratory Press,1989.6.46-6.48.〔J.萨姆布鲁克,E.F.弗里奇,T.曼尼阿蒂斯著.金冬雁,黎孟枫译.从哺乳动物细胞中分离高分子量DNA分子克隆实验指南.第2版.北京:科学出版社,1992.463-468.〕
收稿日期:1999-06-08, 百拇医药