甲磺酸去铁胺对抗庆大霉素耳毒性的实验研究
作者:陈阳 王锦玲 黄维国 乔莉 刘顺利 稽宪生
单位:第四军医大学西京医院耳鼻咽喉科(西安 710032)
关键词:庆大霉素;耳毒性;去铁胺;预防
听力学及言语疾病杂志990309
【摘要】 目的 观察铁螯合剂――甲磺酸去铁胺(deferoxamine mesylate,DFO)对抗庆大霉素(gentamicin,GM)耳毒性的作用。方法 将豚鼠随机分为GM组、DFO组、GM+DFO组及对照组,采用听性脑干反应(ABR)、耳蜗铺片及透射电镜技术,观察用药前后听阈及形态学改变,并检测DFO对庆大霉素血药浓度的影响。结果 GM组8 kHz ABR阈值逐渐升高40~60 dB;GM+DFO组阈移为15~25 dB,差异显著(P<0.05)。高频听阈损伤明显比低频更重(P<0.01)。形态学变化与听力变化平行。DFO对庆大霉素血药浓度没有影响。结论 证实DFO能有效减轻GM的耳毒性作用,DFO可能成为预防庆大霉素耳毒性的有效药物。
, http://www.100md.com
Study of Deferoxamine Protection Against Gentamicin Ototoxicity
Chen Yang,Wang Jinling,Huang Weiguo,et al.
(Department of Otolaryngology,Xijing Hospital FourthMillitary Medical University,Xi'an, 710032)
【Abstract】 Objective In order to study the prevention of gentamicin(GM) ototoxicity by deferoxamine mesylate(DFO) in guinea pig.Methods Auditory brainstem response(ABR) and cochlear preparation transmision electron microscope were used to evaluate effects on hearing threshold and morphology.Serum levels of GM was also tested.It was comprised of four groups of eight animals each in which GM and DFO was tested alone and in combination,besides control group.Results GM group developed a progressive threshold shift reaching 40~60 dB at 8 kHz.GM+DFO group showed the threshold shift to 15~25 dB(P<0.05).Injury in high frequency was significantly more severe than that in low frequency(P<0.01).Morphological results were consistant with functional results.DFO did not affect serum levels of GM.Conclusion These results suggest that DFO may be a promising therapeutic agent to reduce gentamicin ototoxicity.
, http://www.100md.com
【Key words】 Gentamicin Ototoxicity Deferoxamine Prevention
氨基糖甙类抗生素的耳毒性已广为人知,其作用机理至今仍在研讨中。由于这类药物对革兰氏阴性杆菌具有较强的杀菌作用,目前仍被广泛应用,因此,除了要求临床医师注意合理用药、严禁滥用耳毒性抗生素外,积极研究有效的拮抗剂,减轻其耳毒作用仍十分必要。最新研究表明,庆大霉素(gentamicin,GM)耳毒性作用是由于庆大霉素进入体内后形成庆大霉素―铁复合物产生的自由基损伤毛细胞致聋,采用甲磺酸去铁胺(deferoxamine mesylate, DFO)竟争游离铁,可预防庆大霉素耳毒性作用[1,2]。本实验通过ABR检测、耳蜗铺片及透射电镜技术,观察豚鼠应用GM及DFO后听阈及耳蜗毛细胞、血管纹的改变,以探讨DFO对抗GM的耳毒性作用。
1 材料与方法
1.1 实验动物 耳廓反射正常的健康雄性杂色豚鼠32只,体重250~350g,随机分成4组,每组8只,GM组:硫酸庆大霉素(西北第二合成药厂生产,批号970818)120 mg/kg皮下注射,每天一次,连续19天;DFO组:DFO(美国密西根大学医学中心Kresge听力研究所提供,美国Sigma公司生产)100 mg/kg皮下注射,每天二次,间隔4小时,连续19天;GM+DFO组:第一次DFO和GM同时注射,间隔4小时第二次注射DFO,剂量同上;对照组:生理盐水等量皮下注射,每天一次,连续19天。动物实验期间每天秤体重以调整药量。用药前及用药后第9天、19天、4周、6周检测ABR,第4次测ABR后每组2只豚鼠断头活杀。一耳供透射电镜观察耳蜗螺旋器和血管纹,另一耳供光镜观察耳蜗铺片。
, http://www.100md.com
1.2 ABR听阈检测 动物在戊巴比妥钠40 mg/kg腹腔注射麻醉后,针型记录电极置刺激耳外耳道口后上皮下,参考电极置前额正中皮下,鼻尖接地。用SS-1型声刺激器,286计算机自动采样,采用短音(Tone pip,1、2、4、8 kHz)刺激,声输出范围0~100 dB SPL,间隔75 ms,扫描时间20 ms,叠加256次,带通滤波80~1500 Hz,在屏蔽隔音室内常规测试。
1.3 透射电镜标本制备 动物断头处死,听泡置2.5%戊二醛内,解剖显微镜下摘除镫骨,刺破圆窗,挑开蜗顶,灌流固定后浸渍固定24小时,磷酸缓冲液漂洗后解剖标本,取出各圈基底膜及血管纹,1%饿酸后固定,丙酮脱水,环氧树脂包埋,超薄切片,铀铅染色。
1.4 耳蜗硬铺片标本制备 动物活杀断头处死,取出听泡,用尖针在蜗尖刺一小孔,使镫骨脱位,刺破圆窗;用0.5%AgNO3(4℃)灌流浸泡15 min;0.1 mol/L的磷酸缓冲液(pH=7.4)漂洗;2.5%戊二醛固定2 h,爆光40~60 min,再置2.5%戊二醛固定液(4℃)24 h,解剖显微镜下挑开骨壳,去除血管纹、螺旋韧带、前庭膜、盖膜,分离各圈基底膜,甘油封片。
, http://www.100md.com
1.5 微生物纸片扩散法测定庆大霉素血药浓度[3] GM组和GM+DFO组动物第9天和19天注射庆大霉素后1小时剪爪取血,测定血清抑菌环直径,再查标准曲线图,得出血清庆大霉素浓度。
2 结果
2.1 实验中GM组两只动物分别于用药第11天和19天死亡,死前均消瘦、耳廓反射消失、厌食、呆滞、无力。GM+DFO组、DFO组和对照组中无死亡。GM组动物体重比对照组明显减轻(P<0.05),停药后恢复体重增长;而GM+DFO组、DFO组和对照组之间无明显差异(P>0.05)。
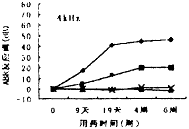
2.2 ABR 检测 用药后各组动物ABR结果见图1。豚鼠ABR以Ⅲ波为主波,以此为观察指标。虽然实验动物对药物的反应具有一定的个体差异性,但GM+DFO组听阈损害较GM组明显减轻。用药后第4周,GM组1 kHz及8 kHz阈值分别平均升高44±18 dB及60±17 dB,而GM+DFO组则分别平均升高16±5 dB及21±5 dB,两组差异显著(P<0.05),且损伤具有频率差异,高频明显比低频的损伤重(P<0.01)。DFO组和对照组阈值变化不明显(P>0.05)。



, 百拇医药
图1 用药后各组ABR听阈变化
2.3 耳蜗铺片及透射电镜所见 耳蜗铺片显示GM组用药后三排外毛细胞损伤明显,且从顶回至底回逐渐加重,外毛细胞损伤较内毛细胞重(图2);透射电镜见GM组耳蜗外毛细胞胞浆细胞器减少,呈空泡变性(图3);内毛细胞出现较多多泡体结构(图4);传入神经突触线粒体空化(图5);血管纹边缘细胞突起中的少数线粒体亦出现嵴减少、空化(图6);GM+DFO组则显示损伤较轻(图7,8,9)。DFO组与对照组用药前后改变不明显。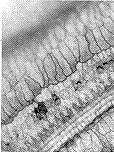



图2 GM组第二圈外毛细胞损伤明显;内毛细胞亦见损伤
, 百拇医药
图3 GM组外毛细胞胞浆稀疏呈空泡变性,胞核浓缩,TEM x2925
图4 GM组内毛细胞中形成许多多泡体,TEM x2925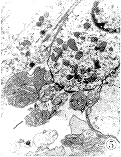

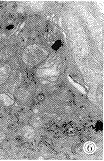

图5 GM组传人神经突触线粒体空化,TEM x3660
图6 GM组血管纹边缘细胞线粒体部分空化,TEM x9900
图7 GM+ DFO组血管纹边缘细胞损伤较轻,TEMx3795



, 百拇医药
图8 GM+ DFO组第二圈外毛细胞损伤较轻,内毛细胞无缺失图9 GM+ DFO组传人神经突触基本正常,TEM x52852.4 GM血清浓度检测 GM组和GM+DFO组动物的血清庆大霉素浓度没有显著差别(P>0.05)。第9天测定值分别为(75±12)mg/L和(80±9)ml/L,第19天测定值分别为(110±12(mg/L和(114±9)mg/L。
3 讨论
氨基糖甙类抗生素的耳毒作用机理尚未完全明了。有关学说很多,其中之一为自由基学说,1981年Pierson等[4]报道自由基清除剂WR2721可延缓卡那霉素耳中毒的发生并减轻听力损失程度,但随后各家实验的结果不相一致,不同的自由基清除剂治疗得到不同的结果。Garets[5]和Lautermann[6]都证实谷氨酰胺可减轻庆大霉素耳毒性,但仅对疾病状态下或营养缺乏的动物有效,这表明应用自由基清除剂防护庆大霉素耳毒性作用的不确定性。最近Priuska[7]证明庆大霉素的耳毒作用是通过与游离铁离子形成复合物,催化产生自由基的反应而发挥耳毒性作用,并报道采用DFO螯合游离铁,减少庆大霉素-铁复合物而预防庆大霉素耳中毒。
, 百拇医药
DFO是一种螯合剂,主要与铁离子和三价铝离子形成复合物,其复合物形成常数分别为1031和1025。由于其螯合特性,无论是游离的、或者与铁蛋白和含铁血黄素结合的铁离子,DFO均能与之结合,形成铁胺螯合物。DFO还可动员和螯合与组织结合之铝离子,形成铝胺螯合物。这两种复合物通过胆汁和尿途径完全排泄,因此而减少铁或铝在器官的病理性沉积。临床用于治疗输血所致的含铁血黄素沉着病和地中海贫血等急、慢性铁中毒[8]。临床曾报道DFO作长期治疗时,尤其所用剂量超过推荐剂量和/或其剂量未按低血清铁蛋白或血清铝浓度而调整时,可引起视力、听力障碍,也有研究证明其长期服用的安全性[9]。该实验所用庆大霉素为临床的20倍,而DFO只是临床剂量的2~4倍,结果显示GM+DFO组听阈升高幅度较GM组明显减轻,差异显著(P<0.05)与Song[1,2]的结果一致。听力损害以高频尤为敏感,8 kHz首先出现阈值升高,且损失较中、低频为甚(P<0.01)。耳蜗毛细胞的损害与阈值升高的程度相平行。DFO组听阈在整个实验过程中保持稳定,表明其安全无毒性。
, 百拇医药
实验结果表明DFO对庆大霉素的耳毒性具有明显的对抗作用,而且这种对抗作用不影响庆大霉素的血药浓度,仍能保持庆大霉素的抗菌效力。至于DFO预防庆大霉素耳毒性的作用机理有待进一步研究。
作者简介:王锦玲 指导者
4 参考文献
1 Song BB,Schacht J.Variable efficacy of radical scavengers and iron chelators to attenuate gentamicin ototoxicity in giunea pig in vivo.Hear Res,1996,94:87.
2 Song BB,Anderson DJ,Schacht J.Protection from gentamicin ototoxicity by iron chelators in guinea pig in vivo.J Pharmacol Exp Ther,1997,282:369.
, 百拇医药
3 Sabath LD,Matsen Jm.Assay of antimicrobial agents.In:Manual of Clinical Microbiology.Ed2.Lennethe EH,Spaulding EH,Truant JP.eds.American Society for Microbiology.Washington,1974.428~430.
4 Pierson Mg,Moller Ar.Prophylaxis of kanamycin-induced ototoxicity by a radioprotectant.Hear Res.1981,4:79.
5 Garets SL,Altschuler RA,Schacht J.Attenuation of gentamicin ototoxicity by glutathione in the guinea pig in vivo.Hear Res,1994,77:81.
, http://www.100md.com
6 Lautermann J,McLaren J,Schacht J.Glutathione protection against gentamicin ototoxicity depends on nutritional status.Hear Res,1995,86:15.
7 Priuska E,Schacht J.Formation of free radicals by gentamicin and iron and evidence for an iron-gentamicin complex.Biochem Pharmacol,1995,50:1749.
8 Hershko C.Iron chelators in medicine.Molec Asp Med,1992,13:113.
9 Shirane M,Harrison RV.The effects of deferoxamine mesylate and hypoxia on the cochlea.Acta otolaryngol(Stockh),1987,16:334.
(1998-09-07收稿 1998-12-15修回), http://www.100md.com
单位:第四军医大学西京医院耳鼻咽喉科(西安 710032)
关键词:庆大霉素;耳毒性;去铁胺;预防
听力学及言语疾病杂志990309
【摘要】 目的 观察铁螯合剂――甲磺酸去铁胺(deferoxamine mesylate,DFO)对抗庆大霉素(gentamicin,GM)耳毒性的作用。方法 将豚鼠随机分为GM组、DFO组、GM+DFO组及对照组,采用听性脑干反应(ABR)、耳蜗铺片及透射电镜技术,观察用药前后听阈及形态学改变,并检测DFO对庆大霉素血药浓度的影响。结果 GM组8 kHz ABR阈值逐渐升高40~60 dB;GM+DFO组阈移为15~25 dB,差异显著(P<0.05)。高频听阈损伤明显比低频更重(P<0.01)。形态学变化与听力变化平行。DFO对庆大霉素血药浓度没有影响。结论 证实DFO能有效减轻GM的耳毒性作用,DFO可能成为预防庆大霉素耳毒性的有效药物。
, http://www.100md.com
Study of Deferoxamine Protection Against Gentamicin Ototoxicity
Chen Yang,Wang Jinling,Huang Weiguo,et al.
(Department of Otolaryngology,Xijing Hospital FourthMillitary Medical University,Xi'an, 710032)
【Abstract】 Objective In order to study the prevention of gentamicin(GM) ototoxicity by deferoxamine mesylate(DFO) in guinea pig.Methods Auditory brainstem response(ABR) and cochlear preparation transmision electron microscope were used to evaluate effects on hearing threshold and morphology.Serum levels of GM was also tested.It was comprised of four groups of eight animals each in which GM and DFO was tested alone and in combination,besides control group.Results GM group developed a progressive threshold shift reaching 40~60 dB at 8 kHz.GM+DFO group showed the threshold shift to 15~25 dB(P<0.05).Injury in high frequency was significantly more severe than that in low frequency(P<0.01).Morphological results were consistant with functional results.DFO did not affect serum levels of GM.Conclusion These results suggest that DFO may be a promising therapeutic agent to reduce gentamicin ototoxicity.
, http://www.100md.com
【Key words】 Gentamicin Ototoxicity Deferoxamine Prevention
氨基糖甙类抗生素的耳毒性已广为人知,其作用机理至今仍在研讨中。由于这类药物对革兰氏阴性杆菌具有较强的杀菌作用,目前仍被广泛应用,因此,除了要求临床医师注意合理用药、严禁滥用耳毒性抗生素外,积极研究有效的拮抗剂,减轻其耳毒作用仍十分必要。最新研究表明,庆大霉素(gentamicin,GM)耳毒性作用是由于庆大霉素进入体内后形成庆大霉素―铁复合物产生的自由基损伤毛细胞致聋,采用甲磺酸去铁胺(deferoxamine mesylate, DFO)竟争游离铁,可预防庆大霉素耳毒性作用[1,2]。本实验通过ABR检测、耳蜗铺片及透射电镜技术,观察豚鼠应用GM及DFO后听阈及耳蜗毛细胞、血管纹的改变,以探讨DFO对抗GM的耳毒性作用。
1 材料与方法
1.1 实验动物 耳廓反射正常的健康雄性杂色豚鼠32只,体重250~350g,随机分成4组,每组8只,GM组:硫酸庆大霉素(西北第二合成药厂生产,批号970818)120 mg/kg皮下注射,每天一次,连续19天;DFO组:DFO(美国密西根大学医学中心Kresge听力研究所提供,美国Sigma公司生产)100 mg/kg皮下注射,每天二次,间隔4小时,连续19天;GM+DFO组:第一次DFO和GM同时注射,间隔4小时第二次注射DFO,剂量同上;对照组:生理盐水等量皮下注射,每天一次,连续19天。动物实验期间每天秤体重以调整药量。用药前及用药后第9天、19天、4周、6周检测ABR,第4次测ABR后每组2只豚鼠断头活杀。一耳供透射电镜观察耳蜗螺旋器和血管纹,另一耳供光镜观察耳蜗铺片。
, http://www.100md.com
1.2 ABR听阈检测 动物在戊巴比妥钠40 mg/kg腹腔注射麻醉后,针型记录电极置刺激耳外耳道口后上皮下,参考电极置前额正中皮下,鼻尖接地。用SS-1型声刺激器,286计算机自动采样,采用短音(Tone pip,1、2、4、8 kHz)刺激,声输出范围0~100 dB SPL,间隔75 ms,扫描时间20 ms,叠加256次,带通滤波80~1500 Hz,在屏蔽隔音室内常规测试。
1.3 透射电镜标本制备 动物断头处死,听泡置2.5%戊二醛内,解剖显微镜下摘除镫骨,刺破圆窗,挑开蜗顶,灌流固定后浸渍固定24小时,磷酸缓冲液漂洗后解剖标本,取出各圈基底膜及血管纹,1%饿酸后固定,丙酮脱水,环氧树脂包埋,超薄切片,铀铅染色。
1.4 耳蜗硬铺片标本制备 动物活杀断头处死,取出听泡,用尖针在蜗尖刺一小孔,使镫骨脱位,刺破圆窗;用0.5%AgNO3(4℃)灌流浸泡15 min;0.1 mol/L的磷酸缓冲液(pH=7.4)漂洗;2.5%戊二醛固定2 h,爆光40~60 min,再置2.5%戊二醛固定液(4℃)24 h,解剖显微镜下挑开骨壳,去除血管纹、螺旋韧带、前庭膜、盖膜,分离各圈基底膜,甘油封片。
, http://www.100md.com
1.5 微生物纸片扩散法测定庆大霉素血药浓度[3] GM组和GM+DFO组动物第9天和19天注射庆大霉素后1小时剪爪取血,测定血清抑菌环直径,再查标准曲线图,得出血清庆大霉素浓度。
2 结果
2.1 实验中GM组两只动物分别于用药第11天和19天死亡,死前均消瘦、耳廓反射消失、厌食、呆滞、无力。GM+DFO组、DFO组和对照组中无死亡。GM组动物体重比对照组明显减轻(P<0.05),停药后恢复体重增长;而GM+DFO组、DFO组和对照组之间无明显差异(P>0.05)。
2.2 ABR 检测 用药后各组动物ABR结果见图1。豚鼠ABR以Ⅲ波为主波,以此为观察指标。虽然实验动物对药物的反应具有一定的个体差异性,但GM+DFO组听阈损害较GM组明显减轻。用药后第4周,GM组1 kHz及8 kHz阈值分别平均升高44±18 dB及60±17 dB,而GM+DFO组则分别平均升高16±5 dB及21±5 dB,两组差异显著(P<0.05),且损伤具有频率差异,高频明显比低频的损伤重(P<0.01)。DFO组和对照组阈值变化不明显(P>0.05)。





, 百拇医药
图1 用药后各组ABR听阈变化
2.3 耳蜗铺片及透射电镜所见 耳蜗铺片显示GM组用药后三排外毛细胞损伤明显,且从顶回至底回逐渐加重,外毛细胞损伤较内毛细胞重(图2);透射电镜见GM组耳蜗外毛细胞胞浆细胞器减少,呈空泡变性(图3);内毛细胞出现较多多泡体结构(图4);传入神经突触线粒体空化(图5);血管纹边缘细胞突起中的少数线粒体亦出现嵴减少、空化(图6);GM+DFO组则显示损伤较轻(图7,8,9)。DFO组与对照组用药前后改变不明显。




图2 GM组第二圈外毛细胞损伤明显;内毛细胞亦见损伤
, 百拇医药
图3 GM组外毛细胞胞浆稀疏呈空泡变性,胞核浓缩,TEM x2925
图4 GM组内毛细胞中形成许多多泡体,TEM x2925




图5 GM组传人神经突触线粒体空化,TEM x3660
图6 GM组血管纹边缘细胞线粒体部分空化,TEM x9900
图7 GM+ DFO组血管纹边缘细胞损伤较轻,TEMx3795




, 百拇医药
图8 GM+ DFO组第二圈外毛细胞损伤较轻,内毛细胞无缺失图9 GM+ DFO组传人神经突触基本正常,TEM x52852.4 GM血清浓度检测 GM组和GM+DFO组动物的血清庆大霉素浓度没有显著差别(P>0.05)。第9天测定值分别为(75±12)mg/L和(80±9)ml/L,第19天测定值分别为(110±12(mg/L和(114±9)mg/L。
3 讨论
氨基糖甙类抗生素的耳毒作用机理尚未完全明了。有关学说很多,其中之一为自由基学说,1981年Pierson等[4]报道自由基清除剂WR2721可延缓卡那霉素耳中毒的发生并减轻听力损失程度,但随后各家实验的结果不相一致,不同的自由基清除剂治疗得到不同的结果。Garets[5]和Lautermann[6]都证实谷氨酰胺可减轻庆大霉素耳毒性,但仅对疾病状态下或营养缺乏的动物有效,这表明应用自由基清除剂防护庆大霉素耳毒性作用的不确定性。最近Priuska[7]证明庆大霉素的耳毒作用是通过与游离铁离子形成复合物,催化产生自由基的反应而发挥耳毒性作用,并报道采用DFO螯合游离铁,减少庆大霉素-铁复合物而预防庆大霉素耳中毒。
, 百拇医药
DFO是一种螯合剂,主要与铁离子和三价铝离子形成复合物,其复合物形成常数分别为1031和1025。由于其螯合特性,无论是游离的、或者与铁蛋白和含铁血黄素结合的铁离子,DFO均能与之结合,形成铁胺螯合物。DFO还可动员和螯合与组织结合之铝离子,形成铝胺螯合物。这两种复合物通过胆汁和尿途径完全排泄,因此而减少铁或铝在器官的病理性沉积。临床用于治疗输血所致的含铁血黄素沉着病和地中海贫血等急、慢性铁中毒[8]。临床曾报道DFO作长期治疗时,尤其所用剂量超过推荐剂量和/或其剂量未按低血清铁蛋白或血清铝浓度而调整时,可引起视力、听力障碍,也有研究证明其长期服用的安全性[9]。该实验所用庆大霉素为临床的20倍,而DFO只是临床剂量的2~4倍,结果显示GM+DFO组听阈升高幅度较GM组明显减轻,差异显著(P<0.05)与Song[1,2]的结果一致。听力损害以高频尤为敏感,8 kHz首先出现阈值升高,且损失较中、低频为甚(P<0.01)。耳蜗毛细胞的损害与阈值升高的程度相平行。DFO组听阈在整个实验过程中保持稳定,表明其安全无毒性。
, 百拇医药
实验结果表明DFO对庆大霉素的耳毒性具有明显的对抗作用,而且这种对抗作用不影响庆大霉素的血药浓度,仍能保持庆大霉素的抗菌效力。至于DFO预防庆大霉素耳毒性的作用机理有待进一步研究。
作者简介:王锦玲 指导者
4 参考文献
1 Song BB,Schacht J.Variable efficacy of radical scavengers and iron chelators to attenuate gentamicin ototoxicity in giunea pig in vivo.Hear Res,1996,94:87.
2 Song BB,Anderson DJ,Schacht J.Protection from gentamicin ototoxicity by iron chelators in guinea pig in vivo.J Pharmacol Exp Ther,1997,282:369.
, 百拇医药
3 Sabath LD,Matsen Jm.Assay of antimicrobial agents.In:Manual of Clinical Microbiology.Ed2.Lennethe EH,Spaulding EH,Truant JP.eds.American Society for Microbiology.Washington,1974.428~430.
4 Pierson Mg,Moller Ar.Prophylaxis of kanamycin-induced ototoxicity by a radioprotectant.Hear Res.1981,4:79.
5 Garets SL,Altschuler RA,Schacht J.Attenuation of gentamicin ototoxicity by glutathione in the guinea pig in vivo.Hear Res,1994,77:81.
, http://www.100md.com
6 Lautermann J,McLaren J,Schacht J.Glutathione protection against gentamicin ototoxicity depends on nutritional status.Hear Res,1995,86:15.
7 Priuska E,Schacht J.Formation of free radicals by gentamicin and iron and evidence for an iron-gentamicin complex.Biochem Pharmacol,1995,50:1749.
8 Hershko C.Iron chelators in medicine.Molec Asp Med,1992,13:113.
9 Shirane M,Harrison RV.The effects of deferoxamine mesylate and hypoxia on the cochlea.Acta otolaryngol(Stockh),1987,16:334.
(1998-09-07收稿 1998-12-15修回), http://www.100md.com