高效液相色谱法测定利福平血药浓度
作者:支爱玉1 李玉萍1 李东2 方芳2
单位:1 温州医学院附一院(325000); 2 温州医学院检验系(325027)
关键词:
温州医学院学报990120 利福平(RFP)虽是一种广谱抗生素,但其血药浓度个体差异很大,且属肝药酶诱导剂,长期服用可引起t1/2减少,血药浓度降低[1],故对该药血浓度监测有重要意义。目前国内测定利福平血药浓度的方法主要为薄层法[2,3]和紫外分光法[5],但两者在灵敏度和特异性上都尚不尽如人意。我们发明的高效液相色谱测定法,具有灵敏度高、特异性好、用血量少的优点。
1 材料和方法
, 百拇医药
1.1 仪器与试剂:美国Beckman 332型高效液相色谱仪;日本岛津UV2201紫外可见分光光度计;利福平(上海福达制药有限公司)和卡马西平(CBZ,上海黄河制药厂赠送);二氯甲烷、磷酸氢二钠、甲醇、二乙胺均为分析纯。
1.2 溶液配制:分别精确称取RFP、CBZ适量,加甲醇溶解并稀释成1000mg/L标准储备液,再将CBZ用甲醇稀释至50mg/L作为内标。
1.3 色谱条件: YWG—C18柱(4.6mm×250mm, 大连化物所), 流动相为甲醇—二乙胺—水溶液(75∶0.04∶25,V/V),流速1.0ml/min,检测波长254nm,灵敏度0.020AUFS,纸速2mm/min。
1.4 实验方法:取血清0.25ml,加内标25μl、0.2mol/L磷酸氢二钠250μl、二氯甲烷2.0ml,轻轻振摇1min,然后以4000RPM离心5min,弃上层水相,取有机相1.6ml置于尖底塑料离心管内,避光氮气吹干,残渣用流动相100μl溶解,取20μl进样。
, 百拇医药
2 实验结果
2.1 色谱图:在本法色谱条件下,RFP保留时间为7min,CBZ保留时间为5min,其代谢产物由于无标准品,未能定量;空白血清无干扰。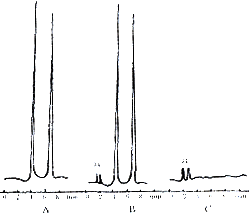 附图 利福平血药浓度测定色谱图
附图 利福平血药浓度测定色谱图
A.纯标准 B.病人血清 C.无药血清(不加内标)
1.CBZ(内标) 2.RFP 3.4.杂峰
2.2 标准曲线制备:准确吸取RFP标准储备液6份于具塞磨口刻度试管中,氮气吹干,加入正常人血清,混匀,RFP浓度分别配成0.2μg/ml、0.5μg/ml、1.0μg/ml、3.0μg/ml、6.0μg/ml、12.0μg/ml。按“实验方法”操作进样。结果,药物与内标峰高比(y)及药物浓度(x)线性良好。回归方程为:y=0.175x+0.013,相关系数r=0.9991。
, 百拇医药
2.3 回收率及精密度试验:取正常血清三份加入RFP标准液,分别配成每RFP2.7μg/ml、5.5μg/ml、10.8μg/ml,按实验方法操作;用回归方程计算出回收浓度和回收率分别为97.1%、99.6%、98.7%。再取10.8μg/mlRFP血清溶液按实验方法测定10次,平均值为10.7μg/ml,变异系数为2.5%。
2.4 不同方法的比较:将同一样品分别按本法和文献[5]介绍的方法进行测定。比较两者结果,后者由于灵敏度和特异性较低,在低浓度时准确度较差。结果见表1。
表1 不同方法的比较(n=8) 样品
本法
(μg/ml)
文献[5]法
, http://www.100md.com
(μg/ml)
偏 差
(μg/ml)
相对误差
(%)
1
0.52
0.68
0.16
30.7
2
2.24
1.95
, 百拇医药
0.29
12.9
3
11.81
12.05
0.24
2.03
4
10.85
11.21
0.36
3.50
2.5 临床应用:用高效液相色谱法测定我院呼吸科结核病人13例(年龄不限,服药用4d以上,清晨采血),其血药浓度在0.4~10.8μg/ml之间,与文献[5]报道一致。
, 百拇医药
3 讨论
3.1 1990年版《中国药典》第二部收载的利福平血药浓度测定方法为薄层法[2,3]和分光光度法[5]。此二法用血量大,数据可靠性差。本文采用高效液相色谱法测定血中RFP浓度,灵敏度高,特异性好,临床使用结果令人满意。
3.2 本文选用CBZ为内标,虽然其与RFP在结构上差异较大,但在本法抽提条件下,两者抽提率较一致且回收率较高。
3.3 利福平在pH4~8环境下,抽提率随碱性增加而增加,在pH8以上抽提率较一致,考虑到CBZ的的抽提率,故选用0.2mol/L磷酸氢二钠为提取缓冲液。
3.4 干扰试验:用临床常用药物进行干扰试验,结果,茶碱、吡嗪酰胺、异烟肼、乙胺丁醇、扑热息痛等皆无干扰。
, 百拇医药 4 参考文献
[1] 王培生.中国抗结核药物的研究进展.中国临床药理学杂志,1990,6(4)∶218
[2] 倪福英,袁天兴,刘为新.薄层扫描法测定血清中几种抗结核药物的浓度.人民军医药学专刊,1992,(2)∶38
[3] Argekar AP,Kunjirss,Purandare KS,Simultaneous determination of rifampicin,isoniazid and pyrazinamid by high thin layer chromatograph.J Pharm Biomed Anal,1996,14(11)∶1645
[4] George J,Bhatia VN,Balakrishnan S.Microbiological assay versus spectrophotometry for determination of rifampicin in urine.Indian J Lepr,1988,60(1)∶47
[5] 倪福英,魏荣.紫外分光光度法测定利福平血药浓度.中国医院药学杂志,1996,16(5)∶223
(收稿:1997-09-13,修回:1997-12-18), 百拇医药(支爱玉1 李玉萍1 李东2 方芳2)
单位:1 温州医学院附一院(325000); 2 温州医学院检验系(325027)
关键词:
温州医学院学报990120 利福平(RFP)虽是一种广谱抗生素,但其血药浓度个体差异很大,且属肝药酶诱导剂,长期服用可引起t1/2减少,血药浓度降低[1],故对该药血浓度监测有重要意义。目前国内测定利福平血药浓度的方法主要为薄层法[2,3]和紫外分光法[5],但两者在灵敏度和特异性上都尚不尽如人意。我们发明的高效液相色谱测定法,具有灵敏度高、特异性好、用血量少的优点。
1 材料和方法
, 百拇医药
1.1 仪器与试剂:美国Beckman 332型高效液相色谱仪;日本岛津UV2201紫外可见分光光度计;利福平(上海福达制药有限公司)和卡马西平(CBZ,上海黄河制药厂赠送);二氯甲烷、磷酸氢二钠、甲醇、二乙胺均为分析纯。
1.2 溶液配制:分别精确称取RFP、CBZ适量,加甲醇溶解并稀释成1000mg/L标准储备液,再将CBZ用甲醇稀释至50mg/L作为内标。
1.3 色谱条件: YWG—C18柱(4.6mm×250mm, 大连化物所), 流动相为甲醇—二乙胺—水溶液(75∶0.04∶25,V/V),流速1.0ml/min,检测波长254nm,灵敏度0.020AUFS,纸速2mm/min。
1.4 实验方法:取血清0.25ml,加内标25μl、0.2mol/L磷酸氢二钠250μl、二氯甲烷2.0ml,轻轻振摇1min,然后以4000RPM离心5min,弃上层水相,取有机相1.6ml置于尖底塑料离心管内,避光氮气吹干,残渣用流动相100μl溶解,取20μl进样。
, 百拇医药
2 实验结果
2.1 色谱图:在本法色谱条件下,RFP保留时间为7min,CBZ保留时间为5min,其代谢产物由于无标准品,未能定量;空白血清无干扰。
 附图 利福平血药浓度测定色谱图
附图 利福平血药浓度测定色谱图A.纯标准 B.病人血清 C.无药血清(不加内标)
1.CBZ(内标) 2.RFP 3.4.杂峰
2.2 标准曲线制备:准确吸取RFP标准储备液6份于具塞磨口刻度试管中,氮气吹干,加入正常人血清,混匀,RFP浓度分别配成0.2μg/ml、0.5μg/ml、1.0μg/ml、3.0μg/ml、6.0μg/ml、12.0μg/ml。按“实验方法”操作进样。结果,药物与内标峰高比(y)及药物浓度(x)线性良好。回归方程为:y=0.175x+0.013,相关系数r=0.9991。
, 百拇医药
2.3 回收率及精密度试验:取正常血清三份加入RFP标准液,分别配成每RFP2.7μg/ml、5.5μg/ml、10.8μg/ml,按实验方法操作;用回归方程计算出回收浓度和回收率分别为97.1%、99.6%、98.7%。再取10.8μg/mlRFP血清溶液按实验方法测定10次,平均值为10.7μg/ml,变异系数为2.5%。
2.4 不同方法的比较:将同一样品分别按本法和文献[5]介绍的方法进行测定。比较两者结果,后者由于灵敏度和特异性较低,在低浓度时准确度较差。结果见表1。
表1 不同方法的比较(n=8) 样品
本法
(μg/ml)
文献[5]法
, http://www.100md.com
(μg/ml)
偏 差
(μg/ml)
相对误差
(%)
1
0.52
0.68
0.16
30.7
2
2.24
1.95
, 百拇医药
0.29
12.9
3
11.81
12.05
0.24
2.03
4
10.85
11.21
0.36
3.50
2.5 临床应用:用高效液相色谱法测定我院呼吸科结核病人13例(年龄不限,服药用4d以上,清晨采血),其血药浓度在0.4~10.8μg/ml之间,与文献[5]报道一致。
, 百拇医药
3 讨论
3.1 1990年版《中国药典》第二部收载的利福平血药浓度测定方法为薄层法[2,3]和分光光度法[5]。此二法用血量大,数据可靠性差。本文采用高效液相色谱法测定血中RFP浓度,灵敏度高,特异性好,临床使用结果令人满意。
3.2 本文选用CBZ为内标,虽然其与RFP在结构上差异较大,但在本法抽提条件下,两者抽提率较一致且回收率较高。
3.3 利福平在pH4~8环境下,抽提率随碱性增加而增加,在pH8以上抽提率较一致,考虑到CBZ的的抽提率,故选用0.2mol/L磷酸氢二钠为提取缓冲液。
3.4 干扰试验:用临床常用药物进行干扰试验,结果,茶碱、吡嗪酰胺、异烟肼、乙胺丁醇、扑热息痛等皆无干扰。
, 百拇医药 4 参考文献
[1] 王培生.中国抗结核药物的研究进展.中国临床药理学杂志,1990,6(4)∶218
[2] 倪福英,袁天兴,刘为新.薄层扫描法测定血清中几种抗结核药物的浓度.人民军医药学专刊,1992,(2)∶38
[3] Argekar AP,Kunjirss,Purandare KS,Simultaneous determination of rifampicin,isoniazid and pyrazinamid by high thin layer chromatograph.J Pharm Biomed Anal,1996,14(11)∶1645
[4] George J,Bhatia VN,Balakrishnan S.Microbiological assay versus spectrophotometry for determination of rifampicin in urine.Indian J Lepr,1988,60(1)∶47
[5] 倪福英,魏荣.紫外分光光度法测定利福平血药浓度.中国医院药学杂志,1996,16(5)∶223
(收稿:1997-09-13,修回:1997-12-18), 百拇医药(支爱玉1 李玉萍1 李东2 方芳2)