合并使用烟酰胺对早期胰岛素依赖型糖尿病患儿的疗效影响
作者:麻玲玲 颜纯 倪桂臣 朱逞
单位:100045 首都医科大学附属北京儿童医院内分泌科
关键词:糖尿病;胰岛素依赖型;烟酰胺
中华儿科杂志/980914 【摘要】 目的 探讨合并使用烟酰胺(NA)对早期胰岛素依赖型糖尿病(IDDM)疗效的影响。方法 对新诊IDDM患儿进行加用NA治疗的对照研究。将新诊IDDM患儿按随机双盲法分为两个组即Ⅰ组(加用烟酰胺组)和Ⅱ组(单纯胰岛素组),分别予NA及安慰剂50mg*kg-1*d-1,早晚餐前各服1次。结果 (1)Ⅰ组在用药后6、9、12个月时餐后2小时血糖,24小时尿糖及糖化血红蛋白均低于Ⅱ组,差异有显著意义。(2)Ⅰ组空腹C肽和刺激性C肽在用药后6、9、12个月时均高于Ⅱ组,差异有显著意义;Ⅰ组C肽水平在治疗后半年内显著高于治疗前,疗程6~12个月时回落至治疗前水平,Ⅱ组在治疗3个月后,C肽水平逐渐下降。(3)在随访的各时点Ⅰ组胰岛素用量均低于Ⅱ组,差异有显著意义。(4)Ⅰ组缓解期和缓解率均长于和高于Ⅱ组。结论 合并使用NA可使早期胰岛素依赖型糖尿病患儿代谢控制状况得到更大改善,以6~9个月时效果最为显著。
, 百拇医药
A double blind clinical trial of nicotinamide in treatment of newly-diagnosed patients with insulin-dependent diabetes mellitus.
Ma Lingling, Yan Chun, Ni Guichen, et al. Beijing Children's Hospital affiliated to the Capital University of Medical Sciences, Beijing 100045
【Abstract】 Objective This double blind trial was designed to determine whether nicotinamide (NA) treatment could improve the integrated parameters of metabolic control, β-cell function , and the remission phase. Methods Twenty-one newly-diagnosed insulin-dependent diabetes mellitus (IDDM) children were divided into two groups with randomized double blind fasion. In addition to intensive insulin therapy and routine treatment, the two groups received either NA (group Ⅰ) or placebo (group Ⅱ), respectively, at a dose of 50 mg*kg-1*d-1 for 12 months. Blood glucose , HbA1c, fasting and stimulated C-peptide were measured at enrollment and every 3 months thereafter. Results (1) Levels of 2 h postprandial blood glucose , HbA1c, 24 h urine glucose of group Ⅰ were significantly lower than those of group Ⅱ after 6, 9 and 12 months therapy. (2) Levels of fasting and stimulated C-peptide of groupⅠ were significantly higher than those of groupⅡ after 6, 9 and 12 months therapy; the levels of C-peptide of groupⅠafter 6 months therapy were significantly higher than the pretreatment level, and dropped down to the pretreatment level after 6~12 months therapy. The levels of C-peptide of groupⅡ decreased after 3 months therapy. (3) Insulin dose of groupⅠ was significantly less than that of groupⅡ at each time point of the follow-up year . (4) The remission phase and remission rate of group Ⅰ were longer and higher than those of group Ⅱ. Conclusion In this study NA showed a beneficial effect on keeping the good metabolic control during the first year after onset of IDDM. The best effects appeared during the 6 to 9 months period after therapy.
, 百拇医药
【Key words】 Diabetes mellitus, insulin-dependent Niacinamide
胰岛素依赖型糖尿病(IDDM)的主要特点之一是患者自身胰岛细胞功能呈进行性下降,需终生注射外源性胰岛素进行治疗。近年来,国外研究发现烟酰胺(NA)对早期IDDM患者有保留残余胰岛细胞功能、延长缓解期的作用[1~3]。我们对新诊IDDM 患儿进行了加用NA治疗的对照研究,以初步探讨合并使用NA对早期IDDM患儿治疗效果的影响。
对象和方法
一、研究对象
1995年9月至1996年3月我院内分泌科收治的新诊IDDM患儿21例。符合下列条件:(1)符合1985年WHO公布的IDDM诊断标准;(2)均为我院首诊首治的患者,未在外院使用过胰岛素;(3)诊断时的病程小于3个月,诊断时的年龄小于15岁;(4)无其他慢性合并症。
, 百拇医药
表1 不同时间两组血糖、尿糖及糖化血红蛋白的动态变化(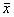 ±s
±s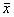 ) 随访
) 随访
时间
空腹血糖(mmol/L)
餐后2小时血糖(mmol/L)
24小时尿糖(g/24h)
糖化血红蛋白(%)
Ⅰ组
Ⅱ组
Ⅰ组
, 百拇医药
Ⅱ组
Ⅰ组
Ⅱ组
Ⅰ组
Ⅱ组
治疗前
14.1±0.9
16.7±1.0
12.0±1.6
14.4±1.6
36.6±9.3
27.2±5.0
10.0±0.9
, http://www.100md.com
11.0±0.5
治疗后
3月
8.4±0.8*
12.5±1.8
6.9±0.6
12.7±1.7
6.1±1.2
9.5±2.0
7.1±0.4
9.4±0.8
6月
, http://www.100md.com
8.2±1.0**
12.9±1.4
7.4±1.8*
13.9±1.7
6.9±1.7*
22.1±3.2
7.7±0.4*
11.4±0.8
9月
9.6±1.1*
14.4±1.2
, 百拇医药
6.7±0.7*
15.2±1.3
7.3±1.1*
25.0±4.1
8.1±0.6*
11.6±0.6
12月
12.4±1.8
14.0±1.4
8.6±1.1*
14.9±1.5
, 百拇医药
8.7±1.7*
25.2±4.5
9.5±0.8*
11.6±0.5
F值
7.315
2.522
4.425
0.401
9.406
5.288
3.273
, 百拇医药
2.201
P值
<0.01
>0.05
<0.01
>0.05
<0.01
<0.01
<0.05
>0.05
注:Ⅰ组10例,Ⅱ组11例;与Ⅱ组比较(秩和检验)* P<0.01,** P<0.05 二、研究方法
, 百拇医药
1.将新诊IDDM患儿按随机双盲法分为Ⅰ组(加用NA组)和Ⅱ组(单纯胰岛素组)。两组患儿在年龄、性别构成及病程、病情严重程度等方面差异均无显著意义。主要观察指标:空腹血糖、餐后2小时血糖、24小时尿糖、糖化血红蛋白、空腹C肽、刺激后C肽、胰岛素用量等两组患儿差异亦无显著意义。体块指数(BMI)从开始观察至随访结束的全过程中无大幅度波动。胰岛细胞抗体(ICA)、胰岛素自身抗体(IAA)及谷氨酸脱羧酶抗体(GAD-Ab)在两组患儿中的阳性率差异均无显著意义。
2.两组患儿入院确诊后均在保持常规胰岛素治疗和管理的情况下,分别加服NA和安慰剂,剂量均为50 mg*kg-1*d-1,两次口服,早晚餐前各服1次(酮症酸中毒患儿在酮症酸中毒纠正后,服标准餐,测定C肽水平,再开始服药)。对所有病例于用药前、用药后3、6、9、12个月进行下列指标观察:空腹血糖、餐后2小时血糖、24小时尿糖、糖化血红蛋白、空腹C肽、刺激后C肽及胰岛素用量。
, 百拇医药
3.临床缓解期的判定按Niclewicz标准:即在维持良好代谢控制,即空腹血糖小于7.8 mmol/L,24小时尿糖小于11.1 mmol/L,糖化血红蛋白小于7.5%的条件下,(1)完全不用胰岛素为完全缓解;(2)需用胰岛素小于0.25 IU*kg-1*d-1为部分缓解;(3)需用胰岛素大于0.25 IU*kg-1*d-1为未缓解。
三、统计学处理
计量资料结果以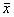 ±s
±s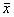 表示,各指标两组间比较时采用秩和检验,各组自身前后比较采用配对秩和检验及单因素方差分析、q检验,相关分析采用spearman检验及Fisher检验,数据处理由SYSTAT软件完成。
表示,各指标两组间比较时采用秩和检验,各组自身前后比较采用配对秩和检验及单因素方差分析、q检验,相关分析采用spearman检验及Fisher检验,数据处理由SYSTAT软件完成。
, 百拇医药
结果
一、NA对代谢控制的影响
1.血糖、尿糖及糖化血红蛋白的变化:I组空腹血糖在用药后6、9个月时均低于Ⅱ组(P值分别为0.017、0.010)。Ⅰ组餐后2小时血糖在用药后3、6、9、12个月时均低于Ⅱ组。Ⅰ组24小时尿糖和糖化血红蛋白在用药后6、9、12个月时均低于Ⅱ组。(表1)
从各组用药前后自身的变化看,Ⅰ组空腹血糖在3~9个月阶段在控制良好的水平上,略高于正常值。至12个月时明显上升;Ⅱ组空腹血糖在3个月之后一直处于较高水平。Ⅰ组餐后2小时血糖在病程9个月之内各时点的均值基本平稳在正常值以下,显著低于用药前的水平;Ⅱ组餐后2小时血糖在3个月后呈大幅度上升,之后各时点之间变化不大,稳定在一较高的水平,远高于正常值。Ⅰ组糖化血红蛋白水平在用药3个月时最低,之后逐渐上升,但各时点间值差异无显著意义;Ⅱ组糖化血红蛋白水平3个月时亦最低,之后的3个时点都停留在较高水平。Ⅰ组24小时尿糖全年维持在一低水平,略高于正常值;Ⅱ组24小时尿糖在3个月时显著下降,之后6、9、12个月均显著高于3个月时,但这3个时点之间差异无显著意义。
, 百拇医药
总的看来,Ⅰ组各项代谢指标在用药后3个月最好,之后缓慢退步,但差异无显著意义,一年之内平稳地维持在略高于正常的水平,Ⅱ组同样是在3个月时代谢控制较好,之后代谢状况迅速退步,各项指标差于I组。
2.胰岛素用量的变化:全年中各个时点Ⅰ组胰岛素用量均低于Ⅱ组。从两组用药前后自身变化
表2 不同时间两组胰岛素剂量及C肽的动态变化(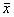 ±s
±s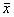 ) 随访
) 随访
时间
胰岛素剂量(IU*kg-1*d-1)
空腹C肽(nmol/L)
, 百拇医药
刺激后C肽(nmol/L)
Ⅰ组
Ⅱ组
Ⅰ组
Ⅱ组
Ⅰ组
Ⅱ组
治疗前
0.71±0.05
0.83±0.04
0.24±0.04
0.20±0.05
0.44±0.05
, 百拇医药
0.41±0.11
治疗后
3月
0.28±0.03
0.44±0.04
0.44±0.09
0.25±0.05
0.69±0.12
0.38±0.07
6月
0.29±0.05*
0.47±0.07
, http://www.100md.com
0.29±0.03**
0.16±0.03
0.60±0.13*
0.25±0.06
9月
0.31±0.05*
0.55±0.07
0.20±0.05*
0.09±0.02
0.39±0.11*
, http://www.100md.com 0.13±0.03
12月
0.35±0.07*
0.56±0.07
0.21±0.05*
0.06±0.02
0.34±0.10*
0.12±0.05
F值
12.429
5.216
, 百拇医药
3.199
6.112
4.939
3.858
P值
<0.01
<0.01
<0.05
<0.01
<0.01
<0.01
注:Ⅰ组10例,Ⅱ组11例;与Ⅱ组比较(秩和检验)* P<0.05,** P<0.01看,两组的胰岛素用量在1年中分别稳定在高低两种水平上,这两种水平间差异具有显著意义,这与糖代谢控制情况也相互符合(表2)。 二、NA对胰岛细胞功能的影响
, 百拇医药
1.空腹C肽:用药后3个月时Ⅰ组空腹C肽达1年中的峰值,用药后6、9、12个月的空腹C肽水平较前渐下降,但差异无显著意义。12个月时与治疗前在同一水平。而Ⅱ组疗程3个月后,每时点空腹C肽水平均较前下降,差异有显著意义(表2)。用药后各时点的空腹C肽水平,Ⅰ组均高于Ⅱ组。
2.刺激后C肽:Ⅰ组在用药后6、9、12个月的刺激后C肽水平均高于Ⅱ组。从两组用药前后自身的变化看,Ⅰ组用药后3~6个月阶段刺激后C肽高于发病时,并保持在全年的峰值水平段,9~12个月阶段较前半年下降,与发病时水平持平。Ⅱ组3个月时刺激后C肽水平与发病时相比无下降,之后连续下降,至12个月时下降速度减缓,全年表现为较快速的下降趋势(表2)。
三、烟酰胺对缓解率和缓解期的影响
1.缓解率:Ⅰ组共缓解6例(60%),Ⅱ组共缓解2例(18%),前者高于后者,但差异无显著性意义(P>0.05)。Ⅰ组6例缓解,其中1例为完全缓解,Ⅱ组2例均为部分缓解。
, http://www.100md.com
2.缓解期:Ⅰ组平均缓解期为7个月,Ⅱ组为4.5个月。前者高于后者,但差异无显著意义。
四、药物副作用的观察
在随访过程中,无1例出现头痛、恶心、呕吐、腹泻、面红、脱发等症状,两次复查肝功、肾功和全血象,无1例异常。认为NA在大剂量使用时无明显副作用,为一种较为安全的药物。
讨论
本研究观察结果显示,两组患儿在发病后3个月内,代谢控制情况均有较大程度好转,胰岛素用量显著减少。与发病时各项代谢指标比较,加用烟酰胺组比单纯胰岛素组好转的程度更大,但差异尚无显著意义。这与IDDM自然病程中出现的“蜜月期”有关,NA的作用在这一阶段尚不明显。用药后6~12个月内,Ⅰ组总体代谢状况显著好于Ⅱ组,尤以6~9个月阶段为显著,多项代谢指标差异有非常显著意义,烟酰胺效果明显,将“蜜月期”的良好状态延续至病程9个月。从1年随访过程看,烟酰胺可使代谢状况维持在良好的水平。
, 百拇医药
代谢控制指标的变化趋势与C肽水平变化趋势基本平行,表明代谢控制好转的原因可能与胰岛细胞功能的恢复和提高有关。烟酰胺可通过以下途径保护胰岛细胞:(1)烟酰胺可直接补充烟酰胺腺嘌呤二核苷酸池,促进DNA修复,保证三羧酸循环的进行,避免细胞死亡;(2)烟酰胺具有抑制白细胞介素-1β诱导细胞产生一氧化氮和减轻白细胞介素-1β抑制胰岛素释放的作用;(3)烟酰胺可促进胰岛细胞再生。本研究结果显示NA使胰岛细胞功能在发病后半年内显著提高,在病程的后半年可有效保留残余胰岛细胞功能。单纯胰岛素组C肽水平在病程3个月之后呈显著下降,提示β细胞功能在发病后1年内下降速度快,故应早期服用NA进行阻断,以便尽可能多地保留患者残余胰岛细胞功能。
两组患儿的缓期率和缓解期虽然差异无显著意义,但前者分别高于和长于后者,表明NA对提高缓解率,延长缓解期具有一定作用。这与Pozzilli等[4]的结果基本一致。本研究有待积累更多的病例。
值得一提的是,胰岛细胞抗体及谷胺酸脱羧酶抗体的阳性率与缓解期的出现呈某种密切关系。两组患儿8例缓解者7例呈ICA和(或)GAD-Ab阳性,5例为双阳性,阳性率显著高于非缓解患儿。表明抗体的阳性可能有助于NA作用的发挥。Rabinovitch[5]认为,IDDM发生过程中存在体液免疫与细胞免疫反应失衡的现象,即细胞免疫反应强于体液免疫反应使机体免疫系统紊乱而发病。抗体阳性患者可能存在较强的体液免疫反应,细胞免疫反应相对较弱,而NA的主要作用机理在于抑制局部细胞免疫反应,所以抗体阳性患者出现了缓解状态。
, http://www.100md.com
本研究结果略好于国外同类研究结果。Pozzilli等和Mendola等[4,6]的研究分别采用了18 mg*kg-1*d-1和25 mg*kg-1*d-1的剂量,给药时间也稍迟,所以我们认为早期大剂量加用烟酰胺是取得良好效果的重要因素。
参考文献
1 Pozzilli P, Browne PD, Kolb H, et al. Meta analysis of nicotinamide treatment in patients with recent-onset IDDM. Diabetes Care , 1996, 19:1357-1363.
2 Anderson HU , Jorgensen KH , Egeberg J, et al. Nicotinamide prevents interleukin-1 effects on accumulated insulin release and nitric oxide production in rat islets of Langerhans. Diabetes, 1994, 43:770-775.
, 百拇医药
3 Vague P, Vialette B, Lassamann-Vaugue V, et al. Nicotinamide may extend remission phase in insulin-dependent diabetes. Lancet, 1987,i:619-620.
4 Pozzilli P, Visalli N, Signore A, et al. Double blind trial of nicotinamide in recent-onset IDDM. Diabetologia, 1995, 38:848-852.
5 Rabinovitch A. Immunoregulatory and cytokine imbalance in the pathogenesis of IDDM. Diabetes, 1994, 43:613-622.
6 Mendola G, Casamitjane R, Gomis R. Effect of nicotinamide therapy upon β-cell function in newly-diagnosed type 1 diabetic patients. Diabetologia, 1989,32:A160.
(收稿:1997-09-05 修回:1998-05-27), 百拇医药
单位:100045 首都医科大学附属北京儿童医院内分泌科
关键词:糖尿病;胰岛素依赖型;烟酰胺
中华儿科杂志/980914 【摘要】 目的 探讨合并使用烟酰胺(NA)对早期胰岛素依赖型糖尿病(IDDM)疗效的影响。方法 对新诊IDDM患儿进行加用NA治疗的对照研究。将新诊IDDM患儿按随机双盲法分为两个组即Ⅰ组(加用烟酰胺组)和Ⅱ组(单纯胰岛素组),分别予NA及安慰剂50mg*kg-1*d-1,早晚餐前各服1次。结果 (1)Ⅰ组在用药后6、9、12个月时餐后2小时血糖,24小时尿糖及糖化血红蛋白均低于Ⅱ组,差异有显著意义。(2)Ⅰ组空腹C肽和刺激性C肽在用药后6、9、12个月时均高于Ⅱ组,差异有显著意义;Ⅰ组C肽水平在治疗后半年内显著高于治疗前,疗程6~12个月时回落至治疗前水平,Ⅱ组在治疗3个月后,C肽水平逐渐下降。(3)在随访的各时点Ⅰ组胰岛素用量均低于Ⅱ组,差异有显著意义。(4)Ⅰ组缓解期和缓解率均长于和高于Ⅱ组。结论 合并使用NA可使早期胰岛素依赖型糖尿病患儿代谢控制状况得到更大改善,以6~9个月时效果最为显著。
, 百拇医药
A double blind clinical trial of nicotinamide in treatment of newly-diagnosed patients with insulin-dependent diabetes mellitus.
Ma Lingling, Yan Chun, Ni Guichen, et al. Beijing Children's Hospital affiliated to the Capital University of Medical Sciences, Beijing 100045
【Abstract】 Objective This double blind trial was designed to determine whether nicotinamide (NA) treatment could improve the integrated parameters of metabolic control, β-cell function , and the remission phase. Methods Twenty-one newly-diagnosed insulin-dependent diabetes mellitus (IDDM) children were divided into two groups with randomized double blind fasion. In addition to intensive insulin therapy and routine treatment, the two groups received either NA (group Ⅰ) or placebo (group Ⅱ), respectively, at a dose of 50 mg*kg-1*d-1 for 12 months. Blood glucose , HbA1c, fasting and stimulated C-peptide were measured at enrollment and every 3 months thereafter. Results (1) Levels of 2 h postprandial blood glucose , HbA1c, 24 h urine glucose of group Ⅰ were significantly lower than those of group Ⅱ after 6, 9 and 12 months therapy. (2) Levels of fasting and stimulated C-peptide of groupⅠ were significantly higher than those of groupⅡ after 6, 9 and 12 months therapy; the levels of C-peptide of groupⅠafter 6 months therapy were significantly higher than the pretreatment level, and dropped down to the pretreatment level after 6~12 months therapy. The levels of C-peptide of groupⅡ decreased after 3 months therapy. (3) Insulin dose of groupⅠ was significantly less than that of groupⅡ at each time point of the follow-up year . (4) The remission phase and remission rate of group Ⅰ were longer and higher than those of group Ⅱ. Conclusion In this study NA showed a beneficial effect on keeping the good metabolic control during the first year after onset of IDDM. The best effects appeared during the 6 to 9 months period after therapy.
, 百拇医药
【Key words】 Diabetes mellitus, insulin-dependent Niacinamide
胰岛素依赖型糖尿病(IDDM)的主要特点之一是患者自身胰岛细胞功能呈进行性下降,需终生注射外源性胰岛素进行治疗。近年来,国外研究发现烟酰胺(NA)对早期IDDM患者有保留残余胰岛细胞功能、延长缓解期的作用[1~3]。我们对新诊IDDM 患儿进行了加用NA治疗的对照研究,以初步探讨合并使用NA对早期IDDM患儿治疗效果的影响。
对象和方法
一、研究对象
1995年9月至1996年3月我院内分泌科收治的新诊IDDM患儿21例。符合下列条件:(1)符合1985年WHO公布的IDDM诊断标准;(2)均为我院首诊首治的患者,未在外院使用过胰岛素;(3)诊断时的病程小于3个月,诊断时的年龄小于15岁;(4)无其他慢性合并症。
, 百拇医药
表1 不同时间两组血糖、尿糖及糖化血红蛋白的动态变化(
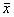 ±s
±s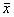 ) 随访
) 随访时间
空腹血糖(mmol/L)
餐后2小时血糖(mmol/L)
24小时尿糖(g/24h)
糖化血红蛋白(%)
Ⅰ组
Ⅱ组
Ⅰ组
, 百拇医药
Ⅱ组
Ⅰ组
Ⅱ组
Ⅰ组
Ⅱ组
治疗前
14.1±0.9
16.7±1.0
12.0±1.6
14.4±1.6
36.6±9.3
27.2±5.0
10.0±0.9
, http://www.100md.com
11.0±0.5
治疗后
3月
8.4±0.8*
12.5±1.8
6.9±0.6
12.7±1.7
6.1±1.2
9.5±2.0
7.1±0.4
9.4±0.8
6月
, http://www.100md.com
8.2±1.0**
12.9±1.4
7.4±1.8*
13.9±1.7
6.9±1.7*
22.1±3.2
7.7±0.4*
11.4±0.8
9月
9.6±1.1*
14.4±1.2
, 百拇医药
6.7±0.7*
15.2±1.3
7.3±1.1*
25.0±4.1
8.1±0.6*
11.6±0.6
12月
12.4±1.8
14.0±1.4
8.6±1.1*
14.9±1.5
, 百拇医药
8.7±1.7*
25.2±4.5
9.5±0.8*
11.6±0.5
F值
7.315
2.522
4.425
0.401
9.406
5.288
3.273
, 百拇医药
2.201
P值
<0.01
>0.05
<0.01
>0.05
<0.01
<0.01
<0.05
>0.05
注:Ⅰ组10例,Ⅱ组11例;与Ⅱ组比较(秩和检验)* P<0.01,** P<0.05 二、研究方法
, 百拇医药
1.将新诊IDDM患儿按随机双盲法分为Ⅰ组(加用NA组)和Ⅱ组(单纯胰岛素组)。两组患儿在年龄、性别构成及病程、病情严重程度等方面差异均无显著意义。主要观察指标:空腹血糖、餐后2小时血糖、24小时尿糖、糖化血红蛋白、空腹C肽、刺激后C肽、胰岛素用量等两组患儿差异亦无显著意义。体块指数(BMI)从开始观察至随访结束的全过程中无大幅度波动。胰岛细胞抗体(ICA)、胰岛素自身抗体(IAA)及谷氨酸脱羧酶抗体(GAD-Ab)在两组患儿中的阳性率差异均无显著意义。
2.两组患儿入院确诊后均在保持常规胰岛素治疗和管理的情况下,分别加服NA和安慰剂,剂量均为50 mg*kg-1*d-1,两次口服,早晚餐前各服1次(酮症酸中毒患儿在酮症酸中毒纠正后,服标准餐,测定C肽水平,再开始服药)。对所有病例于用药前、用药后3、6、9、12个月进行下列指标观察:空腹血糖、餐后2小时血糖、24小时尿糖、糖化血红蛋白、空腹C肽、刺激后C肽及胰岛素用量。
, 百拇医药
3.临床缓解期的判定按Niclewicz标准:即在维持良好代谢控制,即空腹血糖小于7.8 mmol/L,24小时尿糖小于11.1 mmol/L,糖化血红蛋白小于7.5%的条件下,(1)完全不用胰岛素为完全缓解;(2)需用胰岛素小于0.25 IU*kg-1*d-1为部分缓解;(3)需用胰岛素大于0.25 IU*kg-1*d-1为未缓解。
三、统计学处理
计量资料结果以
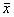 ±s
±s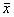 表示,各指标两组间比较时采用秩和检验,各组自身前后比较采用配对秩和检验及单因素方差分析、q检验,相关分析采用spearman检验及Fisher检验,数据处理由SYSTAT软件完成。
表示,各指标两组间比较时采用秩和检验,各组自身前后比较采用配对秩和检验及单因素方差分析、q检验,相关分析采用spearman检验及Fisher检验,数据处理由SYSTAT软件完成。, 百拇医药
结果
一、NA对代谢控制的影响
1.血糖、尿糖及糖化血红蛋白的变化:I组空腹血糖在用药后6、9个月时均低于Ⅱ组(P值分别为0.017、0.010)。Ⅰ组餐后2小时血糖在用药后3、6、9、12个月时均低于Ⅱ组。Ⅰ组24小时尿糖和糖化血红蛋白在用药后6、9、12个月时均低于Ⅱ组。(表1)
从各组用药前后自身的变化看,Ⅰ组空腹血糖在3~9个月阶段在控制良好的水平上,略高于正常值。至12个月时明显上升;Ⅱ组空腹血糖在3个月之后一直处于较高水平。Ⅰ组餐后2小时血糖在病程9个月之内各时点的均值基本平稳在正常值以下,显著低于用药前的水平;Ⅱ组餐后2小时血糖在3个月后呈大幅度上升,之后各时点之间变化不大,稳定在一较高的水平,远高于正常值。Ⅰ组糖化血红蛋白水平在用药3个月时最低,之后逐渐上升,但各时点间值差异无显著意义;Ⅱ组糖化血红蛋白水平3个月时亦最低,之后的3个时点都停留在较高水平。Ⅰ组24小时尿糖全年维持在一低水平,略高于正常值;Ⅱ组24小时尿糖在3个月时显著下降,之后6、9、12个月均显著高于3个月时,但这3个时点之间差异无显著意义。
, 百拇医药
总的看来,Ⅰ组各项代谢指标在用药后3个月最好,之后缓慢退步,但差异无显著意义,一年之内平稳地维持在略高于正常的水平,Ⅱ组同样是在3个月时代谢控制较好,之后代谢状况迅速退步,各项指标差于I组。
2.胰岛素用量的变化:全年中各个时点Ⅰ组胰岛素用量均低于Ⅱ组。从两组用药前后自身变化
表2 不同时间两组胰岛素剂量及C肽的动态变化(
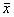 ±s
±s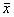 ) 随访
) 随访时间
胰岛素剂量(IU*kg-1*d-1)
空腹C肽(nmol/L)
, 百拇医药
刺激后C肽(nmol/L)
Ⅰ组
Ⅱ组
Ⅰ组
Ⅱ组
Ⅰ组
Ⅱ组
治疗前
0.71±0.05
0.83±0.04
0.24±0.04
0.20±0.05
0.44±0.05
, 百拇医药
0.41±0.11
治疗后
3月
0.28±0.03
0.44±0.04
0.44±0.09
0.25±0.05
0.69±0.12
0.38±0.07
6月
0.29±0.05*
0.47±0.07
, http://www.100md.com
0.29±0.03**
0.16±0.03
0.60±0.13*
0.25±0.06
9月
0.31±0.05*
0.55±0.07
0.20±0.05*
0.09±0.02
0.39±0.11*
, http://www.100md.com 0.13±0.03
12月
0.35±0.07*
0.56±0.07
0.21±0.05*
0.06±0.02
0.34±0.10*
0.12±0.05
F值
12.429
5.216
, 百拇医药
3.199
6.112
4.939
3.858
P值
<0.01
<0.01
<0.05
<0.01
<0.01
<0.01
注:Ⅰ组10例,Ⅱ组11例;与Ⅱ组比较(秩和检验)* P<0.05,** P<0.01看,两组的胰岛素用量在1年中分别稳定在高低两种水平上,这两种水平间差异具有显著意义,这与糖代谢控制情况也相互符合(表2)。 二、NA对胰岛细胞功能的影响
, 百拇医药
1.空腹C肽:用药后3个月时Ⅰ组空腹C肽达1年中的峰值,用药后6、9、12个月的空腹C肽水平较前渐下降,但差异无显著意义。12个月时与治疗前在同一水平。而Ⅱ组疗程3个月后,每时点空腹C肽水平均较前下降,差异有显著意义(表2)。用药后各时点的空腹C肽水平,Ⅰ组均高于Ⅱ组。
2.刺激后C肽:Ⅰ组在用药后6、9、12个月的刺激后C肽水平均高于Ⅱ组。从两组用药前后自身的变化看,Ⅰ组用药后3~6个月阶段刺激后C肽高于发病时,并保持在全年的峰值水平段,9~12个月阶段较前半年下降,与发病时水平持平。Ⅱ组3个月时刺激后C肽水平与发病时相比无下降,之后连续下降,至12个月时下降速度减缓,全年表现为较快速的下降趋势(表2)。
三、烟酰胺对缓解率和缓解期的影响
1.缓解率:Ⅰ组共缓解6例(60%),Ⅱ组共缓解2例(18%),前者高于后者,但差异无显著性意义(P>0.05)。Ⅰ组6例缓解,其中1例为完全缓解,Ⅱ组2例均为部分缓解。
, http://www.100md.com
2.缓解期:Ⅰ组平均缓解期为7个月,Ⅱ组为4.5个月。前者高于后者,但差异无显著意义。
四、药物副作用的观察
在随访过程中,无1例出现头痛、恶心、呕吐、腹泻、面红、脱发等症状,两次复查肝功、肾功和全血象,无1例异常。认为NA在大剂量使用时无明显副作用,为一种较为安全的药物。
讨论
本研究观察结果显示,两组患儿在发病后3个月内,代谢控制情况均有较大程度好转,胰岛素用量显著减少。与发病时各项代谢指标比较,加用烟酰胺组比单纯胰岛素组好转的程度更大,但差异尚无显著意义。这与IDDM自然病程中出现的“蜜月期”有关,NA的作用在这一阶段尚不明显。用药后6~12个月内,Ⅰ组总体代谢状况显著好于Ⅱ组,尤以6~9个月阶段为显著,多项代谢指标差异有非常显著意义,烟酰胺效果明显,将“蜜月期”的良好状态延续至病程9个月。从1年随访过程看,烟酰胺可使代谢状况维持在良好的水平。
, 百拇医药
代谢控制指标的变化趋势与C肽水平变化趋势基本平行,表明代谢控制好转的原因可能与胰岛细胞功能的恢复和提高有关。烟酰胺可通过以下途径保护胰岛细胞:(1)烟酰胺可直接补充烟酰胺腺嘌呤二核苷酸池,促进DNA修复,保证三羧酸循环的进行,避免细胞死亡;(2)烟酰胺具有抑制白细胞介素-1β诱导细胞产生一氧化氮和减轻白细胞介素-1β抑制胰岛素释放的作用;(3)烟酰胺可促进胰岛细胞再生。本研究结果显示NA使胰岛细胞功能在发病后半年内显著提高,在病程的后半年可有效保留残余胰岛细胞功能。单纯胰岛素组C肽水平在病程3个月之后呈显著下降,提示β细胞功能在发病后1年内下降速度快,故应早期服用NA进行阻断,以便尽可能多地保留患者残余胰岛细胞功能。
两组患儿的缓期率和缓解期虽然差异无显著意义,但前者分别高于和长于后者,表明NA对提高缓解率,延长缓解期具有一定作用。这与Pozzilli等[4]的结果基本一致。本研究有待积累更多的病例。
值得一提的是,胰岛细胞抗体及谷胺酸脱羧酶抗体的阳性率与缓解期的出现呈某种密切关系。两组患儿8例缓解者7例呈ICA和(或)GAD-Ab阳性,5例为双阳性,阳性率显著高于非缓解患儿。表明抗体的阳性可能有助于NA作用的发挥。Rabinovitch[5]认为,IDDM发生过程中存在体液免疫与细胞免疫反应失衡的现象,即细胞免疫反应强于体液免疫反应使机体免疫系统紊乱而发病。抗体阳性患者可能存在较强的体液免疫反应,细胞免疫反应相对较弱,而NA的主要作用机理在于抑制局部细胞免疫反应,所以抗体阳性患者出现了缓解状态。
, http://www.100md.com
本研究结果略好于国外同类研究结果。Pozzilli等和Mendola等[4,6]的研究分别采用了18 mg*kg-1*d-1和25 mg*kg-1*d-1的剂量,给药时间也稍迟,所以我们认为早期大剂量加用烟酰胺是取得良好效果的重要因素。
参考文献
1 Pozzilli P, Browne PD, Kolb H, et al. Meta analysis of nicotinamide treatment in patients with recent-onset IDDM. Diabetes Care , 1996, 19:1357-1363.
2 Anderson HU , Jorgensen KH , Egeberg J, et al. Nicotinamide prevents interleukin-1 effects on accumulated insulin release and nitric oxide production in rat islets of Langerhans. Diabetes, 1994, 43:770-775.
, 百拇医药
3 Vague P, Vialette B, Lassamann-Vaugue V, et al. Nicotinamide may extend remission phase in insulin-dependent diabetes. Lancet, 1987,i:619-620.
4 Pozzilli P, Visalli N, Signore A, et al. Double blind trial of nicotinamide in recent-onset IDDM. Diabetologia, 1995, 38:848-852.
5 Rabinovitch A. Immunoregulatory and cytokine imbalance in the pathogenesis of IDDM. Diabetes, 1994, 43:613-622.
6 Mendola G, Casamitjane R, Gomis R. Effect of nicotinamide therapy upon β-cell function in newly-diagnosed type 1 diabetic patients. Diabetologia, 1989,32:A160.
(收稿:1997-09-05 修回:1998-05-27), 百拇医药