α干扰素治疗伴有HIV感染的慢性乙型肝炎患者的临床观察
作者:江家骥 林彩文 S.pol P.Berthelot
单位:江家骥、林彩文 350001 福州市传染病医院;S.Pol、P.Berthelot Necker医院,巴黎
关键词:
中华传染病杂志990122
乙型肝炎病毒(HBV)常与人类免疫缺陷病毒(HIV)共同感染[1],HBV感染能促进HIV感染的发病和加速HIV感染的病程[2],感染了HIV的慢性乙型肝炎,肝脏的病变往往更加严重[3]。因此,需要在感染了HIV的慢性乙型肝炎患者中进行抗HBV治疗,防止肝衰竭或艾滋病的发生。为此,我们尝试了用α干扰素治疗伴有HIV感染的慢性乙型肝炎患者,评价α干扰素对此类患者的疗效。
材料和方法
, 百拇医药
一、病例来源
35例伴有HIV感染的慢性乙型肝炎患者为Necker医院肝科1991年9月~1993年10月住院患者,男性30例,女性5例,平均年龄34岁。慢性乙型肝炎的诊断标准为肝脏组织学证实为慢性活动型肝炎,且血中HBsAg、HBeAg、HBV DNA阳性超过6个月。35例患者中17例接受了α干扰素治疗的为治疗组,另外18例未接受α干扰素的为对照组。治疗组有2例,对照组有7例已发展至肝硬化。治疗组有7例抗-HCV阳性,对照组在检测了的11例中,无1例检出抗-HCV,两组均无发现HDV的重迭感染。两组患者均不属于CDC制定的HIV感染分类的第四级。两组患者治疗前的情况对比见表1。
表1 治疗前两组情况对比(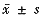 ) 组别
) 组别
, 百拇医药
感染时间
(年)
CD4计数
P24抗原
HBV DNA
(pg/ml)
ALT(IU/L)
AST(IU/L)
治疗组
(n=17)
3.2±2.0
470±234
, http://www.100md.com
6(35.2%)
346±386
148±148
108±95
对照组
(n=18)
2.6±2.7
426±202
2(25%)*
457±414
89±83
55±34
, 百拇医药
*本组中仅8例检测了P24抗原
二、治疗方法
治疗组接受干扰能(Intron A)6MU,皮下注射,每周3次,疗程为6个月。所有患者于疗程结束后,随访至少一年以上。治疗组中76.5%(13/17)的患者同时接受AZT(100~500mg/d),对照组中44.4%(8/18)的患者亦接受AZT(100~500mg/d)治疗。
三、病毒学检测
(一) HBV 使用Diagnostic Pasteur,Paris,France的试剂盒,用ELISA法检测HBsAg、HBeAg和抗-HBs、抗-HBe、抗-HBc。HBV DNA检测的分子杂交法,按试剂生产厂家(Genostics,Abbott Laboratories,Chicago.USA)说明书进行。
, 百拇医药
(二) HCV 采用ELISA法检测抗-HCV,试剂为Chiron Corporation Emeryville,USA的第二代产品。
(三) HDV 酶免疫试验检测HDAg,抗-HDV。试剂为Organon Teknika (Oss,The Netherlands)产品。
(四) HIV 酶免法检测抗-HIV和P24抗原。同时采用Wellcome Foundation,Dartford,England和Abbott Laboratories的试剂,以两种试剂的一致结果判定试验结果。
(五) CD4计数 以流式细胞仪,采用荧光单克隆抗体(Coulter/Immunotech公司产品)检测。
结 果
一、乙型肝炎病毒学
, http://www.100md.com
治疗组中6例(35.3%)患者分别于疗程中第1、2、2、2、4及6个月时,血清HBV DNA和HBeAg阴转,但是在疗程结束时及随后的随访期间,无1例出现抗-HBe。其中1例患者于疗程结束后7个月,血清HBsAg阴转,但是直至本研究结束,亦无抗-HBs产生。6例治疗有反应者中,4例在疗程中血清转氨酶一过性增高至少2倍以上,随后伴随着血清HBeAg和HBV DNA的阴转。1例患者于血清HBV DNA阴转后3个月,血中重新出现HBV复制标志。6例中除1例(同时抗-HCV阳性)在血清HBV DNA阴转后血清ALT仍异常增高外,其余5例患者均随着HBV DNA的阴转而血清ALT亦恢复正常。
对照组中仅2例(11.1%)患者分别于观察期间的第2、4个月,血清HBV DNA和HBeAg阴转,并伴随抗-HBe产生,这种情况持续至研究结束。无1例血清HBsAg阴转。
两组患者于疗程结束及随访结束时的HBV标志的比较见表2。
, http://www.100md.com
表2 疗程结束和随访结束时血中HBV标志的对比 组别
疗程结束
随访结束
HBV DNA(-)
HBeAg(-)
抗-HBe(+)
HBV DNA(-)
HBeAg(-)
抗-HBe(+)
治疗组
(n=17)
6(35.3%)
, http://www.100md.com
6(35.3%)
0(0%)
5(29.4%)
5(29.4%)
0
对照组
(n=18)
2(11.1%)
2(11.1%)
2(11.1)
2(11.1%)
2(11.1%)
, 百拇医药
2(11.1%)
二、治疗反应与HIV感染状态
治疗组6例有反应者中,3例(50%)血中P24抗原阳性,而11例无反应者中只有3例(27%)血清中可检测出P24抗原。此外,治疗组中6例反应者的平均CD4计数(255±246/mm3)却比无反应者的平均CD4计数(393±437/mm3)低。
三、副反应
除在开始治疗的1周内有感冒样反应外,所有17例患者均能很好地耐受并完成6个月疗程,未发现明显的毒副作用。讨 论
我们的研究结果初步证实了α干扰素对约1/3的感染了HIV的慢性乙型肝炎患者有效,表现为血中HBeAg、HBV DNA阴转和血清转氨酶的复常,疗效明显地高于HBeAg和/或HBV DNA的自然阴转率。
, 百拇医药
HIV感染者的免疫功能低下,而机体的免疫功能又与是否能有效地清除HBV感染密切相关;另一方面,HIV感染者由于免疫缺陷,造成体内HBV的高水平复制,而HBV的高水平复制又影响了α干扰素抗HBV的疗效,所以通常认为仅约18%的HIV感染者对α干扰素治疗有效,能清除血中的HBeAg[4]。本研究治疗组6例有效者中3例血中HIV的P24抗原持续存在,6例有效者平均CD4计数较无反应者的平均CD4计数更低,表明了患者的免疫状态并不明显地影响α干扰素的疗效,这与Hoofnagle等[5]的α干扰素的反应率与HIV感染状态无关的观察是一致的。本研究治疗组中慢性乙型肝炎患者,尽管同时有HIV感染,部分病例还伴有HCV感染,但仍有35.5%的患者对α干扰素治疗有反应,提示除了通常用来判定α干扰素治疗反应的预测因素外,还有另外的某些因素也影响了α干扰素的疗效反应。此外,由于治疗组中约3/4的患者同时接受了AZT治疗,所以AZT与α干扰素在抗-HBV中的协同作用也不能完全排除。
, 百拇医药
6例有效者中有4例,在HBeAg和HBV DNA消失之前,血清ALT较治疗前至少升高2倍以上。这种血清转氨酶的升高通常与有效的抗病毒治疗反应有关,反映了机体免疫功能的增强和对HBV复制的抑制。但是尽管6例有效者都清除了血中HBeAg和HBV DNA,其中一例患者甚至在疗程结束后7个月,血清HBsAg亦阴转,但是无1例出现抗-HBe和抗-HBs,这可能说明了HIV感染相关的免疫功能的紊乱,但是却无法解释为什么对照组中2例HBeAg自然阴转者却如同免疫功能正常者那样出现抗-HBe。
由于HBV和HIV常有共同的感染途径,两种病毒的协同作用常使病情迅速加重,我们初步尝试的结果支持,感染了HIV的慢性乙型肝炎患者同样应该接受α干扰素的治疗。
(本研究的部分工作系在法国巴黎Necker医院完成)
参考文献
1 Rustgi VK,Hoofnagle JH,Gerin JL,et
, 百拇医药
al.Hepatitis B virus infection in the acquired immunodeficiency syndrome.Ann Intern Med,1984,101:795-797.
2 Scharschmidt BF,Held MJ,Hollander
HH,et al.Hepatitis B in patients with HIV infection:relationship to AIDS and patient survival.Ann Intern Med,1992,117:837-838.
3 Housset C,Pol S,Carnot F,et al.Interactions between human immunodeficiency virus-1,hepatitis delta virus and hepatitis B virus infection in 260 chronic carriers of hepatitis B virus.Hepatology, 1992,15:578-583.
, 百拇医药
4 Davis GL.Interferon treatment of viral hepatitis in immunocompromised patients.Semin Liv Dis,1989,9:267-272.
5 Hoofnagle JH,Peters M,Mullen KD,et al.Randomized,controlled trial of recombinant human a-interferon in patients with Chronic hepatitis B.Gastroenterology,1988,95:1318-1325.
(收稿:1997-04-28 修回:1998-06-09), http://www.100md.com
单位:江家骥、林彩文 350001 福州市传染病医院;S.Pol、P.Berthelot Necker医院,巴黎
关键词:
中华传染病杂志990122
乙型肝炎病毒(HBV)常与人类免疫缺陷病毒(HIV)共同感染[1],HBV感染能促进HIV感染的发病和加速HIV感染的病程[2],感染了HIV的慢性乙型肝炎,肝脏的病变往往更加严重[3]。因此,需要在感染了HIV的慢性乙型肝炎患者中进行抗HBV治疗,防止肝衰竭或艾滋病的发生。为此,我们尝试了用α干扰素治疗伴有HIV感染的慢性乙型肝炎患者,评价α干扰素对此类患者的疗效。
材料和方法
, 百拇医药
一、病例来源
35例伴有HIV感染的慢性乙型肝炎患者为Necker医院肝科1991年9月~1993年10月住院患者,男性30例,女性5例,平均年龄34岁。慢性乙型肝炎的诊断标准为肝脏组织学证实为慢性活动型肝炎,且血中HBsAg、HBeAg、HBV DNA阳性超过6个月。35例患者中17例接受了α干扰素治疗的为治疗组,另外18例未接受α干扰素的为对照组。治疗组有2例,对照组有7例已发展至肝硬化。治疗组有7例抗-HCV阳性,对照组在检测了的11例中,无1例检出抗-HCV,两组均无发现HDV的重迭感染。两组患者均不属于CDC制定的HIV感染分类的第四级。两组患者治疗前的情况对比见表1。
表1 治疗前两组情况对比(
, 百拇医药
感染时间
(年)
CD4计数
P24抗原
HBV DNA
(pg/ml)
ALT(IU/L)
AST(IU/L)
治疗组
(n=17)
3.2±2.0
470±234
, http://www.100md.com
6(35.2%)
346±386
148±148
108±95
对照组
(n=18)
2.6±2.7
426±202
2(25%)*
457±414
89±83
55±34
, 百拇医药
*本组中仅8例检测了P24抗原
二、治疗方法
治疗组接受干扰能(Intron A)6MU,皮下注射,每周3次,疗程为6个月。所有患者于疗程结束后,随访至少一年以上。治疗组中76.5%(13/17)的患者同时接受AZT(100~500mg/d),对照组中44.4%(8/18)的患者亦接受AZT(100~500mg/d)治疗。
三、病毒学检测
(一) HBV 使用Diagnostic Pasteur,Paris,France的试剂盒,用ELISA法检测HBsAg、HBeAg和抗-HBs、抗-HBe、抗-HBc。HBV DNA检测的分子杂交法,按试剂生产厂家(Genostics,Abbott Laboratories,Chicago.USA)说明书进行。
, 百拇医药
(二) HCV 采用ELISA法检测抗-HCV,试剂为Chiron Corporation Emeryville,USA的第二代产品。
(三) HDV 酶免疫试验检测HDAg,抗-HDV。试剂为Organon Teknika (Oss,The Netherlands)产品。
(四) HIV 酶免法检测抗-HIV和P24抗原。同时采用Wellcome Foundation,Dartford,England和Abbott Laboratories的试剂,以两种试剂的一致结果判定试验结果。
(五) CD4计数 以流式细胞仪,采用荧光单克隆抗体(Coulter/Immunotech公司产品)检测。
结 果
一、乙型肝炎病毒学
, http://www.100md.com
治疗组中6例(35.3%)患者分别于疗程中第1、2、2、2、4及6个月时,血清HBV DNA和HBeAg阴转,但是在疗程结束时及随后的随访期间,无1例出现抗-HBe。其中1例患者于疗程结束后7个月,血清HBsAg阴转,但是直至本研究结束,亦无抗-HBs产生。6例治疗有反应者中,4例在疗程中血清转氨酶一过性增高至少2倍以上,随后伴随着血清HBeAg和HBV DNA的阴转。1例患者于血清HBV DNA阴转后3个月,血中重新出现HBV复制标志。6例中除1例(同时抗-HCV阳性)在血清HBV DNA阴转后血清ALT仍异常增高外,其余5例患者均随着HBV DNA的阴转而血清ALT亦恢复正常。
对照组中仅2例(11.1%)患者分别于观察期间的第2、4个月,血清HBV DNA和HBeAg阴转,并伴随抗-HBe产生,这种情况持续至研究结束。无1例血清HBsAg阴转。
两组患者于疗程结束及随访结束时的HBV标志的比较见表2。
, http://www.100md.com
表2 疗程结束和随访结束时血中HBV标志的对比 组别
疗程结束
随访结束
HBV DNA(-)
HBeAg(-)
抗-HBe(+)
HBV DNA(-)
HBeAg(-)
抗-HBe(+)
治疗组
(n=17)
6(35.3%)
, http://www.100md.com
6(35.3%)
0(0%)
5(29.4%)
5(29.4%)
0
对照组
(n=18)
2(11.1%)
2(11.1%)
2(11.1)
2(11.1%)
2(11.1%)
, 百拇医药
2(11.1%)
二、治疗反应与HIV感染状态
治疗组6例有反应者中,3例(50%)血中P24抗原阳性,而11例无反应者中只有3例(27%)血清中可检测出P24抗原。此外,治疗组中6例反应者的平均CD4计数(255±246/mm3)却比无反应者的平均CD4计数(393±437/mm3)低。
三、副反应
除在开始治疗的1周内有感冒样反应外,所有17例患者均能很好地耐受并完成6个月疗程,未发现明显的毒副作用。讨 论
我们的研究结果初步证实了α干扰素对约1/3的感染了HIV的慢性乙型肝炎患者有效,表现为血中HBeAg、HBV DNA阴转和血清转氨酶的复常,疗效明显地高于HBeAg和/或HBV DNA的自然阴转率。
, 百拇医药
HIV感染者的免疫功能低下,而机体的免疫功能又与是否能有效地清除HBV感染密切相关;另一方面,HIV感染者由于免疫缺陷,造成体内HBV的高水平复制,而HBV的高水平复制又影响了α干扰素抗HBV的疗效,所以通常认为仅约18%的HIV感染者对α干扰素治疗有效,能清除血中的HBeAg[4]。本研究治疗组6例有效者中3例血中HIV的P24抗原持续存在,6例有效者平均CD4计数较无反应者的平均CD4计数更低,表明了患者的免疫状态并不明显地影响α干扰素的疗效,这与Hoofnagle等[5]的α干扰素的反应率与HIV感染状态无关的观察是一致的。本研究治疗组中慢性乙型肝炎患者,尽管同时有HIV感染,部分病例还伴有HCV感染,但仍有35.5%的患者对α干扰素治疗有反应,提示除了通常用来判定α干扰素治疗反应的预测因素外,还有另外的某些因素也影响了α干扰素的疗效反应。此外,由于治疗组中约3/4的患者同时接受了AZT治疗,所以AZT与α干扰素在抗-HBV中的协同作用也不能完全排除。
, 百拇医药
6例有效者中有4例,在HBeAg和HBV DNA消失之前,血清ALT较治疗前至少升高2倍以上。这种血清转氨酶的升高通常与有效的抗病毒治疗反应有关,反映了机体免疫功能的增强和对HBV复制的抑制。但是尽管6例有效者都清除了血中HBeAg和HBV DNA,其中一例患者甚至在疗程结束后7个月,血清HBsAg亦阴转,但是无1例出现抗-HBe和抗-HBs,这可能说明了HIV感染相关的免疫功能的紊乱,但是却无法解释为什么对照组中2例HBeAg自然阴转者却如同免疫功能正常者那样出现抗-HBe。
由于HBV和HIV常有共同的感染途径,两种病毒的协同作用常使病情迅速加重,我们初步尝试的结果支持,感染了HIV的慢性乙型肝炎患者同样应该接受α干扰素的治疗。
(本研究的部分工作系在法国巴黎Necker医院完成)
参考文献
1 Rustgi VK,Hoofnagle JH,Gerin JL,et
, 百拇医药
al.Hepatitis B virus infection in the acquired immunodeficiency syndrome.Ann Intern Med,1984,101:795-797.
2 Scharschmidt BF,Held MJ,Hollander
HH,et al.Hepatitis B in patients with HIV infection:relationship to AIDS and patient survival.Ann Intern Med,1992,117:837-838.
3 Housset C,Pol S,Carnot F,et al.Interactions between human immunodeficiency virus-1,hepatitis delta virus and hepatitis B virus infection in 260 chronic carriers of hepatitis B virus.Hepatology, 1992,15:578-583.
, 百拇医药
4 Davis GL.Interferon treatment of viral hepatitis in immunocompromised patients.Semin Liv Dis,1989,9:267-272.
5 Hoofnagle JH,Peters M,Mullen KD,et al.Randomized,controlled trial of recombinant human a-interferon in patients with Chronic hepatitis B.Gastroenterology,1988,95:1318-1325.
(收稿:1997-04-28 修回:1998-06-09), http://www.100md.com