慢性粒细胞白血病特异性单、双及三单位核酶载体的构建*
作者:冯琦 孙秉中 赵永同 孙凯 颜真 韩苇 张英起
单位:冯琦,孙秉中:第四军医大学,西京医院血液内科;赵永同,颜真,韩苇,张英起:生物技术中心;孙凯:西医院肝胆外科,西安,710032
关键词:慢性粒细胞白血病;bcr-abl;单核酶;双核酶;三核酶
细胞与分子免疫学杂志990209
摘 要:本文拟针对在慢性粒细胞白血病发病中起关键作用的bcr-abl融合基因,构建特异性的系列核酶载体。为此,我们针对bcr-abl融合位点设计、合成了3个相邻的锤头状核酶。通过基因重组将3个单核酶按顺序定向克隆入改建的pGEM-3zf载体中,构建了bcr-abl单核酶、双核酶及三核酶体外转录载体,并在此基础上将三单位核酶克隆入pDoRneo载体中构建三核酶逆转录病毒载体。此外,通过PCR方法,扩增了bcr-abl融合位点附近约376bp的序列,成功地构建了bcr-abl融合基因体外转录载体。本文构建的bcr-abl特异性系列载体,为今后遴选特异、高效的核酶打下了基础,并为将核酶用于自体骨髓移植的体外骨髓净化创造了条件。
, 百拇医药
中国图书资料分类号:R557.1
Construction and identification of single-,double- and triple-
unit ribozymes for treatment of chronic myeloid leukemia
Feng Qi, Sun Bingzhong, Zhao Yongtong1, Sun Kai2, Yan Zhen1, Han Wei1 and Zhang Yingqi1
(Department of Hematology, and 2Department of Hapatobiliary Surgery, Xijing Hospital; 1Biotechnology Center of the Fourth Military Medical University, Xi'an 710032)
, 百拇医药
Keywords:chronic myeloid leukemia, bcr-abl, single-unit ribozyme, double-unit ribozyme, triple-unit ribozyme
Abstract:Bcr-abl fusion gene plays an important role in mechanism of chronic myeloid leukemia. To investigate the ribozyme's potential application in the treatment of CML, series vectors containing bcr abl specific ribozymes were designed and constructed in this paper. Firstly, three hammer-head ribozymes specific to the fusion point of bcr-abl were designed and cloned into a modified in vitro transcription vector pDES. After recombination, a group of single- , double- and triple- unit ribozyme in vitro transcription vectors and a triple-unit ribozyme retroviral vector were constructed. The successful construction of recombinant vector was identified by DNA sequencing. Secondary, a 376bp fragment containing the bcr- abl fusion site was amplified by PCR. This fragment was cloned into pBluescript-KS to be used as the template vector for in vitro cleavage experiment. The construction of series of bcr-abl specific ribozyme vectors made a solid foundation for further specificity and efficiency identification of different bcr-abl ribozymes. It was also the basement for using ribozyme in auto bone marrow transplantation.
, http://www.100md.com
慢性粒细胞白血病(chronic myeloid leukemia,CML)是一种起源于骨髓多能造血干细胞的恶性增殖性疾病,临床上采用化疗和放疗仅能减轻其症状,尚无肯定证据证明能延长患者的生命。异基因骨髓移植由于需要骨髓配型限制了其应用,而自体骨髓转移植又存在残留白血病的问题[1],目前尚缺乏有效地治疗方法。几乎95%以上的CML患者具有特征性的Ph染色体,即9,22号染色体的易位形成bcr-abl融合基因,编码具有异常蛋白酪氨酸激酶活性的相对分子质量(Mr)为2.1×104的蛋白,是慢粒发病的分子生物学基础[2]。核酶是具有切割酶活性的RNA分子,能特异性地结合并切割靶RNA[3],可在RNA的水平阻断基因的表达,是CML治疗的新思路。
1 材料和方法
1.1 质粒及试剂 含bcr-abl基因的pGD210载体,由美国Whitehead研究所Daley教授惠赠;其余载体及菌株由本校赵永同博士惠赠。各种内切酶、核酸酶、连接酶及Taq酶,均购自华美公司。质粒提取和纯化试剂盒分别购自Promega和Clonetech公司。核酶单链及PCR引物由上海生工生物工程有限公司合成。
, 百拇医药
1.2 pGEM-3zf载体的改建 为便于核酶间的相互连接及逆转录载体的构建,首先需改建载体,去除EcoRI和SphI位点。质粒提取、酶切、连接及转化按《分子克隆》一书进行[4]。以EcoRI酶切pGEM-3zf载体后Klenow补平,再以SphI酶切,S1核酸酶削平后平端连接,命名为pDES。
1.3 bcr-abl单、双及三单位核酶体外转录载体的构建及测序 将RZ1定向克隆入pDES的BamH I和Sal I酶切位点,重组子命名为pDES-RZ1。再将RZ2定向克隆入pDES-RZ1的Sph I和EcoR I位点间,重组子命名为pDES-RZ12。而后将RZ3定向克隆入pDES-RZ12的EcoR I,Sal I位点间,重组子命名为pDES-RZ123。经全自动核酸序列分析鉴定,而后根据核酶侧翼的不同酶切位点,在pDES-RZ123及pDES-RZ12基础上,通过酶切、Klenow补平的方法,构建单核酶pDES-RZ2,pDES-RZ3及双核酶pDES-RZ23体外转录载体。载体鉴定采用双酶切、PAGE电泳及硝酸银染色。
, 百拇医药
1.4 bcr-abl三单位核酶体逆转录病毒载体的构建 将BamH I及Sal I双酶切载体pDES-RZ123,以低熔点琼脂糖电泳回收三单位核酶片段,定向克隆入pDoRneo的相应位点,重组子命名为pDoRneo-RZ123。
1.5 bcr-abl体外转录载体的构建 bcr-abl融合位点上游引物为:5′CGTCTAGAGATGCTGACCAA CTCGTGTG3′,下游引物为:5′CCCTGCAGACACCATTCCCCATTGTGAT3′,分别含有XbalI及PstI位点。以pGD210为模板,进行PCR反应:95℃,60s;60℃,80s;72℃,120s;共35个循环。72℃延长反应10min。PCR产物纯化回收后,定向克隆入pBluescriptKS,重组子命名为pBS210,纯化后进行全自动核酸序列分析。
2 结果
2.1 多核酶载体的设计 针对bcr-abl融合基因cDNA序列,通过计算机辅助设计,在融合位点上游-29bp,-1bp及下游+15bp处,分别设计3个锤头状核酶,为便于3个核酶之间的相互连接,在RZ1的5′端加入BamHI位点及保护碱基,在其3′端加入Sph I、EcoR I及Sal I位点。RZ2两端分别为Sph I和EcoR I位点,RZ3两端分别为EcoR I、和Sal I位点。经计算机程序模拟测定及基因库检索,以上3个核酶均可特异性结合于融合基因相应位点。3个单核酶的系列如下(酶切位点已用下划线标出):
, http://www.100md.com
RZ1:GCGGATCCGAATGTCATCGTTTCGTCCTCACGGACTCATCAGCACTCAGCCACGCATGCAGGAATTCAGAGTCGACCG
RZ2:GCGCATGCTTAAGCAGAGTTTCGTCCTCACGGACTCATCAGCAAAAGCCCTGAATTCCG
RZ3:GCGAATTCTCAGCGGCCAGTTTCGTCCTCACGGACTCATCAGGCATCTGACTGTCGACCG
2.2 pGEM-3zf改建载体的鉴定 经酶切、补平或削平、重新连接后,相应的酶切位点被敲除,方便了下一步的基因重组,其酶切电泳鉴定的图略。
2.3 bcr-abl系列核酶体外转录载体的鉴定 pDES-RZ123载体经序列测定后证实,3个单核酶的序列均正确。依实验方法中所述,最终获得3个单核酶、2个双核酶及1个三核酶,构建策略见图1,载体鉴定见图2。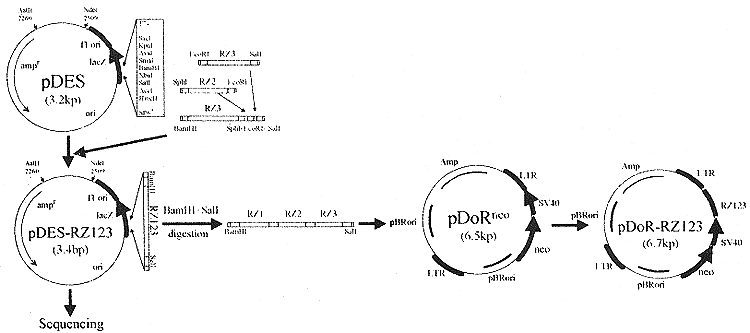
, http://www.100md.com
图1 bcr-abl特异性序列核酶载体的构建
Fig1 Construction of series bcr-abl specific ribozyme vectors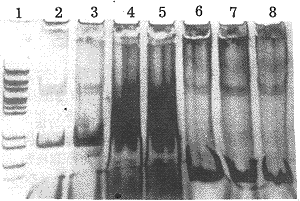
图2 系列核酶载体的鉴定(12%PAGE电泳)
Fig2 Identification of series bcr-abl ribozyme vectors by 12% PAGE,stained by silver nitrate
1: pGEM-3zf(+)/HaeIII marker(587,458,434,323,314,289,267,174,142,102,80,18,11bp); 2: pDoRneo-RZ123 digested by BamH I+Sal I,produce a 150 bp fragment; 3~8: pDES-RZ123, pDES-RZ23, pDES-RZ12, pDES-RZ3, pDES-RZ2 and pDES-RZ1 digested by Kpn I+HincI I,produce 157 bp,120bp,116bp,71bp,79bp and 76bp fragments,respectively
, http://www.100md.com
2.4 bcr-abl三单位核酶逆转录病毒载体的鉴定 三核酶体外转录载体pDES-RZ123经BamHI和SalI双酶切,回收156bp三核酶片段,定向克隆入pDoRneo后获得三单位核酶逆转录病毒载体pDoRneo-RZ123。酶切鉴定见图2。
2.5 bcr-abl体外转录载体的鉴定 经PCR扩增得到376bp含bcr-abl融合位点的模板序列,融合位点位于序列正中。序列测定后与GeneBank中bcr-abl基因序列相符,测序及酶切、PCR鉴定的结果略。
3 讨论
核酶为具有切割酶活性的RNA分子,能够通过特异性的三联密码子GUX(X:A,U,C)与靶RNA结合,并在无蛋白存在的条件下切割该RNA分子[3]。核酶是近年来基因治疗的新手段,其应用研究主要集中于肿瘤及感染性疾病。由于bcr-abl融合基因在CML的发病中起重要作用,而且在融合位点的上游29bp,1bp及下游+15bp处恰好存在3个相邻的核酶切割位点(分别为GUC,GUU及GUA),所以通过核酶基因治疗可有效地抑制bcr-abl融合基因的转录及表达,成为CML治疗的新思路。由于其直接针对CML的病因,有望从根本上治愈CML,因此成为当前的研究热点。国内外实验均证实,核酶能够有效地抑制bcr-abl融合基因的表达[5,6,7],但目前仅停留在将核酶碱基直接导入细胞进行实验研究的阶段,费用及操作的复杂均限制了对其进一步的应用,故目前尚未进入动物及临床实验。
, 百拇医药
本研究通过基因重组技术,构建了针对融合基因的系列核酶体外转录载体及多核酶逆转录病毒载体,不仅能够在体外进一步比较不同位点核酶的切割效率及特异性,为今后遴选特异、高效的核酶载体提供依据;而且三单位核酶逆转录病毒载体的构建成功,使核酶基因进入病变造血干细胞、直接抑制融合基因表达成为可能,为用多核酶进行体外骨髓净化奠定了基础。我国利用核酶技术进行基因治疗的研究刚刚起步,在白血病治疗研究方面尚属空白。本实验研究为进一步开展CML多核酶基因治疗创造了条件。
*国家自然科学基金资助项目,No.39670330
作者简介:冯琦,女,27岁,博士生。西安长乐西路15号,Tel.(029)3242969,E-mail:feng.qi @263.net
参考文献
[1]Gale RP, Butturini A. How do transplants cure chronic myelogenous leukemia? Bone Marrow Transplant, 1992; 9:83~86
, 百拇医药
[2]Lichtman MA, and Williams WJ. Chronic myelogenous leukemia and related disorders in hematology. 4th Edition, McGrawHill, New York, 1990: 205~212
[3]Eckstein F. RNA interactions: ribozymes and antisense. Bio Soci Trans, 1996; 24: 601~ 604
[4]金冬雁,黎孟枫,编译.北京:《分子克隆实验指南》.第2版,科学出版社,1992:1~395
[5]Daley GQ, Van ER, Baltimore D. Induction of chronic myelogenous leukemia in mice by the p210 bcr/abl gene of the Philadelphia chromosome.Science,1990; 247: 824~830
, 百拇医药
[6]Shore SK, Nabissa PM, Reddy EP. Ribozyme-mediated cleavage of the BCRABL oncogene transcript: in vitro cleavage of RNA and in vivo loss of p210 protein kinase activity. Oncogene, 1993; 8: 3183~3188
[7]Leopold LH, Shore SK,Reddy EP. Multi-unit anti-bcr-abl ribozyme therapy in chronic myelogenous leukemia. Leukemia & Lymphoma, 1996;22: 365~373
收稿:1999-02-01
修回:1999-02-02, 百拇医药
单位:冯琦,孙秉中:第四军医大学,西京医院血液内科;赵永同,颜真,韩苇,张英起:生物技术中心;孙凯:西医院肝胆外科,西安,710032
关键词:慢性粒细胞白血病;bcr-abl;单核酶;双核酶;三核酶
细胞与分子免疫学杂志990209
摘 要:本文拟针对在慢性粒细胞白血病发病中起关键作用的bcr-abl融合基因,构建特异性的系列核酶载体。为此,我们针对bcr-abl融合位点设计、合成了3个相邻的锤头状核酶。通过基因重组将3个单核酶按顺序定向克隆入改建的pGEM-3zf载体中,构建了bcr-abl单核酶、双核酶及三核酶体外转录载体,并在此基础上将三单位核酶克隆入pDoRneo载体中构建三核酶逆转录病毒载体。此外,通过PCR方法,扩增了bcr-abl融合位点附近约376bp的序列,成功地构建了bcr-abl融合基因体外转录载体。本文构建的bcr-abl特异性系列载体,为今后遴选特异、高效的核酶打下了基础,并为将核酶用于自体骨髓移植的体外骨髓净化创造了条件。
, 百拇医药
中国图书资料分类号:R557.1
Construction and identification of single-,double- and triple-
unit ribozymes for treatment of chronic myeloid leukemia
Feng Qi, Sun Bingzhong, Zhao Yongtong1, Sun Kai2, Yan Zhen1, Han Wei1 and Zhang Yingqi1
(Department of Hematology, and 2Department of Hapatobiliary Surgery, Xijing Hospital; 1Biotechnology Center of the Fourth Military Medical University, Xi'an 710032)
, 百拇医药
Keywords:chronic myeloid leukemia, bcr-abl, single-unit ribozyme, double-unit ribozyme, triple-unit ribozyme
Abstract:Bcr-abl fusion gene plays an important role in mechanism of chronic myeloid leukemia. To investigate the ribozyme's potential application in the treatment of CML, series vectors containing bcr abl specific ribozymes were designed and constructed in this paper. Firstly, three hammer-head ribozymes specific to the fusion point of bcr-abl were designed and cloned into a modified in vitro transcription vector pDES. After recombination, a group of single- , double- and triple- unit ribozyme in vitro transcription vectors and a triple-unit ribozyme retroviral vector were constructed. The successful construction of recombinant vector was identified by DNA sequencing. Secondary, a 376bp fragment containing the bcr- abl fusion site was amplified by PCR. This fragment was cloned into pBluescript-KS to be used as the template vector for in vitro cleavage experiment. The construction of series of bcr-abl specific ribozyme vectors made a solid foundation for further specificity and efficiency identification of different bcr-abl ribozymes. It was also the basement for using ribozyme in auto bone marrow transplantation.
, http://www.100md.com
慢性粒细胞白血病(chronic myeloid leukemia,CML)是一种起源于骨髓多能造血干细胞的恶性增殖性疾病,临床上采用化疗和放疗仅能减轻其症状,尚无肯定证据证明能延长患者的生命。异基因骨髓移植由于需要骨髓配型限制了其应用,而自体骨髓转移植又存在残留白血病的问题[1],目前尚缺乏有效地治疗方法。几乎95%以上的CML患者具有特征性的Ph染色体,即9,22号染色体的易位形成bcr-abl融合基因,编码具有异常蛋白酪氨酸激酶活性的相对分子质量(Mr)为2.1×104的蛋白,是慢粒发病的分子生物学基础[2]。核酶是具有切割酶活性的RNA分子,能特异性地结合并切割靶RNA[3],可在RNA的水平阻断基因的表达,是CML治疗的新思路。
1 材料和方法
1.1 质粒及试剂 含bcr-abl基因的pGD210载体,由美国Whitehead研究所Daley教授惠赠;其余载体及菌株由本校赵永同博士惠赠。各种内切酶、核酸酶、连接酶及Taq酶,均购自华美公司。质粒提取和纯化试剂盒分别购自Promega和Clonetech公司。核酶单链及PCR引物由上海生工生物工程有限公司合成。
, 百拇医药
1.2 pGEM-3zf载体的改建 为便于核酶间的相互连接及逆转录载体的构建,首先需改建载体,去除EcoRI和SphI位点。质粒提取、酶切、连接及转化按《分子克隆》一书进行[4]。以EcoRI酶切pGEM-3zf载体后Klenow补平,再以SphI酶切,S1核酸酶削平后平端连接,命名为pDES。
1.3 bcr-abl单、双及三单位核酶体外转录载体的构建及测序 将RZ1定向克隆入pDES的BamH I和Sal I酶切位点,重组子命名为pDES-RZ1。再将RZ2定向克隆入pDES-RZ1的Sph I和EcoR I位点间,重组子命名为pDES-RZ12。而后将RZ3定向克隆入pDES-RZ12的EcoR I,Sal I位点间,重组子命名为pDES-RZ123。经全自动核酸序列分析鉴定,而后根据核酶侧翼的不同酶切位点,在pDES-RZ123及pDES-RZ12基础上,通过酶切、Klenow补平的方法,构建单核酶pDES-RZ2,pDES-RZ3及双核酶pDES-RZ23体外转录载体。载体鉴定采用双酶切、PAGE电泳及硝酸银染色。
, 百拇医药
1.4 bcr-abl三单位核酶体逆转录病毒载体的构建 将BamH I及Sal I双酶切载体pDES-RZ123,以低熔点琼脂糖电泳回收三单位核酶片段,定向克隆入pDoRneo的相应位点,重组子命名为pDoRneo-RZ123。
1.5 bcr-abl体外转录载体的构建 bcr-abl融合位点上游引物为:5′CGTCTAGAGATGCTGACCAA CTCGTGTG3′,下游引物为:5′CCCTGCAGACACCATTCCCCATTGTGAT3′,分别含有XbalI及PstI位点。以pGD210为模板,进行PCR反应:95℃,60s;60℃,80s;72℃,120s;共35个循环。72℃延长反应10min。PCR产物纯化回收后,定向克隆入pBluescriptKS,重组子命名为pBS210,纯化后进行全自动核酸序列分析。
2 结果
2.1 多核酶载体的设计 针对bcr-abl融合基因cDNA序列,通过计算机辅助设计,在融合位点上游-29bp,-1bp及下游+15bp处,分别设计3个锤头状核酶,为便于3个核酶之间的相互连接,在RZ1的5′端加入BamHI位点及保护碱基,在其3′端加入Sph I、EcoR I及Sal I位点。RZ2两端分别为Sph I和EcoR I位点,RZ3两端分别为EcoR I、和Sal I位点。经计算机程序模拟测定及基因库检索,以上3个核酶均可特异性结合于融合基因相应位点。3个单核酶的系列如下(酶切位点已用下划线标出):
, http://www.100md.com
RZ1:GCGGATCCGAATGTCATCGTTTCGTCCTCACGGACTCATCAGCACTCAGCCACGCATGCAGGAATTCAGAGTCGACCG
RZ2:GCGCATGCTTAAGCAGAGTTTCGTCCTCACGGACTCATCAGCAAAAGCCCTGAATTCCG
RZ3:GCGAATTCTCAGCGGCCAGTTTCGTCCTCACGGACTCATCAGGCATCTGACTGTCGACCG
2.2 pGEM-3zf改建载体的鉴定 经酶切、补平或削平、重新连接后,相应的酶切位点被敲除,方便了下一步的基因重组,其酶切电泳鉴定的图略。
2.3 bcr-abl系列核酶体外转录载体的鉴定 pDES-RZ123载体经序列测定后证实,3个单核酶的序列均正确。依实验方法中所述,最终获得3个单核酶、2个双核酶及1个三核酶,构建策略见图1,载体鉴定见图2。

, http://www.100md.com
图1 bcr-abl特异性序列核酶载体的构建
Fig1 Construction of series bcr-abl specific ribozyme vectors

图2 系列核酶载体的鉴定(12%PAGE电泳)
Fig2 Identification of series bcr-abl ribozyme vectors by 12% PAGE,stained by silver nitrate
1: pGEM-3zf(+)/HaeIII marker(587,458,434,323,314,289,267,174,142,102,80,18,11bp); 2: pDoRneo-RZ123 digested by BamH I+Sal I,produce a 150 bp fragment; 3~8: pDES-RZ123, pDES-RZ23, pDES-RZ12, pDES-RZ3, pDES-RZ2 and pDES-RZ1 digested by Kpn I+HincI I,produce 157 bp,120bp,116bp,71bp,79bp and 76bp fragments,respectively
, http://www.100md.com
2.4 bcr-abl三单位核酶逆转录病毒载体的鉴定 三核酶体外转录载体pDES-RZ123经BamHI和SalI双酶切,回收156bp三核酶片段,定向克隆入pDoRneo后获得三单位核酶逆转录病毒载体pDoRneo-RZ123。酶切鉴定见图2。
2.5 bcr-abl体外转录载体的鉴定 经PCR扩增得到376bp含bcr-abl融合位点的模板序列,融合位点位于序列正中。序列测定后与GeneBank中bcr-abl基因序列相符,测序及酶切、PCR鉴定的结果略。
3 讨论
核酶为具有切割酶活性的RNA分子,能够通过特异性的三联密码子GUX(X:A,U,C)与靶RNA结合,并在无蛋白存在的条件下切割该RNA分子[3]。核酶是近年来基因治疗的新手段,其应用研究主要集中于肿瘤及感染性疾病。由于bcr-abl融合基因在CML的发病中起重要作用,而且在融合位点的上游29bp,1bp及下游+15bp处恰好存在3个相邻的核酶切割位点(分别为GUC,GUU及GUA),所以通过核酶基因治疗可有效地抑制bcr-abl融合基因的转录及表达,成为CML治疗的新思路。由于其直接针对CML的病因,有望从根本上治愈CML,因此成为当前的研究热点。国内外实验均证实,核酶能够有效地抑制bcr-abl融合基因的表达[5,6,7],但目前仅停留在将核酶碱基直接导入细胞进行实验研究的阶段,费用及操作的复杂均限制了对其进一步的应用,故目前尚未进入动物及临床实验。
, 百拇医药
本研究通过基因重组技术,构建了针对融合基因的系列核酶体外转录载体及多核酶逆转录病毒载体,不仅能够在体外进一步比较不同位点核酶的切割效率及特异性,为今后遴选特异、高效的核酶载体提供依据;而且三单位核酶逆转录病毒载体的构建成功,使核酶基因进入病变造血干细胞、直接抑制融合基因表达成为可能,为用多核酶进行体外骨髓净化奠定了基础。我国利用核酶技术进行基因治疗的研究刚刚起步,在白血病治疗研究方面尚属空白。本实验研究为进一步开展CML多核酶基因治疗创造了条件。
*国家自然科学基金资助项目,No.39670330
作者简介:冯琦,女,27岁,博士生。西安长乐西路15号,Tel.(029)3242969,E-mail:feng.qi @263.net
参考文献
[1]Gale RP, Butturini A. How do transplants cure chronic myelogenous leukemia? Bone Marrow Transplant, 1992; 9:83~86
, 百拇医药
[2]Lichtman MA, and Williams WJ. Chronic myelogenous leukemia and related disorders in hematology. 4th Edition, McGrawHill, New York, 1990: 205~212
[3]Eckstein F. RNA interactions: ribozymes and antisense. Bio Soci Trans, 1996; 24: 601~ 604
[4]金冬雁,黎孟枫,编译.北京:《分子克隆实验指南》.第2版,科学出版社,1992:1~395
[5]Daley GQ, Van ER, Baltimore D. Induction of chronic myelogenous leukemia in mice by the p210 bcr/abl gene of the Philadelphia chromosome.Science,1990; 247: 824~830
, 百拇医药
[6]Shore SK, Nabissa PM, Reddy EP. Ribozyme-mediated cleavage of the BCRABL oncogene transcript: in vitro cleavage of RNA and in vivo loss of p210 protein kinase activity. Oncogene, 1993; 8: 3183~3188
[7]Leopold LH, Shore SK,Reddy EP. Multi-unit anti-bcr-abl ribozyme therapy in chronic myelogenous leukemia. Leukemia & Lymphoma, 1996;22: 365~373
收稿:1999-02-01
修回:1999-02-02, 百拇医药