乙氧苯柳胺的高效液相电化学测定
作者:周 健 李 俊 汤晓林 金 涌 李常玉 徐叔云
单位:周 健 口腔系、临床药理研究所,合肥 230032;李 俊 汤晓林 金 涌 李常玉 徐叔云 安徽医科大学
关键词:乙氧苯柳胺; 高效液相色谱;;电化学
摘要 目的 建立乙氧苯柳胺
摘要 目的 建立乙氧苯柳胺(ETOF)软膏皮肤用药后的血药浓度测定方法。方法 采用高效液相联用电化学检测器。结果 ETOF在6.25~ 100μg.L-1呈线型关系,日间差5%~6%,日内差2.1%~6.1%,回收率86%~98%,最低检测限125pg.L-1. ETOF软膏(1g含ETOF 150mg)分别涂在4名健康志愿者前臂屈侧 4cm×4cm皮肤后,血液中ETOF能很快被检出。结论 该方法灵敏度高,重现性好,误差小 ,能满足ETOF临床药代动力学研究需要。
, http://www.100md.com
中国图书分类号 R 969.1; R 986
文献标识码 A 文章编号 1001-1987(1999)04-0375-03
Determination of etofesalamide by high performance liquid
chromatography with electrochemical detection
ZHOU Jian,LI Jun, TANG Xiao-Lin, JIN Yong, LI Chang-Yu,XU Shu-Yun
(Faculty of Stomatology, Institute of Clinical Pharmacology, Anhui Medic al University, Hefei 230032)
, 百拇医药
ABSTRACT AIM To establish detecting method o f etofesalamide(ETOF) in the healthy volunteers following skin application of ETOF ointment. METHODS High performance liquid chromatography with electrochemical detector. RESULTS The rank of ETOF from 6 .25~100μg.L-1 showed good correlation and the recovery ratesex tracted from plasma were in the range of 86%~98%. The variations of within-day and day to day were 2.1%~6.0% and 5%~6.1% respectively. 125pg.L-1 was minimal limit of detection. The plasma concentration was rapidly measured after ETOF oi ntment was spread on the skins of healthy volunteers. CONCLUSIONS The method is fit for pharmacokinetic study of ETOF in phase I clinica l trial.
, http://www.100md.com
KEY WORDS etofesalamide; high performance liquid chromatography ; electrochemistr
乙氧苯柳胺(etofesalamide,ETOF)是由沈阳药学院开发研制的治疗多种皮肤疾病的外用药,是国家Ⅰ类新药。临床前药理毒理研究表明,该药具有抗炎、抗过敏作用,对丙酸杆菌有一定抑制作用。急性、长期毒性实验观察无明显毒性作用。为了进行ETOF的Ⅰ期临床试验,本文采用高效液相联用电化学检测器(high performance liquid chromatography with ele ctrochemical detector, HPLC-ECD),建立了ETOF的血药浓度检测方法。
1 材料与方法
1.1 药品与试剂 ETOF软膏,含ETOF 15 %,由沈阳药学院提供,批号:9402250 5;甲醇,分析纯,上海振兴第一化工厂;乙醚,分析纯,上海马陆制药厂;磷酸氢二钠,磷酸二氢钠,分析纯,上海试剂二厂;乙二胺四乙酸二钠(EDTA),分析纯,成都化学试剂厂。
, 百拇医药
1.2 仪器 高效液相色谱仪LC-6A系统,日本岛津产,包括:L-ECD-6A电化学检测器,LC-6A输液泵,SCL-6A系统控制器,CTO-6A柱温箱和CR3 A数据处理机。pH计,上海第二分析仪器厂。
1.3 HPLC-ECD检测条件 色谱柱Shimpack CLC-ODS C18反相柱6mm×150mm。采用碳糊电极和Ag/AgCl参比电极。流动相:0.01mol.L-1磷酸缓冲液(pH 8.4):甲醇(65∶35,V/V)内含0.1 mmol.L-1 EDTA,流速1.5ml.min-1,检测电压0.8 mV,柱温40℃。进样环20μl。按信号与噪声比>3测定敏感度。
1.4 标准曲线的制备 称取艾迪特标准品,用甲醇溶解,配制成6.25,12.5,25, 50,100 μg.L-1。进样20 μl,以浓度为横坐标,以峰面积为纵坐标计算线性方程。
, http://www.100md.com
1.5 血浆中艾迪特的提取 取1ml血浆加2ml双蒸水,加4 ml乙醚,旋涡振荡1~2min,1 000×g离心15min,收集有机相,再加4ml乙醚,重复提取,合并有机相,在40℃水浴下蒸干,用0.5ml甲醇重溶,供HPLC测定。
1.6 回收率试验 取20份空白血浆,分别加入不同量的艾迪特标准品,使最终浓度分别为6.25,12.5,25,50,100g.L-1,充分混匀后,用上法分离,HP LC检测并计算回收率。
1.7 受试者选择 经体检合格的健康男性志愿者,年龄20~25岁,体重(55±5)kg,试验前半个月停用一切药品,受试期间禁烟酒,试验后重复体检。
1.9 给药方案 健康志愿者4人,于晨8 时用2cm×2cm的双层纱布,涂上ETOF软膏1g ,敷贴于受试者左侧前臂屈侧,其上覆盖单层纱布,周边胶布固定,保留12h。分别于涂药 0,1,2,3,5,7,9,13和24h,从受试者肘静脉抽取3~4ml血,置肝素化的试管内,在700×g离心5min分离血浆,以下按血浆中艾迪特的提取步骤进行。
, http://www.100md.com
2 结果
2.1 艾迪特HPLC分离情况 空白血浆与涂药后血浆提取物及艾迪特标准品分离图见图1。ETOF保留时间12min ,检测下限125pg。
2.2 标准曲线及质量控制 以不同浓度标准品相对应的峰面积作标准曲线,分4 批连续测定4 d,ETOF在6.25~100μg.L-1呈线性关系,其平均值的直线方程为: =178.8
=178.8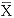 +120.5(r=0.999,P<0.05)。日内差和日间差分别为2.1%~6.1%和5.0%~6.0%,血浆回收率在86%~98%。
+120.5(r=0.999,P<0.05)。日内差和日间差分别为2.1%~6.1%和5.0%~6.0%,血浆回收率在86%~98%。
, 百拇医药
2.3 ETOF的血药浓度测定 表3可知,4名健康志愿者,涂药后1h血液中均能检测出ETOF,2 h时达峰值,而24 h后,4位受试者的血浆中均未能检测出药物。
Fig 1 Separation and detection of etofesalamide by high
performance liquid chromatography-electro-chemical detection
A:standard solution; B:blank plasma; C:etofesalamide separated from plasm a(2 nA full scale).
, http://www.100md.com
Tab 1 Precision of the method
ETOF
/μg.L-1
Day to day
Within-day
Area unit
RSD/%
Area unit
RSD/%
6.25
835±46
, 百拇医药
5.5
806±49
6.1
12.5
1444±71
5.0
1522±51
3.3
25
2788±149
5.0
2614±149
5.6
, http://www.100md.com
50
5239±310
5.9
4771±104
2.1
100
10467±632
6.0
9191±258
2.3
Tab 2 Recovery rates of etofesalamide in plasms
ETOF
, 百拇医药
/μg.L-1
Recovery rate/%
1
2
3
4 ±s
±s
6.25
88.6
105.1
103.6
, 百拇医药
95.0
98.0±7.7
12.5
88.0
84.0
91.0
80.0
86.0±4.7
25
80.2
90.0
94.0
91.0
, 百拇医药
88.8±6.0
50
91.7
93.0
88.6
88.0
90.3±2.4
100
93.4
94.0
86.4
90.6
91.1±3.5
, 百拇医药
Tab 3 Plasma concentration after etofesalamide(1 g)
was spread on the skins of the healthy volunteers
No
Plasma concentration of different time/μg.L-1
1
2
3
5
7
9
, 百拇医药
14
24/h
1
3.91
10.81
10.04
11.46
6.86
4.89
3.15
-
2
3.26
, 百拇医药
19.24
9.83
9.24
6.05
4.96
4.06
-
3
4.99
11.32
9.69
9.26
7.46
, http://www.100md.com
5.93
3.85
-
4
4.21
12.92
9.78
8.76
6.01
4.19
4.09
- ±s
±s
, 百拇医药
4.09
±
0.72
13.57
±
3.80
9.84
±
0.15
9.68
±
1.21
6.59
, 百拇医药
±
0.69
4.99
±
0.72
3.78
±
0.43
-:undetected.
3 讨论
有关ETOF的血药浓度测定,有人曾采用HPLC紫外检测法在动物体内进行,其最低检测下限为50μg.L-1(ETOF动物药代动力学资料,申报资料15号),很难适应皮肤外用后人体的血液浓度测定。ETOF为邻羟基苯胺类化合物,有较低的氧化电位,易于被氧化,可采用电化学检测[1]。为提高检测的灵敏度,本文采用HPLC电化学检测法检测。在试验中,流动相的pH对ETOF的出峰时间影响较大,当pH为7.8,8.0,8.4时,ETOF的出峰时间分别为25,18,12min。ETOF分子上的酚羟基使得自身呈弱酸性,在碱性条件下有部分电离,易于洗脱,为此本文流动相采用pH 8.4。本方法最低检测限为125 pg,日内和日间变异系数分别为2.1%~6.1%和5.0%~6.0%,回收率在86%~98%。受试者皮肤涂药2 cm×2 cm后,血浆中能很快检测出药物,且2h达峰值,表明ETOF易从软膏中释放出来,并能迅速透皮吸收。这与动物透皮吸收和药代动力学实验结果一致。24h后ETOF的血药浓度可能在仪器检测限以下。
, http://www.100md.com
上述试验初步表明,该方法检测灵敏度高,重现性好,误差小,能满足ETOF软膏人体药代动力学研究的需要。
作者简介:周 健,男,45岁,硕士,副教授;
李 俊,男,39岁,教授,博士生导师;
徐叔云,男,教授,博士生导师,中国药理学会副理事长,安徽医科大学名誉校长
参考文献
1 刘国卿. 电化学检测. 见:徐叔云,卞如濂,陈 修主编. 药理实验方法学 ,第2版,北京:人民卫生出版社,1991:286~288
1999-03-10收稿,1999-04-30修回, http://www.100md.com
单位:周 健 口腔系、临床药理研究所,合肥 230032;李 俊 汤晓林 金 涌 李常玉 徐叔云 安徽医科大学
关键词:乙氧苯柳胺; 高效液相色谱;;电化学
摘要 目的 建立乙氧苯柳胺
摘要 目的 建立乙氧苯柳胺(ETOF)软膏皮肤用药后的血药浓度测定方法。方法 采用高效液相联用电化学检测器。结果 ETOF在6.25~ 100μg.L-1呈线型关系,日间差5%~6%,日内差2.1%~6.1%,回收率86%~98%,最低检测限125pg.L-1. ETOF软膏(1g含ETOF 150mg)分别涂在4名健康志愿者前臂屈侧 4cm×4cm皮肤后,血液中ETOF能很快被检出。结论 该方法灵敏度高,重现性好,误差小 ,能满足ETOF临床药代动力学研究需要。
, http://www.100md.com
中国图书分类号 R 969.1; R 986
文献标识码 A 文章编号 1001-1987(1999)04-0375-03
Determination of etofesalamide by high performance liquid
chromatography with electrochemical detection
ZHOU Jian,LI Jun, TANG Xiao-Lin, JIN Yong, LI Chang-Yu,XU Shu-Yun
(Faculty of Stomatology, Institute of Clinical Pharmacology, Anhui Medic al University, Hefei 230032)
, 百拇医药
ABSTRACT AIM To establish detecting method o f etofesalamide(ETOF) in the healthy volunteers following skin application of ETOF ointment. METHODS High performance liquid chromatography with electrochemical detector. RESULTS The rank of ETOF from 6 .25~100μg.L-1 showed good correlation and the recovery ratesex tracted from plasma were in the range of 86%~98%. The variations of within-day and day to day were 2.1%~6.0% and 5%~6.1% respectively. 125pg.L-1 was minimal limit of detection. The plasma concentration was rapidly measured after ETOF oi ntment was spread on the skins of healthy volunteers. CONCLUSIONS The method is fit for pharmacokinetic study of ETOF in phase I clinica l trial.
, http://www.100md.com
KEY WORDS etofesalamide; high performance liquid chromatography ; electrochemistr
乙氧苯柳胺(etofesalamide,ETOF)是由沈阳药学院开发研制的治疗多种皮肤疾病的外用药,是国家Ⅰ类新药。临床前药理毒理研究表明,该药具有抗炎、抗过敏作用,对丙酸杆菌有一定抑制作用。急性、长期毒性实验观察无明显毒性作用。为了进行ETOF的Ⅰ期临床试验,本文采用高效液相联用电化学检测器(high performance liquid chromatography with ele ctrochemical detector, HPLC-ECD),建立了ETOF的血药浓度检测方法。
1 材料与方法
1.1 药品与试剂 ETOF软膏,含ETOF 15 %,由沈阳药学院提供,批号:9402250 5;甲醇,分析纯,上海振兴第一化工厂;乙醚,分析纯,上海马陆制药厂;磷酸氢二钠,磷酸二氢钠,分析纯,上海试剂二厂;乙二胺四乙酸二钠(EDTA),分析纯,成都化学试剂厂。
, 百拇医药
1.2 仪器 高效液相色谱仪LC-6A系统,日本岛津产,包括:L-ECD-6A电化学检测器,LC-6A输液泵,SCL-6A系统控制器,CTO-6A柱温箱和CR3 A数据处理机。pH计,上海第二分析仪器厂。
1.3 HPLC-ECD检测条件 色谱柱Shimpack CLC-ODS C18反相柱6mm×150mm。采用碳糊电极和Ag/AgCl参比电极。流动相:0.01mol.L-1磷酸缓冲液(pH 8.4):甲醇(65∶35,V/V)内含0.1 mmol.L-1 EDTA,流速1.5ml.min-1,检测电压0.8 mV,柱温40℃。进样环20μl。按信号与噪声比>3测定敏感度。
1.4 标准曲线的制备 称取艾迪特标准品,用甲醇溶解,配制成6.25,12.5,25, 50,100 μg.L-1。进样20 μl,以浓度为横坐标,以峰面积为纵坐标计算线性方程。
, http://www.100md.com
1.5 血浆中艾迪特的提取 取1ml血浆加2ml双蒸水,加4 ml乙醚,旋涡振荡1~2min,1 000×g离心15min,收集有机相,再加4ml乙醚,重复提取,合并有机相,在40℃水浴下蒸干,用0.5ml甲醇重溶,供HPLC测定。
1.6 回收率试验 取20份空白血浆,分别加入不同量的艾迪特标准品,使最终浓度分别为6.25,12.5,25,50,100g.L-1,充分混匀后,用上法分离,HP LC检测并计算回收率。
1.7 受试者选择 经体检合格的健康男性志愿者,年龄20~25岁,体重(55±5)kg,试验前半个月停用一切药品,受试期间禁烟酒,试验后重复体检。
1.9 给药方案 健康志愿者4人,于晨8 时用2cm×2cm的双层纱布,涂上ETOF软膏1g ,敷贴于受试者左侧前臂屈侧,其上覆盖单层纱布,周边胶布固定,保留12h。分别于涂药 0,1,2,3,5,7,9,13和24h,从受试者肘静脉抽取3~4ml血,置肝素化的试管内,在700×g离心5min分离血浆,以下按血浆中艾迪特的提取步骤进行。
, http://www.100md.com
2 结果
2.1 艾迪特HPLC分离情况 空白血浆与涂药后血浆提取物及艾迪特标准品分离图见图1。ETOF保留时间12min ,检测下限125pg。
2.2 标准曲线及质量控制 以不同浓度标准品相对应的峰面积作标准曲线,分4 批连续测定4 d,ETOF在6.25~100μg.L-1呈线性关系,其平均值的直线方程为:
, 百拇医药
2.3 ETOF的血药浓度测定 表3可知,4名健康志愿者,涂药后1h血液中均能检测出ETOF,2 h时达峰值,而24 h后,4位受试者的血浆中均未能检测出药物。

Fig 1 Separation and detection of etofesalamide by high
performance liquid chromatography-electro-chemical detection
A:standard solution; B:blank plasma; C:etofesalamide separated from plasm a(2 nA full scale).
, http://www.100md.com
Tab 1 Precision of the method
ETOF
/μg.L-1
Day to day
Within-day
Area unit
RSD/%
Area unit
RSD/%
6.25
835±46
, 百拇医药
5.5
806±49
6.1
12.5
1444±71
5.0
1522±51
3.3
25
2788±149
5.0
2614±149
5.6
, http://www.100md.com
50
5239±310
5.9
4771±104
2.1
100
10467±632
6.0
9191±258
2.3
Tab 2 Recovery rates of etofesalamide in plasms
ETOF
, 百拇医药
/μg.L-1
Recovery rate/%
1
2
3
4
6.25
88.6
105.1
103.6
, 百拇医药
95.0
98.0±7.7
12.5
88.0
84.0
91.0
80.0
86.0±4.7
25
80.2
90.0
94.0
91.0
, 百拇医药
88.8±6.0
50
91.7
93.0
88.6
88.0
90.3±2.4
100
93.4
94.0
86.4
90.6
91.1±3.5
, 百拇医药
Tab 3 Plasma concentration after etofesalamide(1 g)
was spread on the skins of the healthy volunteers
No
Plasma concentration of different time/μg.L-1
1
2
3
5
7
9
, 百拇医药
14
24/h
1
3.91
10.81
10.04
11.46
6.86
4.89
3.15
-
2
3.26
, 百拇医药
19.24
9.83
9.24
6.05
4.96
4.06
-
3
4.99
11.32
9.69
9.26
7.46
, http://www.100md.com
5.93
3.85
-
4
4.21
12.92
9.78
8.76
6.01
4.19
4.09
-
, 百拇医药
4.09
±
0.72
13.57
±
3.80
9.84
±
0.15
9.68
±
1.21
6.59
, 百拇医药
±
0.69
4.99
±
0.72
3.78
±
0.43
-:undetected.
3 讨论
有关ETOF的血药浓度测定,有人曾采用HPLC紫外检测法在动物体内进行,其最低检测下限为50μg.L-1(ETOF动物药代动力学资料,申报资料15号),很难适应皮肤外用后人体的血液浓度测定。ETOF为邻羟基苯胺类化合物,有较低的氧化电位,易于被氧化,可采用电化学检测[1]。为提高检测的灵敏度,本文采用HPLC电化学检测法检测。在试验中,流动相的pH对ETOF的出峰时间影响较大,当pH为7.8,8.0,8.4时,ETOF的出峰时间分别为25,18,12min。ETOF分子上的酚羟基使得自身呈弱酸性,在碱性条件下有部分电离,易于洗脱,为此本文流动相采用pH 8.4。本方法最低检测限为125 pg,日内和日间变异系数分别为2.1%~6.1%和5.0%~6.0%,回收率在86%~98%。受试者皮肤涂药2 cm×2 cm后,血浆中能很快检测出药物,且2h达峰值,表明ETOF易从软膏中释放出来,并能迅速透皮吸收。这与动物透皮吸收和药代动力学实验结果一致。24h后ETOF的血药浓度可能在仪器检测限以下。
, http://www.100md.com
上述试验初步表明,该方法检测灵敏度高,重现性好,误差小,能满足ETOF软膏人体药代动力学研究的需要。
作者简介:周 健,男,45岁,硕士,副教授;
李 俊,男,39岁,教授,博士生导师;
徐叔云,男,教授,博士生导师,中国药理学会副理事长,安徽医科大学名誉校长
参考文献
1 刘国卿. 电化学检测. 见:徐叔云,卞如濂,陈 修主编. 药理实验方法学 ,第2版,北京:人民卫生出版社,1991:286~288
1999-03-10收稿,1999-04-30修回, http://www.100md.com