血管内皮生长因子的研究进展
作者:钱朝南 闵华庆
单位:中山医科大学肿瘤防治中心(广州 510060)
关键词:
血管内皮生长因子的研究进展 Advances in research of vascular endothelial growth factor
QIAN Chao-Nan, MIN Hua-Qing
Cancer Center, Sun Yat-sen University of Medical Sciences, Guangzhou (510060)
【A Review】 Angiogenesis occurs in many physiological and pathological processes. Vascular endothelial growth factor( VEGF) is a key cytokine for up-regulation of angiogenesis. VEGF family includes some new members coded by the genes mapped in different chromosomes, namely ,VEGF-B, VEGF-C, VEGF-D, and PGF. Each member may have some isotypes due to splicing in mRNA transcription. VEGFR-1, VEGFR-2 and VEGFR-3 are three receptors of VEGF family. The combinations of VEGF family with different receptors can induce different functions, including increase vascular permeability, angiogenesis, and lymphangiogenesis. The biological characteristics of VEGF family and their receptors have been applied in diagnosis and experimental therapy of solid tumors, along with experimental therapy of ischemic retinopathy and ischemic heart disease.
, 百拇医药
在某些生理过程,如胚胎发育、卵巢周期、伤口愈合和缺血组织的修复,可出现新生血管的形成;而在某些病理过程,血管生成也是必不可少的环节,如类风湿性关节炎、银屑病糖尿病性视网膜病以及实体瘤的生长和转移[1]。
以往认为,出生后的血管生成(angiogenesis)与胚胎发育过程中的血管发生(vasculogenesis)是两个互相区别的过程:前者是通过分化完全的血管内皮细胞从业己存在的血管中增殖、迁徙和重塑而成;后者是指由中心包含造血干细胞、周边分布成血管细胞(angioblast)的血岛发育而成[1]。但近来的研究发现:出生后的血管生成(包括肿瘤血管生成),也有骨髓造血干细胞的参与[2,3]。骨髓里的造血干细胞在某些细胞因子(如G-CSF,GM-CSF,血小板反应素等)的刺激下,分化成血管内皮祖细胞(endothelial progenitor cells,即是成血管细胞);后者又在其它的因子(如stromal derived factor-l)的作用下进入周围血循环,在生理的以及病理的血管生成处分化成血管内皮细胞。因此现在认为,出生后的血管生成过程中,既有局部血管内皮细胞的增殖、迁徙、重塑,又有来自骨髓的血管内皮祖细胞的分化参与。
, 百拇医药
血管生成的诱导因子有的是直接作用于血管内皮细胞,有的是间接地通过其它的辅助细胞(单核细胞、肥大细胞、T细胞)来诱导血管生成。血管内皮生长因子(vascular endothelial growth factor, VEGF),也称VPF(vascular permeability factor,血管通透因子)或VAS(vasculotropin促血管因子),特异性地直接作用于血管内皮细胞,是上调血管生成的重要因子[1]。虽然VEGF最先是从肿瘤细胞的分泌物中分离出来,但现已证实VEGF及其家族成员不单在肿瘤血管生成,在其它的生理和病理的血管生成中都是必不可少的诱导因子[4]。目前已发现VEGF家族包括5大成员:VEGF-A(即以往发现的VEGF),VEGF-B,VEGF-C,VEGF-D和PGF(placental growth factor,胎盘生长因子)。它们都是二聚体的糖蛋白,都具有与类血小板生长因子蛋白区域(platelet-derived growth factor-like domain)非常相似的结构,即拥有8个完全保守、相隔排列、以二硫键维持二聚体的三维空间结构的半胱氨酸残基[5]。VEGF家族5个成员的基因分别定位于不同的染色体。
, http://www.100md.com
一、VEGF-A:
VEGF-A基因定位于6号染色体短臂1区2带(6 p12)[6]。根据VEGF-A的氨基酸链的长度不同至今已发现了6种异构体:VEGF-A115,VEGF-A121,VEGF-A145,VEGF-A165,VEGF-A189和VEGF-A206。VEGF-A121和VEGF-A165是最丰富的异构体。这些不同的异构体是由同一个基因在转录时按不同的拼接方式产生的[7],为34-42 kD的糖蛋白。VEGF-A基因拥有8个外显子。目前发现的所有VEGF-A异构体均有外显子1-5以及外显子8的表达序列。外显子1-5编码的部分是VEGF-A的核心区域,用于维持二聚体空间结构的8个特征性的半胱氨酸残基就处于这个核心部分。VEGF-A189是全部1-8个外显子编码的氨基酸序列完全表达的蛋白质产物。VEGF-A121缺乏外显子7和8编码的产物。VEGF-A145缺乏外显子7的表达。VEGF-A165缺乏外显子6′的表达。VEGF-A206除了8个外显子都有表达以外,在外显子6编码的氨基酸序列末端多出了一段17个氨基酸的延伸序列,为外显子6的产物。目前已证实VEGF-A121不与肝素结合,是可溶性分泌型蛋白;VEGF-A145也是分泌型蛋白[9];VEGF-A165是部分分泌、部分与细胞表面的硫酸乙酰肝素蛋白多糖结合;VEGF-A189和VEGF-A206是结合型蛋白,与细胞和基质中的蛋白多糖结合。最新报告的VEGF-A115在C-端与VEGF-A121有37个氨基酸的差异,其特性有待阐明[8]。
, 百拇医药
VEGF-A与两个受体高度亲和:VEGFR-1(VEGF受体1)和VEGFR-2(VEGF受体2),并能激活这两个受体。
许多正常组织(如肺、肾、肾上腺、心、卵巢等)的已分化细胞以及肿瘤细胞都可表达VEGF-A。缺氧是诱导VEGF-A及其受体产生的最有效因素。出现K-ras和H-ras突变的肿瘤细胞可以上调VEGF-A的转录,而肿瘤抑制基因VHL的蛋白产物却能下调VEGF-A的合成[5]。
VEGF-A是血管内皮细胞的促分裂原(mitogen)和促运动原(motogen),可诱导血管内皮细胞增殖和迁徙;还能诱导毛细血管管腔的形成、增加血管的通透性、刺激血管内皮细胞产生蛋白酶和其它的小分子物质[5]。虽然其确切的分子机制有待阐明,但目前已发现VEGF-A与其两个受体结合后,不但引起受体的磷酸化,还可产生一系列的蛋白质磷酸化[7]。这些蛋白质包括磷脂酶Cγ,磷脂酰肌醇3激酶,GAP(Ras GTPase-activating protein),两个GTP相关蛋白p190和p62,以及癌基因结合蛋白NcK。近来还发现VEGF-A可激活分裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)。
, 百拇医药
VEGF可非常显著地延长血管内皮细胞的寿命,使血管内皮细胞的倍增次数增加15~20次;同时使血管内皮细胞的某些周期相关基因(p21,p16和p27)的表达减少,但P53表达无改变;同时也减少衰老标记物中性β-半乳糖苷酶的表达[10]。
VEGF-A增加血管通透性的作用可能是通过增强了血管内皮细胞中的囊-泡小体(VVO,vesiculo-vacuolar organelle)的功能而产生的[11]。VVO是近年来发现的、在微静脉和小静脉的内皮细胞质里的一种细胞器,这种似葡萄串的细胞器与内皮细胞的腔内面和腔外面相连,可以占细胞质的20%。VEGF-A可以促进大分子物质经VVO渗出血管外。
二、PGF:
PGF也是一个二聚体,其氨基酸序列与VEGF-A有53%的同源性[7]。其基因定位于14q24-q31[12]。已发现PGF有3个异构体,即PGF-1,PGF-2和PGF-3,是同一基因在转录mRNA时以不同的拼接方式表达的不同产物[7,13]。PGF-1除拥有与VEGF-A相同的、由外显子1-5编码的氨基酸序列,还有一个由外显子7编码的区域。PGF-1的前体是149个氨基酸,其中一段含20个氨基酸的多肽裂解出来后,就形成129个氨基酸的成熟PGF-1。PGF-2的前体含有170个氨基酸,比PGF-1前体多出了一个由外显子6编码的21个氨基酸的序列,成熟PGF-2含152个氨基酸。PGF-3的前体含有219个氨基酸,比PGF-1多出的70个氨基酸是由一段在外显子4和5之间插入的核苷酸序列编码。PGF-3与PGF-1一样缺乏外显子6的表达[13]。PGF-2与肝素高度亲和,主要分布于细胞表面和基质中;PGF-1和PGF-3与肝素亲和性很低,是分泌型蛋白。PGF可结合并激活VEGFR-1,不与VEGFR-2或VEGFR-3结合(见图1);但PGF的单体可以和VEGF-A的单体形成VEGF/PGF异二聚体,与VEGFR-2牢固结合并激活该受体,促进内皮细胞分裂和迁徙[14]。与VEGF不同的是,PGF的表达只限于血管生成活跃的组织,如胎盘组织(由血管内皮细胞表达)和肿瘤组织(由肿瘤细胞表达),并不见于已分化成熟的细胞。
, http://www.100md.com
与VEGF-A相比,PGF诱导血管内皮细胞分裂和增加血管通透性的作用较弱。然而,PGF可以增强VEGF-A的功能[5]。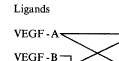

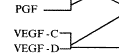

, http://www.100md.com
Fig 1 The correlation between members of VEGF family and their receptors
图1 VEGF家族成员的配体和受体的相互关系
三、VEGF-B:
VEGF-B基因定位于11q13,长约4 kb[15];有7个外显子,其外显子与内含子的组织形式与VEGF-A和PGF基因相似[16]。此基因在转录时以不同的拼接方式产生了两种异构体:VEGF-B167(21 kD)和VEGF-B186(32 kD),两者都与VEGF-A165非常相似,都是以二硫键连接的二聚体。VEGF-B186比VEGF-B167多出了一段在外显子6中插入的、由101碱基对的核酸序列编码的多肽[19]。两个异构体在N-端有相同的115个氨基酸,但C-端却不同:VEGF-B167的C-端为碱性并富含半胱氨酸,可与肝素结合;而VEGF-B186的C-端却富含丙氨酸、脯氨酸、丝氨酸和苏氨酸,不与肝素结合。因此VEGF-B167是细胞相关的分泌型蛋白;而VEGF-B186由于没有高度碱性的基团,可以从细胞自由分泌,并且不与细胞表面或细胞周围的硫酸乙酰肝素蛋白多糖结合[16]。
, http://www.100md.com
VEGF-B的两个异构体都与VEGFR-1结合并激活此受体[17]。VEGF-B也可与VEGF-A形成异二聚体,并可能借此影响VEGF-A的生物功能[18]。许多正常组织都有表达VEGF-B,如心肌、骨骼肌、胰腺、肺、肾脏、卵巢等[18]。
四、VEGF-C:
VEGF-C基因定位于4q34[15]。VEGF-C cDNA的开放阅读区编码一个419个氨基酸的前体蛋白质(46.9 kD)。这一前体蛋白质依次有4个区域:N-端信号多肽,N-端前多肽,VEGF同源区和C-端前多肽。VEGF-C的VEGF同源区与VEGF-A165的有30%同源,与VEGF-B167的有27%同源,与PGF-1的有25%同源[16]。
VEGF-C在许多正常组织都有表达,包括:心肌、骨骼肌、肺脏、肾脏[15]。其受体是VEGFR-2和VEGFR-3。VEGFR-3是第一个被发现的淋巴内皮细胞特异性的标记物[19]。而VEGF-C是第一个被发现的淋巴管生成因子,它可以诱导淋巴内皮细胞增殖、迁徙,并形成淋巴窦[20]。在一个转基因动物实验中,VEGF-C的过度表达可以引起动物皮下淋巴管的异常增生[21]。
, 百拇医药
目前尚无直接证据显示肿瘤细胞会诱导淋巴管生成[22]。相信对VEGF-C的进一步研究将有助于阐明VEGF-C在淋巴管瘤、肿瘤经淋巴道转移以及其它的淋巴系统病变中的作用。
五、VEGF-D:
VEGF-D基因定位于Xp22.1。小鼠的VEGF-D基因的表达是通过转录因子c-fos的诱导作用而产生,因此也称FIGF(c-fos-induced growth factor)基因。此基因跨度50 kb,并有7个外显子和6个内含子[23]。VEGF-D蛋白含有354个氨基酸,与VEGF-C有48%同源,与VEGF-A165有31%同源,与VEGF-B167有28%同源,与PGF有32%同源。在VEGF家族中,其蛋白质结构最接近VEGF-C,表现在:VEGF-D的VEGF同源区最接近VEGF-C(仅计算此区有61%的同源性);只有VEGF-D和VEGF-C拥有长N-端扩展区(此区两者25%同源)和长C-端扩展区(37%同源)。VEGF-D可在许多正常组织大量表达,包括:心、肺、骨骼肌、结肠和小肠[24]。
, http://www.100md.com
不仅结构上与VEGF-C相似,在功能上VEGF-D也与之相似:VEGF-D能与VEGFR-2和VEGFR-3结合并能激活这两个受体,但不能与VEGFR-1结合。初步发现VEGF-D可促进血管内皮细胞分裂[24]。由于VEGF-C和VEGF-D激活相同的受体,因此推测VEGF-D可能会在血管生成和淋巴管生成方面与VEGF-C协同作用。
在一个转基因小鼠的实验中,持续的c-fos表达可诱导动物最终形成骨肉瘤,而c-fos缺失的肿瘤细胞却不具备恶性行为[5]。今后有必要进一步阐明:在c-fos过度表达的肿瘤组织中是否具有高水平的VEGF-D的表达,以及VEGF-D是否通过诱导血管和/或淋巴管生成来参与恶性肿瘤的发生和发展。
六、VEGF家族的受体:
VEGF家族的3个受体分别由3个基因编码[25]。180 kD的VEGFR-1由Flt-1(fms-like tyrosine kinase 1)基因(定位于13q12-q13)编码。200 kD的VEGFR-2由Flk-1/KDR基因(定位于4q11-q13)编码。Flk-1(fetal liver kinase 1)是从小鼠胎肝的cDNA文库中分离出的;而相应地从人血管内皮细胞cDNA文库中分离出的基因称KDR(kinase domain receptor)。180 kD的VEGFR-3是由Flt-4基因(定位于5q33-q34)碥码。三者都是跨膜酪氨酸激酶受体,都有7个免疫球蛋白样的细胞外区域、跨细胞膜区域以及一个含有酪氨酸激酶的细胞内区域。每个血管内皮细胞表面有VEGFR-1约3000个,对VEGF-A的亲和力KD=1-20 Pm;有VEGFR-2约40 000个,对VEGF-A的亲和力KD=50-770 Pm[7]。VEGF-A与VEGFR-1和VEGFR-2的结合位点分别是外显子3和外显子4的编码区[5]。
, 百拇医药
原已发现VEGFR-1和VEGFR-2高度选择性地在血管内皮细胞表达,但近年来有人报告在一些非内皮细胞的组织细胞也有表达[7]。在胚胎发育的早期,血管内皮细胞会表达VEGFR-2和VEGFR-3,但是在发育到胎儿以后,VEGFR-3仅在淋巴内皮细胞表达[19]。VEGFR-3不与VEGF-A结合。
可溶性的VEGFR-1已被发现[26],是VEGFR-1的细胞外片段,可与完整的VEGFR-2形成二聚体后再与VEGF-A结合,阻断VEGF-A对血管内皮细胞的各种诱导作用,是天然的血管生成抑制剂。
最近又发现一个VEGF-A165的异构体专一性受体Neuropilin-1[27]。这个130-135 kD的细胞膜受体只与VEGF-A165结合,结合位点是VEGF-A基因的外显子7编码区。当此受体与VEGFR-2共同表达时,可增强VEGF-A165与VEGFR-2的结合以及VEGF-A165促内皮细胞迁徙的功能。抑制此受体与VEGF-A165结合后,VEGF-A165与VEGFR-2的结合亦被抑制,同时VEGF-A165促血管内皮细胞分裂的作用也被抑制。此受体可由血管内皮细胞和多种肿瘤细胞表达。
, 百拇医药
七、应用研究:
VEGF-A及其受体在肿瘤组织中的高水平表达与多种肿瘤的预后不良有关,这些肿瘤包括星形细胞瘤、肺癌、结肠癌、膀胱癌、头颈鳞癌等(Abdulrauf SI, et al 1998; Takahashi, et al 1998; Crew JP, et al 1997; Volm M, et al 1988; Denhart BC, et al 1997)。VEGF-A在癌症病人的血清和组织液(如腹水)的表达水平高于正常人(Kondo S, et al 1994; Barton DPJ, et al 1997),有必要进一步了解其监测疗效和预后的意义。
动物实验显示:把VEGF-A注入手术皮瓣的供血动脉后可以促进皮瓣的血管生成,从而增加皮瓣的成活面积(Padubidri A, et al 1996)。把能短暂表达VEGF-A121 cDNA而丧失复制能力的腺病毒载体直接注入猪的缺血的心肌组织中,可以诱导侧枝血管的建立,明显提高心肌的灌注和改善心肌的功能(Mack CA, et al 1998)。
, http://www.100md.com
不少缺血性视网膜病引起失明的原因都与视网膜的血管生成有关。动物实验显示:把可溶性VEGFR-1注入玻璃体内,可抑制VEGF-A的活性,从而抑制了视网膜的血管生成(Aiello LP, et al 1995)。
虽然有研究显示使用VEGF-A拮抗剂可以使实体瘤退缩[28],但有人认为这种治疗手段不可取[29]。因为肿瘤细胞除了分泌VEGF-A以外,还分泌其它的血管生长因子;而且肿瘤细胞基因组的高度不稳定性决定了它可以通过分化新的克隆产生新的血管生长因子,从而避开原有的攻击,象耐受临床常规使用的细胞毒性化疗药物一样,最终会对VEGF-A拮抗剂产生耐药。相反,由于血管内皮细胞的基因组高度稳定,通过直接抑制血管内皮细胞来治疗肿瘤就不会产生耐药现象,这已被内皮抑素(endostatin)的实验性治疗所证实[30]。
八、结语:
, 百拇医药 VEGF家族及其受体的复杂性体现了高等生命的具体生物功能受多层次影响、多基因调控的现象。VEGF家族是一类多功能的细胞因子,在血管生成和淋巴管生成中具有直接和间接的调控作用。一方面VEGF家族可以刺激血管内皮细胞增埴、迁徙甚至改变其基因表达;另一方面它们又可以增加血管的通透性,使许多血浆蛋白渗出血管外,这对改造局部的细胞外基质以适应血管生成具有重要作用。大量的血浆蛋白渗出到组织液中会使组织液的渗透压增高。这是实体瘤的瘤内渗透压高于正常组织渗透压的原因之一。而VEGF-C和VEGF-D诱导的淋巴管生成有助于组织液的引流。有关VEGF家族调控的血管生成和淋巴管生成在生理和病理改变中的相互关系将是今后的研究焦点之一。
参考文献
1 Folkman J, Shing Y. Angiogenesis. J Biol Chem, 1992,267(16): 10931.
2 Asahara T, Murohara T, Sullivan A, et al. Isolation of putative progenitor endothelial cells for angiogenesis. Science, 1997, 275: 964.
, 百拇医药
3 Asahara T. Endothelial progenitor cells for post-natal neovascularization. Abstract in the proceeding of AACR special conference in cancer research. Angiogenesis and Cancer, 1998
4 Carmeliet P, Ferreira V, Breier G, et al. Abnormal blood vessel development and lethality in embryos lacking a single VEGF allele. Nature, 1996, 380:435.
5 Bussolino F, Mantovani A, Persico G. Molecular mechanisms of blood vessel formation. TIBS, 1997, 22:251.
, 百拇医药
6 Wei MH, Popescu NC, Lerman MI, et al. Localization of the human vascular endothelial growth factor gene, VEGF, at chromosome 6p12. Hum Genet, 1996, 97(6):794.
7 Brown LF, Detmar M, Claffey K, et al. Vasclular permeability factor/vascular endothelial growth factor: A multifunctional angiogenic cytokine. Exs, 1997, 79:233.
8 Sugihara T, Wadhwa R, Kaul SC, et al. A novel alternatively spliced form of murine vascular endothelial growth factor, VEGF115. J Biol Chem, 1998, 273(5):3 033.
, 百拇医药
9 Poltorak Z, Cohen T, Sivan R, et al. VEGF145, a secreted vascular endothelial growth factor isoform that binds to extracellular matrix. J Biol Chem, 1997, 272(11):7 151.
10 Watanabe Y, Lee SW, Detmar M, et al. Vascular permeability factor/vascular endothelial growth factor (VPF/VEGF) delays and induces escape from senescence in human dermal microvascular endothelial cells. Oncogene, 1997, 14:2 025.
11 Feng D, Nagy JA, Hipp J, et al. Vesiculo-vacuolar organelles and the regulation of venule permeability to macromolecules by vascular permeability factor, histamine, and serotonin. J Exp Med, 1996, 183:1 981.
, http://www.100md.com
12 Mattei MG, Borg JP, Rosnet O, et al. Assignment of vascular endothelial growth factor(VEGF) and placenta growth factor (PlGF) genes to human chromosome 6p12-p21 and 14q24-q31 regions ,respectively. Genomics, 1996, 32(1):168.
13 Cao Y, Ji WR, Qi P, et al. Placenta growth factor: identification and characterization of a novel isoform generated by RNA alternative splicing. Biochem Biophys Res Commun, 1997, 235(3):493.
14 Cao Y, Chen H, Zhou L, et al. Heterodimers of placenta growth factor/vascular endothelial growth factor. J Biol Chem, 1996, 271(6):3 154.
, 百拇医药
15 Paavonen K, Horelli-Kuitunen N, Chilov D, et al. Novel human vascular endothelial growth factor genes VEGF-B and VEGF-C localized to chromosomes 11q13 and 4q34, respectively. Circulation, 1996, 93(6):1 079.
16 Joukov V, Kaipainen A, Jeltsch M, et al. Vascular endothelial growth factors VEGF-B and VEGF-C. J Cell Physiol, 1997, 173:211.
17 Alitalo K, Lymboussakis A, Enhom B, et al. VEGFs and receptors involved in angiogenesis and lymphangiogenesis. Abstract in the proceeding of AACR special conference in cancer research. Angiogenesis and Cancer, 1998.
, 百拇医药
18 Laitinan M, Ristimaki A, Honkasalo M, et al. Differential hormonal regulation of vascular endothelial growth factors VEGF, VEGF-B, and VEGF-C messenger ribonucleic acid levels in cultured human granulosa-luteal cells. Endocrinology, 1997, 138(11):4 748.
19 Kaipainen A, Korhonen J, Mustonen T, et al. Expression of the fms-like tyrosine kinase 4 gene becomes restricted to lymphatic endothelium during development. Proc Natl Acad Sci USA, 1995, 92:3 566.
, 百拇医药
20 Oh SJ, Jeltsch MM, Birkenhager R, et al. VEGF and VEGF-C: specific induction of angiogenesis and lymphangiogenesis in the differentiated avian chorioallantoic membrane. Develop Biol, 1997, 188:96.
21 Jeltsch M, Kaipainen A, Joukov V, et al. Hyperplasia of lymphatic vessels in VEGF-C transgenic mice. Science, 1997, 276:1 423.
22 Folkman J. Angiogenesis and tumor growth [letter; comment; discussion]. N Engl J Med, 1996, 334:921.
, 百拇医药
23 Rocchigiani M, Lestingi M, Luddi A, et al. Human FIGF: cloning, gene structure, and mapping to chromosome Xp22.1 between the PIGA and the GRPR genes. Genomics, 1998, 47(2):207.
24 Achen MG, Jeltsch M, Kukk E, et al. Vascular endothelial growth factor D(VEGF-D) is a ligand for tyrosine kinases VEGF receptor 2(Flk-1) and VEGF receptor 3(Flt-4). Proc Natl Acad Sci USA, 1998, 95:548.
25 Shibuya M. Role of VEGF-FLT receptor system in normal and tumor angiogenesis. Adv Cancer Res, 1995, 67:281.
, 百拇医药
26 Kendall RL, Wang G, Thomas KA. Identification of a natural soluble form of the vascular endothelial growth factor receptor, FLT-1, and its heterodimerization with KDR. Biochem Biophys Res Commun, 1996, 226(2):324.
27 Soker S, Takashima S, Miao HQ, et al. Neuropilin-1 is expressed by endothelial and tumor cells as an isoform-specific receptor for vascular endothelial growth factor. Cell, 1998, 92:735.
28 Benjamin LE, Keshet E. Conditional switching of vascular endothelial growth factor (VEGF) expression in tumors: induction of endothelial cell shedding and regression of hemangioblastoma-like vessels by VEGF withdrawal. Proc Natl Acad Sci USA, 1997, 94:8 761.
29 Kerbel RS. A cancer therapy resistant to resistance. Nature, 1997, 390:335.
30 Boehm T, Folkman J, Browder T, et al. Antiangiogenic therapy of experimental cancer does not induce acquired drug resistance. Nature, 1997, 390:404.
(1998年6月22日收稿,1998年11月6日修回), http://www.100md.com
单位:中山医科大学肿瘤防治中心(广州 510060)
关键词:
血管内皮生长因子的研究进展 Advances in research of vascular endothelial growth factor
QIAN Chao-Nan, MIN Hua-Qing
Cancer Center, Sun Yat-sen University of Medical Sciences, Guangzhou (510060)
【A Review】 Angiogenesis occurs in many physiological and pathological processes. Vascular endothelial growth factor( VEGF) is a key cytokine for up-regulation of angiogenesis. VEGF family includes some new members coded by the genes mapped in different chromosomes, namely ,VEGF-B, VEGF-C, VEGF-D, and PGF. Each member may have some isotypes due to splicing in mRNA transcription. VEGFR-1, VEGFR-2 and VEGFR-3 are three receptors of VEGF family. The combinations of VEGF family with different receptors can induce different functions, including increase vascular permeability, angiogenesis, and lymphangiogenesis. The biological characteristics of VEGF family and their receptors have been applied in diagnosis and experimental therapy of solid tumors, along with experimental therapy of ischemic retinopathy and ischemic heart disease.
, 百拇医药
在某些生理过程,如胚胎发育、卵巢周期、伤口愈合和缺血组织的修复,可出现新生血管的形成;而在某些病理过程,血管生成也是必不可少的环节,如类风湿性关节炎、银屑病糖尿病性视网膜病以及实体瘤的生长和转移[1]。
以往认为,出生后的血管生成(angiogenesis)与胚胎发育过程中的血管发生(vasculogenesis)是两个互相区别的过程:前者是通过分化完全的血管内皮细胞从业己存在的血管中增殖、迁徙和重塑而成;后者是指由中心包含造血干细胞、周边分布成血管细胞(angioblast)的血岛发育而成[1]。但近来的研究发现:出生后的血管生成(包括肿瘤血管生成),也有骨髓造血干细胞的参与[2,3]。骨髓里的造血干细胞在某些细胞因子(如G-CSF,GM-CSF,血小板反应素等)的刺激下,分化成血管内皮祖细胞(endothelial progenitor cells,即是成血管细胞);后者又在其它的因子(如stromal derived factor-l)的作用下进入周围血循环,在生理的以及病理的血管生成处分化成血管内皮细胞。因此现在认为,出生后的血管生成过程中,既有局部血管内皮细胞的增殖、迁徙、重塑,又有来自骨髓的血管内皮祖细胞的分化参与。
, 百拇医药
血管生成的诱导因子有的是直接作用于血管内皮细胞,有的是间接地通过其它的辅助细胞(单核细胞、肥大细胞、T细胞)来诱导血管生成。血管内皮生长因子(vascular endothelial growth factor, VEGF),也称VPF(vascular permeability factor,血管通透因子)或VAS(vasculotropin促血管因子),特异性地直接作用于血管内皮细胞,是上调血管生成的重要因子[1]。虽然VEGF最先是从肿瘤细胞的分泌物中分离出来,但现已证实VEGF及其家族成员不单在肿瘤血管生成,在其它的生理和病理的血管生成中都是必不可少的诱导因子[4]。目前已发现VEGF家族包括5大成员:VEGF-A(即以往发现的VEGF),VEGF-B,VEGF-C,VEGF-D和PGF(placental growth factor,胎盘生长因子)。它们都是二聚体的糖蛋白,都具有与类血小板生长因子蛋白区域(platelet-derived growth factor-like domain)非常相似的结构,即拥有8个完全保守、相隔排列、以二硫键维持二聚体的三维空间结构的半胱氨酸残基[5]。VEGF家族5个成员的基因分别定位于不同的染色体。
, http://www.100md.com
一、VEGF-A:
VEGF-A基因定位于6号染色体短臂1区2带(6 p12)[6]。根据VEGF-A的氨基酸链的长度不同至今已发现了6种异构体:VEGF-A115,VEGF-A121,VEGF-A145,VEGF-A165,VEGF-A189和VEGF-A206。VEGF-A121和VEGF-A165是最丰富的异构体。这些不同的异构体是由同一个基因在转录时按不同的拼接方式产生的[7],为34-42 kD的糖蛋白。VEGF-A基因拥有8个外显子。目前发现的所有VEGF-A异构体均有外显子1-5以及外显子8的表达序列。外显子1-5编码的部分是VEGF-A的核心区域,用于维持二聚体空间结构的8个特征性的半胱氨酸残基就处于这个核心部分。VEGF-A189是全部1-8个外显子编码的氨基酸序列完全表达的蛋白质产物。VEGF-A121缺乏外显子7和8编码的产物。VEGF-A145缺乏外显子7的表达。VEGF-A165缺乏外显子6′的表达。VEGF-A206除了8个外显子都有表达以外,在外显子6编码的氨基酸序列末端多出了一段17个氨基酸的延伸序列,为外显子6的产物。目前已证实VEGF-A121不与肝素结合,是可溶性分泌型蛋白;VEGF-A145也是分泌型蛋白[9];VEGF-A165是部分分泌、部分与细胞表面的硫酸乙酰肝素蛋白多糖结合;VEGF-A189和VEGF-A206是结合型蛋白,与细胞和基质中的蛋白多糖结合。最新报告的VEGF-A115在C-端与VEGF-A121有37个氨基酸的差异,其特性有待阐明[8]。
, 百拇医药
VEGF-A与两个受体高度亲和:VEGFR-1(VEGF受体1)和VEGFR-2(VEGF受体2),并能激活这两个受体。
许多正常组织(如肺、肾、肾上腺、心、卵巢等)的已分化细胞以及肿瘤细胞都可表达VEGF-A。缺氧是诱导VEGF-A及其受体产生的最有效因素。出现K-ras和H-ras突变的肿瘤细胞可以上调VEGF-A的转录,而肿瘤抑制基因VHL的蛋白产物却能下调VEGF-A的合成[5]。
VEGF-A是血管内皮细胞的促分裂原(mitogen)和促运动原(motogen),可诱导血管内皮细胞增殖和迁徙;还能诱导毛细血管管腔的形成、增加血管的通透性、刺激血管内皮细胞产生蛋白酶和其它的小分子物质[5]。虽然其确切的分子机制有待阐明,但目前已发现VEGF-A与其两个受体结合后,不但引起受体的磷酸化,还可产生一系列的蛋白质磷酸化[7]。这些蛋白质包括磷脂酶Cγ,磷脂酰肌醇3激酶,GAP(Ras GTPase-activating protein),两个GTP相关蛋白p190和p62,以及癌基因结合蛋白NcK。近来还发现VEGF-A可激活分裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)。
, 百拇医药
VEGF可非常显著地延长血管内皮细胞的寿命,使血管内皮细胞的倍增次数增加15~20次;同时使血管内皮细胞的某些周期相关基因(p21,p16和p27)的表达减少,但P53表达无改变;同时也减少衰老标记物中性β-半乳糖苷酶的表达[10]。
VEGF-A增加血管通透性的作用可能是通过增强了血管内皮细胞中的囊-泡小体(VVO,vesiculo-vacuolar organelle)的功能而产生的[11]。VVO是近年来发现的、在微静脉和小静脉的内皮细胞质里的一种细胞器,这种似葡萄串的细胞器与内皮细胞的腔内面和腔外面相连,可以占细胞质的20%。VEGF-A可以促进大分子物质经VVO渗出血管外。
二、PGF:
PGF也是一个二聚体,其氨基酸序列与VEGF-A有53%的同源性[7]。其基因定位于14q24-q31[12]。已发现PGF有3个异构体,即PGF-1,PGF-2和PGF-3,是同一基因在转录mRNA时以不同的拼接方式表达的不同产物[7,13]。PGF-1除拥有与VEGF-A相同的、由外显子1-5编码的氨基酸序列,还有一个由外显子7编码的区域。PGF-1的前体是149个氨基酸,其中一段含20个氨基酸的多肽裂解出来后,就形成129个氨基酸的成熟PGF-1。PGF-2的前体含有170个氨基酸,比PGF-1前体多出了一个由外显子6编码的21个氨基酸的序列,成熟PGF-2含152个氨基酸。PGF-3的前体含有219个氨基酸,比PGF-1多出的70个氨基酸是由一段在外显子4和5之间插入的核苷酸序列编码。PGF-3与PGF-1一样缺乏外显子6的表达[13]。PGF-2与肝素高度亲和,主要分布于细胞表面和基质中;PGF-1和PGF-3与肝素亲和性很低,是分泌型蛋白。PGF可结合并激活VEGFR-1,不与VEGFR-2或VEGFR-3结合(见图1);但PGF的单体可以和VEGF-A的单体形成VEGF/PGF异二聚体,与VEGFR-2牢固结合并激活该受体,促进内皮细胞分裂和迁徙[14]。与VEGF不同的是,PGF的表达只限于血管生成活跃的组织,如胎盘组织(由血管内皮细胞表达)和肿瘤组织(由肿瘤细胞表达),并不见于已分化成熟的细胞。
, http://www.100md.com
与VEGF-A相比,PGF诱导血管内皮细胞分裂和增加血管通透性的作用较弱。然而,PGF可以增强VEGF-A的功能[5]。
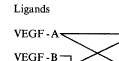

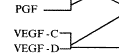

, http://www.100md.com
Fig 1 The correlation between members of VEGF family and their receptors
图1 VEGF家族成员的配体和受体的相互关系
三、VEGF-B:
VEGF-B基因定位于11q13,长约4 kb[15];有7个外显子,其外显子与内含子的组织形式与VEGF-A和PGF基因相似[16]。此基因在转录时以不同的拼接方式产生了两种异构体:VEGF-B167(21 kD)和VEGF-B186(32 kD),两者都与VEGF-A165非常相似,都是以二硫键连接的二聚体。VEGF-B186比VEGF-B167多出了一段在外显子6中插入的、由101碱基对的核酸序列编码的多肽[19]。两个异构体在N-端有相同的115个氨基酸,但C-端却不同:VEGF-B167的C-端为碱性并富含半胱氨酸,可与肝素结合;而VEGF-B186的C-端却富含丙氨酸、脯氨酸、丝氨酸和苏氨酸,不与肝素结合。因此VEGF-B167是细胞相关的分泌型蛋白;而VEGF-B186由于没有高度碱性的基团,可以从细胞自由分泌,并且不与细胞表面或细胞周围的硫酸乙酰肝素蛋白多糖结合[16]。
, http://www.100md.com
VEGF-B的两个异构体都与VEGFR-1结合并激活此受体[17]。VEGF-B也可与VEGF-A形成异二聚体,并可能借此影响VEGF-A的生物功能[18]。许多正常组织都有表达VEGF-B,如心肌、骨骼肌、胰腺、肺、肾脏、卵巢等[18]。
四、VEGF-C:
VEGF-C基因定位于4q34[15]。VEGF-C cDNA的开放阅读区编码一个419个氨基酸的前体蛋白质(46.9 kD)。这一前体蛋白质依次有4个区域:N-端信号多肽,N-端前多肽,VEGF同源区和C-端前多肽。VEGF-C的VEGF同源区与VEGF-A165的有30%同源,与VEGF-B167的有27%同源,与PGF-1的有25%同源[16]。
VEGF-C在许多正常组织都有表达,包括:心肌、骨骼肌、肺脏、肾脏[15]。其受体是VEGFR-2和VEGFR-3。VEGFR-3是第一个被发现的淋巴内皮细胞特异性的标记物[19]。而VEGF-C是第一个被发现的淋巴管生成因子,它可以诱导淋巴内皮细胞增殖、迁徙,并形成淋巴窦[20]。在一个转基因动物实验中,VEGF-C的过度表达可以引起动物皮下淋巴管的异常增生[21]。
, 百拇医药
目前尚无直接证据显示肿瘤细胞会诱导淋巴管生成[22]。相信对VEGF-C的进一步研究将有助于阐明VEGF-C在淋巴管瘤、肿瘤经淋巴道转移以及其它的淋巴系统病变中的作用。
五、VEGF-D:
VEGF-D基因定位于Xp22.1。小鼠的VEGF-D基因的表达是通过转录因子c-fos的诱导作用而产生,因此也称FIGF(c-fos-induced growth factor)基因。此基因跨度50 kb,并有7个外显子和6个内含子[23]。VEGF-D蛋白含有354个氨基酸,与VEGF-C有48%同源,与VEGF-A165有31%同源,与VEGF-B167有28%同源,与PGF有32%同源。在VEGF家族中,其蛋白质结构最接近VEGF-C,表现在:VEGF-D的VEGF同源区最接近VEGF-C(仅计算此区有61%的同源性);只有VEGF-D和VEGF-C拥有长N-端扩展区(此区两者25%同源)和长C-端扩展区(37%同源)。VEGF-D可在许多正常组织大量表达,包括:心、肺、骨骼肌、结肠和小肠[24]。
, http://www.100md.com
不仅结构上与VEGF-C相似,在功能上VEGF-D也与之相似:VEGF-D能与VEGFR-2和VEGFR-3结合并能激活这两个受体,但不能与VEGFR-1结合。初步发现VEGF-D可促进血管内皮细胞分裂[24]。由于VEGF-C和VEGF-D激活相同的受体,因此推测VEGF-D可能会在血管生成和淋巴管生成方面与VEGF-C协同作用。
在一个转基因小鼠的实验中,持续的c-fos表达可诱导动物最终形成骨肉瘤,而c-fos缺失的肿瘤细胞却不具备恶性行为[5]。今后有必要进一步阐明:在c-fos过度表达的肿瘤组织中是否具有高水平的VEGF-D的表达,以及VEGF-D是否通过诱导血管和/或淋巴管生成来参与恶性肿瘤的发生和发展。
六、VEGF家族的受体:
VEGF家族的3个受体分别由3个基因编码[25]。180 kD的VEGFR-1由Flt-1(fms-like tyrosine kinase 1)基因(定位于13q12-q13)编码。200 kD的VEGFR-2由Flk-1/KDR基因(定位于4q11-q13)编码。Flk-1(fetal liver kinase 1)是从小鼠胎肝的cDNA文库中分离出的;而相应地从人血管内皮细胞cDNA文库中分离出的基因称KDR(kinase domain receptor)。180 kD的VEGFR-3是由Flt-4基因(定位于5q33-q34)碥码。三者都是跨膜酪氨酸激酶受体,都有7个免疫球蛋白样的细胞外区域、跨细胞膜区域以及一个含有酪氨酸激酶的细胞内区域。每个血管内皮细胞表面有VEGFR-1约3000个,对VEGF-A的亲和力KD=1-20 Pm;有VEGFR-2约40 000个,对VEGF-A的亲和力KD=50-770 Pm[7]。VEGF-A与VEGFR-1和VEGFR-2的结合位点分别是外显子3和外显子4的编码区[5]。
, 百拇医药
原已发现VEGFR-1和VEGFR-2高度选择性地在血管内皮细胞表达,但近年来有人报告在一些非内皮细胞的组织细胞也有表达[7]。在胚胎发育的早期,血管内皮细胞会表达VEGFR-2和VEGFR-3,但是在发育到胎儿以后,VEGFR-3仅在淋巴内皮细胞表达[19]。VEGFR-3不与VEGF-A结合。
可溶性的VEGFR-1已被发现[26],是VEGFR-1的细胞外片段,可与完整的VEGFR-2形成二聚体后再与VEGF-A结合,阻断VEGF-A对血管内皮细胞的各种诱导作用,是天然的血管生成抑制剂。
最近又发现一个VEGF-A165的异构体专一性受体Neuropilin-1[27]。这个130-135 kD的细胞膜受体只与VEGF-A165结合,结合位点是VEGF-A基因的外显子7编码区。当此受体与VEGFR-2共同表达时,可增强VEGF-A165与VEGFR-2的结合以及VEGF-A165促内皮细胞迁徙的功能。抑制此受体与VEGF-A165结合后,VEGF-A165与VEGFR-2的结合亦被抑制,同时VEGF-A165促血管内皮细胞分裂的作用也被抑制。此受体可由血管内皮细胞和多种肿瘤细胞表达。
, 百拇医药
七、应用研究:
VEGF-A及其受体在肿瘤组织中的高水平表达与多种肿瘤的预后不良有关,这些肿瘤包括星形细胞瘤、肺癌、结肠癌、膀胱癌、头颈鳞癌等(Abdulrauf SI, et al 1998; Takahashi, et al 1998; Crew JP, et al 1997; Volm M, et al 1988; Denhart BC, et al 1997)。VEGF-A在癌症病人的血清和组织液(如腹水)的表达水平高于正常人(Kondo S, et al 1994; Barton DPJ, et al 1997),有必要进一步了解其监测疗效和预后的意义。
动物实验显示:把VEGF-A注入手术皮瓣的供血动脉后可以促进皮瓣的血管生成,从而增加皮瓣的成活面积(Padubidri A, et al 1996)。把能短暂表达VEGF-A121 cDNA而丧失复制能力的腺病毒载体直接注入猪的缺血的心肌组织中,可以诱导侧枝血管的建立,明显提高心肌的灌注和改善心肌的功能(Mack CA, et al 1998)。
, http://www.100md.com
不少缺血性视网膜病引起失明的原因都与视网膜的血管生成有关。动物实验显示:把可溶性VEGFR-1注入玻璃体内,可抑制VEGF-A的活性,从而抑制了视网膜的血管生成(Aiello LP, et al 1995)。
虽然有研究显示使用VEGF-A拮抗剂可以使实体瘤退缩[28],但有人认为这种治疗手段不可取[29]。因为肿瘤细胞除了分泌VEGF-A以外,还分泌其它的血管生长因子;而且肿瘤细胞基因组的高度不稳定性决定了它可以通过分化新的克隆产生新的血管生长因子,从而避开原有的攻击,象耐受临床常规使用的细胞毒性化疗药物一样,最终会对VEGF-A拮抗剂产生耐药。相反,由于血管内皮细胞的基因组高度稳定,通过直接抑制血管内皮细胞来治疗肿瘤就不会产生耐药现象,这已被内皮抑素(endostatin)的实验性治疗所证实[30]。
八、结语:
, 百拇医药 VEGF家族及其受体的复杂性体现了高等生命的具体生物功能受多层次影响、多基因调控的现象。VEGF家族是一类多功能的细胞因子,在血管生成和淋巴管生成中具有直接和间接的调控作用。一方面VEGF家族可以刺激血管内皮细胞增埴、迁徙甚至改变其基因表达;另一方面它们又可以增加血管的通透性,使许多血浆蛋白渗出血管外,这对改造局部的细胞外基质以适应血管生成具有重要作用。大量的血浆蛋白渗出到组织液中会使组织液的渗透压增高。这是实体瘤的瘤内渗透压高于正常组织渗透压的原因之一。而VEGF-C和VEGF-D诱导的淋巴管生成有助于组织液的引流。有关VEGF家族调控的血管生成和淋巴管生成在生理和病理改变中的相互关系将是今后的研究焦点之一。
参考文献
1 Folkman J, Shing Y. Angiogenesis. J Biol Chem, 1992,267(16): 10931.
2 Asahara T, Murohara T, Sullivan A, et al. Isolation of putative progenitor endothelial cells for angiogenesis. Science, 1997, 275: 964.
, 百拇医药
3 Asahara T. Endothelial progenitor cells for post-natal neovascularization. Abstract in the proceeding of AACR special conference in cancer research. Angiogenesis and Cancer, 1998
4 Carmeliet P, Ferreira V, Breier G, et al. Abnormal blood vessel development and lethality in embryos lacking a single VEGF allele. Nature, 1996, 380:435.
5 Bussolino F, Mantovani A, Persico G. Molecular mechanisms of blood vessel formation. TIBS, 1997, 22:251.
, 百拇医药
6 Wei MH, Popescu NC, Lerman MI, et al. Localization of the human vascular endothelial growth factor gene, VEGF, at chromosome 6p12. Hum Genet, 1996, 97(6):794.
7 Brown LF, Detmar M, Claffey K, et al. Vasclular permeability factor/vascular endothelial growth factor: A multifunctional angiogenic cytokine. Exs, 1997, 79:233.
8 Sugihara T, Wadhwa R, Kaul SC, et al. A novel alternatively spliced form of murine vascular endothelial growth factor, VEGF115. J Biol Chem, 1998, 273(5):3 033.
, 百拇医药
9 Poltorak Z, Cohen T, Sivan R, et al. VEGF145, a secreted vascular endothelial growth factor isoform that binds to extracellular matrix. J Biol Chem, 1997, 272(11):7 151.
10 Watanabe Y, Lee SW, Detmar M, et al. Vascular permeability factor/vascular endothelial growth factor (VPF/VEGF) delays and induces escape from senescence in human dermal microvascular endothelial cells. Oncogene, 1997, 14:2 025.
11 Feng D, Nagy JA, Hipp J, et al. Vesiculo-vacuolar organelles and the regulation of venule permeability to macromolecules by vascular permeability factor, histamine, and serotonin. J Exp Med, 1996, 183:1 981.
, http://www.100md.com
12 Mattei MG, Borg JP, Rosnet O, et al. Assignment of vascular endothelial growth factor(VEGF) and placenta growth factor (PlGF) genes to human chromosome 6p12-p21 and 14q24-q31 regions ,respectively. Genomics, 1996, 32(1):168.
13 Cao Y, Ji WR, Qi P, et al. Placenta growth factor: identification and characterization of a novel isoform generated by RNA alternative splicing. Biochem Biophys Res Commun, 1997, 235(3):493.
14 Cao Y, Chen H, Zhou L, et al. Heterodimers of placenta growth factor/vascular endothelial growth factor. J Biol Chem, 1996, 271(6):3 154.
, 百拇医药
15 Paavonen K, Horelli-Kuitunen N, Chilov D, et al. Novel human vascular endothelial growth factor genes VEGF-B and VEGF-C localized to chromosomes 11q13 and 4q34, respectively. Circulation, 1996, 93(6):1 079.
16 Joukov V, Kaipainen A, Jeltsch M, et al. Vascular endothelial growth factors VEGF-B and VEGF-C. J Cell Physiol, 1997, 173:211.
17 Alitalo K, Lymboussakis A, Enhom B, et al. VEGFs and receptors involved in angiogenesis and lymphangiogenesis. Abstract in the proceeding of AACR special conference in cancer research. Angiogenesis and Cancer, 1998.
, 百拇医药
18 Laitinan M, Ristimaki A, Honkasalo M, et al. Differential hormonal regulation of vascular endothelial growth factors VEGF, VEGF-B, and VEGF-C messenger ribonucleic acid levels in cultured human granulosa-luteal cells. Endocrinology, 1997, 138(11):4 748.
19 Kaipainen A, Korhonen J, Mustonen T, et al. Expression of the fms-like tyrosine kinase 4 gene becomes restricted to lymphatic endothelium during development. Proc Natl Acad Sci USA, 1995, 92:3 566.
, 百拇医药
20 Oh SJ, Jeltsch MM, Birkenhager R, et al. VEGF and VEGF-C: specific induction of angiogenesis and lymphangiogenesis in the differentiated avian chorioallantoic membrane. Develop Biol, 1997, 188:96.
21 Jeltsch M, Kaipainen A, Joukov V, et al. Hyperplasia of lymphatic vessels in VEGF-C transgenic mice. Science, 1997, 276:1 423.
22 Folkman J. Angiogenesis and tumor growth [letter; comment; discussion]. N Engl J Med, 1996, 334:921.
, 百拇医药
23 Rocchigiani M, Lestingi M, Luddi A, et al. Human FIGF: cloning, gene structure, and mapping to chromosome Xp22.1 between the PIGA and the GRPR genes. Genomics, 1998, 47(2):207.
24 Achen MG, Jeltsch M, Kukk E, et al. Vascular endothelial growth factor D(VEGF-D) is a ligand for tyrosine kinases VEGF receptor 2(Flk-1) and VEGF receptor 3(Flt-4). Proc Natl Acad Sci USA, 1998, 95:548.
25 Shibuya M. Role of VEGF-FLT receptor system in normal and tumor angiogenesis. Adv Cancer Res, 1995, 67:281.
, 百拇医药
26 Kendall RL, Wang G, Thomas KA. Identification of a natural soluble form of the vascular endothelial growth factor receptor, FLT-1, and its heterodimerization with KDR. Biochem Biophys Res Commun, 1996, 226(2):324.
27 Soker S, Takashima S, Miao HQ, et al. Neuropilin-1 is expressed by endothelial and tumor cells as an isoform-specific receptor for vascular endothelial growth factor. Cell, 1998, 92:735.
28 Benjamin LE, Keshet E. Conditional switching of vascular endothelial growth factor (VEGF) expression in tumors: induction of endothelial cell shedding and regression of hemangioblastoma-like vessels by VEGF withdrawal. Proc Natl Acad Sci USA, 1997, 94:8 761.
29 Kerbel RS. A cancer therapy resistant to resistance. Nature, 1997, 390:335.
30 Boehm T, Folkman J, Browder T, et al. Antiangiogenic therapy of experimental cancer does not induce acquired drug resistance. Nature, 1997, 390:404.
(1998年6月22日收稿,1998年11月6日修回), http://www.100md.com