中药EGb24/6对鼠坐骨神经损伤后神经元保护的实验研究
作者:张烽 顾玉东 徐建光 李继峰
单位:张烽(现在南通医学院附属医院骨科 226001);顾玉东 徐建光 李继峰(上海医科大学华山医院手外科 200040)
关键词:
中华医学杂志000331 周围神经损伤后神经元的变性、死亡对周围神经再生及功能的恢复有着重大的影响[1]。如何保护神经损伤后的神经元,减少其死亡,促进神经再生及功能恢复已引起重视。中药EGb(Extract of Ginkgo biloba)通过对抗脑缺血引起的谷胺酸毒性作用,来保护神经元[2]。我们用EGb对神经损伤后神经元的变化进行了观察。
一、材料与方法
1.动物和分组:雄性SD大鼠18只,体重180~220 g(鼠龄约8~9周)分成损伤对照组和实验组即EGb24/6组(EGb24/6由美国PHARMANEX,INC公司提供)。
, http://www.100md.com
2.手术方法:1%硫苯妥钠(5 μg/100 g)行腹腔麻醉,左侧臀部行1.5 cm切口,在臀肌间隙显露坐骨神经,距梨状肌下缘0.5 cm处切断坐骨神经,近端5~0线双重结扎,远端埋入股二头肌中。手术后神经损伤组给予2 ml生理盐水灌胃。实验组给予EGb24/6 20 mg(溶于生理盐水2 ml)灌胃,每天一次,直至取材,最长的为28 d。
3.取材:术后第7 d、14 d、28 d分别取材,每组3只。大鼠再次麻醉,开胸,将11号针头插入左心室,右心房开一小口。先用生理盐水250 ml灌注,迅速洗净组织内血液,再以4%多聚甲醛PBS液心脏灌注30 min。切取L4-6脊髓和L5背根神经节,标本按常规固定、脱水、包埋、切片、切片厚度5 μm,每隔20张取1张切片,每个标本取5张。分别行HE染色,焦油紫染色和末端脱氧核糖核苷酸转移酶介导的dUTP法[Terminal deoxynucleotidyl transferase(TdT)-mediated digoxingenin-dUTP nicked labeling TUNEL]检测。TUNEL标记的检测是对脊髓运动神经元和背根神经节感觉神经元的凋亡细胞作计数分析。HE焦油紫染色后切片、观察脊髓运动神经元的数目变化。
, http://www.100md.com
4.统计学处理:用Poisson 检验、t检验。
二、结果
1.HE焦油紫染色: 实验组在各时间点脊髓前角运动神经元数目,明显多于对照组。两者差异有显著意义(P<0.01)。TUNEL观察:脊髓运动神经元及背根神经节感觉神经元均标记到凋亡细胞,凋亡细胞其特征为细胞核染色质浓聚、核固缩、细胞碎裂、形成凋亡小体。正常侧脊髓及背根神经节均未检出凋亡细胞。由表1可见术后7、14、28 d运动和感觉神经元标记的凋亡细胞实验组明显少于对照组,统计学上有显著差异(P<0.05)(表1)。
表1 脊髓前角运动神经元及TUNEL标记的运动神经元及背根神经节感觉神经元凋亡细胞 组 别
脊髓前角运动神经元(L/R)(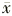 ±
±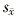 ,%)
,%)
, http://www.100md.com
第7天
第14天
第28天
对照组
83.5±1.2
80.5±1.1
78.6±1.2
EGb24/6
89.5±0.7
87.6±1.2
85.1±1.1
t值
, http://www.100md.com 7.58
7.77
6.87
P值
<0.01
<0.01
<0.01
组 别
TUNEL标记的运动神经元*(个)
第7天
第14天
第28天
对照组
, 百拇医药
7,6,7
8,9,8
7,9,12
EGb24/6
4,1,2
5,2,4
6,4,4,U值
2.5
2.33
2.16
P值
<0.05
<0.05
, 百拇医药
<0.05
组 别
TUNEL标记的感觉神经元*(个)
第7天
第14天
第28天
对照组
15,12,18
16,18,21
35,26,28
EGb24/6
8,6,11
, 百拇医药
12,7,9
18,15,21
U值
2.39
2.96
4.59
P值
<0.05
<0.05
<0.05
*Poisson检验
三、讨论
, http://www.100md.com 最近的研究表明,神经损伤后神经元的死亡即是程序性细胞死亡(凋亡)[3]。由于上述的研究选择的实验动物为胚鼠和新生鼠,它们各自在生长发育过程中本身存在着年龄性细胞死亡(PCD)。因此,我们选择了体重180~220 g的大白鼠(年龄约8~9周)可基本上排除PCD的干扰和影响。研究神经损伤与神经死亡关系,主要采用的动物模型为大鼠坐骨神经或舌下神经挤压伤或神经切断,前者由于大鼠为低等动物神经再生速度很快,加之距离短,神经修复约2周左右的时间、神经生长就能到效应器,一些靶源性神经营养因子可以被摄取并逆行运送到相应的神经元。而成年鼠神经元凋亡的发生始于伤后7 d左右,药物对神经元的保护易受自身神经营养因子等因素的干扰。即使单纯的切断神经,甚至切断后再切除一段,但仍有轴突可以长入与之神经相粘连的肌肉中。而神经切断后,近端结扎远端埋入肌肉,可以阻止神经再生排除靶源性神经营养因子的干扰,是研究药物对神经元保护作用的较理想的实验模型。有关神经损伤神经元凋亡的机制;较为经典的理论是神经元营养丧失学说(trophic factor deprivation)即由于轴突的损伤,阻断了靶源性营养因子的逆行运输,使神经元失去了营养,从而导致了神经元的死亡。我们的实验结果说明,EGb24/6对神经损伤后脊髓运动神经元和背根神经节感觉神经元有一定的保护作用。发生作用的机制可能与EGb中含有内酯B通过降低Ca2+水平对抗谷氨酸神经毒性有关,亦可能与其抑制NOS有关神经损伤后神经元NOs表达上调[4],抑制NOS的药物对神经元有一定的保护作用。除此以外,EGb对抗游离自由基,清除血小板活性因子(PDF)[5]的作用来保护细胞。作为神经损伤后的治疗辅助药物,EGb不但能促进神经再生,而且对神经元有保护作用。该药系中国古树银杏叶的提取物来源广泛,价格低廉具有较大的实用价值。
, 百拇医药
基金项目:上海市领先学科基金资助项目(95-Ⅲ-1);国家卫生部重点学科基金资助项目(96-3);美国中华医学基金资助项目(95-619)
参考文献:
1 罗永湘,方煌,庞清江,等.神经生长因子对周围神经运动纤维再生的影响,中华手外科杂志, 1997,13:3-5.
2 Zhu Li, Wu Juan, Liao Hong, et al. Autagonistic effects of extract from leaves of Ginkgo biloba on glutamate neurotoxicity. Acta Pharmacologica Sinica, 1997; 18: 344-347.
3 Oliveira ALR, Risling M, Deckner M, et al. Neonatal sciatic nerve transection induces TUNEL labling of neurons in the rat spinal cord and DRG. Neuroreport, 1997,8:2837-2840.
, http://www.100md.com
4 Rossiter JP, Riopelle RJ, Bisby MA. Axotomy-induced apoptotic death of neonatal rat fasial motonurons: Time course analysis and relation to NADPH-diaphorase activity. Exp Neurol, 1996,138:33-44.
5 Smith PF. Maclennan K. Darlington CL. The neuroprotective properties of the Ginkgo biloba leaf: a review of the possible relationship to platelet-acting factor (PAF). J Ethnopharmacol ,1996,50:131-139.
收稿日期:1999-05-17, http://www.100md.com
单位:张烽(现在南通医学院附属医院骨科 226001);顾玉东 徐建光 李继峰(上海医科大学华山医院手外科 200040)
关键词:
中华医学杂志000331 周围神经损伤后神经元的变性、死亡对周围神经再生及功能的恢复有着重大的影响[1]。如何保护神经损伤后的神经元,减少其死亡,促进神经再生及功能恢复已引起重视。中药EGb(Extract of Ginkgo biloba)通过对抗脑缺血引起的谷胺酸毒性作用,来保护神经元[2]。我们用EGb对神经损伤后神经元的变化进行了观察。
一、材料与方法
1.动物和分组:雄性SD大鼠18只,体重180~220 g(鼠龄约8~9周)分成损伤对照组和实验组即EGb24/6组(EGb24/6由美国PHARMANEX,INC公司提供)。
, http://www.100md.com
2.手术方法:1%硫苯妥钠(5 μg/100 g)行腹腔麻醉,左侧臀部行1.5 cm切口,在臀肌间隙显露坐骨神经,距梨状肌下缘0.5 cm处切断坐骨神经,近端5~0线双重结扎,远端埋入股二头肌中。手术后神经损伤组给予2 ml生理盐水灌胃。实验组给予EGb24/6 20 mg(溶于生理盐水2 ml)灌胃,每天一次,直至取材,最长的为28 d。
3.取材:术后第7 d、14 d、28 d分别取材,每组3只。大鼠再次麻醉,开胸,将11号针头插入左心室,右心房开一小口。先用生理盐水250 ml灌注,迅速洗净组织内血液,再以4%多聚甲醛PBS液心脏灌注30 min。切取L4-6脊髓和L5背根神经节,标本按常规固定、脱水、包埋、切片、切片厚度5 μm,每隔20张取1张切片,每个标本取5张。分别行HE染色,焦油紫染色和末端脱氧核糖核苷酸转移酶介导的dUTP法[Terminal deoxynucleotidyl transferase(TdT)-mediated digoxingenin-dUTP nicked labeling TUNEL]检测。TUNEL标记的检测是对脊髓运动神经元和背根神经节感觉神经元的凋亡细胞作计数分析。HE焦油紫染色后切片、观察脊髓运动神经元的数目变化。
, http://www.100md.com
4.统计学处理:用Poisson 检验、t检验。
二、结果
1.HE焦油紫染色: 实验组在各时间点脊髓前角运动神经元数目,明显多于对照组。两者差异有显著意义(P<0.01)。TUNEL观察:脊髓运动神经元及背根神经节感觉神经元均标记到凋亡细胞,凋亡细胞其特征为细胞核染色质浓聚、核固缩、细胞碎裂、形成凋亡小体。正常侧脊髓及背根神经节均未检出凋亡细胞。由表1可见术后7、14、28 d运动和感觉神经元标记的凋亡细胞实验组明显少于对照组,统计学上有显著差异(P<0.05)(表1)。
表1 脊髓前角运动神经元及TUNEL标记的运动神经元及背根神经节感觉神经元凋亡细胞 组 别
脊髓前角运动神经元(L/R)(
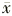 ±
±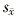 ,%)
,%), http://www.100md.com
第7天
第14天
第28天
对照组
83.5±1.2
80.5±1.1
78.6±1.2
EGb24/6
89.5±0.7
87.6±1.2
85.1±1.1
t值
, http://www.100md.com 7.58
7.77
6.87
P值
<0.01
<0.01
<0.01
组 别
TUNEL标记的运动神经元*(个)
第7天
第14天
第28天
对照组
, 百拇医药
7,6,7
8,9,8
7,9,12
EGb24/6
4,1,2
5,2,4
6,4,4,U值
2.5
2.33
2.16
P值
<0.05
<0.05
, 百拇医药
<0.05
组 别
TUNEL标记的感觉神经元*(个)
第7天
第14天
第28天
对照组
15,12,18
16,18,21
35,26,28
EGb24/6
8,6,11
, 百拇医药
12,7,9
18,15,21
U值
2.39
2.96
4.59
P值
<0.05
<0.05
<0.05
*Poisson检验
三、讨论
, http://www.100md.com 最近的研究表明,神经损伤后神经元的死亡即是程序性细胞死亡(凋亡)[3]。由于上述的研究选择的实验动物为胚鼠和新生鼠,它们各自在生长发育过程中本身存在着年龄性细胞死亡(PCD)。因此,我们选择了体重180~220 g的大白鼠(年龄约8~9周)可基本上排除PCD的干扰和影响。研究神经损伤与神经死亡关系,主要采用的动物模型为大鼠坐骨神经或舌下神经挤压伤或神经切断,前者由于大鼠为低等动物神经再生速度很快,加之距离短,神经修复约2周左右的时间、神经生长就能到效应器,一些靶源性神经营养因子可以被摄取并逆行运送到相应的神经元。而成年鼠神经元凋亡的发生始于伤后7 d左右,药物对神经元的保护易受自身神经营养因子等因素的干扰。即使单纯的切断神经,甚至切断后再切除一段,但仍有轴突可以长入与之神经相粘连的肌肉中。而神经切断后,近端结扎远端埋入肌肉,可以阻止神经再生排除靶源性神经营养因子的干扰,是研究药物对神经元保护作用的较理想的实验模型。有关神经损伤神经元凋亡的机制;较为经典的理论是神经元营养丧失学说(trophic factor deprivation)即由于轴突的损伤,阻断了靶源性营养因子的逆行运输,使神经元失去了营养,从而导致了神经元的死亡。我们的实验结果说明,EGb24/6对神经损伤后脊髓运动神经元和背根神经节感觉神经元有一定的保护作用。发生作用的机制可能与EGb中含有内酯B通过降低Ca2+水平对抗谷氨酸神经毒性有关,亦可能与其抑制NOS有关神经损伤后神经元NOs表达上调[4],抑制NOS的药物对神经元有一定的保护作用。除此以外,EGb对抗游离自由基,清除血小板活性因子(PDF)[5]的作用来保护细胞。作为神经损伤后的治疗辅助药物,EGb不但能促进神经再生,而且对神经元有保护作用。该药系中国古树银杏叶的提取物来源广泛,价格低廉具有较大的实用价值。
, 百拇医药
基金项目:上海市领先学科基金资助项目(95-Ⅲ-1);国家卫生部重点学科基金资助项目(96-3);美国中华医学基金资助项目(95-619)
参考文献:
1 罗永湘,方煌,庞清江,等.神经生长因子对周围神经运动纤维再生的影响,中华手外科杂志, 1997,13:3-5.
2 Zhu Li, Wu Juan, Liao Hong, et al. Autagonistic effects of extract from leaves of Ginkgo biloba on glutamate neurotoxicity. Acta Pharmacologica Sinica, 1997; 18: 344-347.
3 Oliveira ALR, Risling M, Deckner M, et al. Neonatal sciatic nerve transection induces TUNEL labling of neurons in the rat spinal cord and DRG. Neuroreport, 1997,8:2837-2840.
, http://www.100md.com
4 Rossiter JP, Riopelle RJ, Bisby MA. Axotomy-induced apoptotic death of neonatal rat fasial motonurons: Time course analysis and relation to NADPH-diaphorase activity. Exp Neurol, 1996,138:33-44.
5 Smith PF. Maclennan K. Darlington CL. The neuroprotective properties of the Ginkgo biloba leaf: a review of the possible relationship to platelet-acting factor (PAF). J Ethnopharmacol ,1996,50:131-139.
收稿日期:1999-05-17, http://www.100md.com