瘢痕涂膜质量标准的研究
作者:王玉珍 陈再兴 孟宪生 王东 龙沛霞
单位:王玉珍 陈再兴 孟宪生 王东 龙沛霞 辽宁中医学院(沈阳 110032)
关键词:瘢痕涂膜;丹参酮ⅡA;薄层扫描法
瘢痕涂膜质量标准的研究 摘 要 采用薄层色谱法对瘢痕涂膜中五倍子、苦参、冰片、甘草等成分进行鉴别,薄层扫描法测定丹参酮ⅡA的含量,加样回收率为95.4%,RSD=2.1%(n=6)。
瘢痕涂膜系由丹参、川芎、五倍子、苦参、冰片等十二味中药经科学方法提取精制成新型外用新药,用于预防和辅助治疗增生挛缩性瘢痕。经药效学试验和临床观察,疗效显著。为更好地控制本品的内在质量,保证疗效,笔者采用薄层色谱法对其中五倍子等4味药进行化学成分鉴别,用薄层扫描法测定其有效成分丹参酮ⅡA的含量,为本品建立一个较完善的控制质量的标准[1,2]。
, 百拇医药
1 仪器与试药
CS-930薄层扫描仪(日本岛津),硅胶G、硅胶GF254(薄层层析用,青岛海洋化工厂),没食子酸、氧化苦参碱、槐定碱、冰片、甘草酸铵、丹参酮ⅡA对照品由中国药品生物制品检定所提供,瘢痕涂膜由鞍钢华泰药业公司提供,所用试剂均为分析纯。
2 薄层鉴别
2.1 五倍子中没食子酸的鉴别
2.1.1 对照品溶液的制备:取没食子酸对照品,加乙醇制成0.5 mg/mL的溶液,作为对照品溶液。
2.1.2 阴性对照溶液的制备:按处方取除被测药材外的各味药材,照供试品溶液的制备方法制成阴性对照溶液(以下各阴性制照溶液的制备方法相同)。
, 百拇医药 2.1.3 薄层层析:照薄层色谱法(《中国药典》95版一部附录35页)试验,吸取含量测定项下的供试品溶液5 μL,对照品溶液3 μL,分别点于同一用2%氢氧化钠溶液制备的羧甲基纤维素钠为粘合剂的硅胶G薄层板上,以氯仿-甲醇-甲酸(15∶5∶1)为展开剂,在15℃以下展开,取出,晾干,喷以3%三氯化铁乙醇溶液。供试品色谱中,在与对照品色谱相同的位置上,显相同的蓝黑色斑点。
2.2 苦参中氧化苦参碱和槐定碱的鉴别
2.2.1 供试品溶液的制备:取本品20 g置玻板上,铺成薄膜,晾干后剪碎,加入0.2%盐酸溶液100 mL,超声处理1 h,倾出上清液,加浓氨试液,调 pH 8~10,用氯仿提取3次,每次20 mL,合并氯仿提取液,蒸干,残渣加氯仿0.5 mL使溶解,作为供试品溶液。
2.2.2 对照品溶液的制备:取氧化苦参碱和槐定碱对照品,加乙醇制成各含0.2 mg/mL混合溶液,作为对照品溶液。
, 百拇医药
2.2.3 薄层层析:照薄层色谱法(《中国药典》95版一部附录35页)试验,吸取供试品溶液25 μL,对照品溶液5 μL,分别点于同一用2%氢氧化钠溶液制备的硅胶G薄层板上,以环己烷-氯仿-甲醇-浓氨试液(3∶5∶1.5∶0.5)的下层溶液为展开剂,展开,展距约15 cm,取出,晾干,喷以碘化铋钾试液。供试品色谱中在与对照品色谱相应的位置上,显相同的两个红橙色斑点。
2.3 冰片的鉴别
2.3.1 供试品溶液的制备:取本品4 g,置于玻板上,铺成薄膜,晾干后剪碎,置于具塞锥形瓶中,加乙醚10 mL,密塞,振摇,放置过夜,倾出上清液,作为供试品溶液。
2.3.2 对照品溶液的制备:取冰片对照品,加甲醇-氯仿(1∶1)混合液制成5 mg/mL溶液,作为对照品溶液。
2.3.3 薄层层析:照薄层色谱法(《中国药典》1995年版一部附录35页)试验,吸取供试品溶液和对照品溶液各4 μL,分别点于同一以羧甲基纤维基纳为粘合剂的硅胶G薄层板上,以石油醚(30℃~60℃)-醋酸乙酯-氯仿(22∶2∶6)为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,在110℃烘数分钟。供试品色谱中,在于对照品色谱相应的位置上,显两个相同的紫红色斑点。
, 百拇医药
2.4 甘草酸铵的鉴别
2.4.1 供试品溶液的制备:取本品40 g慢慢滴加水40 mL,边加边搅拌,滤过,滤液用正丁醇提取3次,每次20 mL,合并正丁醇液,用水洗涤3次,每次10 mL,正丁醇提取液置水浴上蒸干,残渣加甲醇5 mL使溶解,作为供试品溶液。
2.4.2 对照品溶液的制备:取甘草酸铵对照品,加甲醇制成2 mg/mL溶液,作为对照品溶液。
2.4.3 薄层层析:照薄层色谱法(《中国药典》1995年版一部附录35页)试验,吸取供试品溶液和对照品溶液各5 μL,分别点于同一以羧甲基纤维素钠为粘合剂的硅胶GF254薄层板上,以正丁醇-浓氨试液-乙醇(2∶6∶7)为展开剂展开,取出,晾干,置紫外光灯(254 mm)下检视。供试品色谱中,在对照品色谱相应的位置上,显相同的蓝褐色斑点。见图1。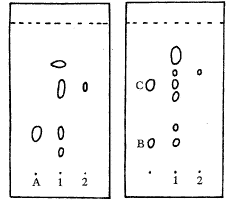
, 百拇医药
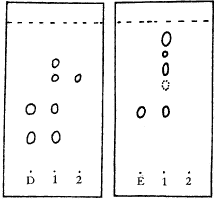
A-没食子酸 B-氧化苦参碱 C-槐定碱 D-冰片 E-甘草酸铵 1-供试品 2-阴性对照
图1 薄层色谱图
3 丹参酮ⅡA的含量测定
3.1 薄层层析及扫描条件:薄层板:含3%羧甲基纤维素钠为粘合剂的硅胶G薄层板,厚0.3 mm,105℃~110℃活化30 min;展开剂:石油醚(60℃~90℃)-苯-醋酸乙酯(15∶5∶1),饱和10 min,展距8 cm;反射法锯齿扫描;λs=480 nm,λR=700 nm;Sx=3。
3.2 丹参酮ⅡA提取方法的选择:丹参酮ⅡA为丹参中脂溶性成分,溶于乙醇、醋酸乙酯、乙醚等溶剂。本品所用成膜材料聚乙烯醇缩丁醛也溶于乙醇和醋酸乙醋,但不溶于乙醚,故选用乙醚做提取溶剂。提取方法:将样品铺成薄膜,挥散溶剂,分别用乙醚①冷浸24 h;②超声提取30 min;③索氏提取器提取至无色;第④种方法是取样后,直接往样品中加乙醚至基质析出,放置,取上清液进行测定。用上述4种方法提取后,测定丹参酮ⅡA的含量,试验结果表明,用第④种方法提取丹参酮ⅡA效率高。
, http://www.100md.com
3.3 供试品溶液的制备:取本品20 g,精密称定,逐步滴加乙醚50 mL,边加边搅拌,定量转移至100 mL棕色量瓶中,加乙醚稀释至刻度,充分振摇,放置过夜。精密量取上清液50 mL,挥散溶剂至3 mL,滴加乙醚20 mL,边加边搅,定量转移至50 mL棕色量瓶中,用乙醚稀释至刻度,摇匀,放置4 h。精密量取上清液25 mL,用水15 mL洗涤,取乙醚层,蒸干,残渣用氯仿-无水乙醇(4∶1)混合液溶解,定量转移至2 mL棕色量瓶中,用上述混合液稀释至刻度,摇匀,作为供试品溶液。
3.4 对照品溶液的制备:取丹参酮ⅡA对照品,加乙醇溶解并制成0.5 mg/mL溶液,作为对照品溶液。
3.5 线性关系的考查:吸取对照品溶液1.0、2.0、3.0、4.0、5.0 μL,点于薄层板上,按上述薄层色谱条件展开,扫描,以丹参酮ⅡA点样量为横坐标,以吸收度积分值为纵坐标作图,得一直线,回归方程为:Y=346.7+16053.2 X,r=0.9988。测定结果表明,丹参酮ⅡA在0.50~2.50 μg范围内,具有良好的线性关系。由于标准曲线不通过原点,定量时应采用外标二点法。
, http://www.100md.com
3.6 稳定性试验:取供试品溶液10 μL,点于薄层板上,按上述色谱条件展开,取出,晾干后立即扫描,每隔1 h测定1次,试验结果表明,丹参酮ⅡA斑点吸收度积分值在2 h处明显减小。若将薄层板从层析缸中取出晾干后,立即覆盖一玻璃板,重复上述试验,测定结果表明丹参酮ⅡA斑点在5 h内稳定。
供试品溶液稳定性试验:将供试品溶液按0、2、4、6、8、24 h时间隔测定丹参酮ⅡA的含量,结果表明,在24 h内供试品溶液中丹参酮ⅡA的含量基本无变化(RSD=1.6%)。
3.7 精密度试验:在同一薄层板上和不同薄 层板上各点6个同样量(4 μL)对照品溶液,按上述条件展开、扫描测定,计算吸收度积分值的RSD,同板为1.2%,异板为2.9%。
3.8 样品含量测定:照薄层色谱法(《中国药典》1995年版一部附录35页)试验,吸取供试品溶液6 μL,对照品溶液1 与2 μL,分别交叉点于同一薄层板上,按上述条件展开,取出,晾干,扫描,测定斑点吸收度积分值并计算其含量,结果见表1。
, http://www.100md.com
表1 样品丹参酮ⅡA含量斑点测定结果
批 号
含量(%)
RSD(%)
950704
0.0057
2.8
950705
0.0050
2.1
950801
0.0046
, http://www.100md.com
3.3
950802
0.0042
3.0
3.9 回收率测定:取已知含量的样品约10 g,精密称定,分别精密加入丹参酮ⅡA对照品溶液(0.910 mg/mL) 1.0 mL,按含量测定项下方法称定,计算平均回收率为95.4%,RSD=2.1%(n=6)。
4 讨论
4.1 由于本品粘度大,基质对测定干扰严重。在薄层鉴别和含量测定时,供试品溶液的提取、分离、纯化是经反复试验、筛选确定的,可以排除基质干扰,测定结果可靠。
4.2 为全面控制本品质量,对其相对体积质量、pH值、乙醇量和水溶性浸出物进行了测定。
参 考 文 献
1 王宝琴,等.中成药质量标准与标准物质研究.北京:中国医药科技出版社,1994:242
2 刘 燕,等.中国中药杂志,1990,15(3):31
(1998-07-06 收稿), 百拇医药
单位:王玉珍 陈再兴 孟宪生 王东 龙沛霞 辽宁中医学院(沈阳 110032)
关键词:瘢痕涂膜;丹参酮ⅡA;薄层扫描法
瘢痕涂膜质量标准的研究 摘 要 采用薄层色谱法对瘢痕涂膜中五倍子、苦参、冰片、甘草等成分进行鉴别,薄层扫描法测定丹参酮ⅡA的含量,加样回收率为95.4%,RSD=2.1%(n=6)。
瘢痕涂膜系由丹参、川芎、五倍子、苦参、冰片等十二味中药经科学方法提取精制成新型外用新药,用于预防和辅助治疗增生挛缩性瘢痕。经药效学试验和临床观察,疗效显著。为更好地控制本品的内在质量,保证疗效,笔者采用薄层色谱法对其中五倍子等4味药进行化学成分鉴别,用薄层扫描法测定其有效成分丹参酮ⅡA的含量,为本品建立一个较完善的控制质量的标准[1,2]。
, 百拇医药
1 仪器与试药
CS-930薄层扫描仪(日本岛津),硅胶G、硅胶GF254(薄层层析用,青岛海洋化工厂),没食子酸、氧化苦参碱、槐定碱、冰片、甘草酸铵、丹参酮ⅡA对照品由中国药品生物制品检定所提供,瘢痕涂膜由鞍钢华泰药业公司提供,所用试剂均为分析纯。
2 薄层鉴别
2.1 五倍子中没食子酸的鉴别
2.1.1 对照品溶液的制备:取没食子酸对照品,加乙醇制成0.5 mg/mL的溶液,作为对照品溶液。
2.1.2 阴性对照溶液的制备:按处方取除被测药材外的各味药材,照供试品溶液的制备方法制成阴性对照溶液(以下各阴性制照溶液的制备方法相同)。
, 百拇医药 2.1.3 薄层层析:照薄层色谱法(《中国药典》95版一部附录35页)试验,吸取含量测定项下的供试品溶液5 μL,对照品溶液3 μL,分别点于同一用2%氢氧化钠溶液制备的羧甲基纤维素钠为粘合剂的硅胶G薄层板上,以氯仿-甲醇-甲酸(15∶5∶1)为展开剂,在15℃以下展开,取出,晾干,喷以3%三氯化铁乙醇溶液。供试品色谱中,在与对照品色谱相同的位置上,显相同的蓝黑色斑点。
2.2 苦参中氧化苦参碱和槐定碱的鉴别
2.2.1 供试品溶液的制备:取本品20 g置玻板上,铺成薄膜,晾干后剪碎,加入0.2%盐酸溶液100 mL,超声处理1 h,倾出上清液,加浓氨试液,调 pH 8~10,用氯仿提取3次,每次20 mL,合并氯仿提取液,蒸干,残渣加氯仿0.5 mL使溶解,作为供试品溶液。
2.2.2 对照品溶液的制备:取氧化苦参碱和槐定碱对照品,加乙醇制成各含0.2 mg/mL混合溶液,作为对照品溶液。
, 百拇医药
2.2.3 薄层层析:照薄层色谱法(《中国药典》95版一部附录35页)试验,吸取供试品溶液25 μL,对照品溶液5 μL,分别点于同一用2%氢氧化钠溶液制备的硅胶G薄层板上,以环己烷-氯仿-甲醇-浓氨试液(3∶5∶1.5∶0.5)的下层溶液为展开剂,展开,展距约15 cm,取出,晾干,喷以碘化铋钾试液。供试品色谱中在与对照品色谱相应的位置上,显相同的两个红橙色斑点。
2.3 冰片的鉴别
2.3.1 供试品溶液的制备:取本品4 g,置于玻板上,铺成薄膜,晾干后剪碎,置于具塞锥形瓶中,加乙醚10 mL,密塞,振摇,放置过夜,倾出上清液,作为供试品溶液。
2.3.2 对照品溶液的制备:取冰片对照品,加甲醇-氯仿(1∶1)混合液制成5 mg/mL溶液,作为对照品溶液。
2.3.3 薄层层析:照薄层色谱法(《中国药典》1995年版一部附录35页)试验,吸取供试品溶液和对照品溶液各4 μL,分别点于同一以羧甲基纤维基纳为粘合剂的硅胶G薄层板上,以石油醚(30℃~60℃)-醋酸乙酯-氯仿(22∶2∶6)为展开剂,展开,取出,晾干,喷以1%香草醛硫酸溶液,在110℃烘数分钟。供试品色谱中,在于对照品色谱相应的位置上,显两个相同的紫红色斑点。
, 百拇医药
2.4 甘草酸铵的鉴别
2.4.1 供试品溶液的制备:取本品40 g慢慢滴加水40 mL,边加边搅拌,滤过,滤液用正丁醇提取3次,每次20 mL,合并正丁醇液,用水洗涤3次,每次10 mL,正丁醇提取液置水浴上蒸干,残渣加甲醇5 mL使溶解,作为供试品溶液。
2.4.2 对照品溶液的制备:取甘草酸铵对照品,加甲醇制成2 mg/mL溶液,作为对照品溶液。
2.4.3 薄层层析:照薄层色谱法(《中国药典》1995年版一部附录35页)试验,吸取供试品溶液和对照品溶液各5 μL,分别点于同一以羧甲基纤维素钠为粘合剂的硅胶GF254薄层板上,以正丁醇-浓氨试液-乙醇(2∶6∶7)为展开剂展开,取出,晾干,置紫外光灯(254 mm)下检视。供试品色谱中,在对照品色谱相应的位置上,显相同的蓝褐色斑点。见图1。


, 百拇医药
A-没食子酸 B-氧化苦参碱 C-槐定碱 D-冰片 E-甘草酸铵 1-供试品 2-阴性对照
图1 薄层色谱图
3 丹参酮ⅡA的含量测定
3.1 薄层层析及扫描条件:薄层板:含3%羧甲基纤维素钠为粘合剂的硅胶G薄层板,厚0.3 mm,105℃~110℃活化30 min;展开剂:石油醚(60℃~90℃)-苯-醋酸乙酯(15∶5∶1),饱和10 min,展距8 cm;反射法锯齿扫描;λs=480 nm,λR=700 nm;Sx=3。
3.2 丹参酮ⅡA提取方法的选择:丹参酮ⅡA为丹参中脂溶性成分,溶于乙醇、醋酸乙酯、乙醚等溶剂。本品所用成膜材料聚乙烯醇缩丁醛也溶于乙醇和醋酸乙醋,但不溶于乙醚,故选用乙醚做提取溶剂。提取方法:将样品铺成薄膜,挥散溶剂,分别用乙醚①冷浸24 h;②超声提取30 min;③索氏提取器提取至无色;第④种方法是取样后,直接往样品中加乙醚至基质析出,放置,取上清液进行测定。用上述4种方法提取后,测定丹参酮ⅡA的含量,试验结果表明,用第④种方法提取丹参酮ⅡA效率高。
, http://www.100md.com
3.3 供试品溶液的制备:取本品20 g,精密称定,逐步滴加乙醚50 mL,边加边搅拌,定量转移至100 mL棕色量瓶中,加乙醚稀释至刻度,充分振摇,放置过夜。精密量取上清液50 mL,挥散溶剂至3 mL,滴加乙醚20 mL,边加边搅,定量转移至50 mL棕色量瓶中,用乙醚稀释至刻度,摇匀,放置4 h。精密量取上清液25 mL,用水15 mL洗涤,取乙醚层,蒸干,残渣用氯仿-无水乙醇(4∶1)混合液溶解,定量转移至2 mL棕色量瓶中,用上述混合液稀释至刻度,摇匀,作为供试品溶液。
3.4 对照品溶液的制备:取丹参酮ⅡA对照品,加乙醇溶解并制成0.5 mg/mL溶液,作为对照品溶液。
3.5 线性关系的考查:吸取对照品溶液1.0、2.0、3.0、4.0、5.0 μL,点于薄层板上,按上述薄层色谱条件展开,扫描,以丹参酮ⅡA点样量为横坐标,以吸收度积分值为纵坐标作图,得一直线,回归方程为:Y=346.7+16053.2 X,r=0.9988。测定结果表明,丹参酮ⅡA在0.50~2.50 μg范围内,具有良好的线性关系。由于标准曲线不通过原点,定量时应采用外标二点法。
, http://www.100md.com
3.6 稳定性试验:取供试品溶液10 μL,点于薄层板上,按上述色谱条件展开,取出,晾干后立即扫描,每隔1 h测定1次,试验结果表明,丹参酮ⅡA斑点吸收度积分值在2 h处明显减小。若将薄层板从层析缸中取出晾干后,立即覆盖一玻璃板,重复上述试验,测定结果表明丹参酮ⅡA斑点在5 h内稳定。
供试品溶液稳定性试验:将供试品溶液按0、2、4、6、8、24 h时间隔测定丹参酮ⅡA的含量,结果表明,在24 h内供试品溶液中丹参酮ⅡA的含量基本无变化(RSD=1.6%)。
3.7 精密度试验:在同一薄层板上和不同薄 层板上各点6个同样量(4 μL)对照品溶液,按上述条件展开、扫描测定,计算吸收度积分值的RSD,同板为1.2%,异板为2.9%。
3.8 样品含量测定:照薄层色谱法(《中国药典》1995年版一部附录35页)试验,吸取供试品溶液6 μL,对照品溶液1 与2 μL,分别交叉点于同一薄层板上,按上述条件展开,取出,晾干,扫描,测定斑点吸收度积分值并计算其含量,结果见表1。
, http://www.100md.com
表1 样品丹参酮ⅡA含量斑点测定结果
批 号
含量(%)
RSD(%)
950704
0.0057
2.8
950705
0.0050
2.1
950801
0.0046
, http://www.100md.com
3.3
950802
0.0042
3.0
3.9 回收率测定:取已知含量的样品约10 g,精密称定,分别精密加入丹参酮ⅡA对照品溶液(0.910 mg/mL) 1.0 mL,按含量测定项下方法称定,计算平均回收率为95.4%,RSD=2.1%(n=6)。
4 讨论
4.1 由于本品粘度大,基质对测定干扰严重。在薄层鉴别和含量测定时,供试品溶液的提取、分离、纯化是经反复试验、筛选确定的,可以排除基质干扰,测定结果可靠。
4.2 为全面控制本品质量,对其相对体积质量、pH值、乙醇量和水溶性浸出物进行了测定。
参 考 文 献
1 王宝琴,等.中成药质量标准与标准物质研究.北京:中国医药科技出版社,1994:242
2 刘 燕,等.中国中药杂志,1990,15(3):31
(1998-07-06 收稿), 百拇医药