破伤风类毒素聚乳酸微球的制备工艺研究
作者:何应 魏树
单位:北京大学药学院药剂学研究室,北京 100083
关键词:破伤风类毒素;聚乳酸;微球;工艺学;制药;粒径大小
北京医科大学学报000313 [摘 要] 目的:研究破伤风类毒素聚乳酸微球(TT-MS)的制备工艺及理化性质。方法:水/油水复乳溶剂挥发法制备微球,并测定粒径及包封率。结果:可制备包封率达90%以上的微球,改变工艺条件,可在30~300 μm范围内控制微球的粒径。结论:研究了微球制备工艺的影响因素,成功地制备了疫苗微球。
[中图分类号] R978.7 [文献标识码] A
[文章编号] 1000-1530(2000)03-0239-05
Study on preparative conditions for polylactide
, http://www.100md.com
microspheres containing tetanus toxoid
HE Ying, WEI Shu-Li
(Department of Pharmaceutics, School of Pharmaceutical Sciences,Peking University, Beijing 100083, China)
ABSTRACT Objective: To prepare and characterize polylactide microspheres containing tetanus toxoid. Methods: The vaccine was entrapped using a (water-in-oil)-in-water emulsion solvent evaporation technique. The effects of process parameters on particle size and protein entrapment were investigated. Results: It was found that microspheres with loading efficiency up to 90% could be produced and 30-300 μm in diameter could be controlled. Conclusion: This paper describes the preparation of polylactide microspheres with an entrapped vaccine, tetanus toxoid.
, 百拇医药
KEY WORDS Tetanus toxoid; Polylactide; Microspheres; Technology, pharmaceutical; Particle size▲
破伤风的全程免疫需要连续3次注射疫苗,由于种种原因许多人只接受了第一次注射而没有完成全程免疫,辍种率高达70%。因此,发展疫苗的单剂量脉冲给药系统,一次注射就实现全程免疫,可以显著提高接种覆盖率,直接降低疾病发生率。制备疫苗微球可以达到减少注射次数的目的[1]。疫苗微球的释放速率取决于载药量、聚合物相对分子质量和成分及颗粒大小。本文对聚合物相对分子质量和影响蛋白质药物包封率及粒径的制备因素进行了考察。
1 材料与方法
1.1 材料与仪器
精制破伤风类毒素(TT, 2 200 Lf.ml-1,卫生部北京生物制品研究所);聚乳酸(polylactide, PLA; 相对分子质量7 000,10 000,20 000,25 000,30 000,35 000,40 000,山东省医疗器械研究所);聚乙烯醇(PVA)17-88(北京有机化工厂);牛血清白蛋白(BSA)、十二烷基硫酸钠(SDS)、BCA(二辛可宁酸,Bicinchoninic acid)试剂(Sigma);其它试剂均为分析纯。
, http://www.100md.com
JC-3超声处理机(通化市超声设备厂);THZ88-1型多用途台式振荡器(江苏省太仓鹿河电讯器材厂);721分光光度计(上海第三分析仪器厂);PMC-1型直流恒速搅拌器(北京大学京医科技开发公司);热分析仪DSC-7(美国P-E公司)。
1.2 实验方法
TT-MS制备:将90 μl TT加至1 ml含0.2 g PLA的有机相中,分散制初乳,然后将该乳液在搅拌转速为900 r.min-1的条件下加至1 ml PVA水溶液(10 g.L-1)中,乳化3 min(室温),再加至外水相中,继续搅拌4 h使有机溶剂挥发完全,所得微球在滤器上抽滤收集,用冷蒸馏水洗涤5次,真空干燥72 h。
粒径大小及分布测定:用显微计数法从测得的150个粒径数据计算其分布的百分数、均径(表1)。
, 百拇医药
微球形态学:用显微镜和扫描电子显微镜研究微球的形态。
含量测定[2]:准确称量20 mg微球,在1 ml NaOH(0.1 mol.L-1)含SDS(50 g.L-1)溶液中振荡24 h,用BCA分析法[3]测定上清液蛋白质含量。
差示扫描量热法(DSC):取空白微球、空白微球-TT机械混合物及载药微球样品7~8 mg,0~300℃,升温速率20℃/min,测定微球的热行为。
表1 TT-MS(相对分子质量20 000,乳化转速1 500 r.min-1)粒径大小及分布
Table 1 Sizes and distributions results of TT-MS(MW.20 000,speed of rotation 1 500 r.min-1) Diameter
, http://www.100md.com
ranges
X1-X2(μm)
d(Extents)
/μm
d(Mid-values)
/μm
Frequencies
N
Percentages
dJ(%)
XdJ
30-45
, http://www.100md.com
15
37.5
16
10.67
400.1
45-60
15
52.5
82
54.67
2870.2
60-75
15
, 百拇医药
67.5
31
20.67
1395.2
75-90
15
82.5
21
14.00
1155.0
ΣN=150
ΣdJ=100
ΣX dJ=5820.5
, 百拇医药
d, diameter; average diameter D=ΣX dJ/ΣdJ=58.2.
2 结果
2.1 含量测定标准曲线
用NaOH/SDS作溶剂,精确配制不同质量浓度(50,100,150,200,250,300 mg.L-1)的蛋白质标准溶液,用BCA分析法测定吸收度,将相应数据回归并制作标准曲线。蛋白质质量浓度在50~300 mg.L-1范围内呈现良好的线性关系,标准曲线A=0.001C+0.019,相关系数r=0.998 8,临界值r1-0.01(4)=0.917,r>r1-0.01(4),相关性极显著(α=0.01)。
2.2 微球制备工艺的影响因素
, 百拇医药
制备微球所用的PLA相对分子质量范围是7 000~40 000,分别制备各相对分子质量的微球,以下结果均有一致的规律性,结果以相对分子质量20 000的PLA微球为代表来说明。
2.2.1 乳化转速的影响 依微球制备方法中各项,固定其它条件,只将乳化转速按600, 900, 1 200, 1 500 r.min-1依次变化,测定相应条件下所得微球的含量和粒径(表2)。其中包封率=实际含量/加入量。
2.2.2 PVA质量浓度的影响 依微球制备方法中各项,固定其它条件,只将PVA质量浓度按5, 10, 20, 30 g.L-1依次变化,测定相应条件下所得微球的含量和粒径(表3)
2.2.3 有机相/水相相比的影响 依微球制备方法中各项,固定其它条件,只将有机相/水相相比按1/1, 1/2, 1/3依次变化,测定相应条件下所得微球的含量和粒径(表4)。相比是1/1,微球形态好,呈球形;相比是1/2,微球有椭球形;相比是1/3,微球有较多椭球形,球壁有缺损。
, 百拇医药
2.2.4 有机相中PLA质量浓度的影响 依微球制备方法中各项,固定其它条件,只将有机相中PLA质量浓度按50、100、200 g.L-1依次变化,测定相应条件下所得微球的含量和粒径(表5)。
表2 乳化转速对PLA微球性能的影响
Table 2 Influences on properties of microspheres by speed of rotation Speed of
rotation
(n/r.min-1)
Quantities
added in
, http://www.100md.com
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
diameters
(d/μm, ±s)
±s)
600
, 百拇医药
1.20
0.66
54.87
170.7±43.6
900
1.20
0.81
67.94
149.9±35.0
1 200
1.20
0.84
70.18
, 百拇医药
126.6±25.1
1 500
1.20
0.64
53.56
58.2±11.4
n, rotational fregnency; d, diametor. 表3 PVA质量浓度对PLA微球性能的影响
Table 3 Influences on properties of microspheres by mass concentrations of PVA ρ(PVA)/g.L-1
Quantities
, 百拇医药
added in
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
diameters
(d/μm, ±s)
±s)
, 百拇医药
5
1.20
0.58
48.59
195.3±46.4
10
1.20
0.81
67.94
149.9±35.0
20
1.20
0.82
, 百拇医药
68.81
84.2±17.1
30
1.20
0.85
70.69
42.9± 8.9
ρ, mass concentration; d, diameter.表4 有机相/水相相比对PLA微球性能的影响
Table 4 Influences on properties of microspheres by the volume ratio of solvent phase to aqueous phase Volume ratio of solvent
, 百拇医药
phase to aqueous phase
[V(solvent phase)/
V(aqueous phase)]
Quantities
added in
(%)
Quantities
determined
(%)
Loading
efficiencies
, 百拇医药
(%)
Average
diameters
(d/μm, ±s)
±s)
1/1
1.20
0.81
67.94
149.9±35.0
1/2
1.20
, 百拇医药
0.77
64.73
192.0±33.9
1/3
1.20
0.81
68.02
260.6±56.8
V, volume; d, diameter. 表5 有机相中PLA质量浓度对PLA微球性能的影响
Table 5 Influences on properties of microspheres by mass concentrations of PLA in the solvent ρ(PLA)/g.L-1
, 百拇医药
Quantities added in
(%)
Quantities determined
(%)
Loading efficiencies
(%)
Average diameters
(d/μm, ±s)
±s)
50
4.78
, http://www.100md.com
1.23
25.75
95.7±25.2
100
2.39
1.05
43.94
135.2±20.9
200
1.20
0.81
67.94
149.9±35.0
, 百拇医药
ρ, mass concentration; d, diameter..
2.2.5 TT/PLA投料比的影响 依微球制备方法中各项,固定其它条件,只将TT的投料量按45、90、180 μl依次变化,测定相应条件下所得微球的含量和粒径(表6)。
2.2.6 相对分子质量的影响 依微球制备方法,乳化转速900 r.min-1,PVA质量浓度20 g.L-1,有机相/水相相比1/1,有机相中PLA质量浓度200 g.L-1,TT投料量90 μl,分别制备各相对分子质量的PLA微球,测定各相对分子质量微球的含量和粒径(表7)。
表6 TT/PLA投料比对PLA微球性能的影响
Table 6 Influences on properties of microspheres by the quantity ratio of TT putted in to PLA Quantity ratio
, 百拇医药
of TT to PLA
[m(TT)/m(PLA)]
Quantities
added in
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
, http://www.100md.com
diameters
(d/μm, ±s)
±s)
0.0060∶1
0.60
0.19
32.38
128.4±39.6
0.0120∶1
1.20
0.81
67.94
, 百拇医药
149.9±35.0
0.0239∶1
2.39
2.27
94.89
173.7±37.2
d, diameter.表7 相对分子质量对PLA微球性能的影响
Table 7 Influences on properties of microspheres by the molecular weight of PLA Mr(PLA)
Quantities
added in
, 百拇医药
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
diameters
(d/μm, ±s, μm)
±s, μm)
7 000
, 百拇医药
1.20
0.80
66.98
75.1±17.9
10 000
1.20
0.68
56.50
73.0±18.5
20 000
1.20
0.82
68.81
, 百拇医药
84.2±17.1
25 000
1.20
0.78
65.54
96.7±26.0
30 000
1.20
0.74
62.23
92.1±19.8
35 000
, 百拇医药 1.20
0.76
63.20
115.5±20.3
40 000
1.20
0.74
62.23
134.4±26.1
Mr, relative molecula mass; d, diameter.
2.3 制备工艺的重现性
按1.2方法制备微球,PVA浓度是30 g.L-1,该过程重复5次,考察制备工艺的重现性(表8)。
, http://www.100md.com
表8的数据说明制备工艺的重现性很好,控制以上讨论的影响因素,可以制备所需载药量和粒径范围的微球。
表8 制备工艺的重现性
Table 8 Re-appearances of pharmaceutical-technology Numbers
Quantities added in
(%)
Quantities determined
(%)
Loading efficiencies
(%)
, 百拇医药
Average diameters
(d/μm, ±s)
±s)
1
1.20
0.82
68.18
39.1±8.6
2
1.20
0.81
67.78
, 百拇医药
38.3±9.2
3
1.20
0.85
70.75
38.6±9.7
4
1.20
0.86
72.30
37.8±8.3
5
1.20
, 百拇医药
0.83
69.27
39.0±9.3
d, diameter.
2.4 微球形态学
显微镜下和扫描电子显微镜下观察的微球呈圆形,表面光滑,不粘连,流动性好,分布均匀。经过NaOH/SDS处理的微球表面有穿孔(图1~3)。
2.5 差示扫描量热法
空白微球的玻璃化温度(tg)是47.15℃,机械混合物tg是48.99℃,载药微球tg是41.12℃,降低了6℃,说明药物被包进微球中,而不是吸附在微球表面。空白微球、机械混合物以及载药微球的热流-温度曲线分别见图4~6。
, 百拇医药
3 讨论
文献[4]报道含量测定方法:称量60 mg微球,溶于2 ml CH2Cl2中,每次加入1 ml蒸馏水与CH2Cl2液在旋涡混合器上混合,离心后分离出水层,共加入3 ml水,将水层合并,用BCA分析法测定水层中的蛋白质含量。但是,本实验证明这种方法不能把蛋白质抽提到水层中,在水层与CH2Cl2层之间形成白色絮状物,因为蛋白质分子有两亲性而互相聚集,绝大部分蛋白质存在于界面,所以此方法不能测定微球中的蛋白质。文献[5]报道的方法也存在同样的问题。本实验采用的NaOH/SDS抽提法效率高且重现性好。文献[6]报道用同位素标记法测定NaOH/SDS抽提法的回收率达(93±2)%。
图1 显微镜下观察的微球形态 ×33
, 百拇医药
Figure 1 Morphology of microspheres by the microscope ×33
图2 扫描电子显微镜下观察的微球形态(左)
Figure 2 Morphology of microspheres by the SEM(left)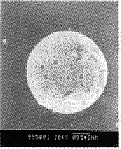
图3 扫描电子显微镜下观察的经过NaOH/SDS
处理的微球的形态(右)
Figure 3 Morphology of microspheres treated with NaOH/SDS
, 百拇医药
by the SEM(right)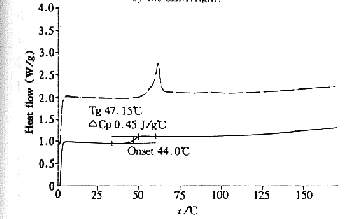
图4 空白微球的热流-温度曲线
Figure 4 Heat flow-temperature curve of blank microspheres
微球制备工艺的影响因素中,对粒径有影响的是PVA质量浓度、有机相/水相相比、乳化转速,PVA质量浓度增大、有机相/水相相比减小、以及乳化转速增大,均使微球粒径减小,并且分布范围缩小;对包封率有影响的是TT/PLA投料比、有机相浓度,投料比增大、有机相浓度增大,均使微球包封率增加,乳化转速、有机相/水相相比对包封率没有影响,这与脂溶性药物的规律不同,PVA质量浓度增大,包封率略微增加,是因为水相粘度增大,并形成坚固的界面膜,阻碍水溶性药物向水相中扩散和损失,使包封率有所增加。PLA相对分子质量对粒径的影响总趋势是相对分子质量增大,粒径也增大;相对分子质量对包封率没有影响,相同条件制备的微球的包封率也相近。
, http://www.100md.com
溶剂挥发法通常用于脂溶性药物微球的制备,应用这种技术制备水溶性微球,尤其是制备蛋白质类药物微球的工作尚不多见。本实验使用7种相对分子质量的PLA,制备了大量微球,反复实验,制备的微球能有效地包封蛋白质类药物,重现性较好,并且发现了一定的规律,为溶剂挥发法制备水溶性药物微球提供了参考。■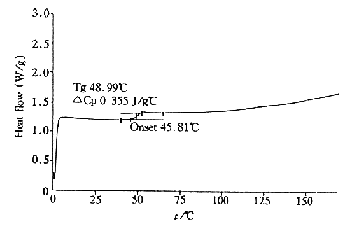
图5 机械混合物的热流-温度曲线
Figure 5 Heat flow-temperature curve of mechanical mixtures
图6 载药微球的热流-温度曲线
Figure 6 Heat flow-temperature curve of TT-loaded microspheres
, 百拇医药
基金项目:国家自然科学基金(39770878)资助项目。
参考文献
[1]Aguado MT. Future approaches to vaccine development: Single-dose vaccines using controlled-release delivery systems[J]. Vaccine, 1993, 11: 596-597
[2]Jeffery H, Davis SS, O'Hagan DT. Preparation and characterisation of poly(lactide-co-glycolide) microspheres Ⅱ: Water-in-oil-in-water emulsion solvent evaporation[J]. Pharm Res, 1993, 10: 362-368
, http://www.100md.com
[3]Smith PK, Krohn RI, Hermanson GT, et al. Measurement of protein using bicinchoninic acid[J]. Anal Biochem, 1985, 150: 76-85
[4]Cohen S, Yoshioka T, Lucarelli M, et al. Controlled delivery systems for proteins based on poly(lactic/glycolic) microspheres[J]. Pharm Res , 1991, 8: 713-720
[5]Gupta RK, Chang AC, Griffin P, et al. Determination of protein loading in biodegradable polymer microspheres containing tetanus toxoid[J]. Vaccine, 1997, 15(6/7): 672-678
[6]Sharif S, O'Hagan DT. A comparison of alternative methods for the determination of the levels of proteins entrapped in poly(lactide-co-glycolide) microparticles[[J]. Int J Pharm , 1995, 115: 259-263
收稿日期:1999-06-16, 百拇医药
单位:北京大学药学院药剂学研究室,北京 100083
关键词:破伤风类毒素;聚乳酸;微球;工艺学;制药;粒径大小
北京医科大学学报000313 [摘 要] 目的:研究破伤风类毒素聚乳酸微球(TT-MS)的制备工艺及理化性质。方法:水/油水复乳溶剂挥发法制备微球,并测定粒径及包封率。结果:可制备包封率达90%以上的微球,改变工艺条件,可在30~300 μm范围内控制微球的粒径。结论:研究了微球制备工艺的影响因素,成功地制备了疫苗微球。
[中图分类号] R978.7 [文献标识码] A
[文章编号] 1000-1530(2000)03-0239-05
Study on preparative conditions for polylactide
, http://www.100md.com
microspheres containing tetanus toxoid
HE Ying, WEI Shu-Li
(Department of Pharmaceutics, School of Pharmaceutical Sciences,Peking University, Beijing 100083, China)
ABSTRACT Objective: To prepare and characterize polylactide microspheres containing tetanus toxoid. Methods: The vaccine was entrapped using a (water-in-oil)-in-water emulsion solvent evaporation technique. The effects of process parameters on particle size and protein entrapment were investigated. Results: It was found that microspheres with loading efficiency up to 90% could be produced and 30-300 μm in diameter could be controlled. Conclusion: This paper describes the preparation of polylactide microspheres with an entrapped vaccine, tetanus toxoid.
, 百拇医药
KEY WORDS Tetanus toxoid; Polylactide; Microspheres; Technology, pharmaceutical; Particle size▲
破伤风的全程免疫需要连续3次注射疫苗,由于种种原因许多人只接受了第一次注射而没有完成全程免疫,辍种率高达70%。因此,发展疫苗的单剂量脉冲给药系统,一次注射就实现全程免疫,可以显著提高接种覆盖率,直接降低疾病发生率。制备疫苗微球可以达到减少注射次数的目的[1]。疫苗微球的释放速率取决于载药量、聚合物相对分子质量和成分及颗粒大小。本文对聚合物相对分子质量和影响蛋白质药物包封率及粒径的制备因素进行了考察。
1 材料与方法
1.1 材料与仪器
精制破伤风类毒素(TT, 2 200 Lf.ml-1,卫生部北京生物制品研究所);聚乳酸(polylactide, PLA; 相对分子质量7 000,10 000,20 000,25 000,30 000,35 000,40 000,山东省医疗器械研究所);聚乙烯醇(PVA)17-88(北京有机化工厂);牛血清白蛋白(BSA)、十二烷基硫酸钠(SDS)、BCA(二辛可宁酸,Bicinchoninic acid)试剂(Sigma);其它试剂均为分析纯。
, http://www.100md.com
JC-3超声处理机(通化市超声设备厂);THZ88-1型多用途台式振荡器(江苏省太仓鹿河电讯器材厂);721分光光度计(上海第三分析仪器厂);PMC-1型直流恒速搅拌器(北京大学京医科技开发公司);热分析仪DSC-7(美国P-E公司)。
1.2 实验方法
TT-MS制备:将90 μl TT加至1 ml含0.2 g PLA的有机相中,分散制初乳,然后将该乳液在搅拌转速为900 r.min-1的条件下加至1 ml PVA水溶液(10 g.L-1)中,乳化3 min(室温),再加至外水相中,继续搅拌4 h使有机溶剂挥发完全,所得微球在滤器上抽滤收集,用冷蒸馏水洗涤5次,真空干燥72 h。
粒径大小及分布测定:用显微计数法从测得的150个粒径数据计算其分布的百分数、均径(表1)。
, 百拇医药
微球形态学:用显微镜和扫描电子显微镜研究微球的形态。
含量测定[2]:准确称量20 mg微球,在1 ml NaOH(0.1 mol.L-1)含SDS(50 g.L-1)溶液中振荡24 h,用BCA分析法[3]测定上清液蛋白质含量。
差示扫描量热法(DSC):取空白微球、空白微球-TT机械混合物及载药微球样品7~8 mg,0~300℃,升温速率20℃/min,测定微球的热行为。
表1 TT-MS(相对分子质量20 000,乳化转速1 500 r.min-1)粒径大小及分布
Table 1 Sizes and distributions results of TT-MS(MW.20 000,speed of rotation 1 500 r.min-1) Diameter
, http://www.100md.com
ranges
X1-X2(μm)
d(Extents)
/μm
d(Mid-values)
/μm
Frequencies
N
Percentages
dJ(%)
XdJ
30-45
, http://www.100md.com
15
37.5
16
10.67
400.1
45-60
15
52.5
82
54.67
2870.2
60-75
15
, 百拇医药
67.5
31
20.67
1395.2
75-90
15
82.5
21
14.00
1155.0
ΣN=150
ΣdJ=100
ΣX dJ=5820.5
, 百拇医药
d, diameter; average diameter D=ΣX dJ/ΣdJ=58.2.
2 结果
2.1 含量测定标准曲线
用NaOH/SDS作溶剂,精确配制不同质量浓度(50,100,150,200,250,300 mg.L-1)的蛋白质标准溶液,用BCA分析法测定吸收度,将相应数据回归并制作标准曲线。蛋白质质量浓度在50~300 mg.L-1范围内呈现良好的线性关系,标准曲线A=0.001C+0.019,相关系数r=0.998 8,临界值r1-0.01(4)=0.917,r>r1-0.01(4),相关性极显著(α=0.01)。
2.2 微球制备工艺的影响因素
, 百拇医药
制备微球所用的PLA相对分子质量范围是7 000~40 000,分别制备各相对分子质量的微球,以下结果均有一致的规律性,结果以相对分子质量20 000的PLA微球为代表来说明。
2.2.1 乳化转速的影响 依微球制备方法中各项,固定其它条件,只将乳化转速按600, 900, 1 200, 1 500 r.min-1依次变化,测定相应条件下所得微球的含量和粒径(表2)。其中包封率=实际含量/加入量。
2.2.2 PVA质量浓度的影响 依微球制备方法中各项,固定其它条件,只将PVA质量浓度按5, 10, 20, 30 g.L-1依次变化,测定相应条件下所得微球的含量和粒径(表3)
2.2.3 有机相/水相相比的影响 依微球制备方法中各项,固定其它条件,只将有机相/水相相比按1/1, 1/2, 1/3依次变化,测定相应条件下所得微球的含量和粒径(表4)。相比是1/1,微球形态好,呈球形;相比是1/2,微球有椭球形;相比是1/3,微球有较多椭球形,球壁有缺损。
, 百拇医药
2.2.4 有机相中PLA质量浓度的影响 依微球制备方法中各项,固定其它条件,只将有机相中PLA质量浓度按50、100、200 g.L-1依次变化,测定相应条件下所得微球的含量和粒径(表5)。
表2 乳化转速对PLA微球性能的影响
Table 2 Influences on properties of microspheres by speed of rotation Speed of
rotation
(n/r.min-1)
Quantities
added in
, http://www.100md.com
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
diameters
(d/μm,
 ±s)
±s)600
, 百拇医药
1.20
0.66
54.87
170.7±43.6
900
1.20
0.81
67.94
149.9±35.0
1 200
1.20
0.84
70.18
, 百拇医药
126.6±25.1
1 500
1.20
0.64
53.56
58.2±11.4
n, rotational fregnency; d, diametor. 表3 PVA质量浓度对PLA微球性能的影响
Table 3 Influences on properties of microspheres by mass concentrations of PVA ρ(PVA)/g.L-1
Quantities
, 百拇医药
added in
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
diameters
(d/μm,
 ±s)
±s), 百拇医药
5
1.20
0.58
48.59
195.3±46.4
10
1.20
0.81
67.94
149.9±35.0
20
1.20
0.82
, 百拇医药
68.81
84.2±17.1
30
1.20
0.85
70.69
42.9± 8.9
ρ, mass concentration; d, diameter.表4 有机相/水相相比对PLA微球性能的影响
Table 4 Influences on properties of microspheres by the volume ratio of solvent phase to aqueous phase Volume ratio of solvent
, 百拇医药
phase to aqueous phase
[V(solvent phase)/
V(aqueous phase)]
Quantities
added in
(%)
Quantities
determined
(%)
Loading
efficiencies
, 百拇医药
(%)
Average
diameters
(d/μm,
 ±s)
±s)1/1
1.20
0.81
67.94
149.9±35.0
1/2
1.20
, 百拇医药
0.77
64.73
192.0±33.9
1/3
1.20
0.81
68.02
260.6±56.8
V, volume; d, diameter. 表5 有机相中PLA质量浓度对PLA微球性能的影响
Table 5 Influences on properties of microspheres by mass concentrations of PLA in the solvent ρ(PLA)/g.L-1
, 百拇医药
Quantities added in
(%)
Quantities determined
(%)
Loading efficiencies
(%)
Average diameters
(d/μm,
 ±s)
±s)50
4.78
, http://www.100md.com
1.23
25.75
95.7±25.2
100
2.39
1.05
43.94
135.2±20.9
200
1.20
0.81
67.94
149.9±35.0
, 百拇医药
ρ, mass concentration; d, diameter..
2.2.5 TT/PLA投料比的影响 依微球制备方法中各项,固定其它条件,只将TT的投料量按45、90、180 μl依次变化,测定相应条件下所得微球的含量和粒径(表6)。
2.2.6 相对分子质量的影响 依微球制备方法,乳化转速900 r.min-1,PVA质量浓度20 g.L-1,有机相/水相相比1/1,有机相中PLA质量浓度200 g.L-1,TT投料量90 μl,分别制备各相对分子质量的PLA微球,测定各相对分子质量微球的含量和粒径(表7)。
表6 TT/PLA投料比对PLA微球性能的影响
Table 6 Influences on properties of microspheres by the quantity ratio of TT putted in to PLA Quantity ratio
, 百拇医药
of TT to PLA
[m(TT)/m(PLA)]
Quantities
added in
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
, http://www.100md.com
diameters
(d/μm,
 ±s)
±s)0.0060∶1
0.60
0.19
32.38
128.4±39.6
0.0120∶1
1.20
0.81
67.94
, 百拇医药
149.9±35.0
0.0239∶1
2.39
2.27
94.89
173.7±37.2
d, diameter.表7 相对分子质量对PLA微球性能的影响
Table 7 Influences on properties of microspheres by the molecular weight of PLA Mr(PLA)
Quantities
added in
, 百拇医药
(%)
Quantities
determined
(%)
Loading
efficiencies
(%)
Average
diameters
(d/μm,
 ±s, μm)
±s, μm)7 000
, 百拇医药
1.20
0.80
66.98
75.1±17.9
10 000
1.20
0.68
56.50
73.0±18.5
20 000
1.20
0.82
68.81
, 百拇医药
84.2±17.1
25 000
1.20
0.78
65.54
96.7±26.0
30 000
1.20
0.74
62.23
92.1±19.8
35 000
, 百拇医药 1.20
0.76
63.20
115.5±20.3
40 000
1.20
0.74
62.23
134.4±26.1
Mr, relative molecula mass; d, diameter.
2.3 制备工艺的重现性
按1.2方法制备微球,PVA浓度是30 g.L-1,该过程重复5次,考察制备工艺的重现性(表8)。
, http://www.100md.com
表8的数据说明制备工艺的重现性很好,控制以上讨论的影响因素,可以制备所需载药量和粒径范围的微球。
表8 制备工艺的重现性
Table 8 Re-appearances of pharmaceutical-technology Numbers
Quantities added in
(%)
Quantities determined
(%)
Loading efficiencies
(%)
, 百拇医药
Average diameters
(d/μm,
 ±s)
±s)1
1.20
0.82
68.18
39.1±8.6
2
1.20
0.81
67.78
, 百拇医药
38.3±9.2
3
1.20
0.85
70.75
38.6±9.7
4
1.20
0.86
72.30
37.8±8.3
5
1.20
, 百拇医药
0.83
69.27
39.0±9.3
d, diameter.
2.4 微球形态学
显微镜下和扫描电子显微镜下观察的微球呈圆形,表面光滑,不粘连,流动性好,分布均匀。经过NaOH/SDS处理的微球表面有穿孔(图1~3)。
2.5 差示扫描量热法
空白微球的玻璃化温度(tg)是47.15℃,机械混合物tg是48.99℃,载药微球tg是41.12℃,降低了6℃,说明药物被包进微球中,而不是吸附在微球表面。空白微球、机械混合物以及载药微球的热流-温度曲线分别见图4~6。
, 百拇医药
3 讨论
文献[4]报道含量测定方法:称量60 mg微球,溶于2 ml CH2Cl2中,每次加入1 ml蒸馏水与CH2Cl2液在旋涡混合器上混合,离心后分离出水层,共加入3 ml水,将水层合并,用BCA分析法测定水层中的蛋白质含量。但是,本实验证明这种方法不能把蛋白质抽提到水层中,在水层与CH2Cl2层之间形成白色絮状物,因为蛋白质分子有两亲性而互相聚集,绝大部分蛋白质存在于界面,所以此方法不能测定微球中的蛋白质。文献[5]报道的方法也存在同样的问题。本实验采用的NaOH/SDS抽提法效率高且重现性好。文献[6]报道用同位素标记法测定NaOH/SDS抽提法的回收率达(93±2)%。

图1 显微镜下观察的微球形态 ×33
, 百拇医药
Figure 1 Morphology of microspheres by the microscope ×33

图2 扫描电子显微镜下观察的微球形态(左)
Figure 2 Morphology of microspheres by the SEM(left)

图3 扫描电子显微镜下观察的经过NaOH/SDS
处理的微球的形态(右)
Figure 3 Morphology of microspheres treated with NaOH/SDS
, 百拇医药
by the SEM(right)

图4 空白微球的热流-温度曲线
Figure 4 Heat flow-temperature curve of blank microspheres
微球制备工艺的影响因素中,对粒径有影响的是PVA质量浓度、有机相/水相相比、乳化转速,PVA质量浓度增大、有机相/水相相比减小、以及乳化转速增大,均使微球粒径减小,并且分布范围缩小;对包封率有影响的是TT/PLA投料比、有机相浓度,投料比增大、有机相浓度增大,均使微球包封率增加,乳化转速、有机相/水相相比对包封率没有影响,这与脂溶性药物的规律不同,PVA质量浓度增大,包封率略微增加,是因为水相粘度增大,并形成坚固的界面膜,阻碍水溶性药物向水相中扩散和损失,使包封率有所增加。PLA相对分子质量对粒径的影响总趋势是相对分子质量增大,粒径也增大;相对分子质量对包封率没有影响,相同条件制备的微球的包封率也相近。
, http://www.100md.com
溶剂挥发法通常用于脂溶性药物微球的制备,应用这种技术制备水溶性微球,尤其是制备蛋白质类药物微球的工作尚不多见。本实验使用7种相对分子质量的PLA,制备了大量微球,反复实验,制备的微球能有效地包封蛋白质类药物,重现性较好,并且发现了一定的规律,为溶剂挥发法制备水溶性药物微球提供了参考。■

图5 机械混合物的热流-温度曲线
Figure 5 Heat flow-temperature curve of mechanical mixtures

图6 载药微球的热流-温度曲线
Figure 6 Heat flow-temperature curve of TT-loaded microspheres
, 百拇医药
基金项目:国家自然科学基金(39770878)资助项目。
参考文献
[1]Aguado MT. Future approaches to vaccine development: Single-dose vaccines using controlled-release delivery systems[J]. Vaccine, 1993, 11: 596-597
[2]Jeffery H, Davis SS, O'Hagan DT. Preparation and characterisation of poly(lactide-co-glycolide) microspheres Ⅱ: Water-in-oil-in-water emulsion solvent evaporation[J]. Pharm Res, 1993, 10: 362-368
, http://www.100md.com
[3]Smith PK, Krohn RI, Hermanson GT, et al. Measurement of protein using bicinchoninic acid[J]. Anal Biochem, 1985, 150: 76-85
[4]Cohen S, Yoshioka T, Lucarelli M, et al. Controlled delivery systems for proteins based on poly(lactic/glycolic) microspheres[J]. Pharm Res , 1991, 8: 713-720
[5]Gupta RK, Chang AC, Griffin P, et al. Determination of protein loading in biodegradable polymer microspheres containing tetanus toxoid[J]. Vaccine, 1997, 15(6/7): 672-678
[6]Sharif S, O'Hagan DT. A comparison of alternative methods for the determination of the levels of proteins entrapped in poly(lactide-co-glycolide) microparticles[[J]. Int J Pharm , 1995, 115: 259-263
收稿日期:1999-06-16, 百拇医药