�������˼�����Ѫ���С��������ϸ����Ӱ��
���ߣ����� ������ ���� �ɻ�
��λ������(450042 ֣�ݣ���ž���153����ҽԺ��ҽѧ��)��������(450042 ֣�ݣ���ž���153����ҽԺ��ҽѧ��)������(��һ��ҽ��ѧ��ԭҽѧ������)���ɻ�(������ҽ��ѧ�������о���)
�ؼ��ʣ�
�л�����ҽѧ�������־000519 Ϊ��̽�ֹ������ϸ������ո�����������Ѫ�����ϰ�֮��Ĺ�ϵ���۲��˲�ͬ�����Ħ������������估�����������ͬʱ��Թ������ϸ�����˵�Ӱ�졣ͬ��С�����˺�ͬʱ���Ѫ��Ի���ϸ�������ʺͻ�����ϸ��(CFU-F)�����γɵ�Ӱ�죬�Լ��������˸�������Ѫ������������Ĺ������ϸ�������á�
һ�����Ϻͷ���
1.ʵ�鶯������ֽ���С���۸��룬����(18��22) g���ɵ�һ��ҽ��ѧʵ�鶯�������ṩ��
, ��Ĵҽҩ
2.����С��Ѫ����Ʊ������ݹ�ʽS(cm)2=9.13W2/3(W=���أ�g)���㶯����������������ë��3%����������7 s����15% �������(������Ƭ֤ʵ)����������ǻע��������ˮ2 ml���ֱ����˺��1��3��5��7��9��11��13��15 dȡѪ���ֳ�Ѫ�壬��-20������ڱ�����á�
3.�������ϸ������������Dexter������ϵ[1]��
4.ʵ����飺�����õ�ϸ�������Ϊ��1.���������飻2.��ͬ���������飺�ּ�Ѫ����Ͳ���Ѫ����(�����ܼ����ֱ�Ϊ��10��30��50��70��100 Gy��60Co ����������6 Gy*min-1���պ�����ʱ��ֱ�Ϊ0��3��6��12��24 h)��ÿ���������ÿ��ʱ���Ϊһ���۲���(6ƿϸ��)��ÿ����������������������顣
5.��ͬ����������պ�������ͬʱ��Թ������ϸ������(���������ͻ���)�IJ��ԣ������õĹ������ϸ��������ǰ������Ѫ����������60Co ������(6 Gy*min-1)���������������Ȼ��ֱ�����0��3��6��12��24 h���������ִ�������HEȾɫǰ������HEȾɫ����(����5����Ұ��ȡ��ƽ��ֵ)�ֳ�������������ռ�����ı�������FCM����ǰϸ��������PI��Ⱦ�ⶨ������ϸ�������ʡ�
, ��Ĵҽҩ
6.����С��Ѫ�帴�Ϸ������˶Թ������ϸ�����õIJ��ԣ������õĹ������ϸ������ǰ6 h������ƿ�ڵ�Һ����������10%С�����˺��15 d��Ѫ�壬����ǰ������Ѫ����������60Co ���������������������������ǰ�ĺ�����С��Ѫ����������ֱ�����0��3��6��12��24 h��(����ָ��ͬ��)��
7.����С��Ѫ��Թ������ϸ��24 h�����ʵ�Ӱ�죺�����������ϸ������������������10%Ԥ���Ʊ���С�����˺�ͬʱ���Ѫ�壬Ȼ�������12���������У�ÿ��2 ml��ÿ���۲�ָ�겻����6�ײ�����ȵIJ���Ѫ����������գ���37�桢5%CO2������ʪ�ȵ�������������24 hȡ�������壬�û��������1 min����ȥҺ�壬PBSϴ�����Σ���������0.25%���ȵ���ø����Һ����2 min����ȥ����Һ����ȷ����1.5 ml PBS�������ܴ������徵�¼��������ռ����ϸ�����İٷ��ʼ�Ϊ�����ʡ�
8.����С��Ѫ��Թ��������ϸ��(CFU-F)�����γɵ�Ӱ�죺���������ʡ�������������2��(�м������Һ)��ֹ������PBSϴ�ӣ�Wright-GiemsaȾɫ����㺬50�����Ϸ�Բ��ϸ����ϸ����(CFU-F����)������������ԡ�CFU-F/106BMC����ʾ��
, ��Ĵҽҩ
9.ͳ�Ʒ�����Ӧ��SPSSͳ�������ĵ����غͶ����ط�������Խ�����д����������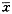 ��s��ʾ��
��s��ʾ��
�������
1.��ͬ��������������պ�������ͬʱ���BMSC�����ͻ�����Ӱ��
��������������BMSC�Ļ����͵������������С��50 Gyʱ��BMSC�ĵ����ͻ���Ҫ�ϳ�ʱ����ܱ��ֳ��������ӵķ��ȱȽ�С����������50 Gy���ӵ�70 Gy����ʱ�������ӷ��ȱȽϴ��������������϶�ʱ����ֳ���������������70 Gyʱ��BMSC��������Ҫ����Ϊ�����ʵ�������ߡ��������˸�������Ѫ���BMSC��Ӱ�����Է�������Ϊ�����ص㣬Ѫ��ֻ��50��70 Gy�������BMSC����
��1 ��ͬ������������ķ������˼��պ�������ͬʱ���BMSC������(%)��Ӱ��(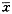 ��s) ������
��s) ������
, ��Ĵҽҩ
(Gy)
�� �� �� ͬ ʱ ��(h)
0
3
6
12
24
0
0.73��0.31
0.8��0.20
0.80��0.20
0.80��0.20
0.78��0.21
, ��Ĵҽҩ
10
0.60��0.34
0.67��0.30
0.83��0.25
0.93��0.23
0.90��0.45
30
0.83��0.06
1.47��0.32**##
1.23��0.15*#
1.90��0.36**##
, ��Ĵҽҩ
2.70��0.36**##
50
1.67��0.25*
2.50��0.45**##
4.53��0.45**##
4.00��1.13**##
5.42��0.76**##
70
6.63��0.51**
16.31��1.91**##
, ��Ĵҽҩ
11.92��2.03**##
9.67��1.60**##
13.47��1.71**##
100
9.33��1.57**
12.52��0.75**##
11.23��2.06**##
11.43��1.88**##
10.77��1.10**##
, http://www.100md.com
ע��ͬһʱ��������Ӧ0(Gy)��ȣ�*P<0.05,**P<0.01;ͬһ����������Ӧ0(ʱ)��ȣ���P<0.05,##P<0.01��2 ��ͬ������������ķ������˼��պ�������ͬʱ���BMSC������(%)��Ӱ��(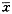 ��s) ������
��s) ������
(Gy)
�� �� �� ͬ ʱ ��(h)
0
3
6
12
24
, ��Ĵҽҩ
0
0.97��0.31
1.23��0.21
0.98��0.20
1.11��0.20
1.07��0.31
10
0.60��0.20
1.37��0.25
1.47��0.21*#
1.00��0.06
0.97��0.12
, http://www.100md.com
30
0.81��0.20*
1.47��0.31*#
1.93��0.06**##
2.77��0.21**##
2.86��0.21**##
50
1.93��0.15*
2.67��0.49**##
4.27��0.47**##
, ��Ĵҽҩ
5.20��1.25**##
4.90��0.44**##
70
11.93��0.76**
11.03��0.99**##
12.03��0.98**##
19.50��3.24**##
18.03��1.86**##
100
, http://www.100md.com 16.33��2.72**
24.03��2.39**##
33.83��1.70**##
28.03��1.40**##
30.83��1.30**##
ע��ͬһʱ��������Ӧ0(Gy)��ȣ�*P<0.05,**P<0.01;ͬһ����������Ӧ0(ʱ)��ȣ���P<0.05,##P<0.01��3 ����Ѫ���BMSC�����ͻ�����(%)��Ӱ��(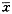 ��s) ������
��s) ������
, ��Ĵҽҩ
(Gy)
�� �� �� ͬ ʱ ��(h)
0
3
6
12
24
50(S)
����
1.47��0.41
1.84��0.51��
2.76��0.83**
, ��Ĵҽҩ
3.12��0.46**
3.64��0.61**
50
����
1.67��0.25
2.50��0.45
4.53��0.45
4.00��1.13
5.42��0.76
50(S)
����
1.42��0.21*
, ��Ĵҽҩ
2.12��0.30*
3.00��0.37*
4.10��0.24**
3.06��0.77**
50
����
1.93��0.15
2.67��0.49
4.27��0.47
5.20��1.25
4.90��0.44
, ��Ĵҽҩ
70(S)
����
5.76��1.01
12.01��0.96**
8.42��1.04**
9.04��0.97
12.18��2.02
70
����
6.63��0.51
16.31��1.91
11.92��2.03
, http://www.100md.com
9.67��1.60
13.47��1.71
70(S)
����
8.42��1.03**
9.02��0.84**
9.31��1.21**
13.45��1.62**
14.36��1.72**
70
, ��Ĵҽҩ ����
11.93��0.76
11.03��0.99
12.03��0.98
19.50��3.24
18.03��1.16
ע������Ӧ����Ѫ����ȣ�*P<0.05,**P<0.01 ����������(P<0.01)��
2.С������Ѫ��Է������˺��BMSC������������Ӱ��
50 Gy���������Ѫ���0ʱ�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ���������𣬻����������½�(P<0.05)��3 h�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ������ʺͻ����������½�(P<0.05)��6��12��24 h�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ������ʺͻ������½�����(P<0.01)��70 Gy���������Ѫ���0��12��24 h�۲���ĵ�����ͬ����Ӧ�IJ���Ѫ����Ƚ����죬�������½�����(P<0.01)��3��6 h�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ������ʺͻ����������½�(P<0.01)��
, ��Ĵҽҩ
3 ����С��Ѫ��Թ������ϸ��24 h������(%)�����������ϸ��(CFU-F/106BMC)�����γɵ�Ӱ��
�������ϸ��������1��15 d��Ѫ�����벻��Ѫ����Ƚϣ�����1��9���⣬���������в���(P<0.05��0.01)����Ѫ�����3��5���������ͬ����Ѫ������Ӧ��ʱ���Ƚ����Խ��ͣ���11��15��ͬ��Ӧ�IJ���Ѫ����Ƚ���������(P<0.01)����Ѫ����������ϸ���������ʵ�5����͡�1��15 d��CFU-F�����γ�������Ѫ���벻��Ѫ���ʱ���۲�����бȽϣ�1��11���Ѫ�����CFU-F��������Ӧ�IJ���Ѫ�������Լ���(P<0.01)��13��15 d���죻��Ѫ����CFU-F������1��5����ͣ���7�쿪ʼ�������ӣ�����13������Ӧ�IJ���Ѫ�������졣��4 ��ͬʱ�������Ѫ���BMSC������(AR)��CFU-F�γɵ�Ӱ��(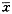 ��s) ���
��s) ���
, ��Ĵҽҩ �� �� �� ͬ ʱ ��(d)
1
3
5
7
9
11
13
15
AR*
3.35��0.50
4.13��0.54
4.68��0.18
, http://www.100md.com
3.92��0.37
3.56��0.24
3.67��0.28
4.47��0.31
3.72��0.54
AR-S
3.32��0.22
3.25��0.76��
2.78��0.42##
5.02��0.96##
3.29��0.14
, ��Ĵҽҩ
4.98��0.05#
5.69��0.19#
5.69��0.13#
CFU-F
28.7��1.5
32.7��2.1
28.0��2.0
30.7��2.1
28.7��2.1
31.0��1.7
31.7��2.1
, http://www.100md.com
32.7��4.2
CFU-F-S��
16.0��2.0##
19.0��2.0##
16.3��1.2##
21.7��2.1##
20.0��2.0##
26.0��3.6##
28.7��2.5
32.0��2.6
, http://www.100md.com
ע��AR*��CFU-F-S*�ֱ�ΪBMSC 24 h������(%)���������ϸ��(CFU-F/106BMC)�����γ�����S����������ͬʱ��������Ѫ�壬��Ѫ���벻��Ѫ����Ƚ�#P<0.05��##P<0.01 ��������
�йع������ϸ���Է��������������һ������������⡣���嶯���������������ϸ������ЧӦ���о��������������ϸ�����нϸߵķ��������ԣ�������ȹ����ͼ��Է��䲡�Ħ��������������������Ѫ�����Ĺ���ȱ��[2]���������������Ĺ������ϸ�����������о��������������ϸ�����н�ǿ�Ŀ�������������40 Gy ���������䲻Ӱ���伯��̼��������ɣ���100 Gy �����������Ա�������Ҫ��ճ���ṹ��϶����[3]����ʵ����������������Ĺ������ϸ������ϸ���������Ծ��н�ǿ�Ŀ�������������С��50 Gy�Ħ����������24 h��������ͻ����ʽ�Ϊ�۲�ϸ����ʮ��֮һ��������ϸ�����˿��ܻ�������Ӱ�����ϸ������ϸ�����Ӻ�֧����Ѫ�Ĺ��ܡ�
, ��Ĵҽҩ
Ŀǰ��Ϊ��ϸ��������Ҫ�����ַ�ʽ�������͵������������շ����ڶ���;�����������䡢�������ӵȾ����շ�ϸ���ĵ���[4]�������Ĺ����漰�������źŵĴ��ݣ����ɻ���ļ���(��c-fos��c-jun��p53��c-myc�Ȼ���ļ���)����һ���ಽ��Ĺ��̡���ʵ���������������������������������Ĺ������ϸ���ĵ����ͻ�����������в������Ŀǰ��Ϊ���������������йأ�(1)ROS��ROS(reactive oxygen species)�����Ļ����м��壬��Դ���������������ữ������ϸ��ɫ��P450ϵͳ����ĤNAD(P)H����ø���������������ӷ�Ӧ���Ӷ�ֱ������ӻ�ͨ����ʽ��Ӧʹ���ɻ���һ������Ӵ��ݵ�����һ������ӣ����¶�ϸ���ṹ�Ĺ㷺�ƻ���������������ROS�IJ�����������Ƿ�������������ϸ��������ԭ��֮һ��(2)ϸ�����ӣ�Ŀǰ��Ϊ��������������-��(TNF-��)���յ��������͵���֯ϸ��������������Ҫ���أ�TNF-���ǹ������ϸ���Է����ڵ���Ѫ��������֮һ�����Ƿ�����������Ĺ������ϸ���ĵ��������д���һ��֤ʵ��
, http://www.100md.com
�������ϸ���ɷ�����Ѫ�̼����ӣ����ϸ������(SCF)�Ⱥ���Ѫ�������ӣ����������ת������(TGF-��)��[5]��С��������ϸ���������˺������SCF��TGF-�µ�ϸ�����Ӷ��ᷢ����Ӧ�ı仯[6]���о�������TGF-�¿�������SCF�ı���[7]��SCF�дٽ����忹�ź����Ʒʴ�ϸ������������[8]�����������Ĺ������ϸ���Ŀ���������(���������ͻ���)�Ƿ�ͬ��Щ���ӵı仯�д���һ���о�������ϸ��������һ�������ġ��ܻ�����ƵĹ��̣�����ϳ��µĴ����(�絰����)�����Է����������µ����ı�����Ҫһ����ʱ�䡣��ʵ���У�����50 Gy�����ռ���������ϸ��������ͬ���������ʱ��Ĺ�ϵҲ֧����һ�۵㣻��������70 Gy�������ϸ��ʱ��Ҳ�������ڷ����ϸ�������˹���ǿ�ң�ϸ���������ϳ�ͬ�����йص����ʾͽ����ˣ����Ա���Ϊ�����ʵ���Խ��ͺͻ����ʵ�������ߡ�
����С��Ѫ����һ�־��ж��ֻ��Գɷֵĸ������ɷ���һ����ʱ�������˺��ʱ����仯�����������Ĺ������ϸ��������һ��ƽ����ϵ������50 Gy����������������ϸ����ϸ��ͨ����������ϸ�����ӵķ��ڱ仯�����Եֿ����ķ������ˣ�����Ҫ����ϸ�����Ӳ��롣����ϸ�������ַ���ϸ�����ӵ��ȿ��ܾ������������˵ļ�����Χ���������������Χ(��70 Gy)���������˾��ң�ϸ������������ͨ�������ĵ��ڱ仯������ʹ����翹�����ӵIJ���Ҳ���ܸı�ϸ�����������ˡ�50��70 Gy����������Χ��Ҳ������ϸ�������ڶ���翹�����ӵ����нΣ�����Ѫ����ֳ��Է������˵ı������ã����ֱ���������Ѫ���еĺ��ֳɷ��й��д���һ��֤ʵ��
, ��Ĵҽҩ
IL-3���Դٽ��������ϸ����������[9��10]��С�����˺�ͬʱ���Ѫ��Ի���ϸ�������ʺ�CFU-F�����γɵ�Ӱ���Ƿ�ͬѪ���еı仯�й��д��о���
������Ŀ��ȫ������ָ���Կ���������Ŀ(96L045)
�����
1��Dexter TM.Conditions controlling the proliferation of hamopoidetic stem cells in vitro.J Cell Physiol,1977, 91:335-338.
2�����һ����ɻ�������������.�������˹��������л���ϸ�������ڣ�DNA��������̬�仯�Ĺ۲�.��ž�ҽѧ��־��1999��24��10-14.
3��Greenber TS.Toxic effects on the hematopoietic microenvironment.Exp-Hematol,1991,19:1101-1109.
, ��Ĵҽҩ
4��������.�����о����ȵ�-ϸ������.ʵ��ѪҺѧ��־��1996��4��113-117.
5����ά�����¼���.��Ѫ����ϸ������Ѫ����.�й�ʵ��ѪҺѧ��־��1993��1��97-99.
6��Richard J.Consequence of extremely high dose of irradiation on bone marrow stromal cells and the release of hematopoietic growth factors.Exp-Hematol,1987,15:952-957.
7��By Michael C,Heinrich,Douglas C,et al. Transforming Growth Factor beta 1 inhibits expression of the gene products for Steel Factor and its Receptor(c-kit).Blood,1995,85:1769-1780.
, ��Ĵҽҩ
8��Yee-NS,Peak-��,Besmer-P.Role of kit-ligand in proliferation and supression of apoptosis in mast cells.J-Exp-Med 1994,176:1777-1787.
9��Collins MK,Marvel J,Malde P,et al.Interleukin-3 protects murine bone marrow cells from apoptosis induced by DNA damaging agents.J-Exp-Med,1992,176:1043-1051.
10������ϼ���ƾ������ң���.����ϸ������-3����Һ�ٽ�С��������ϸ������������۲�.����ѧ����1993��24��305-309.
(�ո�����:1999-04-10), http://www.100md.com
��λ������(450042 ֣�ݣ���ž���153����ҽԺ��ҽѧ��)��������(450042 ֣�ݣ���ž���153����ҽԺ��ҽѧ��)������(��һ��ҽ��ѧ��ԭҽѧ������)���ɻ�(������ҽ��ѧ�������о���)
�ؼ��ʣ�
�л�����ҽѧ�������־000519 Ϊ��̽�ֹ������ϸ������ո�����������Ѫ�����ϰ�֮��Ĺ�ϵ���۲��˲�ͬ�����Ħ������������估�����������ͬʱ��Թ������ϸ�����˵�Ӱ�졣ͬ��С�����˺�ͬʱ���Ѫ��Ի���ϸ�������ʺͻ�����ϸ��(CFU-F)�����γɵ�Ӱ�죬�Լ��������˸�������Ѫ������������Ĺ������ϸ�������á�
һ�����Ϻͷ���
1.ʵ�鶯������ֽ���С���۸��룬����(18��22) g���ɵ�һ��ҽ��ѧʵ�鶯�������ṩ��
, ��Ĵҽҩ
2.����С��Ѫ����Ʊ������ݹ�ʽS(cm)2=9.13W2/3(W=���أ�g)���㶯����������������ë��3%����������7 s����15% �������(������Ƭ֤ʵ)����������ǻע��������ˮ2 ml���ֱ����˺��1��3��5��7��9��11��13��15 dȡѪ���ֳ�Ѫ�壬��-20������ڱ�����á�
3.�������ϸ������������Dexter������ϵ[1]��
4.ʵ����飺�����õ�ϸ�������Ϊ��1.���������飻2.��ͬ���������飺�ּ�Ѫ����Ͳ���Ѫ����(�����ܼ����ֱ�Ϊ��10��30��50��70��100 Gy��60Co ����������6 Gy*min-1���պ�����ʱ��ֱ�Ϊ0��3��6��12��24 h)��ÿ���������ÿ��ʱ���Ϊһ���۲���(6ƿϸ��)��ÿ����������������������顣
5.��ͬ����������պ�������ͬʱ��Թ������ϸ������(���������ͻ���)�IJ��ԣ������õĹ������ϸ��������ǰ������Ѫ����������60Co ������(6 Gy*min-1)���������������Ȼ��ֱ�����0��3��6��12��24 h���������ִ�������HEȾɫǰ������HEȾɫ����(����5����Ұ��ȡ��ƽ��ֵ)�ֳ�������������ռ�����ı�������FCM����ǰϸ��������PI��Ⱦ�ⶨ������ϸ�������ʡ�
, ��Ĵҽҩ
6.����С��Ѫ�帴�Ϸ������˶Թ������ϸ�����õIJ��ԣ������õĹ������ϸ������ǰ6 h������ƿ�ڵ�Һ����������10%С�����˺��15 d��Ѫ�壬����ǰ������Ѫ����������60Co ���������������������������ǰ�ĺ�����С��Ѫ����������ֱ�����0��3��6��12��24 h��(����ָ��ͬ��)��
7.����С��Ѫ��Թ������ϸ��24 h�����ʵ�Ӱ�죺�����������ϸ������������������10%Ԥ���Ʊ���С�����˺�ͬʱ���Ѫ�壬Ȼ�������12���������У�ÿ��2 ml��ÿ���۲�ָ�겻����6�ײ�����ȵIJ���Ѫ����������գ���37�桢5%CO2������ʪ�ȵ�������������24 hȡ�������壬�û��������1 min����ȥҺ�壬PBSϴ�����Σ���������0.25%���ȵ���ø����Һ����2 min����ȥ����Һ����ȷ����1.5 ml PBS�������ܴ������徵�¼��������ռ����ϸ�����İٷ��ʼ�Ϊ�����ʡ�
8.����С��Ѫ��Թ��������ϸ��(CFU-F)�����γɵ�Ӱ�죺���������ʡ�������������2��(�м������Һ)��ֹ������PBSϴ�ӣ�Wright-GiemsaȾɫ����㺬50�����Ϸ�Բ��ϸ����ϸ����(CFU-F����)������������ԡ�CFU-F/106BMC����ʾ��
, ��Ĵҽҩ
9.ͳ�Ʒ�����Ӧ��SPSSͳ�������ĵ����غͶ����ط�������Խ�����д����������
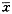 ��s��ʾ��
��s��ʾ���������
1.��ͬ��������������պ�������ͬʱ���BMSC�����ͻ�����Ӱ��
��������������BMSC�Ļ����͵������������С��50 Gyʱ��BMSC�ĵ����ͻ���Ҫ�ϳ�ʱ����ܱ��ֳ��������ӵķ��ȱȽ�С����������50 Gy���ӵ�70 Gy����ʱ�������ӷ��ȱȽϴ��������������϶�ʱ����ֳ���������������70 Gyʱ��BMSC��������Ҫ����Ϊ�����ʵ�������ߡ��������˸�������Ѫ���BMSC��Ӱ�����Է�������Ϊ�����ص㣬Ѫ��ֻ��50��70 Gy�������BMSC����
��1 ��ͬ������������ķ������˼��պ�������ͬʱ���BMSC������(%)��Ӱ��(
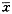 ��s) ������
��s) ������, ��Ĵҽҩ
(Gy)
�� �� �� ͬ ʱ ��(h)
0
3
6
12
24
0
0.73��0.31
0.8��0.20
0.80��0.20
0.80��0.20
0.78��0.21
, ��Ĵҽҩ
10
0.60��0.34
0.67��0.30
0.83��0.25
0.93��0.23
0.90��0.45
30
0.83��0.06
1.47��0.32**##
1.23��0.15*#
1.90��0.36**##
, ��Ĵҽҩ
2.70��0.36**##
50
1.67��0.25*
2.50��0.45**##
4.53��0.45**##
4.00��1.13**##
5.42��0.76**##
70
6.63��0.51**
16.31��1.91**##
, ��Ĵҽҩ
11.92��2.03**##
9.67��1.60**##
13.47��1.71**##
100
9.33��1.57**
12.52��0.75**##
11.23��2.06**##
11.43��1.88**##
10.77��1.10**##
, http://www.100md.com
ע��ͬһʱ��������Ӧ0(Gy)��ȣ�*P<0.05,**P<0.01;ͬһ����������Ӧ0(ʱ)��ȣ���P<0.05,##P<0.01��2 ��ͬ������������ķ������˼��պ�������ͬʱ���BMSC������(%)��Ӱ��(
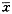 ��s) ������
��s) ������(Gy)
�� �� �� ͬ ʱ ��(h)
0
3
6
12
24
, ��Ĵҽҩ
0
0.97��0.31
1.23��0.21
0.98��0.20
1.11��0.20
1.07��0.31
10
0.60��0.20
1.37��0.25
1.47��0.21*#
1.00��0.06
0.97��0.12
, http://www.100md.com
30
0.81��0.20*
1.47��0.31*#
1.93��0.06**##
2.77��0.21**##
2.86��0.21**##
50
1.93��0.15*
2.67��0.49**##
4.27��0.47**##
, ��Ĵҽҩ
5.20��1.25**##
4.90��0.44**##
70
11.93��0.76**
11.03��0.99**##
12.03��0.98**##
19.50��3.24**##
18.03��1.86**##
100
, http://www.100md.com 16.33��2.72**
24.03��2.39**##
33.83��1.70**##
28.03��1.40**##
30.83��1.30**##
ע��ͬһʱ��������Ӧ0(Gy)��ȣ�*P<0.05,**P<0.01;ͬһ����������Ӧ0(ʱ)��ȣ���P<0.05,##P<0.01��3 ����Ѫ���BMSC�����ͻ�����(%)��Ӱ��(
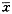 ��s) ������
��s) ������, ��Ĵҽҩ
(Gy)
�� �� �� ͬ ʱ ��(h)
0
3
6
12
24
50(S)
����
1.47��0.41
1.84��0.51��
2.76��0.83**
, ��Ĵҽҩ
3.12��0.46**
3.64��0.61**
50
����
1.67��0.25
2.50��0.45
4.53��0.45
4.00��1.13
5.42��0.76
50(S)
����
1.42��0.21*
, ��Ĵҽҩ
2.12��0.30*
3.00��0.37*
4.10��0.24**
3.06��0.77**
50
����
1.93��0.15
2.67��0.49
4.27��0.47
5.20��1.25
4.90��0.44
, ��Ĵҽҩ
70(S)
����
5.76��1.01
12.01��0.96**
8.42��1.04**
9.04��0.97
12.18��2.02
70
����
6.63��0.51
16.31��1.91
11.92��2.03
, http://www.100md.com
9.67��1.60
13.47��1.71
70(S)
����
8.42��1.03**
9.02��0.84**
9.31��1.21**
13.45��1.62**
14.36��1.72**
70
, ��Ĵҽҩ ����
11.93��0.76
11.03��0.99
12.03��0.98
19.50��3.24
18.03��1.16
ע������Ӧ����Ѫ����ȣ�*P<0.05,**P<0.01 ����������(P<0.01)��
2.С������Ѫ��Է������˺��BMSC������������Ӱ��
50 Gy���������Ѫ���0ʱ�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ���������𣬻����������½�(P<0.05)��3 h�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ������ʺͻ����������½�(P<0.05)��6��12��24 h�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ������ʺͻ������½�����(P<0.01)��70 Gy���������Ѫ���0��12��24 h�۲���ĵ�����ͬ����Ӧ�IJ���Ѫ����Ƚ����죬�������½�����(P<0.01)��3��6 h�۲���ͬ����Ӧ�IJ���Ѫ����Ƚϣ������ʺͻ����������½�(P<0.01)��
, ��Ĵҽҩ
3 ����С��Ѫ��Թ������ϸ��24 h������(%)�����������ϸ��(CFU-F/106BMC)�����γɵ�Ӱ��
�������ϸ��������1��15 d��Ѫ�����벻��Ѫ����Ƚϣ�����1��9���⣬���������в���(P<0.05��0.01)����Ѫ�����3��5���������ͬ����Ѫ������Ӧ��ʱ���Ƚ����Խ��ͣ���11��15��ͬ��Ӧ�IJ���Ѫ����Ƚ���������(P<0.01)����Ѫ����������ϸ���������ʵ�5����͡�1��15 d��CFU-F�����γ�������Ѫ���벻��Ѫ���ʱ���۲�����бȽϣ�1��11���Ѫ�����CFU-F��������Ӧ�IJ���Ѫ�������Լ���(P<0.01)��13��15 d���죻��Ѫ����CFU-F������1��5����ͣ���7�쿪ʼ�������ӣ�����13������Ӧ�IJ���Ѫ�������졣��4 ��ͬʱ�������Ѫ���BMSC������(AR)��CFU-F�γɵ�Ӱ��(
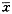 ��s) ���
��s) ���, ��Ĵҽҩ �� �� �� ͬ ʱ ��(d)
1
3
5
7
9
11
13
15
AR*
3.35��0.50
4.13��0.54
4.68��0.18
, http://www.100md.com
3.92��0.37
3.56��0.24
3.67��0.28
4.47��0.31
3.72��0.54
AR-S
3.32��0.22
3.25��0.76��
2.78��0.42##
5.02��0.96##
3.29��0.14
, ��Ĵҽҩ
4.98��0.05#
5.69��0.19#
5.69��0.13#
CFU-F
28.7��1.5
32.7��2.1
28.0��2.0
30.7��2.1
28.7��2.1
31.0��1.7
31.7��2.1
, http://www.100md.com
32.7��4.2
CFU-F-S��
16.0��2.0##
19.0��2.0##
16.3��1.2##
21.7��2.1##
20.0��2.0##
26.0��3.6##
28.7��2.5
32.0��2.6
, http://www.100md.com
ע��AR*��CFU-F-S*�ֱ�ΪBMSC 24 h������(%)���������ϸ��(CFU-F/106BMC)�����γ�����S����������ͬʱ��������Ѫ�壬��Ѫ���벻��Ѫ����Ƚ�#P<0.05��##P<0.01 ��������
�йع������ϸ���Է��������������һ������������⡣���嶯���������������ϸ������ЧӦ���о��������������ϸ�����нϸߵķ��������ԣ�������ȹ����ͼ��Է��䲡�Ħ��������������������Ѫ�����Ĺ���ȱ��[2]���������������Ĺ������ϸ�����������о��������������ϸ�����н�ǿ�Ŀ�������������40 Gy ���������䲻Ӱ���伯��̼��������ɣ���100 Gy �����������Ա�������Ҫ��ճ���ṹ��϶����[3]����ʵ����������������Ĺ������ϸ������ϸ���������Ծ��н�ǿ�Ŀ�������������С��50 Gy�Ħ����������24 h��������ͻ����ʽ�Ϊ�۲�ϸ����ʮ��֮һ��������ϸ�����˿��ܻ�������Ӱ�����ϸ������ϸ�����Ӻ�֧����Ѫ�Ĺ��ܡ�
, ��Ĵҽҩ
Ŀǰ��Ϊ��ϸ��������Ҫ�����ַ�ʽ�������͵������������շ����ڶ���;�����������䡢�������ӵȾ����շ�ϸ���ĵ���[4]�������Ĺ����漰�������źŵĴ��ݣ����ɻ���ļ���(��c-fos��c-jun��p53��c-myc�Ȼ���ļ���)����һ���ಽ��Ĺ��̡���ʵ���������������������������������Ĺ������ϸ���ĵ����ͻ�����������в������Ŀǰ��Ϊ���������������йأ�(1)ROS��ROS(reactive oxygen species)�����Ļ����м��壬��Դ���������������ữ������ϸ��ɫ��P450ϵͳ����ĤNAD(P)H����ø���������������ӷ�Ӧ���Ӷ�ֱ������ӻ�ͨ����ʽ��Ӧʹ���ɻ���һ������Ӵ��ݵ�����һ������ӣ����¶�ϸ���ṹ�Ĺ㷺�ƻ���������������ROS�IJ�����������Ƿ�������������ϸ��������ԭ��֮һ��(2)ϸ�����ӣ�Ŀǰ��Ϊ��������������-��(TNF-��)���յ��������͵���֯ϸ��������������Ҫ���أ�TNF-���ǹ������ϸ���Է����ڵ���Ѫ��������֮һ�����Ƿ�����������Ĺ������ϸ���ĵ��������д���һ��֤ʵ��
, http://www.100md.com
�������ϸ���ɷ�����Ѫ�̼����ӣ����ϸ������(SCF)�Ⱥ���Ѫ�������ӣ����������ת������(TGF-��)��[5]��С��������ϸ���������˺������SCF��TGF-�µ�ϸ�����Ӷ��ᷢ����Ӧ�ı仯[6]���о�������TGF-�¿�������SCF�ı���[7]��SCF�дٽ����忹�ź����Ʒʴ�ϸ������������[8]�����������Ĺ������ϸ���Ŀ���������(���������ͻ���)�Ƿ�ͬ��Щ���ӵı仯�д���һ���о�������ϸ��������һ�������ġ��ܻ�����ƵĹ��̣�����ϳ��µĴ����(�絰����)�����Է����������µ����ı�����Ҫһ����ʱ�䡣��ʵ���У�����50 Gy�����ռ���������ϸ��������ͬ���������ʱ��Ĺ�ϵҲ֧����һ�۵㣻��������70 Gy�������ϸ��ʱ��Ҳ�������ڷ����ϸ�������˹���ǿ�ң�ϸ���������ϳ�ͬ�����йص����ʾͽ����ˣ����Ա���Ϊ�����ʵ���Խ��ͺͻ����ʵ�������ߡ�
����С��Ѫ����һ�־��ж��ֻ��Գɷֵĸ������ɷ���һ����ʱ�������˺��ʱ����仯�����������Ĺ������ϸ��������һ��ƽ����ϵ������50 Gy����������������ϸ����ϸ��ͨ����������ϸ�����ӵķ��ڱ仯�����Եֿ����ķ������ˣ�����Ҫ����ϸ�����Ӳ��롣����ϸ�������ַ���ϸ�����ӵ��ȿ��ܾ������������˵ļ�����Χ���������������Χ(��70 Gy)���������˾��ң�ϸ������������ͨ�������ĵ��ڱ仯������ʹ����翹�����ӵIJ���Ҳ���ܸı�ϸ�����������ˡ�50��70 Gy����������Χ��Ҳ������ϸ�������ڶ���翹�����ӵ����нΣ�����Ѫ����ֳ��Է������˵ı������ã����ֱ���������Ѫ���еĺ��ֳɷ��й��д���һ��֤ʵ��
, ��Ĵҽҩ
IL-3���Դٽ��������ϸ����������[9��10]��С�����˺�ͬʱ���Ѫ��Ի���ϸ�������ʺ�CFU-F�����γɵ�Ӱ���Ƿ�ͬѪ���еı仯�й��д��о���
������Ŀ��ȫ������ָ���Կ���������Ŀ(96L045)
�����
1��Dexter TM.Conditions controlling the proliferation of hamopoidetic stem cells in vitro.J Cell Physiol,1977, 91:335-338.
2�����һ����ɻ�������������.�������˹��������л���ϸ�������ڣ�DNA��������̬�仯�Ĺ۲�.��ž�ҽѧ��־��1999��24��10-14.
3��Greenber TS.Toxic effects on the hematopoietic microenvironment.Exp-Hematol,1991,19:1101-1109.
, ��Ĵҽҩ
4��������.�����о����ȵ�-ϸ������.ʵ��ѪҺѧ��־��1996��4��113-117.
5����ά�����¼���.��Ѫ����ϸ������Ѫ����.�й�ʵ��ѪҺѧ��־��1993��1��97-99.
6��Richard J.Consequence of extremely high dose of irradiation on bone marrow stromal cells and the release of hematopoietic growth factors.Exp-Hematol,1987,15:952-957.
7��By Michael C,Heinrich,Douglas C,et al. Transforming Growth Factor beta 1 inhibits expression of the gene products for Steel Factor and its Receptor(c-kit).Blood,1995,85:1769-1780.
, ��Ĵҽҩ
8��Yee-NS,Peak-��,Besmer-P.Role of kit-ligand in proliferation and supression of apoptosis in mast cells.J-Exp-Med 1994,176:1777-1787.
9��Collins MK,Marvel J,Malde P,et al.Interleukin-3 protects murine bone marrow cells from apoptosis induced by DNA damaging agents.J-Exp-Med,1992,176:1043-1051.
10������ϼ���ƾ������ң���.����ϸ������-3����Һ�ٽ�С��������ϸ������������۲�.����ѧ����1993��24��305-309.
(�ո�����:1999-04-10), http://www.100md.com