人白细胞介素-18的基因克隆及原核表达
作者:缪海珍 杨吉成 盛伟华 阳小卫 李丽娥
单位:苏州医学院基因工程研究室,苏州,215007
关键词:人白细胞介素-18;RT-PCR;大肠杆菌;表达
苏州医学院学报000906 摘要 目的 为进一步研究人白细胞介素(hIL-18)的生物学特性打下基础,进行hIL-18的基因克隆及原核表达。方法 采用反转录PCR(RT-PCR)法从正常人外周血白细胞中克隆hIL-18基因,并重组于PBV220表达载体上,经酶切初步鉴定后进行DNA序列分析,继而观察重组hIL-18基因在大肠杆菌中不同诱导时间表达量的差异。结果 所克隆的基因与预期结果一致,并在42℃诱导5h时表达量最高。结论 成功地克隆了hIL-18基因,并使获得高效表达。
中图法分类号 R392.13
, 百拇医药
Cloning and Expression of Human Interleukin-18 Gene in E.coli
Miao Haizhen, Yang Jichen, Sheng Weihua, et al
(Department of Gene Research,Suzhou Medical College,Suzhou,215007)
Abstract Objective In order to study hIL-18 biological characteristics in a more advanced way,we proceed this study.Mehods The hIL-18 gene by RT-PCR from human peripheral white blood cells was amplified and recombined into a thermo-sensitive expression vector PBV220,then the competent cells of E.coli DH5α was introduced into.Finally,we analyzed the different expression level of hIL-18 gene at different inducing time.Results With the identification of enzyme map and sequncing,we find our cloned gene in acconformity with the published papers about hIL-18,and the expression rate was highest when induced 5h at 42℃.Conclusion we clone hIL-18 gene successfully and obtain high rate expression.
, 百拇医药
Key words human interleukin-18;RT-PCR;E.coli;expression
白细胞介素18(Interleukin 18,IL-18)是一种新发现的免疫调节细胞因子[1~3],主要由单核巨噬细胞产生,具有诱导T细胞产生IFN-γ[4],促进NK细胞杀伤活性[5],增强Fas/FasL介导的细胞毒作用[6],具有明显的抗肿瘤效果[7]。本研究采用逆转录PCR技术克隆hIL-18的cDNA,并观察其在大肠杆菌中的表达,结果报道如下。
1 材料与方法
1.1 主要材料 克隆载体PUC19、表达载体PBV220及大肠杆菌DH5α均为本实验室保存,TRIZOL总RNA试剂盒(Prmega),M-MoLV逆转录酶(MBI),Oligo(bT)15(Promega),DNA聚合酶Taq(Promega),T4DNA连接酶(MBI),限制性内切酶EcoRI、BamHI(华美生物工程公司),RPMI 1640培养基(Gibco),PBR322/MspI DNA Marker(华美生物工程公司),低分子量标准白质(上海丽珠东风生物技术有限公司)
, 百拇医药
1.2 方法
1.2.1 正常人外周血白细胞(PBMC)的分离 取正常人外周血10ml,用Ficoll按常规方法分离白细胞,以3×106个/ml的浓度在含10%的小牛血清的RPMI1640培养基中培养过夜。
1.2.2 hIL-18的RT-PCR克隆 按说明书用TRIZOL总RNA试剂盒提取PBMC的总RNA,取3μg总RNA与0.5μg Oligo(dT)15混合,进行反转录。PCR扩增的上游引物为5’-GGAATTCATGTACTTTGGCAAGCTTG(含EcoRI位点及起始密码子ATG),下游引物为5’-CGGGATCCTTAGTCTT-CGTTTTGAAC(含BamHI位点及终止密码子TAA)(上海生工生物工程公司合成)。PCR反应体积为50μl,引物浓度为0.6μmol/L,扩增参数为94℃ 5min、94℃45s、55℃60s、72℃90s,30个循环后72℃延伸10min。扩增产物行1.5%琼脂糖凝胶电泳分析。1.2.3 hIL-18表达载体PBV-IL-8的构建及筛选鉴定 hIL-18cDNA PCR产物与抽提的PBV220表达载体的质粒分别经EcoRI、BamHI双酶切后行1.5%的琼脂糖电泳,并用1.0%的低熔点琼脂糖回收,按常规方法用T4连接酶将两者连接并转化至大肠杆菌DH5α的感受态,挑选阳性克隆进行酶切鉴定,酶切产物行1.5%琼脂糖凝胶电泳。
, 百拇医药
1.2.4 hIL-18h基因的序列分析 将从PBV-IL-18重组质粒切下的约480bp的基因片段定向插入PUC19克隆载体,由上海基康生物技术有限公司进行测序。
1.2.5 hIL-18的表达及SDS-PAGE电泳分析 hIL-18经温控诱导表达后进行15%SDS-PAGE 200V恒压电泳,经考马斯亮蓝染色及脱色后观察hIL-18在不同诱导时间(3h、4h、5h、6h)表达量的差别。
2 结果
2.1 hIL-18 RT-PCR产物的电泳分析 hIL-18 RT-PCR产物进行1.5%琼脂糖电泳,发现RT-PCR产物为单一条带,大小约为490bp。
2.2 hIL-18的表达载体 PBV-hIL-18的构建、转化大肠杆菌及筛选鉴定 PBV-IL-18的转化大肠杆菌的阳性克隆进行,双酶切鉴定,酶切产物作1.5%琼脂糖电泳鉴定,发现其小片段大小约为490bp,与预期结果一致。
, 百拇医药
2.3 PBV-IL-18的序列分析 序列分析结果如
下,与人IL-8的成熟肽的基因序列[3]一致。GAA
TTCATGTACTTTGGCAAGCTTGAATCTAAATT
ATCAGTCATAAGAAATTTGAATGACCAAGTTC
TCTTCATTGACCAAGGAAATCGGCCTCTATTT
GAAGATATGACTGATTCTGACTGTAGAGATAA
TGCACCCCGGACCATATTTATTATAAGTATGT
ATAAAGATAGCCCAGCCTAGAGGTATGGCTGT
, 百拇医药
AACTATCTCTGTGAAGTGTGAGAAAATTTCAA
CTCTCTCCTGTGAGAACAAAATTATTTCCTTT
AAGGAAATGAATCCTCCTGATAACATCAAGGA
TACAAAAAGTGACATCATATTCTTTCAGAGAA
GTGTCCCAGGACATGATAATAAGATGCAATTT
GAATCTTCATCATACGAAGGATACTTTCTAGC
TTGTGAAAAAGAGAGAGACCTTTTTAAACTCA
TTTTGAAAAAAGAGGATGAATTGGGGGATAGA
, 百拇医药
TCTATAATGTTCACTGTTCAAAACGAAGACTA
ACCTAGG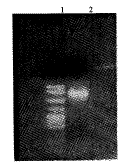
图1 RT-PCR电泳图谱
1.PBR322/MspIDNA marker622,527,404,309,242,238,217 2.RT-PCR产物
图2 酶切鉴定图谱
1.PBR322/MspI DNA marker 2.PBV-IL-18双酶切产物 3.PBV220双酶切产物 4.λDNA/HindIII markdr:23130,9416,4361,2322,2027,564,125
, 百拇医药
2.4 PBV-IL-18的最佳表达条件的确定 PBV-IL-18大肠杆菌表达产物经SDS-PAGE电泳表明,IL-18蛋白分子量约为18kd,与预期结果一致,而表达的最佳条件为在42℃下诱导5h为最佳。
3 讨论
本文结果表明,采用RT-PCR从正常人外周血中克隆hIL-18 cDNA重组于高效表达载体PBV220上,经鉴定后在大肠杆菌中获得高效表达。全长hIL-18基因编码含193个氨基酸的前体蛋白,缺乏N-糖基化位点和疏水样信号肽,但其N-端有一结构特殊的36个氨基酸的前导序列,经ICE(IL-1 β converting enayme)特异水解肽链,去除N-端前导序列而活化,并且促进IL-18的分泌[3,8]。我们在设计PCR引物时,去掉了hIL-18的引导序列,并在上游引物上加上限制性酶切位点EcoRI及起码始密码子ATG,在下游引物上加上限制性酶切位点BamHI及终止密码子TAA(考虑大肠杆菌密码子的偏爱性),并在引物5’端加上几个无关碱基,以保证限制性内切酶位点能被限制性内切酶正常酶切。
, 百拇医药
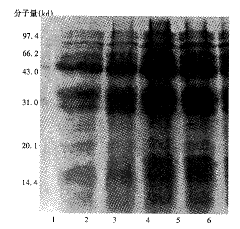
图3 PBV-IL-18不同诱导时间 (1.低分子量标准蛋白质,2 PBV-IL-18未诱导表达(30℃培养),3.PBV-IL-18在 42℃经3h诱导表达,4.PBV-IL-18在42℃4h经诱导表达,5.PBV-IL-18在 42℃5h经诱导表达,6.PBV-IL-18在 42℃6h经诱导表达)
PBV220表达载体由候云德教授实验室构建,具有PLPR启动子,该位点受抑制物CI蛋白的负调控,CI蛋白由DNA片段CIts857编码,为温度敏感型,在30℃时抑制启动子的活性,42℃时失活而失去抑制启动子的活性,故可通过温控来调节hIL-18的表达。
由于hIL-18在抗病毒和肿瘤免疫治疗方面具有广泛的应用潜力,我们在大肠杆菌中表达hIL-18,为进一步进行hIL-18的生物学活性研究及将其开发为基因工程药物打下了基础。
, http://www.100md.com
缪海珍,硕士研究生;杨吉成,导师
参 考 文 献
1,Okamura H,Nagata K,Komastu T,et al.A novel costimulatory factor for gamma interferon induction found in the livers of mice causes endotoxic shock.Infeet Immun,1995,63∶3966
2,Okamura H,Nagata K,Komastu T,et al.Cloning of a new cytokine that introduces IFN-gamma production by Tcells.Nature,1995,378∶88
3,Shimpei Ushio,Motoshi Namba,Takanori Okura,et al.Cloning of the cDNA for human IFN-γ-inducing factor,expression in escherichia coli,and studies on the biologic activities of the protein.J Immunology,1996,156∶4274
, 百拇医药
4,Tomura M,Maruo S,Mu J,et al.Differential capacities of CD4+,CD8-T cell subsets to express IL-18 receptor and produce IFN-gamma in response to IL-18.J Immunol,1998,160(8)∶3759
5,Tomura M,Zhou XY,Maruo S,et al.A critical role for IL-18 in the proliferation and activation of NK1.1+CD3- cells.J Immunol,1998,160(10)∶4738
6,Dao T,Ohashi K,Kayano T,et al.Interferon-gamma-inducing factor,a novel cytokine,enhances Fas ligand-mediated cytotoxicity of murine T helper 1 cells.Cell Immunol,1996,173(2)∶230
, http://www.100md.com
7,Osaki T,Peron JM,Cai Q,et al.IFN-gamma-inducing factor /IL-18 administration mediater IFN-gamma-and IL-12-indepent antitumor effects.J Immunol,1998,160(4)∶1742
8,Gu Y,Kuida K,Tsutsui H,et al.Activities of interferon-gamma inducing factor mediated by interleukin-1 beta converting enzyme.Science,1997,275∶206
2000年1月30日收稿, 百拇医药
单位:苏州医学院基因工程研究室,苏州,215007
关键词:人白细胞介素-18;RT-PCR;大肠杆菌;表达
苏州医学院学报000906 摘要 目的 为进一步研究人白细胞介素(hIL-18)的生物学特性打下基础,进行hIL-18的基因克隆及原核表达。方法 采用反转录PCR(RT-PCR)法从正常人外周血白细胞中克隆hIL-18基因,并重组于PBV220表达载体上,经酶切初步鉴定后进行DNA序列分析,继而观察重组hIL-18基因在大肠杆菌中不同诱导时间表达量的差异。结果 所克隆的基因与预期结果一致,并在42℃诱导5h时表达量最高。结论 成功地克隆了hIL-18基因,并使获得高效表达。
中图法分类号 R392.13
, 百拇医药
Cloning and Expression of Human Interleukin-18 Gene in E.coli
Miao Haizhen, Yang Jichen, Sheng Weihua, et al
(Department of Gene Research,Suzhou Medical College,Suzhou,215007)
Abstract Objective In order to study hIL-18 biological characteristics in a more advanced way,we proceed this study.Mehods The hIL-18 gene by RT-PCR from human peripheral white blood cells was amplified and recombined into a thermo-sensitive expression vector PBV220,then the competent cells of E.coli DH5α was introduced into.Finally,we analyzed the different expression level of hIL-18 gene at different inducing time.Results With the identification of enzyme map and sequncing,we find our cloned gene in acconformity with the published papers about hIL-18,and the expression rate was highest when induced 5h at 42℃.Conclusion we clone hIL-18 gene successfully and obtain high rate expression.
, 百拇医药
Key words human interleukin-18;RT-PCR;E.coli;expression
白细胞介素18(Interleukin 18,IL-18)是一种新发现的免疫调节细胞因子[1~3],主要由单核巨噬细胞产生,具有诱导T细胞产生IFN-γ[4],促进NK细胞杀伤活性[5],增强Fas/FasL介导的细胞毒作用[6],具有明显的抗肿瘤效果[7]。本研究采用逆转录PCR技术克隆hIL-18的cDNA,并观察其在大肠杆菌中的表达,结果报道如下。
1 材料与方法
1.1 主要材料 克隆载体PUC19、表达载体PBV220及大肠杆菌DH5α均为本实验室保存,TRIZOL总RNA试剂盒(Prmega),M-MoLV逆转录酶(MBI),Oligo(bT)15(Promega),DNA聚合酶Taq(Promega),T4DNA连接酶(MBI),限制性内切酶EcoRI、BamHI(华美生物工程公司),RPMI 1640培养基(Gibco),PBR322/MspI DNA Marker(华美生物工程公司),低分子量标准白质(上海丽珠东风生物技术有限公司)
, 百拇医药
1.2 方法
1.2.1 正常人外周血白细胞(PBMC)的分离 取正常人外周血10ml,用Ficoll按常规方法分离白细胞,以3×106个/ml的浓度在含10%的小牛血清的RPMI1640培养基中培养过夜。
1.2.2 hIL-18的RT-PCR克隆 按说明书用TRIZOL总RNA试剂盒提取PBMC的总RNA,取3μg总RNA与0.5μg Oligo(dT)15混合,进行反转录。PCR扩增的上游引物为5’-GGAATTCATGTACTTTGGCAAGCTTG(含EcoRI位点及起始密码子ATG),下游引物为5’-CGGGATCCTTAGTCTT-CGTTTTGAAC(含BamHI位点及终止密码子TAA)(上海生工生物工程公司合成)。PCR反应体积为50μl,引物浓度为0.6μmol/L,扩增参数为94℃ 5min、94℃45s、55℃60s、72℃90s,30个循环后72℃延伸10min。扩增产物行1.5%琼脂糖凝胶电泳分析。1.2.3 hIL-18表达载体PBV-IL-8的构建及筛选鉴定 hIL-18cDNA PCR产物与抽提的PBV220表达载体的质粒分别经EcoRI、BamHI双酶切后行1.5%的琼脂糖电泳,并用1.0%的低熔点琼脂糖回收,按常规方法用T4连接酶将两者连接并转化至大肠杆菌DH5α的感受态,挑选阳性克隆进行酶切鉴定,酶切产物行1.5%琼脂糖凝胶电泳。
, 百拇医药
1.2.4 hIL-18h基因的序列分析 将从PBV-IL-18重组质粒切下的约480bp的基因片段定向插入PUC19克隆载体,由上海基康生物技术有限公司进行测序。
1.2.5 hIL-18的表达及SDS-PAGE电泳分析 hIL-18经温控诱导表达后进行15%SDS-PAGE 200V恒压电泳,经考马斯亮蓝染色及脱色后观察hIL-18在不同诱导时间(3h、4h、5h、6h)表达量的差别。
2 结果
2.1 hIL-18 RT-PCR产物的电泳分析 hIL-18 RT-PCR产物进行1.5%琼脂糖电泳,发现RT-PCR产物为单一条带,大小约为490bp。
2.2 hIL-18的表达载体 PBV-hIL-18的构建、转化大肠杆菌及筛选鉴定 PBV-IL-18的转化大肠杆菌的阳性克隆进行,双酶切鉴定,酶切产物作1.5%琼脂糖电泳鉴定,发现其小片段大小约为490bp,与预期结果一致。
, 百拇医药
2.3 PBV-IL-18的序列分析 序列分析结果如
下,与人IL-8的成熟肽的基因序列[3]一致。GAA
TTCATGTACTTTGGCAAGCTTGAATCTAAATT
ATCAGTCATAAGAAATTTGAATGACCAAGTTC
TCTTCATTGACCAAGGAAATCGGCCTCTATTT
GAAGATATGACTGATTCTGACTGTAGAGATAA
TGCACCCCGGACCATATTTATTATAAGTATGT
ATAAAGATAGCCCAGCCTAGAGGTATGGCTGT
, 百拇医药
AACTATCTCTGTGAAGTGTGAGAAAATTTCAA
CTCTCTCCTGTGAGAACAAAATTATTTCCTTT
AAGGAAATGAATCCTCCTGATAACATCAAGGA
TACAAAAAGTGACATCATATTCTTTCAGAGAA
GTGTCCCAGGACATGATAATAAGATGCAATTT
GAATCTTCATCATACGAAGGATACTTTCTAGC
TTGTGAAAAAGAGAGAGACCTTTTTAAACTCA
TTTTGAAAAAAGAGGATGAATTGGGGGATAGA
, 百拇医药
TCTATAATGTTCACTGTTCAAAACGAAGACTA
ACCTAGG

图1 RT-PCR电泳图谱
1.PBR322/MspIDNA marker622,527,404,309,242,238,217 2.RT-PCR产物

图2 酶切鉴定图谱
1.PBR322/MspI DNA marker 2.PBV-IL-18双酶切产物 3.PBV220双酶切产物 4.λDNA/HindIII markdr:23130,9416,4361,2322,2027,564,125
, 百拇医药
2.4 PBV-IL-18的最佳表达条件的确定 PBV-IL-18大肠杆菌表达产物经SDS-PAGE电泳表明,IL-18蛋白分子量约为18kd,与预期结果一致,而表达的最佳条件为在42℃下诱导5h为最佳。
3 讨论
本文结果表明,采用RT-PCR从正常人外周血中克隆hIL-18 cDNA重组于高效表达载体PBV220上,经鉴定后在大肠杆菌中获得高效表达。全长hIL-18基因编码含193个氨基酸的前体蛋白,缺乏N-糖基化位点和疏水样信号肽,但其N-端有一结构特殊的36个氨基酸的前导序列,经ICE(IL-1 β converting enayme)特异水解肽链,去除N-端前导序列而活化,并且促进IL-18的分泌[3,8]。我们在设计PCR引物时,去掉了hIL-18的引导序列,并在上游引物上加上限制性酶切位点EcoRI及起码始密码子ATG,在下游引物上加上限制性酶切位点BamHI及终止密码子TAA(考虑大肠杆菌密码子的偏爱性),并在引物5’端加上几个无关碱基,以保证限制性内切酶位点能被限制性内切酶正常酶切。
, 百拇医药

图3 PBV-IL-18不同诱导时间 (1.低分子量标准蛋白质,2 PBV-IL-18未诱导表达(30℃培养),3.PBV-IL-18在 42℃经3h诱导表达,4.PBV-IL-18在42℃4h经诱导表达,5.PBV-IL-18在 42℃5h经诱导表达,6.PBV-IL-18在 42℃6h经诱导表达)
PBV220表达载体由候云德教授实验室构建,具有PLPR启动子,该位点受抑制物CI蛋白的负调控,CI蛋白由DNA片段CIts857编码,为温度敏感型,在30℃时抑制启动子的活性,42℃时失活而失去抑制启动子的活性,故可通过温控来调节hIL-18的表达。
由于hIL-18在抗病毒和肿瘤免疫治疗方面具有广泛的应用潜力,我们在大肠杆菌中表达hIL-18,为进一步进行hIL-18的生物学活性研究及将其开发为基因工程药物打下了基础。
, http://www.100md.com
缪海珍,硕士研究生;杨吉成,导师
参 考 文 献
1,Okamura H,Nagata K,Komastu T,et al.A novel costimulatory factor for gamma interferon induction found in the livers of mice causes endotoxic shock.Infeet Immun,1995,63∶3966
2,Okamura H,Nagata K,Komastu T,et al.Cloning of a new cytokine that introduces IFN-gamma production by Tcells.Nature,1995,378∶88
3,Shimpei Ushio,Motoshi Namba,Takanori Okura,et al.Cloning of the cDNA for human IFN-γ-inducing factor,expression in escherichia coli,and studies on the biologic activities of the protein.J Immunology,1996,156∶4274
, 百拇医药
4,Tomura M,Maruo S,Mu J,et al.Differential capacities of CD4+,CD8-T cell subsets to express IL-18 receptor and produce IFN-gamma in response to IL-18.J Immunol,1998,160(8)∶3759
5,Tomura M,Zhou XY,Maruo S,et al.A critical role for IL-18 in the proliferation and activation of NK1.1+CD3- cells.J Immunol,1998,160(10)∶4738
6,Dao T,Ohashi K,Kayano T,et al.Interferon-gamma-inducing factor,a novel cytokine,enhances Fas ligand-mediated cytotoxicity of murine T helper 1 cells.Cell Immunol,1996,173(2)∶230
, http://www.100md.com
7,Osaki T,Peron JM,Cai Q,et al.IFN-gamma-inducing factor /IL-18 administration mediater IFN-gamma-and IL-12-indepent antitumor effects.J Immunol,1998,160(4)∶1742
8,Gu Y,Kuida K,Tsutsui H,et al.Activities of interferon-gamma inducing factor mediated by interleukin-1 beta converting enzyme.Science,1997,275∶206
2000年1月30日收稿, 百拇医药