玻璃体内持续释放肝素防治牵引性视网膜脱离的实验研究
作者:刘瑜玲 陈改清 张强 徐亮 张士元 何蕾
单位:刘瑜玲(100083北京医科大学第三医院眼科);陈改清(首都医科大学化学教研室);张强 徐亮 张士元 何蕾(北京医科大学药学院)
关键词:生物降解性微球;聚乳酸;肝素;增生性玻璃体视网膜病变
眼科研究000406
摘要 目的研究肝素聚乳酸微球(HEP-MS)对兔牵引性视网膜脱离(TRD)的防治效果。方法溶媒挥发法制备HEP-MS,扫描电镜观察其形态,比色法测定其体外释放;在兔玻璃体内注入成纤维细胞后,分别注入空白微球,不注入/注入载药微球,观察TRD发生情况。结果微球球形较好,平均粒径68.6μm。对照及载药微球组在4周末时TRD的发生率分别为80%和50%,两者有显著性差异(P<0.05)。结论玻璃体内一次性注入HEP-MS能够有效地减少TRD的发生。
, 百拇医药
分类号 R774
Biodegradable microspheres containing heparin in the treatment of
proliferative vitreoretinopathy
Liu Yuling Chen Gaiqing Zhang Qiang et al.
(Department of Ophthalmology,Third Teaching Hospital of Beijing Medical University,Beijing 100083)
Abstract ObjectiveTo investigate the possibility of biodegradable heparin polylactic acid microspheres (HEP-MS) for the treatment of proliferative vitreoretinopathy (PVR) in an experimental rabbit model.MethodsBiodegradable microspheres containing heparin was prepared by solvent evaporation method.Morphology of HEP-MS was examined by the scanning electron microscope.The loading copacity of heparin in HEP-MS was analyzed by a fluorospectro-photometer,and the in vitro release of heparin from the HEP-MS was also investigated.Twenty pigmented rabbits (40 eyes) were divided into two groups.The blank microspheres (10 eyes) and phosphate buffer solution (PBS) (10 eyes) were injected intravitreally as the control.The HEP-MS containing 1.42mg/ml(20 eyes) of HEP were injected into the other group.7d after second gas-compression vitrectomy,2×105 fibroblastes and HEP-MS (or control) were injected into all eyes sequentially.The morbidity of tractional retinal detachment (TRD) were observed by ophthalmoscope for 4 weeks.ResultsThe HEP-MS was quite round,and the mean diameter of HEP-MS was 68.6μm.The loading capacity of heparin in HEP-MS was 1.42%.4 weeks later,the morbidity of TRD in control,1.42mg/ml HEP-MS group was 80%,and 50% respectively.Significant statistical difference was found between the control group and the HEP-MS group(P<0.05).ConclusionThe microspheres containing 1.42mg/ml of HEP can inhibit the occurrence of TRD effectively.
, 百拇医药
Key words biodegradable microspheres polylactic acid heparin proliferative vitreoretinopathy
近年来,探索在玻璃体内导入控释药物输送系统以减少给药次数,提高疗效,已成为多种眼后节疾病药物防治的最新研究方向。本研究采用生物降解性高分子材料聚乳酸(poly-lacticacid,PLA)制备肝素聚乳酸微球(heparin polylactic acid microsphere,HEP-MS),观察其对兔结膜成纤维细胞诱发的牵引性视网膜脱离的防治作用。
1 材料与方法
1.1 主要材料
肝素钠(第二军医大学医用科技实业服务部);乙腈(北京化学试剂公司);PLA(分子量30000,山东省医疗试剂公司);蓖麻油(湖北省天门市第二制药厂);Span-80(北京百利化学品开发中心);Tween-80(上海大众制药厂);灰兔(卫生部生物制品研究所)。
, 百拇医药
1. 2 实验方法
1.2.1 HEP-MS的制备 采用溶媒挥发法[1]制备HEP-MS。取PLA和HEP,加入二氯甲烷,超声分散后,用7号针头快速注入20%PVA的水溶液中,减压下搅拌1h,离心弃去上清液,加水分散沉淀,冷冻干燥即得。
1.2.2 HEP-MS形态观察与粒径测定 用扫描电镜观察HEP-MS的形态,并从电镜照片上随机取250个MS,用测微尺测等方向径,求平均值。
1.2.3 HEP-MS含量测定方法的建立 取HEP-MS样品适量,用二氯甲烷溶解,加水萃取3次,水相合并定容。参照文献方法[2],选用灿烂甲酚兰(BCB)的邻苯二甲酚液为显色剂,在640nm处测定吸收值。本方法在2~7μg/ml范围内,吸收值A与浓度C之间线性良好(A=0.9495-0.0693C,r=0.9996),在PLA存在下,3个浓度的平均回收率为105.87%(RSD=2.57%)。
, 百拇医药
1.2.4 HEP-MS的体外释放试验 取定量的HEP-MS,置于离心管内,加入pH7.4的磷酸缓冲液,在37℃,410cpm的条件下振荡,定期取样,于640 nm处测吸收值,并计算累积释放百分数。
1.2.5 PVR模型的建立 取成年健康灰兔20只,雌雄兼用,体重1.7~2.6kg/只。随机分为对照和HEP-MS组,如附表所示。以复方氯胺酮肌肉麻醉后,眼局部用美多林散瞳。然后行气体压迫玻璃体术[3]。
取兔结膜成纤维细胞,采用Blumen-kranz等人[4]的方法培养。离心细胞,稀释至终浓度2×105/0.1mlPBS。第2次注射气体后第7天,用30号针头在鼻上象限角膜缘后3mm处向玻璃体腔中部注入培养的同种异体成纤维细胞悬液0.1ml。
1.2.6 眼内注射给药 注入成纤维细胞悬液后,用30号针头向对照组(10只)左眼内注入空白微球悬液0.1ml,右眼内注入PBS0.1ml。HEP-MS组注入1.42mg/ml的HEP-MS悬液0.1ml(20眼)。
, 百拇医药
1.2.7 眼底检查及眼底改变的分级 眼内注射给药后1,4,7,14,21和28天用间接检眼镜检查眼底,照像和/或绘图记录玻璃体和视网膜情况。28天时静脉注气处死兔,摘除眼球,以甲醛戊二醛混合液固定眼球,梯度酒精脱水,石蜡包埋,切片,苏木素伊红染色,光镜观察。
眼内的增殖改变参照文献方法[5]分为5个等级:0级:眼底正常,玻璃体无混浊;1级:眼底正常,玻璃体内见增殖的条带;2级:条带牵拉至髓线抬高,或有局限性视网膜脱离;3级:视网膜全脱离或漏斗状脱离。将2,3级累计作为视网膜脱离(retinal detachment,RD)的发生率。
1.2.8 统计学分析 HEP-MS组与对照组间的差异用χ2检验。
2 结果
扫描电镜下可见HEP-MS的球形较规则,多数无粘连(图1)。其平均粒径为68.6μm,HEP-MS中HEP的载药量为1.42%。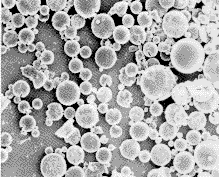
, http://www.100md.com
图1 HEP-MS的扫描电镜图谱
Fig1 Scanning electron photomicrograph of HEP-MS
HEP-MS体外释放测定结果如图2所示。
图2 肝素聚乳酸微球体外释放曲线
Fig2 In vitro release profile of HEP-MS
兔眼玻璃体注入成纤维细胞后,立即在后部玻璃体形成雾状混浊区,并在7天左右逐渐变为灰白色的细小条带,逐渐趋向于视盘和髓线。由于注入PBS和空白微球的眼在各时间点,RD的发生率无统计学差异,因此合并作为对照组。对照组20只眼在28天时,有16只眼(80%)发生了RD;HEP-MS组20只眼在28天时,有10只眼(50%)发生了RD,其中仅有1例发生全脱离。以上结果均经病理检查证实。表1总结了药物治疗的观察结果。
, 百拇医药
表1 HEP-MS给药后的视网膜脱离程度
Tab.1 Morbidity of retinal detachment
after administration of HEP-MS Degree
7d
14d
21d
28d
eye
%
eye
%
, 百拇医药
eye
%
Eye
%
Control* (n=20)
0
8
40
5
25
3
15
0
, http://www.100md.com
1
10
50
6
30
5
25
4
20
2
2
10
8
40
, 百拇医药
8
40
9
45
3
0
1
5
4
20
7
35
1.42mg/ml HEP-MS(n=20)
, http://www.100md.com
0
13
65
8
40
6
30
2
10
1
5
25
8
40
, 百拇医药
8
40
8
40
2
2
10
3
15
4
20
7
35
3
, http://www.100md.com
0
1
5
2
10
3
15
* Nothing and blank MS were injected as the control
表中可见,HEP-MS组与对照组相比,28天时RD的发生率明显减少,有显著差异(P<0.05)。观察还发现,多数药物治疗眼的RD范围较小,大多数局限于髓线及其附近,而对照组则多为视网膜全脱离。
3 讨论
, 百拇医药
迄今为止,国内外关于PVR的药物性防治方面已有较多的研究,但大多局限于一些抗肿瘤的药物如氟脲嘧啶,柔红霉素等。但因此类药物均具有较强的细胞毒作用,故难以在临床上推广应用。以往的研究表明[6,7],肝素类物质除具有传统的抗凝作用外尚具有和防治PVR有关的多种其它生物活性。
关于肝素类物质抑制细胞增殖的机制,至今尚不清楚。有资料表明[8,9],肝素类物质不仅可直接抑制成纤维细胞和RPE细胞等细胞的增殖;还可抑制增殖细胞介导的胶原收缩,通过抑制胶原聚合作用减少玻璃体内纤维条索的形成;另外,肝素类物质还可通过与生长因子(如bFGF,EGF等)的结合而减弱后者对细胞增殖的促进作用,发挥抗PVR的作用。
微球(microspheres)是由高分子材料制成的直径在微米数量级的固体微粒。其中PLA是目前获准用于临床的少数生物降解性高分子物质之一。本研究将PLA制成载带HEP的MS,用于治疗PVR,实验表明HEP-MS可缓慢地较长期释放,一次性玻璃体腔内注入HEP-MS可有效地抑制兔实验性PVR的发生和发展,也就是说,作为玻璃体内释药系统的HEP-MS在PVR的防治方面具有明显的作用。
, http://www.100md.com
本课题受北京市教委科技发展基金资助
参考文献:
1.Wada R,Hyon SH,Ikada Y.Lactic acid oligomer microspheres containing hydrophilic drugs.J Pharm Sci,1990,79∶ 919
2.Johnson EA,Mulloy B.Simple metachromatic assay methods for heparin and protamine.J Pharm Pharmac,1976,28∶ 836
3.Chandler DB,Quansah FA,Hida T,et al.A refined experimental model for proliferative vitreoretinopathy.Graeferch Clin Exp Ophthalmol,1986,224∶ 86
, 百拇医药
4.Blumenkranz MS,Claflin A,Hajek AS.Selection of therapeutic agents for intraocular proliferative disease.Arch Ophthalmol,1984,102∶ 598
5.栾洁,王文吉,陈钦元,等.维甲酸硅油防治实验性增殖性玻璃体视网膜病变.中华眼底病杂志,1997,13(3)∶ 174
6.Lippman MM,Mathews MB.Heparin:Varying effects on cell proliferation in vitro and lack of correlation with anticoaculant activity.Federation Proceedings,1977,36(1)∶ 55
7.Iverson DA,Dailey WD,Hartzer M,et al.The effect of low moleculer weight heparin the mitogenicity of intraocular fluid from pattents with proliferative retinopathies.Invest Ophthalmol Vis Sci,1991,32∶ 879
, http://www.100md.com
8.Wang AM,templeton DM.Inhibition of mitogenesis and c-fos induction in mesangial cells by heparin and heparan sulfates.Kidney International,1996,49∶ 437
9.Castllot JJ.Effect of heparin on Vascular smooth muscle cells:I.Cell metabolism.J Cell Physiol,1985,124∶ 21
收稿:1999-09-03
修回:2000-04-08, 百拇医药
单位:刘瑜玲(100083北京医科大学第三医院眼科);陈改清(首都医科大学化学教研室);张强 徐亮 张士元 何蕾(北京医科大学药学院)
关键词:生物降解性微球;聚乳酸;肝素;增生性玻璃体视网膜病变
眼科研究000406
摘要 目的研究肝素聚乳酸微球(HEP-MS)对兔牵引性视网膜脱离(TRD)的防治效果。方法溶媒挥发法制备HEP-MS,扫描电镜观察其形态,比色法测定其体外释放;在兔玻璃体内注入成纤维细胞后,分别注入空白微球,不注入/注入载药微球,观察TRD发生情况。结果微球球形较好,平均粒径68.6μm。对照及载药微球组在4周末时TRD的发生率分别为80%和50%,两者有显著性差异(P<0.05)。结论玻璃体内一次性注入HEP-MS能够有效地减少TRD的发生。
, 百拇医药
分类号 R774
Biodegradable microspheres containing heparin in the treatment of
proliferative vitreoretinopathy
Liu Yuling Chen Gaiqing Zhang Qiang et al.
(Department of Ophthalmology,Third Teaching Hospital of Beijing Medical University,Beijing 100083)
Abstract ObjectiveTo investigate the possibility of biodegradable heparin polylactic acid microspheres (HEP-MS) for the treatment of proliferative vitreoretinopathy (PVR) in an experimental rabbit model.MethodsBiodegradable microspheres containing heparin was prepared by solvent evaporation method.Morphology of HEP-MS was examined by the scanning electron microscope.The loading copacity of heparin in HEP-MS was analyzed by a fluorospectro-photometer,and the in vitro release of heparin from the HEP-MS was also investigated.Twenty pigmented rabbits (40 eyes) were divided into two groups.The blank microspheres (10 eyes) and phosphate buffer solution (PBS) (10 eyes) were injected intravitreally as the control.The HEP-MS containing 1.42mg/ml(20 eyes) of HEP were injected into the other group.7d after second gas-compression vitrectomy,2×105 fibroblastes and HEP-MS (or control) were injected into all eyes sequentially.The morbidity of tractional retinal detachment (TRD) were observed by ophthalmoscope for 4 weeks.ResultsThe HEP-MS was quite round,and the mean diameter of HEP-MS was 68.6μm.The loading capacity of heparin in HEP-MS was 1.42%.4 weeks later,the morbidity of TRD in control,1.42mg/ml HEP-MS group was 80%,and 50% respectively.Significant statistical difference was found between the control group and the HEP-MS group(P<0.05).ConclusionThe microspheres containing 1.42mg/ml of HEP can inhibit the occurrence of TRD effectively.
, 百拇医药
Key words biodegradable microspheres polylactic acid heparin proliferative vitreoretinopathy
近年来,探索在玻璃体内导入控释药物输送系统以减少给药次数,提高疗效,已成为多种眼后节疾病药物防治的最新研究方向。本研究采用生物降解性高分子材料聚乳酸(poly-lacticacid,PLA)制备肝素聚乳酸微球(heparin polylactic acid microsphere,HEP-MS),观察其对兔结膜成纤维细胞诱发的牵引性视网膜脱离的防治作用。
1 材料与方法
1.1 主要材料
肝素钠(第二军医大学医用科技实业服务部);乙腈(北京化学试剂公司);PLA(分子量30000,山东省医疗试剂公司);蓖麻油(湖北省天门市第二制药厂);Span-80(北京百利化学品开发中心);Tween-80(上海大众制药厂);灰兔(卫生部生物制品研究所)。
, 百拇医药
1. 2 实验方法
1.2.1 HEP-MS的制备 采用溶媒挥发法[1]制备HEP-MS。取PLA和HEP,加入二氯甲烷,超声分散后,用7号针头快速注入20%PVA的水溶液中,减压下搅拌1h,离心弃去上清液,加水分散沉淀,冷冻干燥即得。
1.2.2 HEP-MS形态观察与粒径测定 用扫描电镜观察HEP-MS的形态,并从电镜照片上随机取250个MS,用测微尺测等方向径,求平均值。
1.2.3 HEP-MS含量测定方法的建立 取HEP-MS样品适量,用二氯甲烷溶解,加水萃取3次,水相合并定容。参照文献方法[2],选用灿烂甲酚兰(BCB)的邻苯二甲酚液为显色剂,在640nm处测定吸收值。本方法在2~7μg/ml范围内,吸收值A与浓度C之间线性良好(A=0.9495-0.0693C,r=0.9996),在PLA存在下,3个浓度的平均回收率为105.87%(RSD=2.57%)。
, 百拇医药
1.2.4 HEP-MS的体外释放试验 取定量的HEP-MS,置于离心管内,加入pH7.4的磷酸缓冲液,在37℃,410cpm的条件下振荡,定期取样,于640 nm处测吸收值,并计算累积释放百分数。
1.2.5 PVR模型的建立 取成年健康灰兔20只,雌雄兼用,体重1.7~2.6kg/只。随机分为对照和HEP-MS组,如附表所示。以复方氯胺酮肌肉麻醉后,眼局部用美多林散瞳。然后行气体压迫玻璃体术[3]。
取兔结膜成纤维细胞,采用Blumen-kranz等人[4]的方法培养。离心细胞,稀释至终浓度2×105/0.1mlPBS。第2次注射气体后第7天,用30号针头在鼻上象限角膜缘后3mm处向玻璃体腔中部注入培养的同种异体成纤维细胞悬液0.1ml。
1.2.6 眼内注射给药 注入成纤维细胞悬液后,用30号针头向对照组(10只)左眼内注入空白微球悬液0.1ml,右眼内注入PBS0.1ml。HEP-MS组注入1.42mg/ml的HEP-MS悬液0.1ml(20眼)。
, 百拇医药
1.2.7 眼底检查及眼底改变的分级 眼内注射给药后1,4,7,14,21和28天用间接检眼镜检查眼底,照像和/或绘图记录玻璃体和视网膜情况。28天时静脉注气处死兔,摘除眼球,以甲醛戊二醛混合液固定眼球,梯度酒精脱水,石蜡包埋,切片,苏木素伊红染色,光镜观察。
眼内的增殖改变参照文献方法[5]分为5个等级:0级:眼底正常,玻璃体无混浊;1级:眼底正常,玻璃体内见增殖的条带;2级:条带牵拉至髓线抬高,或有局限性视网膜脱离;3级:视网膜全脱离或漏斗状脱离。将2,3级累计作为视网膜脱离(retinal detachment,RD)的发生率。
1.2.8 统计学分析 HEP-MS组与对照组间的差异用χ2检验。
2 结果
扫描电镜下可见HEP-MS的球形较规则,多数无粘连(图1)。其平均粒径为68.6μm,HEP-MS中HEP的载药量为1.42%。

, http://www.100md.com
图1 HEP-MS的扫描电镜图谱
Fig1 Scanning electron photomicrograph of HEP-MS
HEP-MS体外释放测定结果如图2所示。

图2 肝素聚乳酸微球体外释放曲线
Fig2 In vitro release profile of HEP-MS
兔眼玻璃体注入成纤维细胞后,立即在后部玻璃体形成雾状混浊区,并在7天左右逐渐变为灰白色的细小条带,逐渐趋向于视盘和髓线。由于注入PBS和空白微球的眼在各时间点,RD的发生率无统计学差异,因此合并作为对照组。对照组20只眼在28天时,有16只眼(80%)发生了RD;HEP-MS组20只眼在28天时,有10只眼(50%)发生了RD,其中仅有1例发生全脱离。以上结果均经病理检查证实。表1总结了药物治疗的观察结果。
, 百拇医药
表1 HEP-MS给药后的视网膜脱离程度
Tab.1 Morbidity of retinal detachment
after administration of HEP-MS Degree
7d
14d
21d
28d
eye
%
eye
%
, 百拇医药
eye
%
Eye
%
Control* (n=20)
0
8
40
5
25
3
15
0
, http://www.100md.com
1
10
50
6
30
5
25
4
20
2
2
10
8
40
, 百拇医药
8
40
9
45
3
0
1
5
4
20
7
35
1.42mg/ml HEP-MS(n=20)
, http://www.100md.com
0
13
65
8
40
6
30
2
10
1
5
25
8
40
, 百拇医药
8
40
8
40
2
2
10
3
15
4
20
7
35
3
, http://www.100md.com
0
1
5
2
10
3
15
* Nothing and blank MS were injected as the control
表中可见,HEP-MS组与对照组相比,28天时RD的发生率明显减少,有显著差异(P<0.05)。观察还发现,多数药物治疗眼的RD范围较小,大多数局限于髓线及其附近,而对照组则多为视网膜全脱离。
3 讨论
, 百拇医药
迄今为止,国内外关于PVR的药物性防治方面已有较多的研究,但大多局限于一些抗肿瘤的药物如氟脲嘧啶,柔红霉素等。但因此类药物均具有较强的细胞毒作用,故难以在临床上推广应用。以往的研究表明[6,7],肝素类物质除具有传统的抗凝作用外尚具有和防治PVR有关的多种其它生物活性。
关于肝素类物质抑制细胞增殖的机制,至今尚不清楚。有资料表明[8,9],肝素类物质不仅可直接抑制成纤维细胞和RPE细胞等细胞的增殖;还可抑制增殖细胞介导的胶原收缩,通过抑制胶原聚合作用减少玻璃体内纤维条索的形成;另外,肝素类物质还可通过与生长因子(如bFGF,EGF等)的结合而减弱后者对细胞增殖的促进作用,发挥抗PVR的作用。
微球(microspheres)是由高分子材料制成的直径在微米数量级的固体微粒。其中PLA是目前获准用于临床的少数生物降解性高分子物质之一。本研究将PLA制成载带HEP的MS,用于治疗PVR,实验表明HEP-MS可缓慢地较长期释放,一次性玻璃体腔内注入HEP-MS可有效地抑制兔实验性PVR的发生和发展,也就是说,作为玻璃体内释药系统的HEP-MS在PVR的防治方面具有明显的作用。
, http://www.100md.com
本课题受北京市教委科技发展基金资助
参考文献:
1.Wada R,Hyon SH,Ikada Y.Lactic acid oligomer microspheres containing hydrophilic drugs.J Pharm Sci,1990,79∶ 919
2.Johnson EA,Mulloy B.Simple metachromatic assay methods for heparin and protamine.J Pharm Pharmac,1976,28∶ 836
3.Chandler DB,Quansah FA,Hida T,et al.A refined experimental model for proliferative vitreoretinopathy.Graeferch Clin Exp Ophthalmol,1986,224∶ 86
, 百拇医药
4.Blumenkranz MS,Claflin A,Hajek AS.Selection of therapeutic agents for intraocular proliferative disease.Arch Ophthalmol,1984,102∶ 598
5.栾洁,王文吉,陈钦元,等.维甲酸硅油防治实验性增殖性玻璃体视网膜病变.中华眼底病杂志,1997,13(3)∶ 174
6.Lippman MM,Mathews MB.Heparin:Varying effects on cell proliferation in vitro and lack of correlation with anticoaculant activity.Federation Proceedings,1977,36(1)∶ 55
7.Iverson DA,Dailey WD,Hartzer M,et al.The effect of low moleculer weight heparin the mitogenicity of intraocular fluid from pattents with proliferative retinopathies.Invest Ophthalmol Vis Sci,1991,32∶ 879
, http://www.100md.com
8.Wang AM,templeton DM.Inhibition of mitogenesis and c-fos induction in mesangial cells by heparin and heparan sulfates.Kidney International,1996,49∶ 437
9.Castllot JJ.Effect of heparin on Vascular smooth muscle cells:I.Cell metabolism.J Cell Physiol,1985,124∶ 21
收稿:1999-09-03
修回:2000-04-08, 百拇医药