抗病毒药物抑制转基因小鼠中HBV的复制
作者:张萍萍 万大方 顾健人 李劲松 徐少甫 成勇 成国祥
单位:张萍萍 万大方 顾健人 上海市肿瘤研究所癌基因及相关基因国家重点实验室 (上海 200032);李劲松 徐少甫 成勇 成国祥 扬州大学农学院哺乳动物胚胎工程和遗传工程实验室
关键词:小鼠,转基因;药物;病毒
肿瘤990612 中图分类号:R73-362 文章标识码:A 文章编号:1000-7431(1999)06-0356-02
乙型肝炎(HBV)是严重危害人类健康的传染病,在感染了HBV的人群中,原发性肝癌的发病率比非感染人群高200倍[1]。因此研制特异的抗HBV药物十分重要。然而HBV病毒具有极窄的宿主范围,它仅在人和黑猩猩中感染和复制[2]。Ueda首用细胞系(HB611)感染土拨鼠和鸭作为用于抗HBV理性化合物试验的模型[4~6]。尽管上述模型可以利用,但管理有困难,可产生异源性遗传,结果不能肯定是否适用于人。
, http://www.100md.com
最近几年很多实验室建立了HBV转基因小鼠模型,用以抗病毒药物的筛选以及用以肝炎与肝癌致病机理的研究[5~7]。作者用小鼠α-干扰素、临床使用的戊环乌苷及青霉素处理HBV转基因小鼠,观察他们对HBV DNA复制的影响。
材料与方法
一、动物来源及试剂:
1.动物 复制型HBV(adr)ICR品系转基因小鼠,G4代仔鼠4周龄由扬州大学农学院生物技术研究所,哺乳动物胚胎工程和遗传工程实验室提供。
2.试剂 α-干扰素(murine重组)简称mIFN-α,Zouirax I.V Bam HI及缓冲液试剂购自Life Tecknologies Inc。人用青霉素购自上海先锋药业公司,Taq酶购自上海生工公司。
二、方法
, http://www.100md.com
1.用药实验 复制型HBV(adr)转基因小鼠G4代16只仔鼠1月龄,分成4组用药,mIFN-α组3只小鼠,腹腔内注射mIFN-α每次20单位,每天2次。戊环鸟苷组4只小鼠,每次剂量按0.05 mg/g体重,每天2次。青霉素组6只小鼠,每次按5万单位/g体重,每天2次,另用2只小鼠同步进行注射生理盐水作对照组。以上小鼠均连续注射药物3天。
2.采样 用药后第4天,第9天,第14天分别对以上小鼠进行眼球取血、离心取上层血清,-20℃保存待用。
3.血清处理 20 μl血清加入1 μl BamH I 10 U/μl,1μl缓冲液,37℃温育1 h,再加20 μl血清处理液(1.0 mol KCl,0.5 mol pH 8.3,0.1 mol MgCl2,0.45% NP40,0.45% Tween 20,10 g/L蛋白酶K)55℃温育30 min,90℃ 10 min,离心取上清液作为待测DNA样品。
, http://www.100md.com
4.PCR检测
引物为HBV-C区正向引物:5’CTGTAGGCATAAATTGGTCT3’反向引物为5’AGGGAGTTCTTCTTCTAGGG3’,片段为590 bp。5 μl血清处理样品用于PCR,缓冲液(10 mmol Tris-HCl pH 8.3,50 mmol KCl,1.5 mmol MgCl2,0.01%明胶,80 μmol dNTP,5’和3’各引物为5 mol。2.5单位Taq),总体积25 μl,样品放置在PE公司循环仪上94℃ 45 s,56℃ 45 s,72℃ 1 min,35个循环,72℃ 10 min,样品在4℃中结束反应,样品进行1%琼脂糖凝胶电泳检测,结果见附图。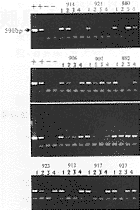
附图:1%琼脂糖凝胶电泳检测图谱
+用生理盐水注射HBV转基因小鼠883.888
, 百拇医药
-正常小鼠
其它实验动物编号及分组见附表内
1.用药前HBV转基因小鼠血样。
2.用药后,第4天采血
3.用药后,第9天采血
4.用药后,第14天采血
结果
mIFN-α组每只小鼠共用mIFN-α 120万单位,可以特异地抑制小鼠体内HBV的合成,其中921,880小鼠第4天HBV DNA复制全部受到抑制,第9天又开始不同程度HBV复制,914只小鼠在第4天还存在HBV DNA复制,但随着时间的延长,第9天,第14天都未能检测到HBV DNA。戊环鸟苷和青霉素只是部分抑制HBV合成,随后全部出现HBV DNA合成上升。对照组HBV DNA复制持续出现(见附表)。
, 百拇医药
附表 药物实验检测结果 药
动物编号
采 血 时 间
第4天
第9天
第14天
mIFN-α
914
+
-
-
921
-
, 百拇医药
-
+
880
-
+
+
青霉素
906
+
+
+
907
+
+
, 百拇医药
+
892
+
±
+
893
+
+
+
894
+
-
+
895
, 百拇医药
+
+
+
戊环乌苷
923
+
+
+
912
-
+
+
917
+
, 百拇医药
-
+
927
-
+
+
生理盐水
883
+
+
+
888
+
+
, http://www.100md.com
+
正常小鼠
-
-
-
正常小鼠
-
-
-
讨论
复制型HBV(adr)转基因小鼠是含HBV全基因组的转基因模型,Southern鉴定及电镜证明这些动物血清(母代)含有病毒(Dane)颗粒,但Dane颗粒的量是非常低的[8]。HBV Dane颗粒基因组是单链仅有一个BamH I位点,它不能被BamH I降解。为了排除淋巴细胞污染整合病毒基因组的扩增。实验血清首先用BamH I降解,然后再检测,为减少实验中的误差,所有的实验样品同步进行检测。
, 百拇医药
作者用mIFN-α能引起腺苷多聚酶干扰病毒HBsAg蛋白特异地抑制HBV的合成。停药后第9天,2只小鼠不同程度可测到HBV DNA,说明必须连续用药才能有效地阻止HBV的合成。用戊环鸟苷和常用青霉素药,参照美国医学实验动物剂量用于HBV转基因小鼠,随着时间延长HBV DNA连续地出现在循环血中。从全部的实验鼠结果看,小鼠用mIFN-α药3天后,HBV的复制被抑制,存在血液中Dane颗粒可能以HBsAg和HBeAg形式保留在血清中,这显示出Dane颗粒在血流中的存在期是很短的。
同时作者观察到小鼠存在个体差异,这可能与个体药物的受体量及免疫系统相关。作者的结果和国外的报道一致[4]。小鼠容易管理,采血和饲养,可做大量的药物实验。该转基因动物模型是用人HBV整合入小鼠的染色体中,小鼠与人都具有哺乳类动物的特征,模型的后代能继续复制、组装并分泌HBV病毒颗粒,这样该模型可以有效地评价新的抗HBV制剂。
作者简介:张萍萍,女,大专,副研究员。
, http://www.100md.com
参考文献
[1]Maynard JE,Deloia,Elawady, et al. Control of hepatitis B by immunization〔C〕. New York:Alan R Liss Inc.1988:967
[2]Tiollais P,Pourcel C,JD,et al. The Hepatitis B virus〔J〕. Nature,1985,317:489
[3]Ueda K, Taks C,Tsurimoto et al. An in vitro system for screening anti-hepatitis B virus drugs〔J〕. Virology,1989,169:213
[4]Hirota K,Julie B,Moustafa K, et al. Effects of oderine arabinoside on serum and intrahepatic replication forms of duck hepatitis B virus in chronic infections〔J〕. Hepatology,1987,7:24
, 百拇医药
[5]Lee B,Luo WS,Robert J, et al. In vitro and in vivo comparison of the abilities of purine and pyrimidine 2′3′-dideoxynuclosides to inhibit duck hepatovirus〔J〕. Antimicrob Agents chemocher 1989,33:336
[6]Tsiquaye KN,Collins P,Framcis V, et al. Antiviral activity of the polybasic anion,suramin and acyclovir in hepadnavirus infection〔J〕. J Antimierob Chemother,1986,18:223
[7]Cavnaugh VJ,Guidotti LG,Chisari FV, et al. Interleukin-12 inhibits hepatits B virus replication in transgenic mice. J Virol,1997,71:4,3236
, 百拇医药
[8]杨静莹,马积庆,万大方,等.复制型HVB(adr)转基因小鼠血清中Dane氏颗粒的免疫电镜检测〔J〕.肿瘤,1996,16(2):87
[9]Takemitsu Nagahata,Kimi Araki,Kenichi Yamamura,et al. Inhibition of intrahepatic hepatits B virus replication by antiviral drugs in a novel transgenic mouse model,Antimicrob Agents Chemother,1992,2042
(收稿日期:1997-10-06 修回日期:1999-06-10), 百拇医药
单位:张萍萍 万大方 顾健人 上海市肿瘤研究所癌基因及相关基因国家重点实验室 (上海 200032);李劲松 徐少甫 成勇 成国祥 扬州大学农学院哺乳动物胚胎工程和遗传工程实验室
关键词:小鼠,转基因;药物;病毒
肿瘤990612 中图分类号:R73-362 文章标识码:A 文章编号:1000-7431(1999)06-0356-02
乙型肝炎(HBV)是严重危害人类健康的传染病,在感染了HBV的人群中,原发性肝癌的发病率比非感染人群高200倍[1]。因此研制特异的抗HBV药物十分重要。然而HBV病毒具有极窄的宿主范围,它仅在人和黑猩猩中感染和复制[2]。Ueda首用细胞系(HB611)感染土拨鼠和鸭作为用于抗HBV理性化合物试验的模型[4~6]。尽管上述模型可以利用,但管理有困难,可产生异源性遗传,结果不能肯定是否适用于人。
, http://www.100md.com
最近几年很多实验室建立了HBV转基因小鼠模型,用以抗病毒药物的筛选以及用以肝炎与肝癌致病机理的研究[5~7]。作者用小鼠α-干扰素、临床使用的戊环乌苷及青霉素处理HBV转基因小鼠,观察他们对HBV DNA复制的影响。
材料与方法
一、动物来源及试剂:
1.动物 复制型HBV(adr)ICR品系转基因小鼠,G4代仔鼠4周龄由扬州大学农学院生物技术研究所,哺乳动物胚胎工程和遗传工程实验室提供。
2.试剂 α-干扰素(murine重组)简称mIFN-α,Zouirax I.V Bam HI及缓冲液试剂购自Life Tecknologies Inc。人用青霉素购自上海先锋药业公司,Taq酶购自上海生工公司。
二、方法
, http://www.100md.com
1.用药实验 复制型HBV(adr)转基因小鼠G4代16只仔鼠1月龄,分成4组用药,mIFN-α组3只小鼠,腹腔内注射mIFN-α每次20单位,每天2次。戊环鸟苷组4只小鼠,每次剂量按0.05 mg/g体重,每天2次。青霉素组6只小鼠,每次按5万单位/g体重,每天2次,另用2只小鼠同步进行注射生理盐水作对照组。以上小鼠均连续注射药物3天。
2.采样 用药后第4天,第9天,第14天分别对以上小鼠进行眼球取血、离心取上层血清,-20℃保存待用。
3.血清处理 20 μl血清加入1 μl BamH I 10 U/μl,1μl缓冲液,37℃温育1 h,再加20 μl血清处理液(1.0 mol KCl,0.5 mol pH 8.3,0.1 mol MgCl2,0.45% NP40,0.45% Tween 20,10 g/L蛋白酶K)55℃温育30 min,90℃ 10 min,离心取上清液作为待测DNA样品。
, http://www.100md.com
4.PCR检测
引物为HBV-C区正向引物:5’CTGTAGGCATAAATTGGTCT3’反向引物为5’AGGGAGTTCTTCTTCTAGGG3’,片段为590 bp。5 μl血清处理样品用于PCR,缓冲液(10 mmol Tris-HCl pH 8.3,50 mmol KCl,1.5 mmol MgCl2,0.01%明胶,80 μmol dNTP,5’和3’各引物为5 mol。2.5单位Taq),总体积25 μl,样品放置在PE公司循环仪上94℃ 45 s,56℃ 45 s,72℃ 1 min,35个循环,72℃ 10 min,样品在4℃中结束反应,样品进行1%琼脂糖凝胶电泳检测,结果见附图。

附图:1%琼脂糖凝胶电泳检测图谱
+用生理盐水注射HBV转基因小鼠883.888
, 百拇医药
-正常小鼠
其它实验动物编号及分组见附表内
1.用药前HBV转基因小鼠血样。
2.用药后,第4天采血
3.用药后,第9天采血
4.用药后,第14天采血
结果
mIFN-α组每只小鼠共用mIFN-α 120万单位,可以特异地抑制小鼠体内HBV的合成,其中921,880小鼠第4天HBV DNA复制全部受到抑制,第9天又开始不同程度HBV复制,914只小鼠在第4天还存在HBV DNA复制,但随着时间的延长,第9天,第14天都未能检测到HBV DNA。戊环鸟苷和青霉素只是部分抑制HBV合成,随后全部出现HBV DNA合成上升。对照组HBV DNA复制持续出现(见附表)。
, 百拇医药
附表 药物实验检测结果 药
动物编号
采 血 时 间
第4天
第9天
第14天
mIFN-α
914
+
-
-
921
-
, 百拇医药
-
+
880
-
+
+
青霉素
906
+
+
+
907
+
+
, 百拇医药
+
892
+
±
+
893
+
+
+
894
+
-
+
895
, 百拇医药
+
+
+
戊环乌苷
923
+
+
+
912
-
+
+
917
+
, 百拇医药
-
+
927
-
+
+
生理盐水
883
+
+
+
888
+
+
, http://www.100md.com
+
正常小鼠
-
-
-
正常小鼠
-
-
-
讨论
复制型HBV(adr)转基因小鼠是含HBV全基因组的转基因模型,Southern鉴定及电镜证明这些动物血清(母代)含有病毒(Dane)颗粒,但Dane颗粒的量是非常低的[8]。HBV Dane颗粒基因组是单链仅有一个BamH I位点,它不能被BamH I降解。为了排除淋巴细胞污染整合病毒基因组的扩增。实验血清首先用BamH I降解,然后再检测,为减少实验中的误差,所有的实验样品同步进行检测。
, 百拇医药
作者用mIFN-α能引起腺苷多聚酶干扰病毒HBsAg蛋白特异地抑制HBV的合成。停药后第9天,2只小鼠不同程度可测到HBV DNA,说明必须连续用药才能有效地阻止HBV的合成。用戊环鸟苷和常用青霉素药,参照美国医学实验动物剂量用于HBV转基因小鼠,随着时间延长HBV DNA连续地出现在循环血中。从全部的实验鼠结果看,小鼠用mIFN-α药3天后,HBV的复制被抑制,存在血液中Dane颗粒可能以HBsAg和HBeAg形式保留在血清中,这显示出Dane颗粒在血流中的存在期是很短的。
同时作者观察到小鼠存在个体差异,这可能与个体药物的受体量及免疫系统相关。作者的结果和国外的报道一致[4]。小鼠容易管理,采血和饲养,可做大量的药物实验。该转基因动物模型是用人HBV整合入小鼠的染色体中,小鼠与人都具有哺乳类动物的特征,模型的后代能继续复制、组装并分泌HBV病毒颗粒,这样该模型可以有效地评价新的抗HBV制剂。
作者简介:张萍萍,女,大专,副研究员。
, http://www.100md.com
参考文献
[1]Maynard JE,Deloia,Elawady, et al. Control of hepatitis B by immunization〔C〕. New York:Alan R Liss Inc.1988:967
[2]Tiollais P,Pourcel C,JD,et al. The Hepatitis B virus〔J〕. Nature,1985,317:489
[3]Ueda K, Taks C,Tsurimoto et al. An in vitro system for screening anti-hepatitis B virus drugs〔J〕. Virology,1989,169:213
[4]Hirota K,Julie B,Moustafa K, et al. Effects of oderine arabinoside on serum and intrahepatic replication forms of duck hepatitis B virus in chronic infections〔J〕. Hepatology,1987,7:24
, 百拇医药
[5]Lee B,Luo WS,Robert J, et al. In vitro and in vivo comparison of the abilities of purine and pyrimidine 2′3′-dideoxynuclosides to inhibit duck hepatovirus〔J〕. Antimicrob Agents chemocher 1989,33:336
[6]Tsiquaye KN,Collins P,Framcis V, et al. Antiviral activity of the polybasic anion,suramin and acyclovir in hepadnavirus infection〔J〕. J Antimierob Chemother,1986,18:223
[7]Cavnaugh VJ,Guidotti LG,Chisari FV, et al. Interleukin-12 inhibits hepatits B virus replication in transgenic mice. J Virol,1997,71:4,3236
, 百拇医药
[8]杨静莹,马积庆,万大方,等.复制型HVB(adr)转基因小鼠血清中Dane氏颗粒的免疫电镜检测〔J〕.肿瘤,1996,16(2):87
[9]Takemitsu Nagahata,Kimi Araki,Kenichi Yamamura,et al. Inhibition of intrahepatic hepatits B virus replication by antiviral drugs in a novel transgenic mouse model,Antimicrob Agents Chemother,1992,2042
(收稿日期:1997-10-06 修回日期:1999-06-10), 百拇医药