聚乳酸膜管复合钙磷陶瓷引导性骨再生的实验研究
作者:于雷 靳安民
单位:第一军医大学珠江医院脊柱外科 510282 广州市
关键词:骨缺损;聚乳酸;磷酸三钙陶瓷;膜引导性骨再生
中国临床解剖学杂志000128摘 要:目的:采用可降解的生物活性材料钙磷陶瓷人工骨置于膜管内、骨断端间。观察其引导性骨再生的效果,探讨机理。方法:选用新西兰成年大白兔30只,平均体重2.5 kg。按体重分成5组,每组6只,以双前肢为对象。采用标准的骨缺损模型,12个对象随机分到M+TCP处理,对侧为对照侧。术后1、3、6、9、12周进行大体、组织和影像学观察分析。结果:处理组随时间全部动物骨缺损处有连续性骨痂通过缺损处。钙磷陶瓷逐渐吸收,组织相容性好。而对照组3周后两断端被增生的皮质骨封闭,未能形成有效连接。结论:引导性骨再生可有效地修复骨缺损,钙磷陶瓷的应用有利于骨缺损的修复。
Experimental study of polylactic acid (PLA) membrane plus tricalcium phosphate(TCP)
, http://www.100md.com
Yu Lei Jin Anmin
(Department of Spinal Surgery,Zhujiang Hospital,The First Military Medical University,Guangzhou 510282)
Abstract:Objective:To observe the result and explore the mechanism of guided bone regeneration with polylactic acid membrane plus tricalcium phosphate ceramics.Methods:Thirty New Zealand adult rabbits weighting 2.5kg were evenly divided into five groups.Standard 10 mm bone defects were created in both radii of each rabbit.Randomly one defect was enveloped with PLA membrane wrapped as a tube plus TCP ceramics in it,the contralateral defect served as an untreated control.General observation,histological and radiological studies were made at 1,3,6,9,12 week postoperatively.Results:The experinental sides consistently healed with callus extended over the gaps in the membranes.The control sides showed nonunion,the bone ends were rounded off and sealed with cortical bone.Both the membrane and the ceramics showed good histocompatibility and degenerated with time.Conclusion:Guided bone regeneration is an effective method in healing bone defects,and synergic results could be achieved when combined with ceramics.
, http://www.100md.com
Key words:Bone defect Polylactic acid Tricalcium phosphate ceramics Membrane guided bone regeneration▲
由于各种原因所致的骨缺损,常常是临床上棘手的问题。引导性骨再生应用隔膜为骨再生创造良好的局部环境,在口腔科已得到应用[1],在长管状骨缺损修复方面也进行了探索,取得一定的效果[2],本实验将膜管与钙磷陶瓷合用,观察修复效果,探讨机理和临床应用的可能性。
1 材料和方法
1.1 材料选用 ①聚乳酸(PLA TUBE) 广州中山大学高分子研究所提供,平均分子量120 000道尔顿(D);②TCP 将磷酸三钙粉末与双氧水按1∶1混合均匀,置于长方形金属模具中,于干燥箱中过夜,再于高温电炉中加热至1000℃ 10h,制成蜂窝状均一的多孔磷酸三钙陶瓷[3]。硬度为5/103 psi,孔隙率:30%,大小为200 μm(图1)。
, http://www.100md.com
图1 实验所用的生物资料(上为聚乳酸膜管,下为磷酸三钙陶瓷)
1.2 动物分组及手术 选用新西兰成年大白兔30只,平均体重2.5 kg。按体重分成5组,每组6只,以双前肢为对象。随机给予一侧聚乳酸膜+TCP处理,另一侧为对照。2%戊巴比妥钠30~40mg/kg右耳缘静脉注射麻醉。前肢剃毛,于前臂前区沿桡尺骨间隙切开皮肤,钝性分离皮下组织、肌肉,止血。避免损伤大血管、神经和肌腱,充分暴露桡骨中段,用手术刀切开骨间筋膜,在桡尺骨间插入消毒后的金属片,保护尺骨用消毒钢尺测量桡骨截除长度,做好标记后,用线锯截除。残存桡骨两游离端各去除长3 mm骨膜,按实验设计给予不同的处理,逐层缝合关闭切口。包扎,不需外固定,因完整尺骨可以起到固定作用。术后3d,每日肌注青霉素80万单位。
1.3 观察方法 术后1、3、6、9、12周处死动物,截取桡骨中段2cm进行大体、组织学HE染色、X线影像学分析。
, http://www.100md.com 2 结果
2.1 大体观察
2.1.1 实验组 膜及膜外的结缔组织,1周时膜管外结缔组织大量增生,与膜相临处形成一筋膜,将膜与膜外结缔组织分开,未见结缔组织长入膜内。膜随着时间降解,但仍然保持外形完好。9、12周时见到膜表面有斑点状小孔,为膜降解(腐蚀)所致。管腔内新生组织,早期为骨断端血肿机化物,钙磷陶瓷的网孔内充满新生肉芽组织,随时间推移逐渐被新生骨组织所填充,新生骨组织依膜管形状而附形,成圆柱状,不长入膜内,与膜较易分离。3、6周时钙磷陶瓷与骨断端之间的间隙模糊,可抵抗轻手力的弯曲。
2.1.2 对照组 结缔组织早期长入两断端间,轻微晃动两断端无阻力感。未见随时间改变。
2.2 组织学观察
2.2.1 膜+TCP(实验)组 1周时膜管内保住了血肿,由于有了三维结构的钙磷陶瓷的存在,血肿细胞布于陶瓷的网孔内,在纵面上的切片上表现为规则的网状,断端与膜管交接处,骨外膜生发层细胞沿膜管内层增生,在断端形成帽状包裹,两端相似,帽的尖端相对,细胞核深染,帽之间为尚未机化的血肿,随着再生过程的向中间推进,逐渐机化,骨化。3、6、9、12周时,以陶瓷骨架为依托,形成多个骨化中心,骨小梁、骨岛遍布于膜管内及两断端间。两断端间骨膜沿膜管内层爬行会合。1周时骨髓即出现,至9周新生骨间充满红骨髓,12周可见成熟脂肪骨髓。膜管外的新生骨在交接处表现为软骨内骨化,形成肥大骨痂,但未能连接两断端(图2,3)。
, 百拇医药
图2 6周时,M+TCP组,骨膜在膜管内增生会合,断端间,骨痂量多,骨小梁成熟度高 HE×200
图3 9周时,M+TCP组,骨髓增生明显,脂肪增多,骨痂成熟 HE×100
2.2.2 对照组 早期两断端的空隙即被周围肌肉等结缔组织充填,纤维组织大量增生,可见成纤维细胞,纤维母细胞,小毛细血管,断端皮质坏死,结构紊乱,随后骨外膜,骨内膜中成骨活性细胞分化,在断端以软骨内骨化形式形成新生骨质,封闭断端,但不能贯通两端(图4)。
图4 对照组,断端闭合,髓腔封闭 HE×100
2.3 X线结果
, 百拇医药
2.3.1 膜+TCP(实验)组 1周时骨断端皮质密度减低,陶瓷与断端间隙清楚可见。3周膜管内见放射性致密物痕迹,6周断端皮质模糊,陶瓷与断端间隙不清。9周陶瓷密度降低表现为蜂窝状,膜下有薄层皮质骨连接两段端。12周膜内骨痂增生明显,陶瓷继续降解为混合密度,长度变短,只是原来的2/3。骨断端皮质模糊,骨髓腔未见再通。膜管开始不可见,随着膜内层骨化进行,可见与膜管外形一致的新生骨(图5,6)。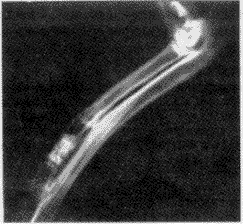
5 9周时,陶瓷降解为蜂窝状,膜下有薄层骨痂连接两断端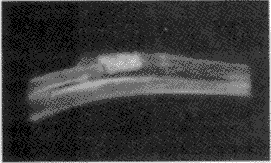
图6 12周时,M+TCP组,膜内骨痂增生明显,陶瓷继续降解为混合密度,长度变短,只是原来的2/3,骨断端皮质模糊
2.3.2 对照组 1、3周时对照组断端间表现为透光区,见到薄骨痂覆盖断端,在膜外延伸2 mm,6、9周时骨端变圆,为皮质骨封闭(图7)。
, 百拇医药
图7 6周时,骨断端变圆,髓腔封闭,形成类似假关节结构
3 讨论
3.1 引导性骨再生膜材料的研究
引导性骨再生是通过膜来实现的,注重对膜材料的开发是研究的中心课题。初期应用的膜主要是不可降解的,如硅酮膜、醋酸纤维素膜、聚四氟乙烯膜[4]、微孔滤膜[5]。按照引导性骨再生概念的要求,当膜片的作用结束以后,应当消失。但非降解膜造价昂贵必须经再手术取出,如果这种膜留在原位,会产生细菌感染等并发症,这些弊端导致了对可降解膜材料的研究[6]。可降解膜材料的研究应注意以下几点:可降解膜材料必须满足GTR对膜的要求;必须保持膜降解时间与组织愈合时间的平衡;降解产物不会引起机体内的不良反应。如何调控好降解膜在体内降解时间并适应各种类型的缺损,是可降解膜材料研究的焦点。各种可降解膜材料在体内降解速度不一:PLA降解时间为3~4月,多聚乳酸多聚乙酸共聚物(PLA/PGA)为4~8周,胶原膜为2~6周。
, 百拇医药
多聚乳酸膜材料的基本组成单位为PLA,其降解速度可由改变其分子量、组成成分、表面积或制成多孔等方式达到。这类可吸收材料应用于GTR,时已取得了满意的临床治疗效果。本实验采用的膜平均分子量为120 000D。经过3个月的实验,膜具有良好的生物相容性,到实验结束时,膜依然完整,保持外形无塌陷,符合GBR的要求。
3.2 磷酸三钙陶瓷简介
磷酸三钙陶瓷人工骨,多孔陶瓷能起到良好的支架作用,引导宿主床新骨长入材料内部,发挥骨传导作用。多孔陶瓷的孔径一般在100~500 μm之间,才能使新生骨有效地长入材料孔内。经烧结作用,在多孔型陶瓷材料的细小颗粒之间可留下许多称为微孔,构成一种大孔/微孔结构,使材料与组织和组织液的接触面积增加。钙磷陶瓷人工骨力学强度不如金属材料、性脆、抗压和抗折强度较低。多孔型钙磷陶瓷的强度与松质骨相似,其抗压和抗折强度分别为1~10/103 psi和0.36/103 psi(正常松质骨分别为6~9/103 psi和0.5/103 psi)。TCP陶瓷具有良好的生物相容性、生物降解性;材料能与骨组织直接结合在一起。钙磷陶瓷在机体内的生物降解有两条途径:液体介导过程和细胞介导过程。钙磷陶瓷生物降解后释放出钙磷离子,它们参与局部骨组织的钙化和进入机体的钙磷库,以正常的方式被利用或排除,而不会使机体主要脏器发生组织学改变或病理性钙化。
, 百拇医药
临床上已开始应用钙磷陶瓷修复骨缺损并取得了满意的修复效果。近年来,开始研究将具有骨诱导能力的或成骨作用的材料或成分与钙磷陶瓷结合,以加强钙磷陶瓷修复骨缺损的作用。
3.3 引导性骨再生的机理
其机理目前还不清楚,在本实验中促进骨缺损修复的机理可能是:①膜的物理屏障作用 术后1周对照组两断端间和实验组的膜外见到大量致密的纤维结缔组织增生,随着时间的进展,对照组和实验组均出现成骨反应,但对照组并不能形成贯通性连接,以纤维瘢痕告终。而实验组在9、12周的时候出现连续性骨痂贯通两断端。12周时,所有动物实验现骨性愈合。由此可见膜管的放置起到了阻止纤维组织的作用,在实验组,无一例有纤维组织长入膜内或两断端间。②骨引导、骨传导作用 已经证明,不依赖于刺激细胞活性,正常的成骨细胞和成骨细胞样细胞即具有在适合表面形成新骨的能力。本实验中膜和陶瓷提供细胞附着生长分化增殖表面,细胞附着其表面上。陶瓷由于多孔的结构更增加了表面积,使更多的细胞得以生长,这与组织学观察到的断端间多个骨岛同时存在相一致。③膜下间隙的重要性[3] 有作者认为由于膜的降解塌陷减少了膜下间隙也减少了成骨量,为了维持膜下间隙,有的用自体骨,有的用同种异体骨。钙磷陶瓷的应用也有这样的效果,在本实验的全过程中,未见到膜管的塌陷,说明膜管本身有足够的强度维持骨再生的空间,另钙磷陶瓷应用起到很好的辅助作用。■
, 百拇医药
参考文献:
[1]Gottlow J,Nyman S,Karring T,et al.New attachment formation as the result of controlledtissue regeneration.J Clin Periodontol,1984,11(8):494
[2]倪 斌,侯春林,贾连顺,等.几丁质膜引导兔桡骨缺损再生的实验研究.中华骨科杂志,1995,15(9):607
[3]Renooij W,Janssen WM,Akkermans LM,et al.Bioresorption of ceramic strontium-85 labelled calcium phosphate implants in dog femora.A pilot study to quantitate bioresorption of ceramic implants of hydroxyapatite and triclcium orthophosphate in vivo.Clin Orthop,1985,197:272
, http://www.100md.com
[4]Dahlin C,Gottlow,J,Lindhe A et al.Healing of maxillary and mandibular bone defects using a membrane technique.Scand J Plast Reconstr Hand Surg,1990,24:13
[5]Greaves P,Martin J M.Malignant fibrous histicytoma in rats at sites of implanted Millipore filters.Am J Pathol,1985,120:207
[6]Minabe M.A critical review of the biologic rationale for guided tissue regeneration.J Periodontol,1991,62:171
收稿日期:1999-07-10, 百拇医药
单位:第一军医大学珠江医院脊柱外科 510282 广州市
关键词:骨缺损;聚乳酸;磷酸三钙陶瓷;膜引导性骨再生
中国临床解剖学杂志000128摘 要:目的:采用可降解的生物活性材料钙磷陶瓷人工骨置于膜管内、骨断端间。观察其引导性骨再生的效果,探讨机理。方法:选用新西兰成年大白兔30只,平均体重2.5 kg。按体重分成5组,每组6只,以双前肢为对象。采用标准的骨缺损模型,12个对象随机分到M+TCP处理,对侧为对照侧。术后1、3、6、9、12周进行大体、组织和影像学观察分析。结果:处理组随时间全部动物骨缺损处有连续性骨痂通过缺损处。钙磷陶瓷逐渐吸收,组织相容性好。而对照组3周后两断端被增生的皮质骨封闭,未能形成有效连接。结论:引导性骨再生可有效地修复骨缺损,钙磷陶瓷的应用有利于骨缺损的修复。
Experimental study of polylactic acid (PLA) membrane plus tricalcium phosphate(TCP)
, http://www.100md.com
Yu Lei Jin Anmin
(Department of Spinal Surgery,Zhujiang Hospital,The First Military Medical University,Guangzhou 510282)
Abstract:Objective:To observe the result and explore the mechanism of guided bone regeneration with polylactic acid membrane plus tricalcium phosphate ceramics.Methods:Thirty New Zealand adult rabbits weighting 2.5kg were evenly divided into five groups.Standard 10 mm bone defects were created in both radii of each rabbit.Randomly one defect was enveloped with PLA membrane wrapped as a tube plus TCP ceramics in it,the contralateral defect served as an untreated control.General observation,histological and radiological studies were made at 1,3,6,9,12 week postoperatively.Results:The experinental sides consistently healed with callus extended over the gaps in the membranes.The control sides showed nonunion,the bone ends were rounded off and sealed with cortical bone.Both the membrane and the ceramics showed good histocompatibility and degenerated with time.Conclusion:Guided bone regeneration is an effective method in healing bone defects,and synergic results could be achieved when combined with ceramics.
, http://www.100md.com
Key words:Bone defect Polylactic acid Tricalcium phosphate ceramics Membrane guided bone regeneration▲
由于各种原因所致的骨缺损,常常是临床上棘手的问题。引导性骨再生应用隔膜为骨再生创造良好的局部环境,在口腔科已得到应用[1],在长管状骨缺损修复方面也进行了探索,取得一定的效果[2],本实验将膜管与钙磷陶瓷合用,观察修复效果,探讨机理和临床应用的可能性。
1 材料和方法
1.1 材料选用 ①聚乳酸(PLA TUBE) 广州中山大学高分子研究所提供,平均分子量120 000道尔顿(D);②TCP 将磷酸三钙粉末与双氧水按1∶1混合均匀,置于长方形金属模具中,于干燥箱中过夜,再于高温电炉中加热至1000℃ 10h,制成蜂窝状均一的多孔磷酸三钙陶瓷[3]。硬度为5/103 psi,孔隙率:30%,大小为200 μm(图1)。

, http://www.100md.com
图1 实验所用的生物资料(上为聚乳酸膜管,下为磷酸三钙陶瓷)
1.2 动物分组及手术 选用新西兰成年大白兔30只,平均体重2.5 kg。按体重分成5组,每组6只,以双前肢为对象。随机给予一侧聚乳酸膜+TCP处理,另一侧为对照。2%戊巴比妥钠30~40mg/kg右耳缘静脉注射麻醉。前肢剃毛,于前臂前区沿桡尺骨间隙切开皮肤,钝性分离皮下组织、肌肉,止血。避免损伤大血管、神经和肌腱,充分暴露桡骨中段,用手术刀切开骨间筋膜,在桡尺骨间插入消毒后的金属片,保护尺骨用消毒钢尺测量桡骨截除长度,做好标记后,用线锯截除。残存桡骨两游离端各去除长3 mm骨膜,按实验设计给予不同的处理,逐层缝合关闭切口。包扎,不需外固定,因完整尺骨可以起到固定作用。术后3d,每日肌注青霉素80万单位。
1.3 观察方法 术后1、3、6、9、12周处死动物,截取桡骨中段2cm进行大体、组织学HE染色、X线影像学分析。
, http://www.100md.com 2 结果
2.1 大体观察
2.1.1 实验组 膜及膜外的结缔组织,1周时膜管外结缔组织大量增生,与膜相临处形成一筋膜,将膜与膜外结缔组织分开,未见结缔组织长入膜内。膜随着时间降解,但仍然保持外形完好。9、12周时见到膜表面有斑点状小孔,为膜降解(腐蚀)所致。管腔内新生组织,早期为骨断端血肿机化物,钙磷陶瓷的网孔内充满新生肉芽组织,随时间推移逐渐被新生骨组织所填充,新生骨组织依膜管形状而附形,成圆柱状,不长入膜内,与膜较易分离。3、6周时钙磷陶瓷与骨断端之间的间隙模糊,可抵抗轻手力的弯曲。
2.1.2 对照组 结缔组织早期长入两断端间,轻微晃动两断端无阻力感。未见随时间改变。
2.2 组织学观察
2.2.1 膜+TCP(实验)组 1周时膜管内保住了血肿,由于有了三维结构的钙磷陶瓷的存在,血肿细胞布于陶瓷的网孔内,在纵面上的切片上表现为规则的网状,断端与膜管交接处,骨外膜生发层细胞沿膜管内层增生,在断端形成帽状包裹,两端相似,帽的尖端相对,细胞核深染,帽之间为尚未机化的血肿,随着再生过程的向中间推进,逐渐机化,骨化。3、6、9、12周时,以陶瓷骨架为依托,形成多个骨化中心,骨小梁、骨岛遍布于膜管内及两断端间。两断端间骨膜沿膜管内层爬行会合。1周时骨髓即出现,至9周新生骨间充满红骨髓,12周可见成熟脂肪骨髓。膜管外的新生骨在交接处表现为软骨内骨化,形成肥大骨痂,但未能连接两断端(图2,3)。

, 百拇医药
图2 6周时,M+TCP组,骨膜在膜管内增生会合,断端间,骨痂量多,骨小梁成熟度高 HE×200

图3 9周时,M+TCP组,骨髓增生明显,脂肪增多,骨痂成熟 HE×100
2.2.2 对照组 早期两断端的空隙即被周围肌肉等结缔组织充填,纤维组织大量增生,可见成纤维细胞,纤维母细胞,小毛细血管,断端皮质坏死,结构紊乱,随后骨外膜,骨内膜中成骨活性细胞分化,在断端以软骨内骨化形式形成新生骨质,封闭断端,但不能贯通两端(图4)。

图4 对照组,断端闭合,髓腔封闭 HE×100
2.3 X线结果
, 百拇医药
2.3.1 膜+TCP(实验)组 1周时骨断端皮质密度减低,陶瓷与断端间隙清楚可见。3周膜管内见放射性致密物痕迹,6周断端皮质模糊,陶瓷与断端间隙不清。9周陶瓷密度降低表现为蜂窝状,膜下有薄层皮质骨连接两段端。12周膜内骨痂增生明显,陶瓷继续降解为混合密度,长度变短,只是原来的2/3。骨断端皮质模糊,骨髓腔未见再通。膜管开始不可见,随着膜内层骨化进行,可见与膜管外形一致的新生骨(图5,6)。

5 9周时,陶瓷降解为蜂窝状,膜下有薄层骨痂连接两断端

图6 12周时,M+TCP组,膜内骨痂增生明显,陶瓷继续降解为混合密度,长度变短,只是原来的2/3,骨断端皮质模糊
2.3.2 对照组 1、3周时对照组断端间表现为透光区,见到薄骨痂覆盖断端,在膜外延伸2 mm,6、9周时骨端变圆,为皮质骨封闭(图7)。

, 百拇医药
图7 6周时,骨断端变圆,髓腔封闭,形成类似假关节结构
3 讨论
3.1 引导性骨再生膜材料的研究
引导性骨再生是通过膜来实现的,注重对膜材料的开发是研究的中心课题。初期应用的膜主要是不可降解的,如硅酮膜、醋酸纤维素膜、聚四氟乙烯膜[4]、微孔滤膜[5]。按照引导性骨再生概念的要求,当膜片的作用结束以后,应当消失。但非降解膜造价昂贵必须经再手术取出,如果这种膜留在原位,会产生细菌感染等并发症,这些弊端导致了对可降解膜材料的研究[6]。可降解膜材料的研究应注意以下几点:可降解膜材料必须满足GTR对膜的要求;必须保持膜降解时间与组织愈合时间的平衡;降解产物不会引起机体内的不良反应。如何调控好降解膜在体内降解时间并适应各种类型的缺损,是可降解膜材料研究的焦点。各种可降解膜材料在体内降解速度不一:PLA降解时间为3~4月,多聚乳酸多聚乙酸共聚物(PLA/PGA)为4~8周,胶原膜为2~6周。
, 百拇医药
多聚乳酸膜材料的基本组成单位为PLA,其降解速度可由改变其分子量、组成成分、表面积或制成多孔等方式达到。这类可吸收材料应用于GTR,时已取得了满意的临床治疗效果。本实验采用的膜平均分子量为120 000D。经过3个月的实验,膜具有良好的生物相容性,到实验结束时,膜依然完整,保持外形无塌陷,符合GBR的要求。
3.2 磷酸三钙陶瓷简介
磷酸三钙陶瓷人工骨,多孔陶瓷能起到良好的支架作用,引导宿主床新骨长入材料内部,发挥骨传导作用。多孔陶瓷的孔径一般在100~500 μm之间,才能使新生骨有效地长入材料孔内。经烧结作用,在多孔型陶瓷材料的细小颗粒之间可留下许多称为微孔,构成一种大孔/微孔结构,使材料与组织和组织液的接触面积增加。钙磷陶瓷人工骨力学强度不如金属材料、性脆、抗压和抗折强度较低。多孔型钙磷陶瓷的强度与松质骨相似,其抗压和抗折强度分别为1~10/103 psi和0.36/103 psi(正常松质骨分别为6~9/103 psi和0.5/103 psi)。TCP陶瓷具有良好的生物相容性、生物降解性;材料能与骨组织直接结合在一起。钙磷陶瓷在机体内的生物降解有两条途径:液体介导过程和细胞介导过程。钙磷陶瓷生物降解后释放出钙磷离子,它们参与局部骨组织的钙化和进入机体的钙磷库,以正常的方式被利用或排除,而不会使机体主要脏器发生组织学改变或病理性钙化。
, 百拇医药
临床上已开始应用钙磷陶瓷修复骨缺损并取得了满意的修复效果。近年来,开始研究将具有骨诱导能力的或成骨作用的材料或成分与钙磷陶瓷结合,以加强钙磷陶瓷修复骨缺损的作用。
3.3 引导性骨再生的机理
其机理目前还不清楚,在本实验中促进骨缺损修复的机理可能是:①膜的物理屏障作用 术后1周对照组两断端间和实验组的膜外见到大量致密的纤维结缔组织增生,随着时间的进展,对照组和实验组均出现成骨反应,但对照组并不能形成贯通性连接,以纤维瘢痕告终。而实验组在9、12周的时候出现连续性骨痂贯通两断端。12周时,所有动物实验现骨性愈合。由此可见膜管的放置起到了阻止纤维组织的作用,在实验组,无一例有纤维组织长入膜内或两断端间。②骨引导、骨传导作用 已经证明,不依赖于刺激细胞活性,正常的成骨细胞和成骨细胞样细胞即具有在适合表面形成新骨的能力。本实验中膜和陶瓷提供细胞附着生长分化增殖表面,细胞附着其表面上。陶瓷由于多孔的结构更增加了表面积,使更多的细胞得以生长,这与组织学观察到的断端间多个骨岛同时存在相一致。③膜下间隙的重要性[3] 有作者认为由于膜的降解塌陷减少了膜下间隙也减少了成骨量,为了维持膜下间隙,有的用自体骨,有的用同种异体骨。钙磷陶瓷的应用也有这样的效果,在本实验的全过程中,未见到膜管的塌陷,说明膜管本身有足够的强度维持骨再生的空间,另钙磷陶瓷应用起到很好的辅助作用。■
, 百拇医药
参考文献:
[1]Gottlow J,Nyman S,Karring T,et al.New attachment formation as the result of controlledtissue regeneration.J Clin Periodontol,1984,11(8):494
[2]倪 斌,侯春林,贾连顺,等.几丁质膜引导兔桡骨缺损再生的实验研究.中华骨科杂志,1995,15(9):607
[3]Renooij W,Janssen WM,Akkermans LM,et al.Bioresorption of ceramic strontium-85 labelled calcium phosphate implants in dog femora.A pilot study to quantitate bioresorption of ceramic implants of hydroxyapatite and triclcium orthophosphate in vivo.Clin Orthop,1985,197:272
, http://www.100md.com
[4]Dahlin C,Gottlow,J,Lindhe A et al.Healing of maxillary and mandibular bone defects using a membrane technique.Scand J Plast Reconstr Hand Surg,1990,24:13
[5]Greaves P,Martin J M.Malignant fibrous histicytoma in rats at sites of implanted Millipore filters.Am J Pathol,1985,120:207
[6]Minabe M.A critical review of the biologic rationale for guided tissue regeneration.J Periodontol,1991,62:171
收稿日期:1999-07-10, 百拇医药