吡哆醇致大鼠睾丸毒性的体内外研究
http://www.100md.com
37c医学网
作者:黄厚今 王瑞淑 徐维光 杨青 张杰
单位:黄厚今 (563003 贵州省 遵义医学院预防医学教研室);王瑞淑 徐维光 杨青 (华西医科大学营养与食品卫生学教研室);张杰 (病理学教研室)
关键词:
吡哆醇致大鼠睾丸毒性的体内外研究 维生素B6是吡哆醇、吡哆醛和吡哆胺的合称。近年来,随着吡哆醇用作治疗、辅助治疗以及保健品成分不断增加,长期大量应用维生素B6的安全性已备受关注。本实验采用体内外方法,探讨吡哆醇对睾丸作用的特点。
一、材料与方法
1.实验动物及分组:SD雄性成年大鼠,体重200~250 g,由华西医科大学动物中心提供。喂养于12/12小时(昼/夜),温度约20℃的环境,常规饲养1周后,随机分为阴性对照组、阳性对照组(甘油组)和3个试验组,每组10只动物。细胞培养用20~25天龄SD幼鼠,体重40~50 g。
, 百拇医药
2.主要试剂:盐酸吡哆醇(C8H11O3N-HCl=205.64,生化试剂,含量99%,上海化学试剂采购供应站分装厂);甘油(生化试剂,天津市东方卫生材料厂);最低必需培养基(MEM,GibcoBRL, 美国);牛血清(华西医科大学分子生物学研究室);胰蛋白酶(1∶250, DIFCO, 美国);胶原酶(Sigma, 美国)。
3.实验方法:
(1)睾丸内注射:用双蒸水溶解吡哆醇-盐酸并配成10、100和200 mg/ml溶液,过滤除菌。大鼠经常规消毒阴囊皮肤,于睾丸中部进针,穿过白膜后推至睾丸中心注药。阴性对照用生理盐水,阳性对照用甘油。所有动物均注射单侧,对侧作对照,容量50 μl,1周后重复1次。至第15天处死动物取材,分别作性腺和副性腺测量及光镜、电镜检查。
(2)细胞分离培养:无菌取出睾丸,初步剪碎。加入0.25%胰蛋白酶,33℃下作用15分钟,中止酶作用后过滤。再经0.1%胶原酶在33℃下消化约15分钟,过滤。将细胞分散于5%小牛血清的MEM中,取少量做苔盼蓝排斥试验,要求蓝染细胞<3%。将细胞浓度调整到1.6×106/ml,每孔加1 ml培养24小时,观察细胞生长情况。
, http://www.100md.com
4.观察指标:
(1)睾丸内注射:实验期末测量双侧睾丸体积,称量性腺及副性腺。取左侧睾丸中心组织用于电镜检查。其余组织及右侧附睾、前列腺和精囊均作光镜检查。
(2)细胞培养:用不含胎牛血清的MEM将吡哆醇分别配制成0.1、1、10和20 mg/ml浓度。细胞经24小时贴壁后,加入含不同浓度吡哆醇的MEM,每组8个复孔,继续培养,于不同时点进行脱落细胞计数,并进行显著性检验。将支持细胞-生精细胞培养片和经低渗处理的支持细胞片进行Coomassie BB染色,观察吡哆醇对支持细胞骨架的作用。
二、结果
1.睾丸内注射吡哆醇对大鼠睾丸及副性腺的影响(表1、2):与对照组比较,10 mg组的睾丸及附睾重量减轻,而20 mg组的睾丸体积与重量,附睾、前列腺重量均减轻,与阳性对照组的变化一致。各剂量组精囊重量无明显变化。
, 百拇医药
表1 睾丸内注射吡哆醇对睾丸体积和重量的影响
(n=10,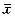 ±s)
±s)
剂量
(mg/睾丸)
睾丸体积(cm3)
睾丸重量(g)
左
右
左
右
, 百拇医药
0
1.836 6±
0.169 4
1.834 4±
0.167 8
1.334 8±
0.120 3
1.339 0±
0.123 5
1
1.898 8±
0.183 0
, 百拇医药
1.781 0±
0.238 0
1.301 4±
0.155 3
1.198 0±
0.225 3
10
1.888 4±
0.262 8
1.717 6±
0.282 0
1.349 4±
, 百拇医药
1.153 1
1.112 4±
0.160 0**
20
1.898 7±
0.249 3
1.367 1±
0.178 3**
1.316 0±
0.155 9
0.909 2±
0.132 3**
, 百拇医药
70%甘油
1.815 9±
0.341 9
1.118 1±
0.267 9**
1.203 3±
0.265 3
0.666 7±
0.145 8**
与对照组比较**P<0.01
表2 睾丸内注射吡哆醇对副性腺的影响(g,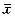 ±s)
±s)
, 百拇医药
剂量
(mg/睾丸)
附睾
前列腺
精囊
左
右
0
0.446 3±
0.069 8
0.464 7±
0.069 9
0.629 1±
, 百拇医药
0.115 3
1.071 7±
0.229 2
1
0.427 1±
0.047 7
0.430 1±
0.065 9
0.646 5±
0.156 5
0.995 1±
0.251 2
, http://www.100md.com
10
0.433 4±
0.038 6
0.395 9±
0.037 9*
0.566 1±
0.130 4
0.926 5±
0.181 9
20
0.429 2±
0.046 9
, 百拇医药
0.378 3±
0.045 7**
0.439 0±
0.072 1**
0.925 5±
0.096 5
70%甘油
0.431 8±
0.060 1
0.358 3±
0.033 0**
, 百拇医药
0.426 3±
0.082 6**
0.886 7±
0.172 3
与对照组比较*P<0.05,**P<0.01
2.睾丸组织病理学的变化:10 mg组在光镜下可见精母细胞水样变性,管腔生精细胞脱落,可见多核细胞,20 mg组表现得更为广泛和严重。小管基膜无明显改变,间质细胞相对增多。阳性组见精曲小管内细胞广泛脱落,轻者以精子细胞脱落为主,重者包括精母细胞,部分管腔萎缩,可见多核细胞和退变生精细胞。电镜下,10和20 mg组均见管腔内大量脱落精子细胞并有变性坏死,精子释放延迟并有异形精子头,支持细胞线粒体扩张,胞浆固缩,微管稀少,内质网扩张。
, 百拇医药
3.量效和时效关系:脱落生精细胞数随吡哆醇浓度和接触时间而增加,与对照组比较,1 mg/ml组在48小时以上、10 mg/ml组在24小时以上和20 mg/ml组在12小时以上差异均有非常显著性(P<0.01)。
4.支持细胞骨架的变化:对照组支持细胞自然伸展、淡染,细胞骨架呈纵向自然伸展。随吡哆醇剂量和接触时间延长,其细胞骨架松弛、回缩、断裂消失,生精细胞脱落。
三、讨论
1.睾丸内注射吡哆醇对睾丸的影响:睾丸内注射吡哆醇后,引起大鼠性腺、副性腺萎缩。光镜观察显示,随着剂量的增加,精曲小管的损伤表现为精子细胞脱落、多核细胞和精子细胞变性坏死。电镜下见精子异形、释放延迟和变性坏死;支持细胞水肿,内质网、线粒体扩张,微管稀疏,重者胞浆固缩等。这些表现在一定程度上相似于腹腔注射吡哆醇所产生的效应。本实验显示,睾丸内注射吡哆醇引起睾丸毒性的最低有效剂量约10 mg/睾丸。
, 百拇医药
2.吡哆醇对睾丸培养细胞的作用:支持细胞-生精细胞共培养中加入吡哆醇后,生精细胞的脱落随剂量和接触时间而增加。在0.1 mg/ml剂量水平,生精细胞脱落数高于对照组,但差异无显著性,估计吡哆醇引起生精细胞脱落的最大无作用浓度在此范围。
3.吡哆醇对大鼠睾丸作用的可能机理:在真核细胞中,细胞骨架与多种功能有关。支持细胞骨架的主要功能是形成血睾屏障,生精细胞的定向和移位,生精细胞的激素和营养支持和残体的吞噬。睾丸内注射特异作用肌动蛋白微丝的松胞菌素,可破坏支持细胞的特化结构,引起血睾丸屏障局部损害、生精细胞定向紊乱。注射秋水仙碱等微管解聚物,可引起支持细胞形态变化,顶部突起脱落,滑面内质网异位,继而导致生精细胞有丝分裂和减数分裂停滞,长精子细胞向顶部迁移受阻,精子头和顶体形状异常等,这些现象在本实验中均可见到。在支持细胞-生精细胞培养中所见到的支持细胞骨架改变,与生精细胞脱落的程度一致。
以上结果显示,大剂量吡哆醇引起大鼠生精细胞的损害,与支持细胞的损害相一致。由于支持细胞在精子发生中的特殊地位,推测支持细胞骨架受损,可能是吡哆醇抑制大鼠睾丸精子发生的原因之一。
收稿日期:1998-04-17 修回日期:1998-10-14, http://www.100md.com
单位:黄厚今 (563003 贵州省 遵义医学院预防医学教研室);王瑞淑 徐维光 杨青 (华西医科大学营养与食品卫生学教研室);张杰 (病理学教研室)
关键词:
吡哆醇致大鼠睾丸毒性的体内外研究 维生素B6是吡哆醇、吡哆醛和吡哆胺的合称。近年来,随着吡哆醇用作治疗、辅助治疗以及保健品成分不断增加,长期大量应用维生素B6的安全性已备受关注。本实验采用体内外方法,探讨吡哆醇对睾丸作用的特点。
一、材料与方法
1.实验动物及分组:SD雄性成年大鼠,体重200~250 g,由华西医科大学动物中心提供。喂养于12/12小时(昼/夜),温度约20℃的环境,常规饲养1周后,随机分为阴性对照组、阳性对照组(甘油组)和3个试验组,每组10只动物。细胞培养用20~25天龄SD幼鼠,体重40~50 g。
, 百拇医药
2.主要试剂:盐酸吡哆醇(C8H11O3N-HCl=205.64,生化试剂,含量99%,上海化学试剂采购供应站分装厂);甘油(生化试剂,天津市东方卫生材料厂);最低必需培养基(MEM,GibcoBRL, 美国);牛血清(华西医科大学分子生物学研究室);胰蛋白酶(1∶250, DIFCO, 美国);胶原酶(Sigma, 美国)。
3.实验方法:
(1)睾丸内注射:用双蒸水溶解吡哆醇-盐酸并配成10、100和200 mg/ml溶液,过滤除菌。大鼠经常规消毒阴囊皮肤,于睾丸中部进针,穿过白膜后推至睾丸中心注药。阴性对照用生理盐水,阳性对照用甘油。所有动物均注射单侧,对侧作对照,容量50 μl,1周后重复1次。至第15天处死动物取材,分别作性腺和副性腺测量及光镜、电镜检查。
(2)细胞分离培养:无菌取出睾丸,初步剪碎。加入0.25%胰蛋白酶,33℃下作用15分钟,中止酶作用后过滤。再经0.1%胶原酶在33℃下消化约15分钟,过滤。将细胞分散于5%小牛血清的MEM中,取少量做苔盼蓝排斥试验,要求蓝染细胞<3%。将细胞浓度调整到1.6×106/ml,每孔加1 ml培养24小时,观察细胞生长情况。
, http://www.100md.com
4.观察指标:
(1)睾丸内注射:实验期末测量双侧睾丸体积,称量性腺及副性腺。取左侧睾丸中心组织用于电镜检查。其余组织及右侧附睾、前列腺和精囊均作光镜检查。
(2)细胞培养:用不含胎牛血清的MEM将吡哆醇分别配制成0.1、1、10和20 mg/ml浓度。细胞经24小时贴壁后,加入含不同浓度吡哆醇的MEM,每组8个复孔,继续培养,于不同时点进行脱落细胞计数,并进行显著性检验。将支持细胞-生精细胞培养片和经低渗处理的支持细胞片进行Coomassie BB染色,观察吡哆醇对支持细胞骨架的作用。
二、结果
1.睾丸内注射吡哆醇对大鼠睾丸及副性腺的影响(表1、2):与对照组比较,10 mg组的睾丸及附睾重量减轻,而20 mg组的睾丸体积与重量,附睾、前列腺重量均减轻,与阳性对照组的变化一致。各剂量组精囊重量无明显变化。
, 百拇医药
表1 睾丸内注射吡哆醇对睾丸体积和重量的影响
(n=10,
剂量
(mg/睾丸)
睾丸体积(cm3)
睾丸重量(g)
左
右
左
右
, 百拇医药
0
1.836 6±
0.169 4
1.834 4±
0.167 8
1.334 8±
0.120 3
1.339 0±
0.123 5
1
1.898 8±
0.183 0
, 百拇医药
1.781 0±
0.238 0
1.301 4±
0.155 3
1.198 0±
0.225 3
10
1.888 4±
0.262 8
1.717 6±
0.282 0
1.349 4±
, 百拇医药
1.153 1
1.112 4±
0.160 0**
20
1.898 7±
0.249 3
1.367 1±
0.178 3**
1.316 0±
0.155 9
0.909 2±
0.132 3**
, 百拇医药
70%甘油
1.815 9±
0.341 9
1.118 1±
0.267 9**
1.203 3±
0.265 3
0.666 7±
0.145 8**
与对照组比较**P<0.01
表2 睾丸内注射吡哆醇对副性腺的影响(g,
, 百拇医药
剂量
(mg/睾丸)
附睾
前列腺
精囊
左
右
0
0.446 3±
0.069 8
0.464 7±
0.069 9
0.629 1±
, 百拇医药
0.115 3
1.071 7±
0.229 2
1
0.427 1±
0.047 7
0.430 1±
0.065 9
0.646 5±
0.156 5
0.995 1±
0.251 2
, http://www.100md.com
10
0.433 4±
0.038 6
0.395 9±
0.037 9*
0.566 1±
0.130 4
0.926 5±
0.181 9
20
0.429 2±
0.046 9
, 百拇医药
0.378 3±
0.045 7**
0.439 0±
0.072 1**
0.925 5±
0.096 5
70%甘油
0.431 8±
0.060 1
0.358 3±
0.033 0**
, 百拇医药
0.426 3±
0.082 6**
0.886 7±
0.172 3
与对照组比较*P<0.05,**P<0.01
2.睾丸组织病理学的变化:10 mg组在光镜下可见精母细胞水样变性,管腔生精细胞脱落,可见多核细胞,20 mg组表现得更为广泛和严重。小管基膜无明显改变,间质细胞相对增多。阳性组见精曲小管内细胞广泛脱落,轻者以精子细胞脱落为主,重者包括精母细胞,部分管腔萎缩,可见多核细胞和退变生精细胞。电镜下,10和20 mg组均见管腔内大量脱落精子细胞并有变性坏死,精子释放延迟并有异形精子头,支持细胞线粒体扩张,胞浆固缩,微管稀少,内质网扩张。
, 百拇医药
3.量效和时效关系:脱落生精细胞数随吡哆醇浓度和接触时间而增加,与对照组比较,1 mg/ml组在48小时以上、10 mg/ml组在24小时以上和20 mg/ml组在12小时以上差异均有非常显著性(P<0.01)。
4.支持细胞骨架的变化:对照组支持细胞自然伸展、淡染,细胞骨架呈纵向自然伸展。随吡哆醇剂量和接触时间延长,其细胞骨架松弛、回缩、断裂消失,生精细胞脱落。
三、讨论
1.睾丸内注射吡哆醇对睾丸的影响:睾丸内注射吡哆醇后,引起大鼠性腺、副性腺萎缩。光镜观察显示,随着剂量的增加,精曲小管的损伤表现为精子细胞脱落、多核细胞和精子细胞变性坏死。电镜下见精子异形、释放延迟和变性坏死;支持细胞水肿,内质网、线粒体扩张,微管稀疏,重者胞浆固缩等。这些表现在一定程度上相似于腹腔注射吡哆醇所产生的效应。本实验显示,睾丸内注射吡哆醇引起睾丸毒性的最低有效剂量约10 mg/睾丸。
, 百拇医药
2.吡哆醇对睾丸培养细胞的作用:支持细胞-生精细胞共培养中加入吡哆醇后,生精细胞的脱落随剂量和接触时间而增加。在0.1 mg/ml剂量水平,生精细胞脱落数高于对照组,但差异无显著性,估计吡哆醇引起生精细胞脱落的最大无作用浓度在此范围。
3.吡哆醇对大鼠睾丸作用的可能机理:在真核细胞中,细胞骨架与多种功能有关。支持细胞骨架的主要功能是形成血睾屏障,生精细胞的定向和移位,生精细胞的激素和营养支持和残体的吞噬。睾丸内注射特异作用肌动蛋白微丝的松胞菌素,可破坏支持细胞的特化结构,引起血睾丸屏障局部损害、生精细胞定向紊乱。注射秋水仙碱等微管解聚物,可引起支持细胞形态变化,顶部突起脱落,滑面内质网异位,继而导致生精细胞有丝分裂和减数分裂停滞,长精子细胞向顶部迁移受阻,精子头和顶体形状异常等,这些现象在本实验中均可见到。在支持细胞-生精细胞培养中所见到的支持细胞骨架改变,与生精细胞脱落的程度一致。
以上结果显示,大剂量吡哆醇引起大鼠生精细胞的损害,与支持细胞的损害相一致。由于支持细胞在精子发生中的特殊地位,推测支持细胞骨架受损,可能是吡哆醇抑制大鼠睾丸精子发生的原因之一。
收稿日期:1998-04-17 修回日期:1998-10-14, http://www.100md.com