按一级吸收(一级并行)米氏过程消除药物的给药方案评价
http://www.100md.com
37c医学网
作者:王秋红 李晶 郭政
单位:王秋红(哈尔滨市药材公司 哈尔滨150000); 李晶(哈尔滨市药材公司 哈尔滨150000 黑龙江中医药大学); 郭政(哈尔滨市药材公司 哈尔滨150000 哈尔滨医科大学基础数学教研室)
关键词:药物动力学;给药方案;米氏消除;苯妥英钠
数理医药学杂志000147
摘 要:讨论了消除符合(一级并行)米氏过程药物的多剂量血管外给药方案的评价方法。应用研制的给药方案设计与评价计算机分析系统,分析了苯妥英钠的若干给药方案
中图分类号:R 969.1
文章编号:1004-4337(2000)01-0081-02▲
, 百拇医药
1 引言
获得了某种药物的动力学参数后,理论上就可预测各种用药方法的血药浓度的时程变化。若已知某药的血药浓度与其药效作用之间的关系,如最低有效浓度与/或最小中毒浓度等,我们就可以按照一定的目标或限制条件根据药物动力学评价该药的给药方案。由于近年来NONMEN法等群体药物动力学分析技术[1]的发展,已有可能结合Bayes反馈法[2]根据多方面的信息计算个体参数,使得临床上个体的药物动力学参数较易获得。所以应用药物动力学方法评价个体化给药方案已初具现实意义[3]。符合一级吸收、(一级并行)米氏消除药物的药物动力学方程不可获得解析解,对其动力学性质,尤其是稳态期间性质的研究较困难,无法对给药方案性质(一般是稳态期间的性质)进行分析[4,5]。本文提出了分析按一级吸收、(一级并行)米氏消除药物的多剂量、等间隔的给药方案评价的精确的数值方法。
2 药物动力学模型与数值方法
, 百拇医药
一般地,我们考虑周期性给药。在一个周期内用药k次,第s次用药量为Ds(s=1,2,…k),经Ts间隔用第s+1次药。多剂量给药后,在一个时刻点吸收室中的药量是各次给药残余量之和。记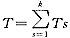 ,是第n个周期中第s次给药瞬间吸收室中的药量D(n,s)及稳态期间第s次用药后瞬间吸收室中的药量D(s)为:
,是第n个周期中第s次给药瞬间吸收室中的药量D(n,s)及稳态期间第s次用药后瞬间吸收室中的药量D(s)为: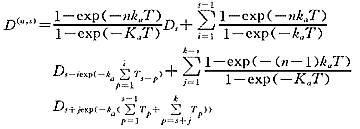
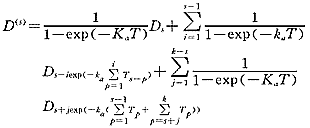
其中Ka为一级吸收速率常数。又记F为生物利用度、V为表现分布客观、K为一级消除速率常数,Vm、Km为米氏消除参数。则第n个周期第s次给药后经t时间血药浓度C(n,s)(t)满足如下动力学方程,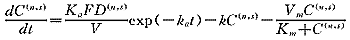 (1)
(1)
, 百拇医药
C(n,s)(0)=C(n,s-1)(Ts-1), 当s>1时
C(n,1)(0)=C(n,s)(Tk), 当n>1时。
在稳态期间第s次用药后经t时间的血药浓度C(s)(t)满足如下动力学方程,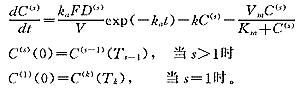 (2)
(2)
下面提出的给药方案评价的数值方法根据方程(1)~(2)的数学性质提出。这些数学性质的证明方法可参考我们以前的工作[6]。为了表达方便,下面在描述有关的算法时,一般仅提出对该算法的直观解释。我们先讨论方程(2)的数值解法:
对方程(2),记C(1)(0)=C(k)(Tk)(=C0)。由 及
及 可得C0的上下、界,记为b1、b2。给定一个a,以C(1)(0)=a为初始点,可用四阶Runge-Kutta法求解方程(2)得到C(k)(Tk)。可证当C(1)(0)>C0时,C(k)(Tk)
可得C0的上下、界,记为b1、b2。给定一个a,以C(1)(0)=a为初始点,可用四阶Runge-Kutta法求解方程(2)得到C(k)(Tk)。可证当C(1)(0)>C0时,C(k)(Tk)(1)(0);当C(1)(0)(k)(Tk)>C(1)(0)。据此可按下述步骤递推计算:取C(1)(0)=(b2+b1)/2=b3代入方程(2)计算C(k)(Tk),若C(k)(Tk)3,则将前步的b2换为b3,b1不变;若C(k)(Tk)>b3,则将前步的b1换为b3,b2不变;取C(1)(0)=(b2+b1)/2=b3代入方程(2)再计算C(k)(Tk)。当|b2-b1|<δ1或|C(k)(Tk)+D1/V-C(1)(0)|<δ2时,停止迭代计算。取δ1=δ2=0.001D1/V,即可达足够的精度。最后一步的b3值即为所求C(1)(0),以C(1)(0)为初始点,可解方程(2)(得到C(k)(Tk)≌C(1)(0))。
, http://www.100md.com
以Cmin表示最低有效浓度,Cmax表示最小中毒浓度,F1与F2表示两个达坪分数;N表示实际或预计给药次数,则一般的设定条件(输入量)可为:Ds、Ts(s=1,2,…k)、Cmin、Cmax、F1、F2、N及动力学参数。根据上述条件,我们可设计算法,计算以下各项评价给药方案的指标:
2.1 稳态、第s次给药期间的平均血药浓度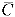 (s)及第n个给药周期第s次给药期间的平均血药浓度
(s)及第n个给药周期第s次给药期间的平均血药浓度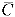 (n,s)为:
(n,s)为: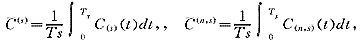
可在用四阶Runge-Kutta法递推解方程(2)的过程中,通过第i步与第(i+1)步时间范围内对应的矩形面积(h为步长)在各个给药间隔内(0到Ts)累加得到AUC后,计算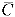 (s)=AUC/Ts获得。由递推方程(1),用Runge-Kutta法可类似地计算各次给药期间的平均血药浓度
(s)=AUC/Ts获得。由递推方程(1),用Runge-Kutta法可类似地计算各次给药期间的平均血药浓度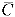 (n,s)。
(n,s)。
, 百拇医药
2.2 稳态时,一个给药周期内平均血药浓度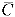 ss及第n个给药周期中的平均血药浓度
ss及第n个给药周期中的平均血药浓度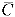 (m)为,
(m)为,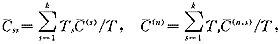
第n个周期用药后的达坪分数为Fn=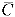 (n)/
(n)/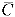 ss。亦可利用此式解出达到指定达坪分数F1(高水平如95%)或F2(低水平如85%)所需用药周期数N1与N2。根据递推方程(1),用Runge-Kutta法逐步计算各次给药期间的平均血药浓度
ss。亦可利用此式解出达到指定达坪分数F1(高水平如95%)或F2(低水平如85%)所需用药周期数N1与N2。根据递推方程(1),用Runge-Kutta法逐步计算各次给药期间的平均血药浓度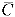 n及达坪分数Fn,直到得到第一个m,使得Fm≥f,则m便是达到指定达坪分数f所需用药次数。
n及达坪分数Fn,直到得到第一个m,使得Fm≥f,则m便是达到指定达坪分数f所需用药次数。
, http://www.100md.com
2.3 稳态第s次给药期间的最大血药浓度C(s)max及达峰时间T(s)max;最小血药浓度C(s)min。第n个给药周期中第s次给药后的最大血药浓度C(n,s)max与达峰时间T(n,s)max及最小血药浓度C(n,s)min。这些指标可在用四阶Runge-Kutta法递推解方程(2)或(1)时,通过逐步比较得到。
2.4 稳态第s次给药期间,血药浓度在最低有效浓度Cmin之上的时间T1与起(t1)止(t2)时间,记为MIN(s):[(t1,t2),T1];在最小中毒浓度Cmax之上的时间T2′与起(t1′)止(t2′)时间,记为MAX(s):[(t1′,t2′),T1′]。类似地记在第n个给药周期、第s次给药后,血药浓度在最低有效浓度Cmin之上的时间与起止时间为MIN(n,s):[(t1,t2),T1];记其在最小中毒浓度Cmax上的时间与起止时间为MAX(n,s):[(t1,t2),T2]。这些指标亦可在用四阶Runge-Kutta法递推解方程(2)或(1)时,通过逐步比较得到。
, http://www.100md.com
3 应用与讨论
采用以上算法,我们编制了按一级吸收、一级并行米氏(米氏)消除药物血管外给药方案评计算机程序。该程序是我们用C语言研制的药物动力学计算机分析系统的一部分。按中文菜单揭示选择问题类型、建立数据文件后,即可运行输出分析结果。
苯妥英钠的最低有效血药浓度为Cmin=10mg/L,最小中毒浓度为Cmax=20mg/L。对某癫痫病患者口服苯妥英钠治疗。若该患者的药动学参数为ka=0.5/h,V=40L,Vm=0.8mg/Lh,Km=10mg/L,而k=0(米氏消除)。维持剂量为每次D=150mg,又若给药间隔τ=8h,计算得到,平均稳态浓度为14.12mg/L;第13次用药后达到85%的达坪分数;第22次用药后达到95%的达坪分数;稳态期间的最低血药浓度为13.11mg/L;峰值为14.67mg/L;达峰时间为2.89h。
计算结果尚输出从第一次给药到达指定高水平达坪分数(95%)所需给药各期间的有关参数,结果显示,前6次给药期间,血药浓度均在有效浓度之下;第7次给药后平均血药浓度为9.63mg/L,达坪分数为68%;该次给药后,血药浓度经3.11h达到峰值为10.11mg/L,且给药后从1.91h到4.10h期间(共2.08h)血药浓度在有效浓度之上;第11次给药后(达坪分数为96%),血药浓度均在有效浓度之上。
, http://www.100md.com
分析结果显示,对该患者若不使用冲击量,在开始用药第3天后才能使血药浓度在部分时间内达到有效浓度之上,起效时间较慢,一般有必要使用冲击量。
本文提出的数值方法与程序可成为一级吸收、(一级并行)米氏消除药物的给药方案评价的一种有效工具。上述根据药物动力学评价给药方案的方法适用于药物效应直接与血药浓工相关的情况。若药物效应与血药浓度的关系高度变异或复杂,应根据药效动力等评价给药方案[7]。■
参考文献:
[1] 郭政,李霞,何颖等.群体药物动力学体非线性混合效应模型的方法与程序.临床医学工程学杂志,1994,2:24~26.
[2] Yamaoka, K., Nakagawa, T., Tanaka, H., et al. A nonlinear multiple regression program, multi2(Bayes),based on bayesian algodrithm for microcomputurs, J Phanmacobio-Dyn, 1985,8:246~256.
, 百拇医药
[3] Thompson, GA.Dosage regimen design: a pharmacokinetic approach, J Clin Pharmacol, 1992,32:210~214.
[4] Sawchuk, RJ., Rector, TS. Steady-state plasma concentrations as a function of the absorbtion rate and dosing interval for drugs exhibing concentration dependent clearane: consequences for phenytion therepy, Ibid, 1979,7:543.
[5] Tsuchiya, T., Levy, G.Relationship between dose and plateall levels of drugs eliminated by parrallel first order and capacity-limited pharmakokinetcs, J Pharm Sci., 1972,61:541~544.
[6] 吕淑娟,郭政.一级并行米氏消除药物最优给药方案的数值方法.生物数学学报,1992,7:127~132.
[7] Williams, RL. Dosage regimen design: pharmacodynamic considerations, J Clin Pharmacol, 1992,32:597~602.
收稿日期:1999-03-08, http://www.100md.com
单位:王秋红(哈尔滨市药材公司 哈尔滨150000); 李晶(哈尔滨市药材公司 哈尔滨150000 黑龙江中医药大学); 郭政(哈尔滨市药材公司 哈尔滨150000 哈尔滨医科大学基础数学教研室)
关键词:药物动力学;给药方案;米氏消除;苯妥英钠
数理医药学杂志000147
摘 要:讨论了消除符合(一级并行)米氏过程药物的多剂量血管外给药方案的评价方法。应用研制的给药方案设计与评价计算机分析系统,分析了苯妥英钠的若干给药方案
中图分类号:R 969.1
文章编号:1004-4337(2000)01-0081-02▲
, 百拇医药
1 引言
获得了某种药物的动力学参数后,理论上就可预测各种用药方法的血药浓度的时程变化。若已知某药的血药浓度与其药效作用之间的关系,如最低有效浓度与/或最小中毒浓度等,我们就可以按照一定的目标或限制条件根据药物动力学评价该药的给药方案。由于近年来NONMEN法等群体药物动力学分析技术[1]的发展,已有可能结合Bayes反馈法[2]根据多方面的信息计算个体参数,使得临床上个体的药物动力学参数较易获得。所以应用药物动力学方法评价个体化给药方案已初具现实意义[3]。符合一级吸收、(一级并行)米氏消除药物的药物动力学方程不可获得解析解,对其动力学性质,尤其是稳态期间性质的研究较困难,无法对给药方案性质(一般是稳态期间的性质)进行分析[4,5]。本文提出了分析按一级吸收、(一级并行)米氏消除药物的多剂量、等间隔的给药方案评价的精确的数值方法。
2 药物动力学模型与数值方法
, 百拇医药
一般地,我们考虑周期性给药。在一个周期内用药k次,第s次用药量为Ds(s=1,2,…k),经Ts间隔用第s+1次药。多剂量给药后,在一个时刻点吸收室中的药量是各次给药残余量之和。记
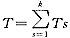 ,是第n个周期中第s次给药瞬间吸收室中的药量D(n,s)及稳态期间第s次用药后瞬间吸收室中的药量D(s)为:
,是第n个周期中第s次给药瞬间吸收室中的药量D(n,s)及稳态期间第s次用药后瞬间吸收室中的药量D(s)为: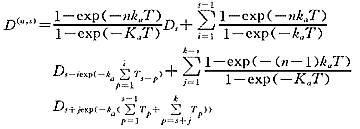
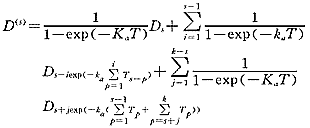
其中Ka为一级吸收速率常数。又记F为生物利用度、V为表现分布客观、K为一级消除速率常数,Vm、Km为米氏消除参数。则第n个周期第s次给药后经t时间血药浓度C(n,s)(t)满足如下动力学方程,
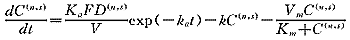 (1)
(1), 百拇医药
C(n,s)(0)=C(n,s-1)(Ts-1), 当s>1时
C(n,1)(0)=C(n,s)(Tk), 当n>1时。
在稳态期间第s次用药后经t时间的血药浓度C(s)(t)满足如下动力学方程,
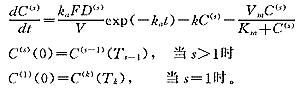 (2)
(2)下面提出的给药方案评价的数值方法根据方程(1)~(2)的数学性质提出。这些数学性质的证明方法可参考我们以前的工作[6]。为了表达方便,下面在描述有关的算法时,一般仅提出对该算法的直观解释。我们先讨论方程(2)的数值解法:
对方程(2),记C(1)(0)=C(k)(Tk)(=C0)。由
 及
及 可得C0的上下、界,记为b1、b2。给定一个a,以C(1)(0)=a为初始点,可用四阶Runge-Kutta法求解方程(2)得到C(k)(Tk)。可证当C(1)(0)>C0时,C(k)(Tk)
可得C0的上下、界,记为b1、b2。给定一个a,以C(1)(0)=a为初始点,可用四阶Runge-Kutta法求解方程(2)得到C(k)(Tk)。可证当C(1)(0)>C0时,C(k)(Tk), http://www.100md.com
以Cmin表示最低有效浓度,Cmax表示最小中毒浓度,F1与F2表示两个达坪分数;N表示实际或预计给药次数,则一般的设定条件(输入量)可为:Ds、Ts(s=1,2,…k)、Cmin、Cmax、F1、F2、N及动力学参数。根据上述条件,我们可设计算法,计算以下各项评价给药方案的指标:
2.1 稳态、第s次给药期间的平均血药浓度
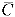 (s)及第n个给药周期第s次给药期间的平均血药浓度
(s)及第n个给药周期第s次给药期间的平均血药浓度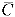 (n,s)为:
(n,s)为: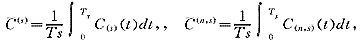
可在用四阶Runge-Kutta法递推解方程(2)的过程中,通过第i步与第(i+1)步时间范围内对应的矩形面积(h为步长)在各个给药间隔内(0到Ts)累加得到AUC后,计算
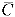 (s)=AUC/Ts获得。由递推方程(1),用Runge-Kutta法可类似地计算各次给药期间的平均血药浓度
(s)=AUC/Ts获得。由递推方程(1),用Runge-Kutta法可类似地计算各次给药期间的平均血药浓度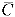 (n,s)。
(n,s)。, 百拇医药
2.2 稳态时,一个给药周期内平均血药浓度
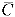 ss及第n个给药周期中的平均血药浓度
ss及第n个给药周期中的平均血药浓度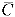 (m)为,
(m)为,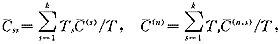
第n个周期用药后的达坪分数为Fn=
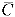 (n)/
(n)/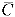 ss。亦可利用此式解出达到指定达坪分数F1(高水平如95%)或F2(低水平如85%)所需用药周期数N1与N2。根据递推方程(1),用Runge-Kutta法逐步计算各次给药期间的平均血药浓度
ss。亦可利用此式解出达到指定达坪分数F1(高水平如95%)或F2(低水平如85%)所需用药周期数N1与N2。根据递推方程(1),用Runge-Kutta法逐步计算各次给药期间的平均血药浓度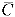 n及达坪分数Fn,直到得到第一个m,使得Fm≥f,则m便是达到指定达坪分数f所需用药次数。
n及达坪分数Fn,直到得到第一个m,使得Fm≥f,则m便是达到指定达坪分数f所需用药次数。, http://www.100md.com
2.3 稳态第s次给药期间的最大血药浓度C(s)max及达峰时间T(s)max;最小血药浓度C(s)min。第n个给药周期中第s次给药后的最大血药浓度C(n,s)max与达峰时间T(n,s)max及最小血药浓度C(n,s)min。这些指标可在用四阶Runge-Kutta法递推解方程(2)或(1)时,通过逐步比较得到。
2.4 稳态第s次给药期间,血药浓度在最低有效浓度Cmin之上的时间T1与起(t1)止(t2)时间,记为MIN(s):[(t1,t2),T1];在最小中毒浓度Cmax之上的时间T2′与起(t1′)止(t2′)时间,记为MAX(s):[(t1′,t2′),T1′]。类似地记在第n个给药周期、第s次给药后,血药浓度在最低有效浓度Cmin之上的时间与起止时间为MIN(n,s):[(t1,t2),T1];记其在最小中毒浓度Cmax上的时间与起止时间为MAX(n,s):[(t1,t2),T2]。这些指标亦可在用四阶Runge-Kutta法递推解方程(2)或(1)时,通过逐步比较得到。
, http://www.100md.com
3 应用与讨论
采用以上算法,我们编制了按一级吸收、一级并行米氏(米氏)消除药物血管外给药方案评计算机程序。该程序是我们用C语言研制的药物动力学计算机分析系统的一部分。按中文菜单揭示选择问题类型、建立数据文件后,即可运行输出分析结果。
苯妥英钠的最低有效血药浓度为Cmin=10mg/L,最小中毒浓度为Cmax=20mg/L。对某癫痫病患者口服苯妥英钠治疗。若该患者的药动学参数为ka=0.5/h,V=40L,Vm=0.8mg/Lh,Km=10mg/L,而k=0(米氏消除)。维持剂量为每次D=150mg,又若给药间隔τ=8h,计算得到,平均稳态浓度为14.12mg/L;第13次用药后达到85%的达坪分数;第22次用药后达到95%的达坪分数;稳态期间的最低血药浓度为13.11mg/L;峰值为14.67mg/L;达峰时间为2.89h。
计算结果尚输出从第一次给药到达指定高水平达坪分数(95%)所需给药各期间的有关参数,结果显示,前6次给药期间,血药浓度均在有效浓度之下;第7次给药后平均血药浓度为9.63mg/L,达坪分数为68%;该次给药后,血药浓度经3.11h达到峰值为10.11mg/L,且给药后从1.91h到4.10h期间(共2.08h)血药浓度在有效浓度之上;第11次给药后(达坪分数为96%),血药浓度均在有效浓度之上。
, http://www.100md.com
分析结果显示,对该患者若不使用冲击量,在开始用药第3天后才能使血药浓度在部分时间内达到有效浓度之上,起效时间较慢,一般有必要使用冲击量。
本文提出的数值方法与程序可成为一级吸收、(一级并行)米氏消除药物的给药方案评价的一种有效工具。上述根据药物动力学评价给药方案的方法适用于药物效应直接与血药浓工相关的情况。若药物效应与血药浓度的关系高度变异或复杂,应根据药效动力等评价给药方案[7]。■
参考文献:
[1] 郭政,李霞,何颖等.群体药物动力学体非线性混合效应模型的方法与程序.临床医学工程学杂志,1994,2:24~26.
[2] Yamaoka, K., Nakagawa, T., Tanaka, H., et al. A nonlinear multiple regression program, multi2(Bayes),based on bayesian algodrithm for microcomputurs, J Phanmacobio-Dyn, 1985,8:246~256.
, 百拇医药
[3] Thompson, GA.Dosage regimen design: a pharmacokinetic approach, J Clin Pharmacol, 1992,32:210~214.
[4] Sawchuk, RJ., Rector, TS. Steady-state plasma concentrations as a function of the absorbtion rate and dosing interval for drugs exhibing concentration dependent clearane: consequences for phenytion therepy, Ibid, 1979,7:543.
[5] Tsuchiya, T., Levy, G.Relationship between dose and plateall levels of drugs eliminated by parrallel first order and capacity-limited pharmakokinetcs, J Pharm Sci., 1972,61:541~544.
[6] 吕淑娟,郭政.一级并行米氏消除药物最优给药方案的数值方法.生物数学学报,1992,7:127~132.
[7] Williams, RL. Dosage regimen design: pharmacodynamic considerations, J Clin Pharmacol, 1992,32:597~602.
收稿日期:1999-03-08, http://www.100md.com