转肽酶A在蛋白质和多肽修饰中的应用
底物,1转肽酶A的作用机制及结构特征,2转肽酶A的蛋白质工程及催化活性的研究,3转肽酶A在蛋白质或多肽修饰中的研究进展,4小结
马颖,刘忞之,王伟转肽酶A在蛋白质和多肽修饰中的应用
马颖,刘忞之,王伟
在20世纪90年代末,Navarre 和 Schneewind[1]首次在金黄色葡萄球菌(Staphylococcus aureus)中发现了转肽酶 A(sortase A),它催化了表面蛋白与多种革兰阳性菌的肽聚糖骨架的共价结合,从而开启了转肽酶A对蛋白质或多肽作用的研究[2-10]。
近年来,人们发现从金黄色葡萄球菌中分离得到的转肽酶A在蛋白质或多肽的合成与修饰中表现出了良好的反应活性和特异性[11]。转肽酶A可以特异性结合蛋白质 C末端的 LPXTG 序列(X 是任意氨基酸),切断苏氨酸和甘氨酸之间的肽键,而后与 N-端含有甘氨酸残基的蛋白质或多肽末端连接形成肽键[11-12]。转肽酶A不仅可以用于修饰蛋白质或多肽增强其稳定性和活性,还可以实现蛋白质和蛋白质、蛋白质和多肽以及多肽和多肽之间的特异性位点的连接[13];其催化反应的高特异性使得转肽酶A在蛋白质或多肽合成与修饰中得到了广泛的应用。本文就转肽酶A的作用机制、结构特征及其在蛋白质和多肽修饰中的应用展开综述。
1 转肽酶A的作用机制及结构特征
转肽酶A是一种膜结合巯基转肽酶[12],能够特异性地识别蛋白质或多肽 C端的保守氨基酸序列 LPXTG(X 指任意氨基酸)。首先,转肽酶A的 184 位半胱氨酸上的巯基进攻苏氨酸(Thr)和甘氨酸(Gly)之间的肽键,生成乙酰化的转肽酶A中间产物,然后另一蛋白质或多肽N端的甘氨酸的氨基亲核进攻硫酯中间体,使得亲核基团和苏氨酸之间的肽键形成,而原有的保守序列 LPXTG 中的甘氨酸残基及其相关部分被切除(图 1)[14-17]。
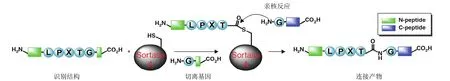
图1 转肽酶A作用机制[17]
对于转肽酶A的三维结构,Bradshaw 等[12]利用 NMR进行了解析(图 2A)。结果显示,转肽酶A包含 2 个短螺旋和 8 个 β 折叠结构。后经其他研究表明,在其第 4 个和第 7 个 β 折叠的筒状结构的一侧具有一个疏水沟,这个结构被 β2-β3、β3-β4、β6-β7 和 β7-β8 四个 loop 结构包围,催化中心 His120、Cys184、Arg197分别位于 β4 和 β7 的尾部以及 β8 起始端的沟中(图 2B)[18-20] ......
您现在查看是摘要页,全文长 19172 字符。