布洛芬颗粒溶出度测定方法研究
 |
 |
 |
 |
【摘要】 目的 建立布洛芬颗粒溶出度测定方法。方法 采用紫外分光光度法测定。测定波长为:220 nm。溶出介质为pH 7.2磷酸盐缓冲液。结果 布洛芬溶液在3.0~15.0 μg/ml范围内,吸收度与浓度呈良好的线性关系, r=0.999 3。样品精密度试验RSD为0.85%,样品供试液在12 h内稳定,样品加样回收率为99.9%,RSD为0.22%。结论 该法操作简便,稳定可靠,专属性强,可以有效测定布洛芬颗粒溶出度,为控制布洛芬颗粒质量提供了依据。
【关键词】 布洛芬;溶出度;测定方法
The study ofibuprofen granules dissolution test method
ZHANG Fang.First Hospital Affiliated to Inner Mongolia Medical College, Huhehaote,Inner Mongolia 010050 China
, http://www.100md.com
【Abstract】 Objective To establish of ibuprofen particle dissolution method. Methods UV determination.Determination wavelength:220 nm.pH 7.2 dissolution medium for PBS. Results Ibuprofen in 3.0 15.0 μg/ml solution, the degree of absorption and concentration was good linear relationship, r = 0.999 3. Test samples precision RSD 0.85%for the sample test solution within 12 h in the stability of the sample recovery rate was 99.9%, RSD was 0.22%. Conclusion This method is simple, stable and reliable, specific and effective determination of ibuprofen particle dissolution, in order to control particle dissolution of ibuprofen provides the basis for quality.
, 百拇医药
【Key words】 Ibuprofen; Dissolution; Test method
1 仪器与试药
Agilent 8453紫外分光光度计、HP化学工作站。布洛芬对照品由中国药品生物制品检定所提供,批号110179-200303,供含量测定用。布洛芬颗粒,批号为:050201,050202,050203,规格0.2 g,自制。
2 方法与结果
2.1 溶出条件的确定
2.1.1 溶出介质的选择 参照《中国药典》2005年版二部 96页布洛芬片项下溶出度测定方法,介质选用磷酸盐缓冲液(pH 7.2)900 ml。
2.1.2 测定方法的选择 本品为颗粒剂,采用浆法,供试品部分会浮于液面,致使溶液浓度不均匀。因此,决定采用转蓝法,即《中国药典》2005年版二部附录溶出度测定法第一法。
, 百拇医药
2.1.3 转速的选择 转蓝法以100 转/min为主,因此,确定转速为:100 转/min。
2.2 溶出度检查的方法学考察
2.2.1 布洛芬对照品储备液的制备 精密称取布洛芬对照品150 mg,置250 ml量瓶中,用磷酸盐缓冲液(pH 7.2)溶解并稀释至刻度,备用。
2.2.2 测定波长的选择 精密量取对照品储备液,用磷酸盐缓冲液(pH 7.2)稀释到一定浓度,摇匀,照分光光度法(《中国药典》2005年版二部附录IVA),在200~400 nm波长处扫描,结果在222 nm波长处有最大吸收,另取处方量的各辅料,照上述方法测定,结果:辅料在222 nm波长处无吸收,辅料不干扰测定,确定测定波长为222 nm。
2.2.3 线性关系考察 精密量取布洛芬对照品储备液(0.60 mg/ml)0.5、1.0、1.5、2.0、2.5 ml分别置100 ml量瓶中,加磷酸盐缓冲液(pH 7.2)稀释至刻度,摇匀,照分光光度法(《中国药典》二部附录ⅣΑ)在222 nm波长处测定吸收度。以吸收度为纵坐标,布洛芬浓度C为横坐标,绘制标准曲线,并进行线性回归,得回归方程:A=0.045 C+0.000 60相关系数r=0.999 3。结果表明:布洛芬溶液在3.0~15.0 μg/ml范围内,吸收度与浓度呈良好的线性关系。
, 百拇医药
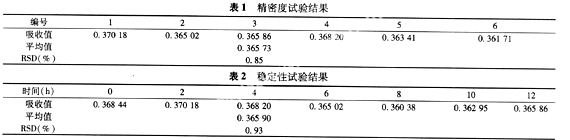
2.2.4 精密度试验 取同一供试品溶液,在222 nm波长处连续测定6次,记录吸收度,结果见表1。
2.2.5 溶液稳定性考察 取上述线性关系项下的浓度为9.0 μg/ml布洛芬对照品溶液,在室温于222 nm波长处分别于放置后的0、2、4、6、8、10、12 h,测定吸收度,结果见表2。RSD为0.93%,表明溶液在12 h内稳定。
2.2.6 回收率试验 按处方,称取一袋量的全处方的辅料9份,分别置250 ml量瓶中,加磷酸盐缓冲液(pH 7.2)适量,再精密加入标示量的80%、100%、120%的对照品各3份,混合溶解后,用上述溶液稀释至刻度,摇匀,滤过,精密量取续滤液1 ml,置100 ml量瓶中,加上述溶液稀释至刻度,摇匀,照分光光度法(《中国药典》2005年版二部附录IVA)在222 nm波长处测定吸收度,计算回收率。结果见表3。
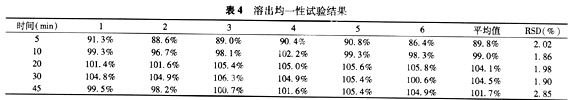
2.2.7 溶出均一性试验 取同一批(050201)样品,以磷酸盐缓冲液(pH 7.2)为溶剂,转速为100转/min,自“分别在5、10、20、30、45 min时取溶液10 ml”起,依法操作,测定溶出度,溶出结果见表4。
, http://www.100md.com
2.2.8 重现性试验 对三批中试样品按上述试验条件进行溶出度测定,结果见表5。绘制溶出曲线,见图1。
根据以上测定结果即溶出曲线,确定溶出度测定方法:采用转蓝法,溶出介质为磷酸盐缓冲液(pH 7.2)900 ml,转速100 r/min,取样时间为20 min,限度为标示量的80%。
3 讨论
3.1 该方法通过精密度、稳定性、重现性、回收率试验及样品测定,证明本方法作为该药品的溶出度测定方法,能够保证药品检测时数据的真实性、可靠性,能够作为保证药品质量的检测依据。
3.2 建立布洛芬颗粒溶出度测定方法可以更好地控制该产品质量。
参考文献
[1] 国家药典委员会.中华人民共和国药典二部.化学工业出版社,2005:96., http://www.100md.com(张 芳)